仿酶固体酸的合成及其纤维素水解性能
2018-09-29王海松,靳书缘,杨超
王 海 松, 靳 书 缘, 杨 超
( 大连工业大学 轻工与化学工程学院, 辽宁 大连 116034 )
0 引 言
纤维素水解产物葡萄糖在食品、医药、日化以及化工领域有广阔应用。近年来,固体酸水解纤维素凭借可回收、腐蚀性小等优点逐渐引起了人们的关注。但由于固体酸和纤维素均不溶于水,两者之间存在严重传质限制,使得固体酸催化水解效率远低于均相液体酸[1]。针对固体酸与纤维素之间的传质障碍问题,多篇文献[2-5]指出,在固体催化剂上引入纤维素结合官能团,合成仿酶型固体催化剂,能提高固体酸的催化性能。Li等[2]以氯甲基聚苯乙烯为载体,通过对氨基苯磺酸载体上部分取代的方式引入酸性位点(—SO3H),氯甲基(—CH2Cl)为结合官能团合成CP-SO3H。该催化剂在120 ℃、48 h条件下水解微晶纤维素,葡萄糖收率为93%。Yang等[1]以交联苄基氯微球为载体,采用发烟硫酸磺化引入磺酸根,氯甲基为结合官能团合成仿酶固体酸。该固体酸在120 ℃水解球磨微晶纤维素24 h,葡萄糖得率为84.9%。Shen等[5]通过碳化三氯蔗糖与对甲苯磺酸混合物合成具有纤维素催化位点(—SO3H)和结合位点(—Cl)的催化剂。该催化剂在离子液体中130 ℃水解微晶纤维素,反应1 h总还原糖得率为67.6%。以上文献均模仿纤维素酶水解过程中结合结构域提高纤维素不溶性底物的可及度从而获得高的水解效率机理,通过在固体酸上引入亲纤维素的Cl基改善水解纤维素的效率,取得了很好的效果,但是因为过程复杂或原料成本问题,离产业化还有些距离,所以本论文将在参考这些文献的基础上,以应用最广泛的工业固体酸催化剂Amberlyst-15(A-15)为原料进行氯甲基化改性并评价其纤维素的水解效率。
A-15是一种强酸性大孔型阳离子交换树脂,具有价廉易得、催化活性高、选择性高、可重复利用等优点[6]。本研究通过B1anc氯甲基化反应制备氯甲基化Amberlyst-15(A-15-Cl),重点考察多聚甲醛、无水四氯化锡、氯磺酸以及反应时间4种因素对A-15-Cl水解球磨微晶纤维素效果的影响;对其反应工艺参数进行系统优化,并与A-15水解效果进行对比,阐明氯甲基化改性提高纤维素水解效率的机理。
1 材料与方法
1.1 材 料
Amberlyst-15,上海阿拉丁生化科技股份有限公司;硝酸银(AgNO3)、多聚甲醛((CHO)n),天津市大茂化学试剂厂;无水四氯化锡(SnCl4),AR,麦克林;氯磺酸(ClSO2OH),山东西亚化学股份有限公司;微晶纤维素,天津市光复精细化工研究所。
1.2 氯甲基化固体酸A-15-Cl的制备
取0.5 g A-15与20 mL 1,2-二氯乙烷(CH2ClCH2Cl)于三口烧瓶中,40 ℃下润胀48 h。升温至55 ℃,加入多聚甲醛、无水四氯化锡与氯磺酸,机械搅拌连续反应。
反应结束后取出固体酸用无水乙醇以及去离子水多次洗涤,直至上清液滴入AgNO3溶液无白色沉淀生成。在真空干燥箱中烘干得A-15-Cl。
1.3 微晶纤维素的水解
1.3.1 微晶纤维素的成分分析
取0.3 g球磨微晶纤维素于耐压瓶中,加入3 mL 72% H2SO4,室温下搅拌2 h,加入84 mL水,混合均匀后,121 ℃反应1 h。反应结束后,使用SBA-40D生物传感分析仪检测葡萄糖含量。
1.3.2 球磨微晶纤维素
使用低温星型球磨机球磨微晶纤维素3 h,通过使纤维素分子间氢键断裂,来降低微晶纤维素的结晶度,提高纤维素的可及度[7]。
1.3.3 水解微晶纤维素
取球磨微晶纤维素0.05 g、固体酸0.1 g与5 mL 水混合,置于15 mL水热合成反应釜中150 ℃反应12 h,结束后离心取液相检测葡萄糖含量。
1.3.4 葡萄糖的检测
用柠檬酸(颗粒)和氢氧化钠(颗粒)将水解液pH调至6.5~7.0后用SBA-40D生物传感分析仪检测葡萄糖质量浓度。
葡萄糖得率=(ρV/mw)×100%
式中:ρ为测得液相葡萄糖质量浓度,mg/mL;V为水解反应加入水的体积,mL;m为微晶纤维素质量,mg;w为原料中葡萄糖质量分数。
1.4 A-15与A-15-Cl表征
A-15与A-15-Cl采用Spectrum One-B型傅里叶变换红外光谱仪对样品进行官能团定性分析;使用Q50热重分析仪进行热稳定性分析;表面形貌及化学元素组成分析采用JSM-7800F场发射扫描电子显微镜和X-Max50能谱仪;比表面积、孔体积、孔径尺寸由ASAP 2020 Plus HD88比表面与孔隙度分析仪测试。
2 结果与讨论
2.1 A-15的氯甲基化工艺的优化
2.1.1 (CHO)n用量的影响
由图1多聚甲醛用量对改性A-15-Cl水解微晶纤维素葡萄糖得率的影响可以看出,随着多聚甲醛用量的增加,葡萄糖得率先增加后减小。当加入多聚甲醛的用量为0.25~0.50 g时,固体酸水解微晶纤维素的葡萄糖得率随多聚甲醛用量的增加而增加。这是因为随着多聚甲醛的加入,甲醛碳正离子浓度增加,氯甲基化程度增加,提高了固体酸和纤维素的吸附力和可及度,改善了纤维素的水解效率。当多聚甲醛用量进一步增加时,葡萄糖得率达到最高点后开始下降。这可能是因为在氯甲基化反应中,苯环上的氯甲基化反应与Friedel-Crafts交联副反应是一对竞争反应,当多聚甲醛用量过多时,氯甲基化反应会在短时间内完成,这也会大大增加Friedel-Crafts副反应程度,导致样品氯含量降低[8]。因此,多聚甲醛最佳用量为0.50 g。
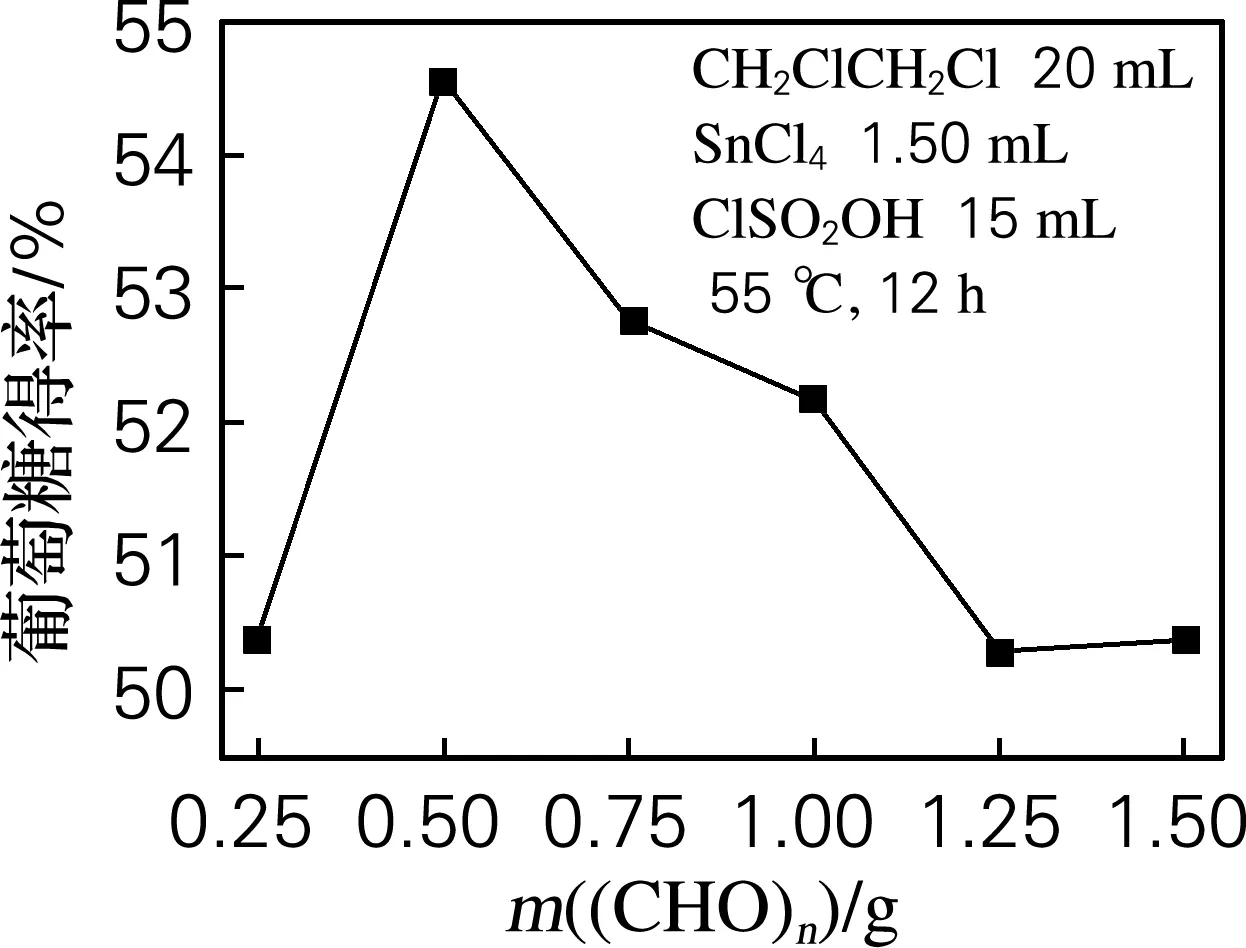
图1 (CHO)n用量对葡萄糖得率的影响
2.1.2 无水SnCl4用量的影响
由图2可知,随着无水SnCl4用量的增加,改性A-15-Cl水解微晶纤维素葡萄糖得率先增加后减小。当无水SnCl4用量在0.50~0.75 mL时,增大无水SnCl4的用量有利于反应体系中烷基碳正离子的生成速率,从而提高体系内烷基碳正离子的浓度,利于亲电取代反应的进行,氯甲基化反应速率加快,氯甲基化程度增加[8],进而纤维素水解效率提高。无水SnCl4的用量为0.75 mL时,葡萄糖得率达到最大,为58.77%。当无水SnCl4用量在0.75~1.75 mL时,会造成整个反应体系中烷基碳正离子的反应速率过快,短时间内存在大量高活性的氯甲基化A-15,从而大大增加了亚甲基桥交联反应的发生,导致氯甲基被消耗,氯含量降低[8],所以葡萄糖得率随无水SnCl4的增加而减小。根据图中纤维素水解糖得率的趋势选择0.75 mL SnCl4为最佳用量。
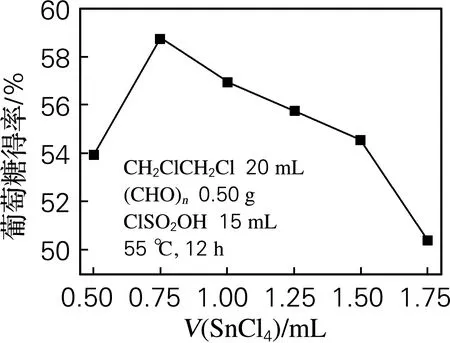
图2 无水SnCl4用量对葡萄糖得率的影响
2.1.3 ClSO2OH用量的影响
由图3可知,随着氯磺酸用量的增加,改性A-15-Cl水解微晶纤维素葡萄糖得率呈现逐渐增加的趋势。当ClSO2OH用量在5~20 mL时,A-15-Cl 水解微晶纤维素葡萄糖得率由55.17%升至61.17%。这是因为随着ClSO2OH用量的增加,反应物分子之间的有效碰撞增加,使反应效率更高,随之氯甲基化程度增加。当ClSO2OH用量从20 mL继续增加到30 mL时,A-15-Cl水解微晶纤维素葡萄糖得率基本维持在61%左右不再增加。可能的原因是当ClSO2OH用量足够多时,烷基正离子的数量对氯甲基化反应的影响逐渐变得不明显,所以产物的氯甲基化程度变化趋于稳定[9];当ClSO2OH用量在20~30 mL时,A-15的氯甲基化程度增加,但是氯元素的吸附能力达到最大,此时葡萄糖的得率取决于A-15-Cl上磺酸根的量[10]。综上所述,选择ClSO2OH最佳用量为20 mL。

图3 ClSO2OH用量对葡萄糖得率的影响
2.1.4 反应时间的影响
由图4可知,反应6~24 h,A-15-Cl水解微晶纤维素葡萄糖得率逐渐提高,继续延长反应时间到48 h时,A-15-Cl水解微晶纤维素葡萄糖得率基本稳定在62%左右。这是因为,反应6~24 h,A-15苯环上有足量的活性位点供氯甲基化反应,所以氯甲基化程度增加,A-15-Cl水解效率提高。超过24 h,有可能A-15 氯甲基化反应达到平衡,A-15氯甲基化程度不再增加,也有可能是在24 h时氯元素的吸附能力达到最大,继续增加氯甲基已不能提高纤维素的水解能力,此时葡萄糖的得率取决于A-15-Cl上磺酸根的量[10]。所以,氯甲基化反应时间选择24 h。

图4 反应时间对葡萄糖得率的影响
2.2 A-15-Cl水解微晶纤维素的再现性实验及与A-15的比较
为了验证优化工艺条件下制备A-15-Cl水解微晶纤维素的再现性,在获得的最佳工艺(CH2ClCH2Cl 20 mL,(CHO)n0.50 g,SnCl40.75 mL,55 ℃,24 h)条件下制备改性A-15-Cl,在150 ℃条件下水解微晶纤维素12 h,与未改性A-15的水解微晶纤维素葡萄得率进行比较,结果显示在优化条件下制备的改性A-15-Cl水解微晶纤维(170 ℃,12 h,固体酸0.05 g,球磨纤维素0.1 g,H2O 5 mL)葡萄糖得率为62.37%,且具有很好的再现性。而未改性A-15水解微晶纤维葡萄糖得率仅为16.19%,改性后的固体酸水解效率相比改性前提高了3.85倍。
2.3 A-15-Cl提高微晶纤维素水解效率的机理
2.3.1 红外光谱分析
由图5A-15 FT-TR谱图可知,3 412.26 cm-1出现羟基伸缩振动特征峰,这属于磺酸根(—SO3H) 以及样品中存在水分子中的O—H,在1 161.00和1 034.07 cm-1归属于—SO3H中S—O的对称和不对称伸缩振动[11]。证明A-15存在—SO3H的特征吸收峰。图5中改性的A-15-Cl 相比A-15的最大区别是,在1 372.54和914.42 cm-1两处出现氯甲基(—CH2Cl)伸缩振动特征吸收峰,证明了改性A-15-Cl中氯甲基的成功引入。但是也有文献[10,12]指出—CH2Cl的特征吸收峰在1 265和678 cm-1,这是因为A-15本身含有的苯环会与—CH2Cl上的H形成σ-π超共轭,且苯环上连有强吸电子基团—SO3H,所以—CH2Cl周围电子云密度减小,使得—CH2Cl特征吸收峰发生蓝移[13]。根据A-15改性前后的FT-TR谱图分析,可以充分说明A-15-Cl的苯环被引入—CH2Cl。而已有文献表明氯甲基可作为纤维素水解过程的结合结构域,提高与纤维素表面的氢键结合和可及度[14],固体酸上的催化基团(—SO3H)破坏纤维素单体的连接键,像纤维素酶水解过程一样改善了纤维素的水解效率,成功实现了仿纤维素酶水解过程的设计。
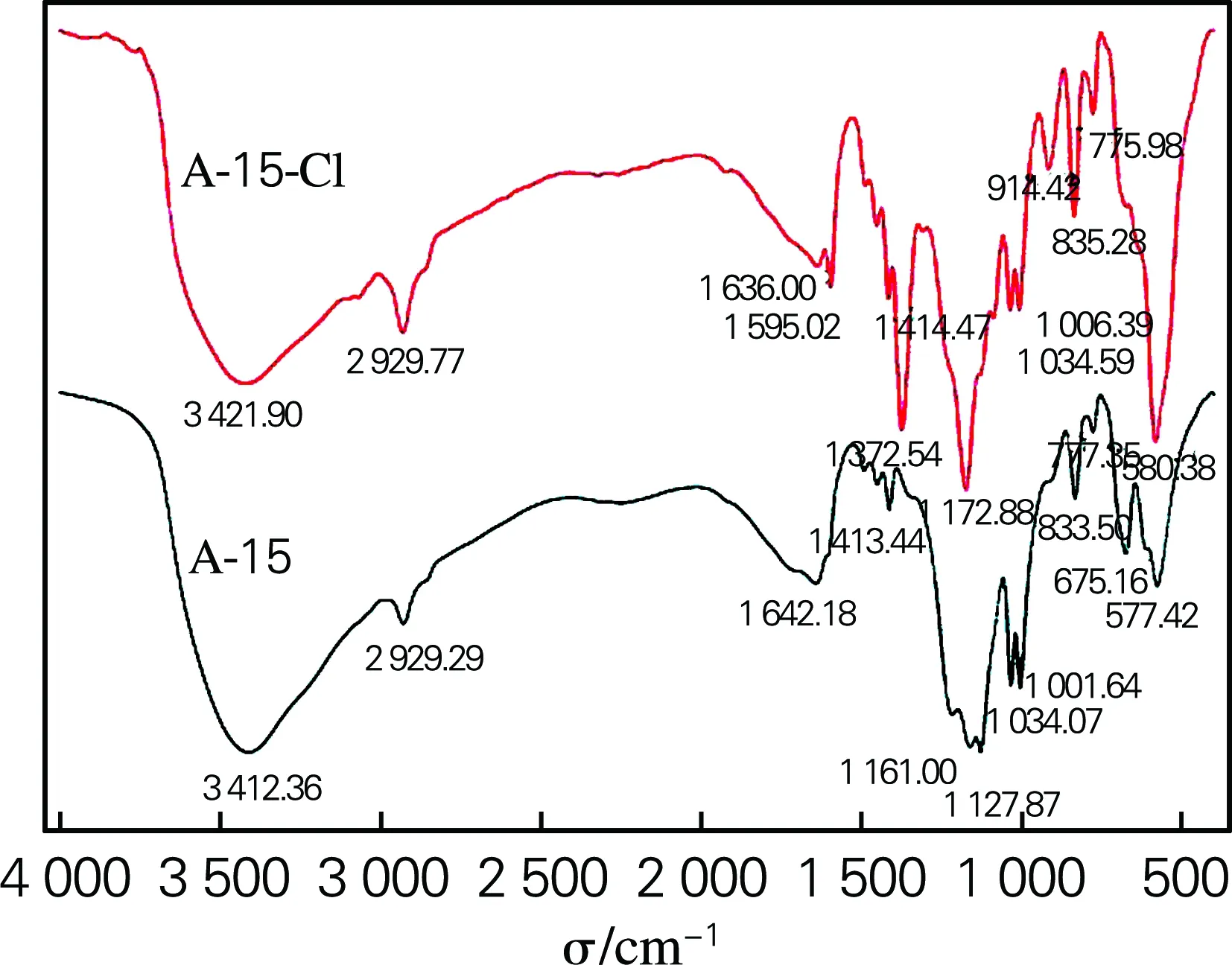
图5 A-15和A-15-Cl的FT-TR谱图
2.3.2 热稳定性分析
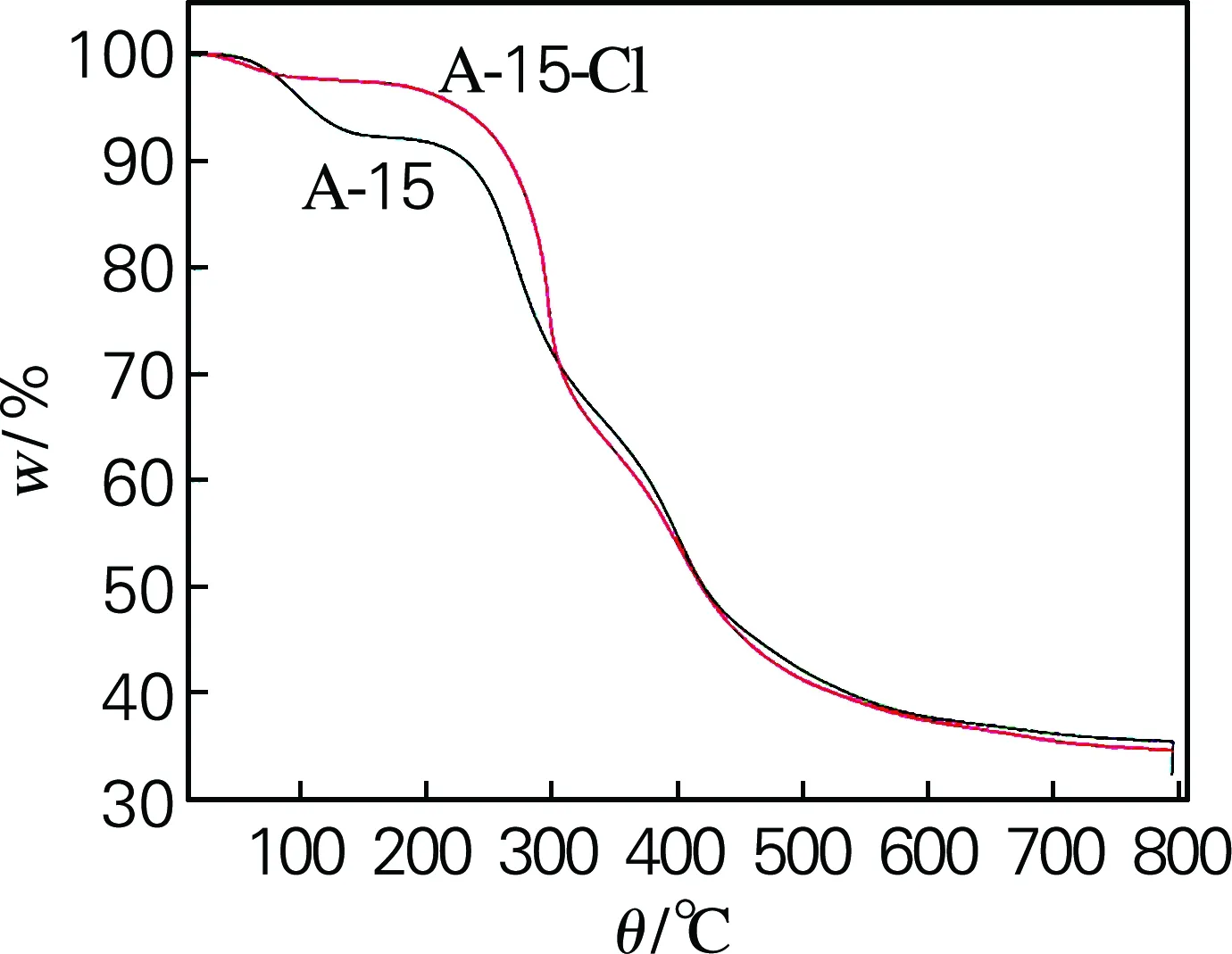
由图6中固体酸的TG曲线和DTG曲线可知,样品的质量损失主要分3个阶段。在第1阶段(低于200 ℃),质量损失主要来源于样品中结合水和自由水的蒸发[15]。在第2阶段(200~350 ℃),主要是聚苯乙烯链的解聚[16]、—SO3H以及—CH2Cl 的分解[14]。在第3阶段(400 ℃以上),质量损失主要来自聚合物主链断裂成小分子,二乙烯基苯发生降解[16]。图6(a)图像表明,A-15-Cl总质量损失65.4%略高于A-15总质量损失64.57%,这主要是因为A-15-Cl相对于A-15 增加了氯甲基。但在其他降解温度和变化趋势方面基本没有变化,说明A-15的氯甲基化没有改变其热稳定性。
2.3.3 扫描电镜图像
由图7(b)可以看出,A-15是由颗粒聚集而成的球状树脂,颗粒之间的缝隙形成了A-15的孔道。对比图7(a)和(c)发现,A-15-Cl相对于A-15表面更加松散、孔数增加。观察图7(b)和(d)明显发现A-15-Cl相对于A-15内部颗粒体积减小,颗粒间空隙数量增加。A-15-Cl孔数增多的原因可能是氯甲基化反应中加入的氯磺酸具有腐蚀性,使其组成颗粒体积减小,进而增加了固体酸的孔隙数量,增大了反应物的比表面积。这也很好解释了改性A-15-Cl改善微晶纤维素葡萄糖水解效率的原因。
(a) TG
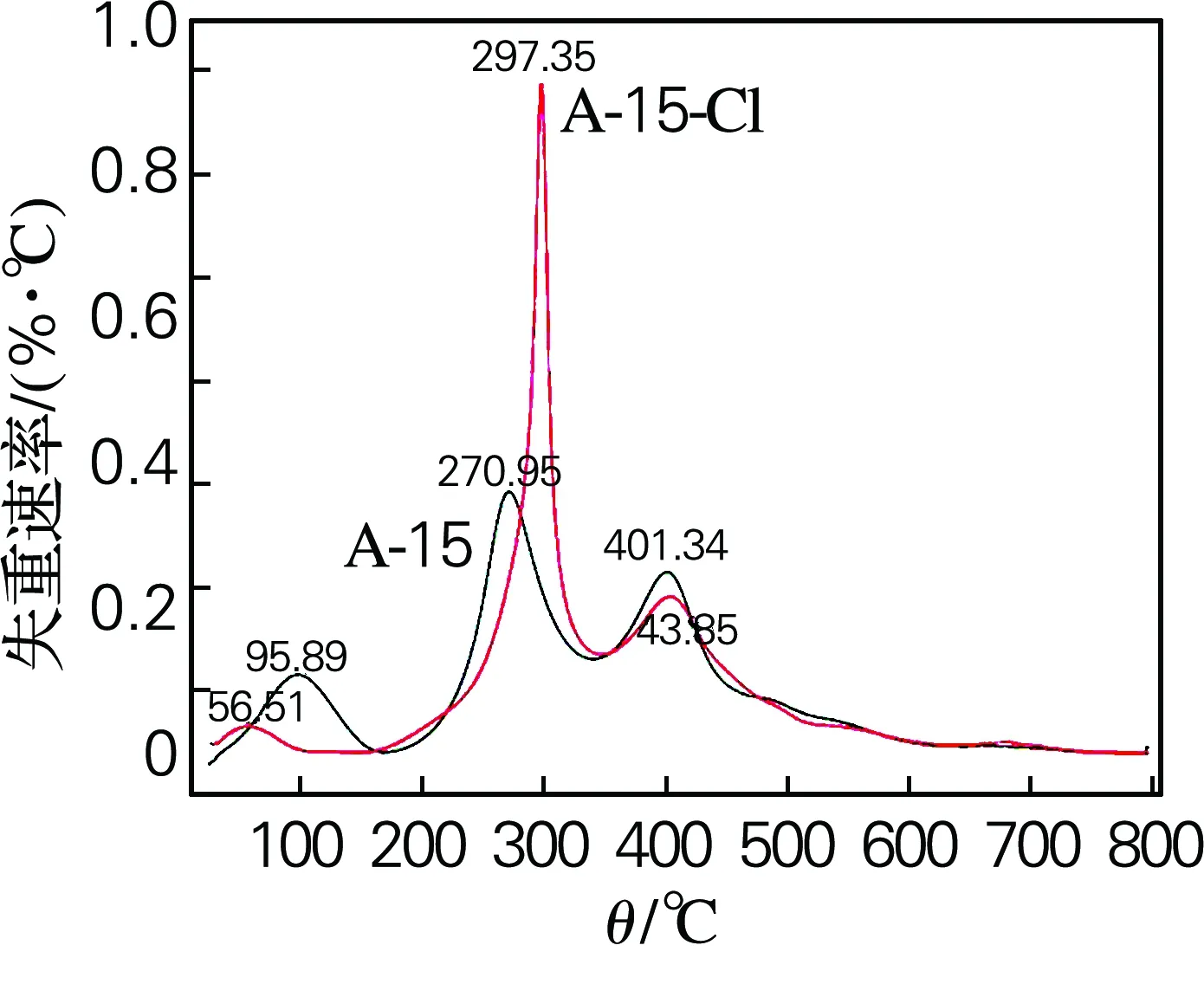
(b) DTG
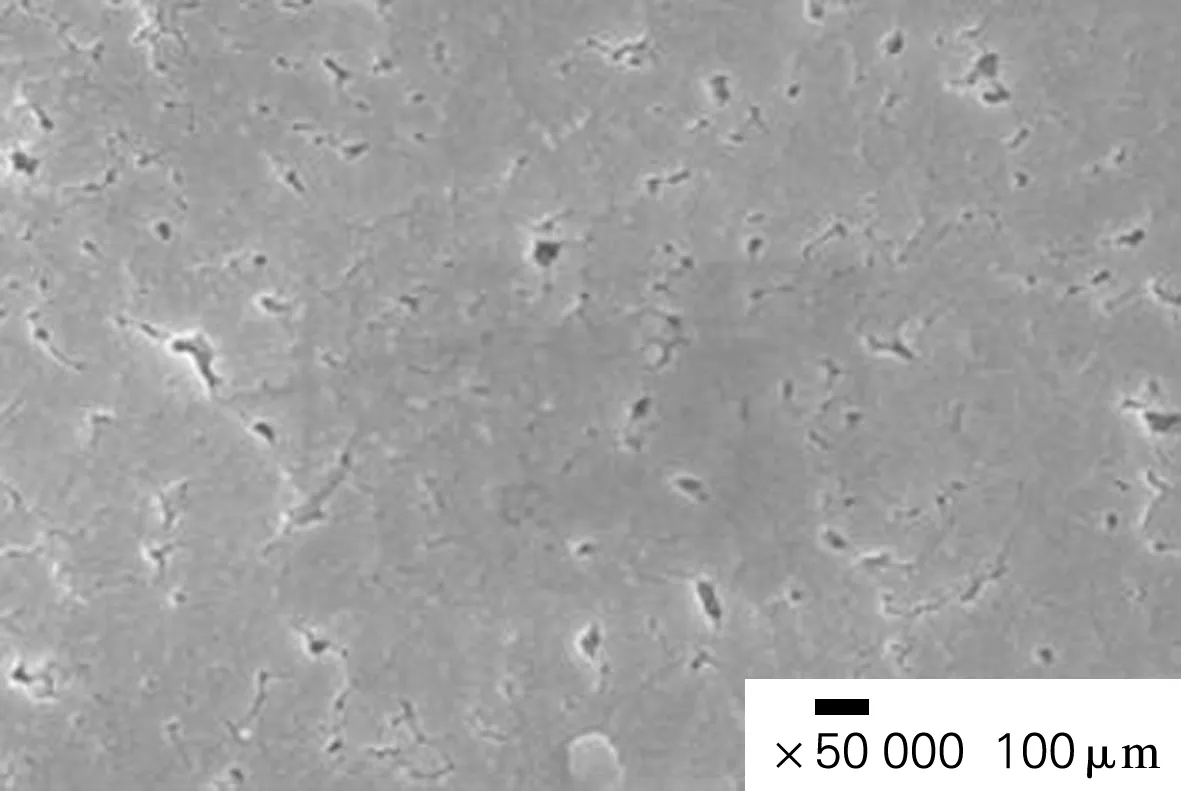
(a) A-15表面图

(c) A-15-Cl表面图
2.3.4 BET及EDS元素分析
从表1中EDS检测A-15和A-15-Cl表面S和Cl含量的数据结果可以看出,改性前后表面的磺酸含量变化不大,但成功引入对纤维素具有亲和性的氯基,与前期红外光谱分析结果是一致的。另外从BET检测的数据可以看出,A-15-Cl相较于A-15平均孔径减小4.52 nm。主要是因为氯磺酸具有腐蚀性,使A-15-Cl的组成颗粒减小,随之大孔缝隙数减少,所以平均孔径减小。由表1可得A-15-Cl的比表面积为65.60 m2/g,相比A-15 比表面积46.36 m2/g提高了41.51%,而且总孔隙体积也略有增加。这是因为A-15-Cl的组成颗粒体积减小,颗粒之间孔隙数量增多,比表面积增加,该结果与电镜分析的结果一致。A-15-Cl水解球磨微晶纤维素的得率增加也得益于其介孔增加,使寡糖进入孔道进而增加有效面积,该理论在多篇文献中都得到证实[7,17]。
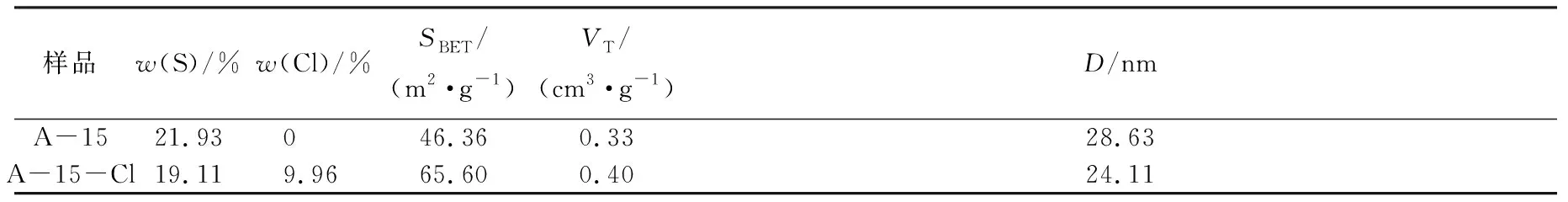
表1 A-15和A-15-Cl的BET及EDS数据
由图8可见,A-15和A-15-Cl的N2吸附-脱附等温线基本一致,符合Ⅱ型等温线且出现H1型滞后环。Ⅱ型等温线说明样品存在分布均匀的两端开口的管径圆筒孔状,H1型滞后环说明样品中存在分布均匀的介孔和大孔[17]。由两图孔径分布图可知,A-15-Cl在孔径为5.5 nm处比A-15 多出现一个峰,表明A-15-Cl相对于A-15孔径的增多。该结果与SEM图像一致,进一步证实氯甲基化反应提高了固体酸介孔含量。
3 结 论
以无水SnCl4为催化剂,(CHO)n/ClSO2OH为氯甲基化试剂,对工业化固体酸A-15进行改性,得到最有利于微晶纤维素水解的氯甲基化条件:CH2ClCH2Cl 20 mL,(CHO)n0.50 g,无水SnCl40.75 mL,ClSO2OH 20 mL,温度55 ℃,时间24 h。此条件下制得A-15-Cl在150 ℃下水解纤维素12 h葡萄糖得率达到62.37%。FT-IR、TGA、BET的表征结果说明,通过A-15氯甲基化反应,成功地实现了仿酶固体酸亲纤维素的结合结构域的引入,极大地改善了固体酸与纤维素的传质障碍,提高了纤维素的水解效率,为将来工业固体酸在纤维素水解上的应用提供了新的设计思路。
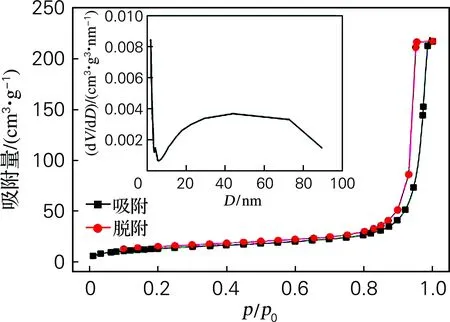
(a) A-15
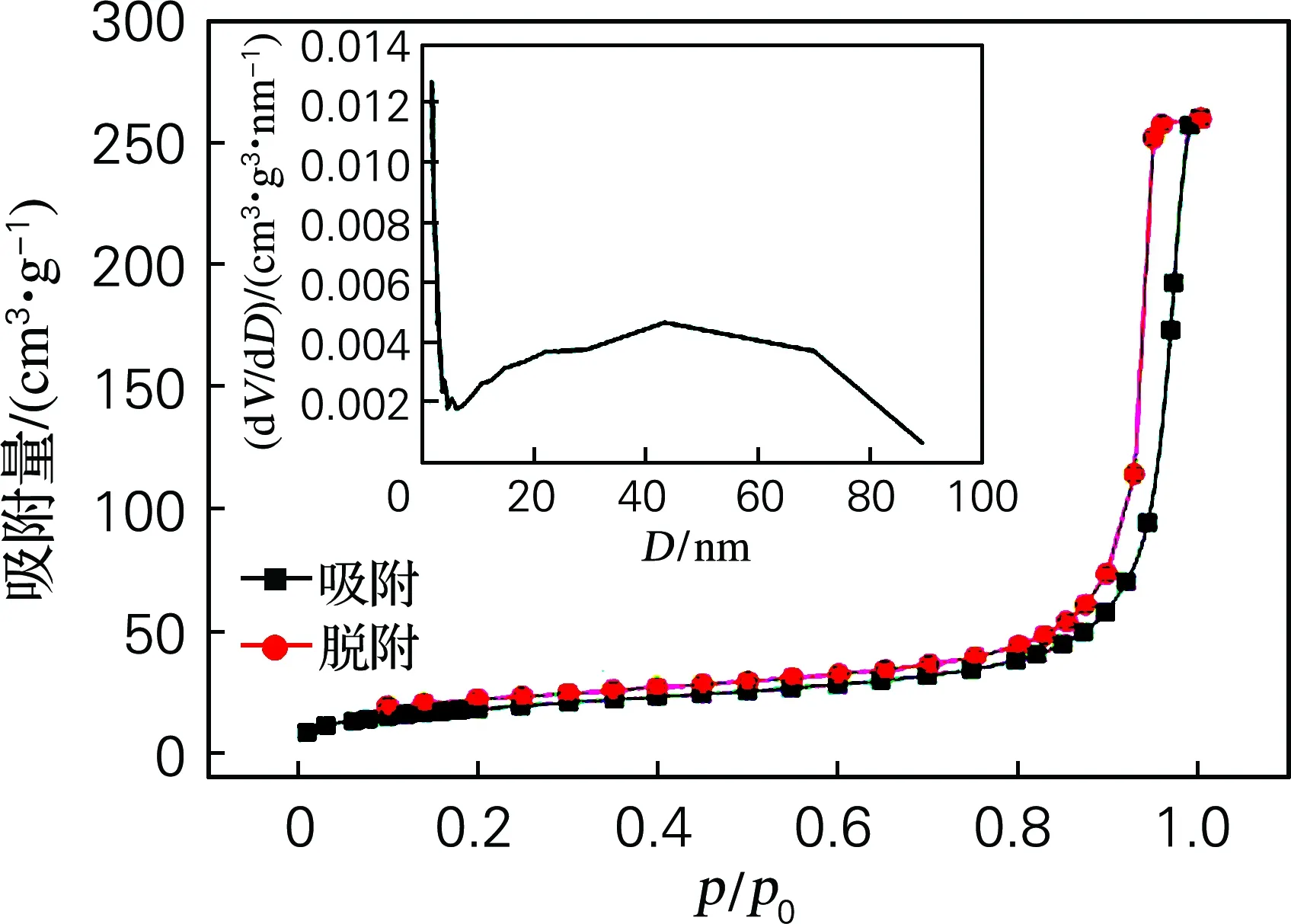
(b) A-15-Cl
