电位滴定法连续测定双氰胺钠及杂质氯化钠含量
2018-09-20孙巍
孙 巍
(本溪市化学工业学校,辽宁 本溪 117004)
双氰胺钠(NaN(CN)2)是一种重要的精细化工原料,广泛应用于制药、树脂、染料和照相等行业[1],双氰胺钠还是制备除草剂苯磺隆,磺胺类杀虫剂的中间体[2],可与多种金属形成新型的配合物[3-4]。双氰胺钠在合成过程中,会有副产品氯化钠(NaCl)产生,为了检测其质量及杂质的含量,本文采用AgNO3为滴定剂,银电极为指示电极,双盐桥饱和甘汞电极为参比电极,电位滴定法连续测定双氰胺钠及其杂质氯化钠的含量。该方法具有选择性好,灵敏度高,仪器设备简单,操作方便等特点。
1 实验部分
1.1 仪器和试剂
仪器:pHS-3C 型酸度计(上海精密科学仪器有限公司);216型银电极(上海电光器件厂);217型双盐桥饱和甘汞电极(上海电光器件厂),内管溶液用氯化钾饱和溶液(3 mol/L),外套管溶液用硝酸钾溶液(1 mol/L);E-201-C型pH复合电极 (上海电光器件厂);79-2 磁力加热搅拌器带有外包聚四氟乙烯套的搅棒(常州国华电器有限公司);GR-202十万分之一分析天平(日本AND)。
试剂:硝酸银(A.R.,中国医药集团上海试剂公司);硝酸钾(G.R.,天津市科密欧化学试剂开发中心);氯化钾(G.R.,国药集团化学试剂有限公司);氯化钠(A.R.,北京化工厂);双氰胺钠(连云港裕立化工有限公司);37%甲醛溶液(A.R.,沈阳市荣兴化工厂);异丙醇(A.R.,北京化工厂);甲醇(A.R.,北京化工厂)。
1.2 实验原理
由于AgN(CN)2和AgCl的溶解度有差异,因此可用AgNO3溶液分别滴定混合物中的NaN(CN)2和NaCl。当混合液中加入AgNO3溶液时,首先生成溶解度小的AgCl沉淀:
Ag++Cl-=AgCl↓(白色)
继续加入AgNO3溶液,则生成 AgN(CN)2沉淀:
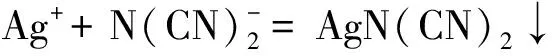
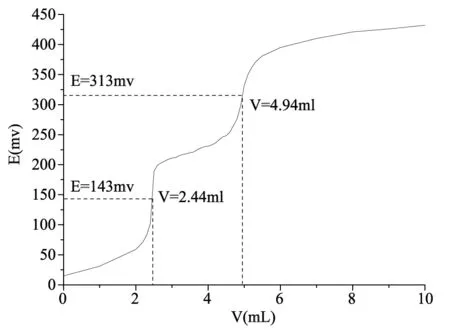
图1 0.1000 mol/L AgNO3连续滴定0.02500 mol/L
用AgNO3连续滴定NaCl 和NaN(CN)2的电位滴定曲线如图1所示,有两个电位突跃。根据二阶微商法确定滴定终点体积和终点电位值,进而确定含量。
1.3 实验方法
1.3.1 溶液的配制
0.1000 mol/L AgNO3标准溶液:准确称取8.4935g AgNO3转移到500 mL棕色容量瓶,定容,摇匀,避光保存。
0.05000 mol/L NaCl溶液:准确称取0.2925g NaCl,转移到100 mL容量瓶,用水定容,摇匀。
0.05000 mol/L NaN(CN)2溶液:准确称取双氰胺钠标样0.4452 g,转移到100 mL容量瓶,用水定容,摇匀。
未知样溶液:准确称取一定质量的未知样转移到100 mL容量瓶,用水定容,摇匀,得到一定浓度未知样溶液。0.1 mol/L NaOH溶液,6.0 mol/L HNO3溶液。实验用水为二次去离子水。
1.3.2 实验步骤
用双盐桥饱和甘汞电极作参比电极,银电极作指示电极,以0.1000 mol/L AgNO3溶液连续滴定0.02500 mol/L NaN(CN)2和NaCl的混合标准溶液或者未知样溶液10 mL,于250 mL烧杯中,将烧杯置于冰浴中直到温度降至5℃以下,加入10 mL HCHO(先用0.1 mol/L NaOH中和至pH 值7.0)冷却10 min,再加80 mL异丙醇,冷却至5℃以下,加入体积比为1∶2的浓HNO3溶液1 mL,用0.1000 mol/L AgNO3溶液滴定,记录实验数据,然后用Origin软件绘制滴定曲线,采用二价微商法确定滴定终点,分别计算NaN(CN)2和NaCl的含量。
2 结果与讨论
2.1 溶剂的选择
实验考察了甲醛、甲醇和异丙醇溶剂的种类及配比的影响,并考察了酸度的影响。
2.2.1 甲醛
由于市售的HCHO中含有少量的甲酸,实验考察了中和(用0.1 mol/L NaOH溶液中和至pH值=7.0)和未中和的甲醛,按实验方法对0.02500 mol/L 的NaCl和NaN(CN)2混合标准溶液连续电位滴定,实验结果表明,使用中和的甲醛作溶剂时,分析结果误差较小,所以实验选用中和的甲醛作溶剂。
2.2.2 醇的种类
取甲醇,异丙醇各80 mL,按实验方法连续测定0.02500 mol/L NaCl和NaN(CN)2混合标准溶液,实验结果表明,使用异丙醇作溶剂时,分析结果误差较小,所以实验选用异丙醇作溶剂。
2.2.3 甲醛和异丙醇用量的影响
按实验方法,考察了甲醛和异丙醇的用量对0.02500 mol/L NaCl和NaN(CN)2混合标准溶液连续电位滴定的影响。实验结果表明,当甲醛用量为10 mL,异丙醇用量为80 mL时,分析结果误差最小,所以实验选择溶剂甲醛和异丙醇的用量分别为10 mL和80 mL。实验结果也表明,异丙醇的用量较大(≥70 mL)时有助于测量,这是由于介电常数较小的有机物质的加入可以降低测量误差。
2.2.4 HNO3的影响
为了考察实验是否需要酸性环境,在加硝酸和无硝酸的情况下,按实验方法对0.02500 mol/L 的NaCl和NaN(CN)2混合标准溶液连续电位滴定,实验结果表明,在酸性条件下有利于NaCl和NaN(CN)2的测定,误差较小。这是因为硝酸的加入,可以防止滴定剂AgNO3水解生成AgOH沉淀,所以实验选择加入体积比为1∶2的HNO3溶液1 mL。
2.2.5 温度的影响
实验考察了室温和冰浴的影响,按实验方法对0.02500 mol/L 的NaCl和NaN(CN)2混合标准溶液连续电位滴定,实验结果表明,冰浴可以明显降低测量误差,所以实验选择冰浴条件下测定未知样。
2.3 空白实验
准确吸取10 mL二次去离子水,按实验方法进行空白实验,实验消耗硝酸银体积不超过0.1 mL,故空白可以忽略。
2.4 样品分析
对标样和未知样,按实验方法平行测定3次,实验结果见表1。可见,该方法准确,可用于未知样中双氰胺钠及杂质氯化钠含量的测定。

表1样品分析(n=3)
3 结论
利用Ag+与N(CN)2-和Cl-能生成沉淀的性质,在连续电位滴定过程中会出现两个电位突跃,从而实现分别滴定。用二阶微商法确定滴定终点时消耗滴定剂的体积,进而计算出未知样中双氰胺钠及杂质氯化钠的含量。该方法具有简单、快速、方便、准确等特点。
