肺动脉内膜剥脱术体外循环管理经验
2018-09-20闫姝洁朱家德李景文吉冰洋宋云虎
楼 松,闫姝洁,朱家德,王 惠,李景文,华 潞,刘 刚,吉冰洋,宋云虎,刘 盛
慢性血栓栓塞性肺动脉高压(chronic thrombo⁃embolic pulmonary hypertension,CTEPH)是肺动脉高压的重要病因之一,为世界卫生组织肺动脉高压分型IV型。CTEPH继发于急性/慢性肺动脉栓塞,文献报道0.57%~3.8%的急性肺栓塞患者可发展为CTEPH,未完全溶解的血栓阻塞肺动脉并伴肺动脉内膜增厚、肺血管重构,导致肺动脉高压,如不干预,最终引起右心衰竭和呼吸衰竭,患者预后差[1-2]。尽管肺动脉内膜剥脱术(pulmonary endarterectomy,PEA)操作复杂,体外循环(cardiopulmonary bypass,CPB)围术期管理难度大,院内死亡率高,依然是治疗CTEPH的首选治疗。PEA清除血栓并剥离双肺增厚的肺动脉内膜,手术成功的关键在于术野的充分暴露、正确建立剥离层面并剥离至亚段以上。这有赖于CPB深低温停循环(deep hypothermic circu⁃latory arrest, DHCA)技术保障无血术野[3-4]。 本研究回顾性分析阜外医院近两年完成的58例PEA手术病例,并总结CPB管理经验。
1 资料与方法
1.1 研究对象与诊治流程 本研究为回顾性研究,纳入2015年11月至2017年12月阜外医院心外科连续完成的58例因CTEPH行PEA手术的患者。所有患者的诊治均按照CTEPH常规流程,由包括内外科医生在内的多学科团队完成。术前均经肺动脉造影、肺通气/灌注扫描检查、肺动脉增强计算机断层摄影(CT)明确诊断CTEPH;行右心导管、超声心动图、动脉血气、6 min步行实验、CT检查评价病情严重程度;行抗磷脂抗体、蛋白S/蛋白C活性、四肢深静脉超声检查评估CTEPH相关病因。所有患者的手术由两名外科主刀医生完成,所有手术均于全麻低温CPB下完成。为保证术野清晰,所有患者均采用DHCA。术中采用单腔或双腔气管插管,监测有创桡动脉血压、中心静脉压和肺动脉压,监测鼻咽温、膀胱温,手术详细操作步骤见本中心既往报道[5],并根据术中所见进行手术分级[6]。 术后早期于术后恢复室继续监测肺动脉压力及肺血管阻力,针对心功能、肺动脉压力给予相应强心、利尿、降肺动脉压力治疗。
1.2 CPB方法 CPB由Stockert S5型人工心肺机完成(STOCKERT S5,StockertInstrumental GmbH,德国)。CPB管路包括离心泵头(Revolution,SORIN,意大利)、膜式氧合器(MAQUET Cardiopulmonary AG7800,德国)、动脉微栓滤器(宁波费拉尔医疗用品有限公司,中国)、超滤器(SORIN,意大利)及非涂层PVC管路(天津塑料研究所,中国)。
预充液常规采用复方电解质注射液1 000 ml(石家庄四药有限公司,中国),20%白蛋白300 ml(百特,奥地利),并在CPB前进行白蛋白预处理,即将含白蛋白预充液以4 L/min流量自循环5 min。
采用胸骨正中切口,全血激活凝血时间(activa⁃ted clotting time,ACT)>410 s后(ACT 检测仪:HE⁃MOCHRON Jr.Signature, 美国),采用升主动脉、上下腔静脉常规插管建立CPB,采用离心泵转流。通过膜式氧合器血流降温及头部冰帽联合降温,降温过程中经右上肺静脉插入左心引流管,游离上腔静脉并显露右肺动脉前壁。于鼻咽温22~25℃阻断升主动脉,经主动脉根部灌注晶体停搏液(HTK液,科勒化学制药,德国)或施尔生液(Institut Georges Lop⁃ez,法国)2 000 ml。于升主动脉与上腔静脉之间切开右肺动脉,清除血栓,在血栓起始部建立剥离层。当鼻咽温至18~20℃时开始停循环,于停循环下剥离肺动脉内膜至亚段。每次停循环时间≤20 min,两段DHCA之间恢复全流量时间≥10 min。先处理右肺动脉再处理左肺动脉。内膜剥离完成后复温,期间于肺动脉置软的右心插管持续吸引,随后开放升主动脉。缓慢复温至鼻咽温35℃时撤除冰帽。复温至鼻咽温36.5℃,膀胱温35.5℃且血流动力学满意时调整停机,CPB结束时予以正性肌力药(多巴胺、多巴酚丁胺),必要时可给与去甲肾上腺素维持外周阻力。停机后鱼精蛋白中和,剩余机血回输。
转中采用α稳态血气管理策略,维持转中桡动脉平均压 50~90 mm Hg,维持ACT>410 s,维持复温和降温过程中水箱与膀胱温差值<10℃,鼻咽温与膀胱温差值<5℃,复温期间鼻咽温≤37.0℃。在降温时通过放血并补充等量的平衡电解质溶液进行血液稀释,停循环前使红细胞比容(hematocrit,HCT)<0.25,在复温时通过常规超滤或输注红细胞使停机前 HCT>0.28。
转中应用神经保护药物,术中维持静脉输注丙泊酚 3~10 mg/(kg·h);糖皮质激素甲泼尼龙分两次于麻醉诱导期间与复温时给药,总量为15~30 mg/kg;20%甘露醇 0.5 g/kg 于膀胱温复温至 28℃时加入回流室。
1.3 资料收集 本研究为回顾性研究,通过查询电子病历回顾性提取术前、术中、术后资料。术前资料包括:患者年龄、性别、身高、体重、体表面积、病程、纽约心功能分级(NYHA)、6 min步行试验、右心导管检查所测肺动脉压力(pulmonary artery pressure,PAP)及肺血管阻力(pulmonary vessel resistance,PVR);术前超声心动图射血分数(ejection fraction,EF)值、脑钠肽前体(NT-ProBNP);下肢深静脉血栓病史,术前蛋白C/蛋白S水平、活化部分凝血活酶时间(activated partial thromboplastin time,APTT);术前肌酐(creatinine,Cr)及 HCT。 术中资料包括:手术分型、转机时间、阻断时间、心脏停搏液类型;术中最低温度、最大鼻咽温和膀胱温差、升主动脉阻断和开放时温度、复温时间;DHCA总次数、总时长、单次DHCA时间;转中输血量、超滤量、尿量;停机后Swan-Gans导管测肺动脉压力,转后动脉血气。术后资料包括:术后机械通气时间、ICU时间、住院时间、末次PAP以及患者预后资料(包括死亡、肺动脉出血、残余肺高压、灌注肺发生率等)。
1.4 统计方法 采用 STATA 12.0进行统计学分析。符合正态分布的计量资料以均数±标准差(±s)表示,两组间比较采用配对t检验;不符合正态分布的计量资料以中位数和四分位间距表示,两组间比较采用Wilcoxon秩和检验;计数资料以频数表示,两组间比较采用Fisher精确检验。P<0.05认为有统计学意义。
2 结 果
2.1 术前资料 58例手术患者术前资料见表1。
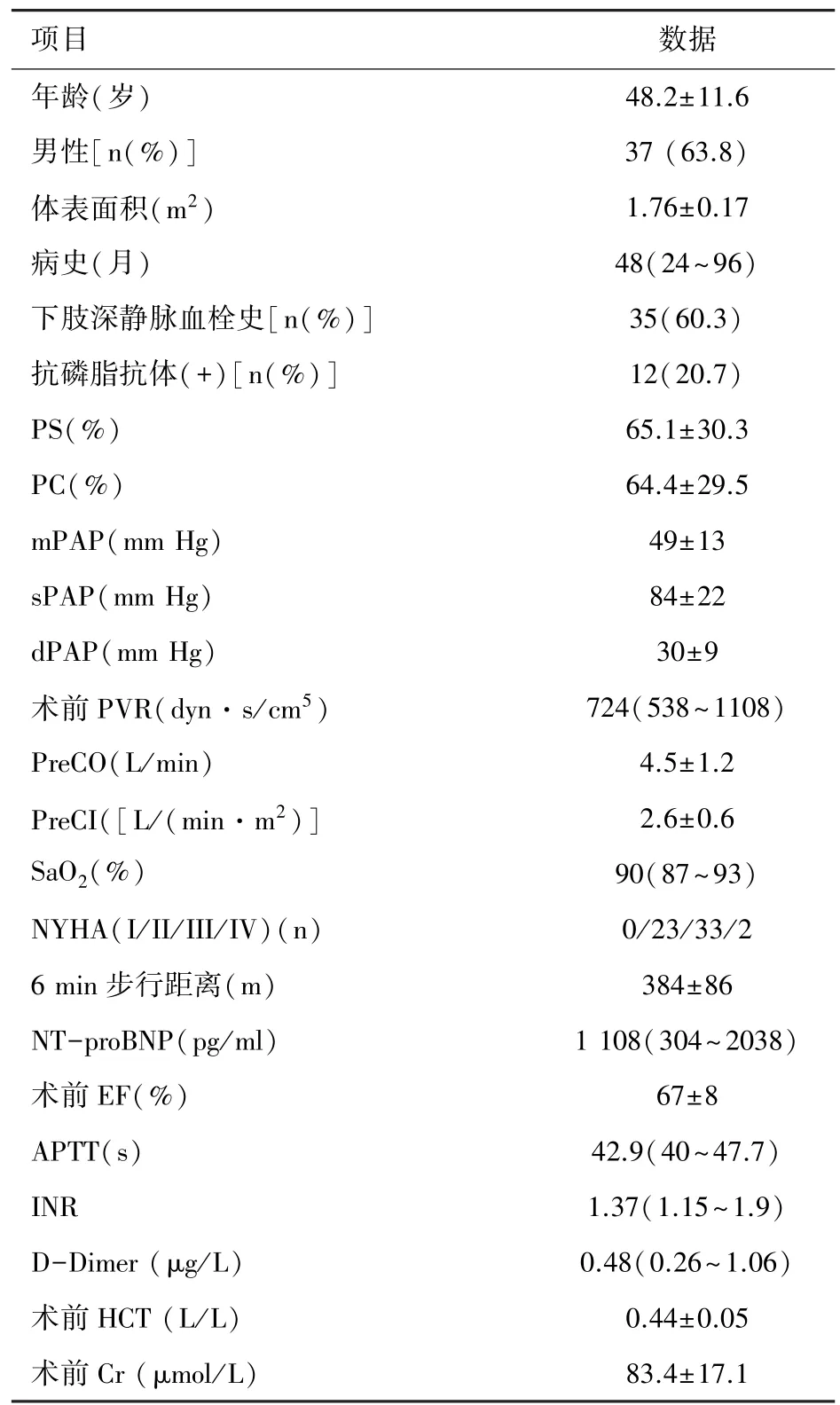
表1 患者术前资料(n=58)
2.2 术中资料 58例CTEPH患者中,JamiesonⅠ型18例(31.0%),Ⅱ型 30 例(51.7%),Ⅲ型 10 例(17.3%)。所有患者均采用离心泵转流,患者术中资料见表2。
58例患者中,6例患者经历1次停循环,30例患者经历2次停循环,21例患者经历3次停循环。另1例患者因停机时出现大量肺动脉出血再次主动脉阻断于DHCA下行肺动脉外膜修补术,共经历6次停循环。大多数患者术前血红蛋白偏高,术中采取放血和血液稀释策略。11例患者于转中输浓缩红细胞2~6 U。

表2 患者术中资料(n=58)
CPB停机时,肺动脉收缩压(pulmonary arterial systolic pressure,sPAP),肺动脉舒张压(pulmonary artery dystolic pressure,dPAP), 肺动脉平均压(mean pulmonary arterial pressure,mPAP)均明显低于术前肺动脉压力(表3)。
2.3 术后资料 患者术后资料见表4。术后大多数患者顺利出院且无手术相关并发症,出院前PAP与术后相比进一步降低(表3)。少数患者出现并发症,两例术后应用ECMO的患者,第一例因术后出现肺动脉高压危象及再灌注肺损伤应用VA-EC⁃MO,辅助8日后肺动脉压力降低且再灌注肺损伤减轻,随后顺利撤机。第二例因术后肺出血应用VA-ECMO,辅助3日后肺出血明显缓解,顺利撤机。这两例患者均存活出院。
患者出院前Cr与术前相比无统计学差异,对患者肾功能未见影响。
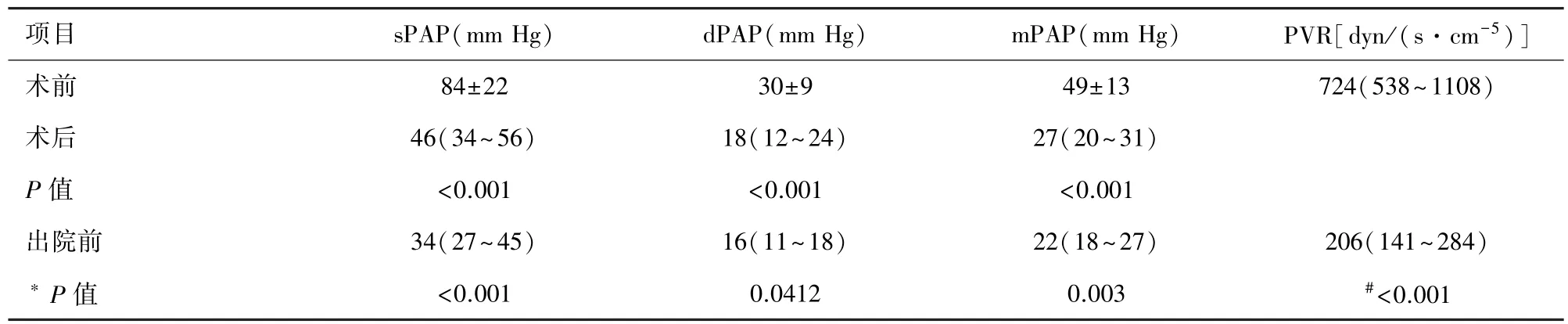
表3 患者PAP及PVR变化(n=58)

表4 患者术后资料(n=58)
3 讨 论
本院是国内最早开展也是最大的PEA中心,从1997年开展PEA术,目前年手术量约30例,PEA在CPB管理方面积累了一些经验。PEA术后患者康复过程,除了与患者本身病理生理改变及病因清除是否彻底有关,长时间CPB及DHCA也对脑、肾等重要脏器产生巨大影响。合适的CPB管理策略对于改善预后至关重要。
本回顾性队列中PEA手术患者在院死亡率为1.7%,且围术期其它并发症发生率也较低,国外大型PEA中心死亡率一般为20%左右[7]。需要特别注意的是,目前PEA在国内尚属于起步阶段。本院仅在近2年才达到年手术量30例左右。在学习曲线的早期,对患者的选择较为谨慎,多为I或Ⅱ型,病变容易清除的病例。随着经验的增长,术者可能会越来越多地挑战Ⅲ型病变。死亡率及术后并发症必然有所增加,优化CPB管理显得更加重要。
灌注策略选择方面,包括圣地亚哥中心在内的多家国际PEA中心均选择DHCA,部分中心选择低温停循环+顺行性脑灌注(antegrade cerebral perfu⁃sion,ACP)。 一项随机对照实验(randomized con⁃trolled trial,RCT)研究结果显示[8],采用 ACP 并不减少术后神经系统并发症和认知功能损伤的发生率。还有少数中心选择低流量策略。笔者认为手术成功关键在于无血术野下建立正确剥离层面,低流量往往无法满足精细的手术需求,反而延长低流量时间。因此笔者坚持采用DHCA,条件允许时停循环期间行近红外光双侧前额部脑氧饱和度监测,脑氧饱和度绝对值<50%,相对值下降>20%可考虑恢复流量[9]。
在血泵选择上,考虑CPB转流时间长,笔者选择对血液破坏更小的离心泵,58例患者中很少出现酱油色血尿。此外,Mlejnsky F等[10]的一项RCT研究发现,离心泵用于PEA手术炎性因子反应激活水平也低于滚压泵。CTEPH患者由于长期慢性缺氧,血红蛋白代偿性增多、血容量多。降温过程中采取放血和血液稀释的策略,有利于减少血液破坏和降低血液黏滞性,促进微循环及组织灌注。笔者认为对于 DHCA 患者,HCT 0.20~0.25是安全的。而在复温阶段,采用血液浓缩策略以期停机时HCT 0.28~0.30,以避免停机后因缺氧导致肺血管收缩痉挛;血液浓缩可减轻患者液体负荷,对减少肺渗出有利。对于CPB剩余机血,停机后继续超滤浓缩,目的也是减轻围术期液体负荷。
预充液方面,最近的一项PEA灌注调查研究虽未得到一致性意见,但是大多数中心倾向于更多地选择胶体液作为预充[11]。再灌注肺损伤是PEA术的重要并发症之一,其发生机制为肺动脉梗阻解除后,肺血流恢复后发生的反应性肺充血。提高胶体渗透压对减轻术后再灌注肺损伤、肺水肿有利。由于白蛋白对于人工胶体的天然优势,本中心选择白蛋白预充。CPB前白蛋白管路预处理可在管路表面形成致密蛋白层,作为保护层可能可以减轻CPB开始后血浆蛋白与管路表面的相互作用,减轻凝血激活与炎症反应,尤其适用于转流时间长的DHCA手术。此前本中心的一项RCT研究显示,白蛋白对管路预处理可显著减少血小板下降的程度,具有血液保护效果[12]。
本中心采用甲泼尼龙、丙泊酚和甘露醇作为脑保护药物。甲泼尼龙与其它糖皮质激素相比,起效快、穿透血脑屏障时间短且对下丘脑-垂体-肾上腺皮质轴影响小。30 mg/kg甲泼尼龙在DHCA手术中的神经保护效果来自动物实验[13],而肺保护效果不明[14]。近期的甲泼尼龙用于常规CPB心脏手术的多中心RCT研究[15]未显示其优越性,其在DHCA手术中的临床价值还有待进一步研究。
本研究存在一些不足。①本研究为回顾性研究,患者资料来自病历资料,存在偏倚。②未来可增加纳入患者例数,进一步分析CPB管理中的具体细节(如DHCA次数、DHCA总时间,糖皮质激素使用剂量等)是否与患者预后有关。
4 结 论
CPB是PEA围术期管理中的重要一环,DHCA是手术成功的关键,CPB期间采取合适的血液保护、脑保护、肺保护策略有助于减轻术后并发症,改善患者预后。
