交联氨基淀粉吸附水中镉离子的影响因素研究
2018-09-14董爱琴
董爱琴,刘 倩,谢 杰
(1.江西农业大学 理学院,江西 南昌 330045;2.江西省农业科学院 土壤肥料与资源环境研究所,江西 南昌 330200; 3.华南农业大学 资源环境学院,广东 广州 510642)
近年来,伴随着工业经济的迅速发展,水体污染,尤其是重金属污染已经成为全球性的环境问题。而其中最引人关注的是Cd、Hg、Cr(Ⅵ)等重金属元素,在这些重金属污染物中,Cd因可以引发胸闷﹑呼吸衰竭、骨痛甚至肾功能衰减等症状,且极易在人体内蓄积,对人类的健康造成严重危害[1],而获得广泛的关注。
为了治理此类废水,人们研究了多种处理方法[2],包括植物修复技术[3],生物去除技术[4],吸附法[5],膜分离法[6]等物理处理技术以及化学沉淀法[7]、铁氧化沉淀法[8]、离子交换法[9]等化学处理技术。然而,各种方法的优缺点都很明显,相比之下,吸附法具有吸附效率高、吸附产物易处理等优点,因此在重金属废水处理中应用较为广泛[10]。然而,吸附剂的种类又有很多种,选择高效廉价的吸附剂是吸附法中最重要的一点[11-12]。有机合成高分子吸附剂的应用比较广泛,具有能吸附多种重金属离子、吸附容量大等优点,但存在单体毒性大、使用寿命短、再生费用高及难降解等缺点[13]。而改性天然高分子材料吸附剂是目前国内外研究的热点,具有原料来源广、成本低、毒性小等优点,且制备过程充分利用了天然材料所富含的官能团,降低了合成工艺难度,最终产品也易于被自然降解[14]。改性天然高分子材料吸附剂中又以天然的多糖及其衍生物为研发重点,如淀粉、壳聚糖、改性纤维素等[15]。在这些天然高分子材料中,淀粉作为一种来源广泛的天然可再生资源,具有可生物降解和活性官能团多的优点,其作为重金属吸附材料的应用得到研究者的关注[16-17]。Guo等[18]研究了磷酸化交联淀粉对铅离子的吸附,谢新玲等[19]分别以阳离子淀粉、磷酸酯淀粉、尿素淀粉等5种改性淀粉为吸附剂,测量吸附后的重金属离子的质量浓度。
相波等[20]用醚化法制备了交联氨基淀粉并研究了其对铜离子的吸附,结果表明交联氨基淀粉对铜离子有较好的吸附效果,但是醚化法制备交联氨基淀粉条件控制比较严格。本文采用玉米淀粉为原料,依次进行碱化交联反应、双醛化反应和氨基化反应制备交联氨基淀粉,研究交联氨基淀粉吸附剂对含Cd2+模拟废水的吸附效果,并研究了交联氨基淀粉使用量、模拟废水pH值和离子强度、吸附反应时间等因素对吸附效果的影响,同时进行了吸附过程动力学和热力学模拟。结果显示,以玉米淀粉为原料制备的交联氨基淀粉吸附剂对Cd2+具有良好的吸附效果,具有工业化应用的良好前景。
1 材料与方法
1.1 试剂和仪器
玉米淀粉:食品级,采购自南昌市场;氯化镉、高碘酸钠、乙二胺、环氧氯丙烷、盐酸、氢氧化钠、硝酸钠:分析纯,国药集团化学试剂有限公司(上海);所有试验用水均为超纯水;含镉废水均采用氯化镉溶液进行模拟。
AA240 型原子吸收分光光度计:Varian,美国;Nicolet-IR200 型傅立叶变换红外光谱仪:Thermo,美国;FE20精密pH计:Mettler Toledo,中国上海;AL204型分析天平:Mettler Toledo,中国上海;SHA-C型恒温震荡器:国华,中国常州;D11921型超纯水机:Thermo,美国。
1.2 实验方法

图1 交联氨基淀粉的制备方程式Fig.1 Chemical equation of preparing process for CASt
1.2.1 交联氨基淀粉吸附剂的制备 交联淀粉(CSt)的制备:室温条件下,将玉米淀粉按比例加入NaOH质量浓度约6.7‰的稀碱液中,搅拌均匀后再缓慢加入环氧氯丙烷,维持碱性环境,反应5 h后停止反应,静置30 min后抽滤、水洗,获得的CSt样品在60 ℃环境下干燥,保存。
双醛淀粉(DASt)的制备[21]:首先将浓度为0.5 mol/L的高碘酸钠溶液加入到三口烧瓶中,用0.5 mol/L的HCl溶液将高碘酸钠溶液pH值调到1.2~1.5,然后将上一步反应得到的交联淀粉加入到三口烧瓶中,避光,搅拌均匀。将三口烧瓶放入恒温水浴锅中,设定温度为25 ℃,避光反应3 h。得到的DASt产品经过抽滤、洗涤后干燥保存。
交联氨基淀粉(CASt)的制备[22]:首先将配制好的乙二胺溶液加入到三口烧瓶中,用浓度为0.5 mol/L的HCl和0.5 mol/L的 NaOH将溶液调至不同的pH值,然后将干燥的双醛氧化淀粉加入到三口烧瓶中,搅拌均匀,恒温反应。反应结束后将三口烧瓶中的溶液抽滤,抽滤产品依次用去离子水和丙酮洗涤,干燥,备用。图1是CASt制备过程的主要方程式。
1.2.2 Cd2+溶液的配制 准确称取1.630 8 g(精确到0.000 1 g)氯化镉,溶解于100 mL去离子水中,定容至1 L,配制成1 000 mg/L的Cd2+标准溶液,并分别稀释至不同浓度的Cd2+溶液备用。
1.2.3 吸附剂投入量实验 在锥形瓶中加入100 mL质量浓度为100 mg/L的Cd2+溶液,分别加入0.10,0.15,0.20,0.40,0.60,1.00,1.20 g的交联氨基淀粉吸附剂,调节溶液pH为6,在室温条件下振荡4 h,静置,过滤,取上清液,用AA240 型原子吸收分光光度计(火焰吸光度法)测定溶液中Cd2+的浓度。
1.2.4 不同pH以及离子强度吸附实验 在锥形瓶中分别加入50 mL不同浓度的(0.2,0.02,0.002 mol/L)NaNO3溶液作为支持电解质,再分别加入50 mL质量浓度为200 mg/L的Cd2+溶液,在每个锥形瓶中投加0.60 g交联氨基淀粉吸附剂,用0.1 mol/L的HCl或0.1 mol/L的NaOH溶液调节反应体系的pH值,在室温条件下振荡4 h,静置,过滤,取上清液,火焰吸光度法测定Cd2+的浓度。
1.2.5 吸附动力学实验 在锥形瓶中加入100 mL 浓度为100 mg/L、pH为6的Cd2+溶液,投加0.60 g交联氨基淀粉吸附剂,在室温条件下振荡20,30,40,50,60,80,120,180 min,静置,过滤,使用火焰吸光度法测定不同吸附时间后溶液中Cd2+的含量。
1.2.6 等温吸附实验 在锥形瓶中加入初始Cd2+浓度为100,200,300,400,500,600 mg/L的模拟废水,在反应温度为恒温25 ℃,交联氨基淀粉投加量为0.60 g,pH为6的条件下,振荡吸附4 h后测定溶液中Cd2+的浓度。所有吸附实验均设置3次重复。
1.2.7 交联氨基淀粉结构的表征 FTIR:将10 mg烘干的样品与1 000 mg光谱纯KBr粉末混匀,于玛瑙研钵中充分磨碎,10 t/cm2下压片,用 Nicolet-IR200红外光谱仪在4 000~400 cm-1波数范围内对玉米原淀粉、交联氨基淀粉及吸附Cd2+后的交联氨基淀粉样品进行扫描。
1.3 结果计算
水溶液中Cd2+的去除率(P)和吸附容量(Q)用下式计算:
(1)
(2)
(1)、(2)式中:P为离子去除率,%;Q为吸附容量,mg/g;V为待测液体积,L;C0为吸附前Cd2+离子浓度,mg/L;C1为吸附后Cd2+离子浓度,mg/L;W为CASt吸附剂干质量,g。
采用准一级动力学模型和准二级动力学模型对吸附过程拟合:
准一级动力学方程:
(3)
准二级动力学方程:
(4)
(3)、(4)式中:Qt为任一时间的吸附容量(由式2计算得到),mg/g;Qe为平衡吸附量,mg/g;t为吸附时间,min;k1为一级吸附速率常数;k2为二级吸附速率常数。
采用Langmuir 等温吸附模型和Freundlich等温吸附模型对吸附过程进行拟合:
Langmuir 等温吸附:
(5)
(5)式中:Qe为平衡吸附量,mg/g;Q0为极限吸附量,mg/g;b为吸附常数;Ce为平衡状态下Cd2+离子浓度,mg/L。
Langmuir吸附等温方程还可以定义一个无量纲的分离因子RL,其表达式为:
(6)
RL可用于表示吸附过程的性质,当0
Freundlich等温吸附:
(7)
(7)式中:Qe为平衡吸附量,mg/g;Ce为平衡状态下Cd2+离子浓度,mg/L;KF为表示吸附能力的相对大小。
1.4 数据处理
使用Microsoft Office2013软件进行数据处理,使用Origin 9.0绘制图表。
2 结果与分析
2.1 交联氨基淀粉及吸附Cd2+后红外光谱分析
使用傅立叶变换红外光谱仪分别对玉米原淀粉、制备得到的交联氨基淀粉以及吸附Cd2+后的交联氨基淀粉进行红外光谱扫描,结果见图2。从图中曲线a可以看到,原淀粉在3 400 cm-1波数附近出现一个明显的宽峰结构,这是羟基中氢氧键(O-H)的伸缩振动峰;2 900 cm-1波数附近出现的尖峰则是碳链上的饱和碳氢键(C-H)的伸缩振动峰。上述两个伸缩振动峰同时存在于3种材料中,所不同的是峰的宽度和形状(图2中曲线a、b、c)。交联氨基淀粉(曲线b)在1 652.78 cm-1的强吸收为碳氮双键的伸缩振动峰,说明对淀粉的改性过程中确实产生了C=N键(1处)。由于淀粉链上有大量的羟基,而O-H和N-H在3 000~3 400 cm-1波数范围内都有强吸收,因而无法准确辨别氨基的伸缩振动峰,干扰了氨基的鉴别。但是,通过对比曲线a和曲线b可以发现,淀粉改性后,3 400 cm-1波数附近宽峰发生了明显变化,说明改性过程确实引入了氨基。同时,曲线b中,在波数范围在1 560~1 640 cm-1附近出现新的谱线,也就是氨基基团的面内振动峰,这也从侧面说明产物中成功引入了氨基基团。

a:淀粉; b:交联氨基淀粉;c:交联氨基淀粉-Cd2+a:Starch;b:CASt;c:CASt-Cd2+图2 交联氨基淀粉的红外光谱Fig.2 IR spectrum of Starch,CASt and CASt-Cd2+

图3 交联氨基淀粉投入量对Cd2+吸附效果的影响Fig.3 Effect of adsorbent dosage on absorption efficiency of Cd2+
吸附Cd2+后的交联氨基淀粉(曲线c)与交联氨基淀粉相比有明显的不同,在3 390 cm-1附近(2处),是氨基、羟基伸缩振动吸收重叠峰,吸附Cd2+后这个吸收峰向低波数移动,同时1 652.78 cm-1处尖峰消失,而1 747 cm-1处出现尖峰(3处),表明原有的C=N键可能打开,同时Cd2+与开键后的N原子结合生成新的N-Cd配位键,由于开键后的N原子有孤对电子,是供电子基团,因此N-Cd配位键的形成使得N原子上的孤对电子移向Cd,N原子周围电子密度的降低使得N-H键伸缩振动所需能量减小,从而导致N-H键的伸缩振动吸收峰向低波数方向移动。
2.2 吸附剂投入量对吸附性能的影响
交联氨基淀粉投入量的变化对吸附剂吸附量和Cd2+去除率的影响结果见图3,很明显,随着交联氨基淀粉使用量的增大,其对重金属Cd2+的去除率明显增强,去除率从添加量为0.1 g时的52.81%逐步上升到添加量为0.6 g时的约92%后基本不再变化,而单位质量吸附剂吸附量却明显下降。这是由于当交联氨基淀粉吸附剂的使用量加大时,反应体系里参与吸附作用的吸附基团的量也增多,这时吸附剂表面可以跟金属离子发生配位反应的活性位点也增多,活性位点的增多使得更多的Cd2+发生配位反应,因此Cd离子的去除率会随着吸附剂使用量的增大而增大[24]。但是,反应体系中Cd2+的总量是不变的,所以当吸附剂与Cd2+的反应饱和后,继续增加吸附剂的用量反而使得多余的吸附位点不能被利用,吸附剂单位质量的吸附量会降低。为了使单位质量重金属吸附量和Cd2+去除率都达到最佳值,交联氨基淀粉的使用量定为模拟废水质量的0.6%,此时的Cd2+去除率为91.58%。
2.3 溶液pH和离子强度对吸附性能的影响
不同离子强度下pH对吸附剂吸附性能的影响见图4。从图4可以看到,Cd2+的去除率和单位质量吸附剂的吸附量随着pH的升高逐渐上升,在pH为6时达到最高,pH为7时与pH=6时基本持平,但是进一步提高pH,两者均出现下降。这是因为,当体系pH值较低时,反应体系中H+的浓度较大,H+可以和交联氨基淀粉上的氨基基团发生质子化反应,交联氨基淀粉中的-NH2可以与H+结合形成质子化的-NH3+,质子化的-NH3+与Cd2+络合能力较小,而可以发生络合反应的-NH2浓度降低,因此在低pH值条件下,交联氨基淀粉对Cd2+的吸附效果较差。随着体系pH值的增大,H+与金属离子的竞争吸附作用减弱,交联氨基淀粉中质子化的-NH3+随着H+浓度的降低逐渐生成游离的-NH2,游离-NH2浓度的增大使得Cd2+去除率逐渐增大。当pH大于7时,Cd2+离子与OH-反应生成沉淀,使得Cd2+的去除率反而有所下降。因此交联氨基淀粉在中性偏酸的废水中能够表现出最佳的吸附活性,其最佳的吸附pH为6。
离子强度是影响交联氨基淀粉对溶液中Cd2+吸附能力的另一重要因素。从图4可以看出,当pH<7时,交联氨基淀粉对溶液中Cd2+吸附量在0.001 mol/L的NaNO3溶液中最高,而在0.1 mol/L的NaNO3溶液中最低。而在相同的pH条件下,随着NaNO3浓度的增大,溶液体系的离子强度增加,交联氨基淀粉对Cd2+的吸附能力逐渐降低,这可能是因为溶液中的Na+是支持电解质离子,支持电解质离子可以与交联氨基淀粉表面的活性吸附位点发生络合反应,这就和Cd2+与交联氨基淀粉表面吸附位点的络合反应产生竞争作用,增大体系中NaNO3的浓度,会增大体系的离子强度,使得参与交联氨基淀粉竞争吸附的Na+浓度增大,从而导致交联氨基淀粉对 Cd2+的结合几率减小;而Cd2+可以跟其周围的负离子形成的“离子氛”,体系离子强度增大时,增大的不仅仅是Na+的浓度,NO3-的浓度也在增大,那么Cd2+的“离子氛”也在增强,从而阻碍Cd2+向交联氨基淀粉吸附位点的靠近。

图4 不同pH条件下离子强度对交联氨基淀粉吸附Cd2+的影响Fig.4 Effect of NaNO3 concentrations on absorption efficiency of Cd2+ at different pH

图5 吸附时间对Cd2+吸附效果的影响Fig.5 Effect of reaction time on absorption efficiency of Cd2+
2.4 吸附动力学
依据吸附动力学实验条件(1.2.5),以不同振荡时间对Cd2+的吸附量作图,结果如图5所示。由图5可以看出,交联氨基淀粉吸附剂对Cd2+的吸附容量随着时间的增加而增大,在吸附起初阶段,吸附量随时间的增大上升速度较快,这可能是因为在吸附剂与吸附质间存在范德华引力,因为范德华引力的作用使得吸附剂对Cd2+有较大的吸附量,这表明这种快速的物理吸附在吸附初始阶段是占主导地位[25];当吸附反应持续一段时间后,吸附剂的吸附容量不再发生明显的变化,最终达到吸附平衡。这是因为,随着吸附反应的进行,交联氨基淀粉吸附剂表面的活性位点较少,同时氨基淀粉的分子链不断扭曲变形与金属离子进行配位,导致吸附能力达到极限。
用准一级动力学模型(式3)和准二级动力学模型(式4)拟合了图5中的数据,并对其动力学机理进行了分析。结果见图6和表1。

图6 交联淀粉吸附Cd2+的准一级(a)和准二级(b)动力学模型拟合曲线Fig.6 The pseudo-first-order (a) and pseudo-second-order (b) plot of Cd2+by CASt
比较表1 中的动力学模型拟合参数可以看出,用准二级动力学模型拟合交联氨基淀粉吸附剂对Cd2+的吸附过程的相关系数R2达到0.983 5,有研究认为,当拟合相关系数R2>0.980时,则可认为此模型可以用来描述该吸附过程的动力学过程[26];且由准二级动力学模型拟合得到的平衡吸附量与平衡吸附容量的实验值吻合的也比较好,因此,准二级动力学模型拟合的效果比一级动力学模型拟合的效果好些。此外,准二级动力学模型表明吸附由表面反应过程控制,而非吸附质扩散过程控制。而一级动力学模型是基于假定吸附受扩散步骤控制而言[27],所以一级动力学模型更适合描述吸附过程的初始阶段而不是全过程。

表1 动力学模型拟合参数

图7 初始浓度对Cd2+吸附效果的影响 Fig.7 Effect of initial concentration on adsorption efficiency of Cd2+
2.5 等温吸附
依据等温吸附试验条件(1.2.6),以不同Cd2+初始浓度振荡吸附4 h,研究平衡浓度与单位吸附剂吸附量之间的关系,结果见图7。由图中看出,当Cd2+初始浓度小于400 mg/L时,随着Cd2+浓度的增加,平衡吸附量也在增加,这是因为随着Cd2+浓度的增大,Cd2+与交联氨基淀粉活性位点的络合几率也增大,吸附反应朝着络合的正方向进行,吸附量增大。但是,当Cd2+初始浓度大于400 mg/L时,体系平衡吸附量却不再增加。这可能是因为,吸附剂表面的吸附点位是有限的,当离子浓度过大时,吸附剂表面不能承载多余的金属离子,因此,在实际应用中吸附剂的用量要根据废水中金属离子的浓度而定。
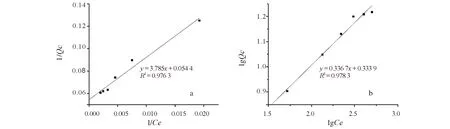
图8 交联淀粉吸附Cd2+的Langmuir方程(a)和Freundlich方程(b)拟合结果Fig.8 Fitting curve of Langmuir (a) and Freundlich (b) adsorption equation of Cd2+ by CASt
以Langmuir(式5)和Freundlich(式7)等温吸附模型对图7中的数据进行拟合[28],数据如拟合结果见图8、表2所示。
由图8和表2的拟合参数可以看出,Langmiur等温线和Freundlich等温线对交联氨基淀粉吸附剂对 Cd2+的吸附过程的拟合参数分别为0.976 3和0.978 3,说明两种方程都可以用来描述交联氨基淀粉吸附剂对 Cd2+的吸附特点。用公式(6)计算得到交联氨基淀粉对Cd2+的RL为0.8,这说明交联氨基淀粉对Cd2+的吸附是优惠吸附。在Langmiur等温吸附模型中,计算出的交联氨基淀粉对Cd2+的最大吸附量为18.38 mg/g,与实验所测得到的结果相近。Langmuir 等温吸附模型是用来描述单分子层吸附的,而化学吸附则是单分子层的反应,说明交联氨基淀粉吸附剂吸附 Cd2+的过程可能以化学吸附为主。

表2 吸附等温线拟合参数
3 结论与讨论
改性剂的选择是制备淀粉基重金属吸附剂的关键,不同的改性剂和改性方法直接影响有效官能团的种类和数量,从而影响吸附剂的效果[22]。相波等[20]以玉米淀粉为原料,在高氯酸引发下合成醚化淀粉,以乙二胺为氨化剂制备了有螯合性能的氨基淀粉衍生物,研究表明氨基淀粉衍生物对铜离子有较好的吸附性能。但是这个方法的醚化阶段需要严格控制高氯酸的浓度,以得到较高氯含量的醚化淀粉,因为过量的高氯酸会导致淀粉的碳化和环氧氯丙烷的过热聚合,而且这个醚化过程要8 h,时间也相对较长。本研究以玉米淀粉为原料、高碘酸钠为氧化剂、乙二胺为氨化剂,制备出一种新型交联氨基淀粉重金属吸附剂。在制备过程中,氧化反应条件比较温和,在室温下即可进行,氧化反应时间也相对较短,从原理和操作性上更易于制备氨基淀粉。
吸附剂的吸附性能不仅与吸附剂本身有关,吸附过程中溶液的pH值和吸附剂投入量是影响吸附效果的重要因素。Zheng等[29]用竞争吸附位理论解释了pH值对吸附剂吸附能力的影响,研究表明,在pH较低时,吸附剂对Cd2+吸附容量随着pH的增大由0.3 mg/g增加至9.6 mg/g,且接枝上去的氰基越多,纤维素的吸附容量也越大。本研究表明,pH<6时,随着pH升高,H+与金属离子的竞争吸附作用减弱,交联氨基淀粉中质子化的-NH3+逐渐生成游离的-NH2,游离-NH2浓度的增大使得Cd2+去除率逐渐增大,这也符合竞争吸附理论。
吸附理论的研究是吸附剂研究过程中的重要组成部分[30-32]。而在常用的等温吸附模型中,Langmuir 等温吸附模型是用来描述单分子层吸附的,而化学吸附通常为单分子层反应[27]。本研究中,交联氨基淀粉对Cd2+吸附过程的Langmiur拟合参数为0.976 3,计算出的最大吸附量与实验测得的结果也最相近,说明交联氨基淀粉吸附Cd2+的过程可能以化学吸附为主。在红外图谱中,吸附Cd2+后的吸附剂在1 652.78 cm-1处尖峰消失,而1 747 cm-1处新的吸收峰,这也表明Cd2+与开键后的N原子结合生成新的N-Cd配位键,交联氨基淀粉对Cd2+的吸附是化学吸附。
随着经济的发展,水体污染日益严重,制备环保、高效的污水处理剂是环境科学研究的重点。氨基改性淀粉用作重金属吸附剂,制备条件温和、反应时间相对较短,是一种制备工艺简单、经济、环保的重金属吸附材料。交联氨基淀粉不仅对Cd2+有较好的吸附效果,对Cu2+、Cr(Ⅵ)的吸附效果也已经证实[22]。但是,在实际生产中,污水本身成分复杂,污水中不仅含有多种重金属离子,还含有多种有机物,污水处理不仅与吸附剂和吸附条件有关,污水环境的多样性是影响处理效果的重要因素,因此开发多功能的吸附剂是今后研究的重点。
