Hybrid血液净化技术治疗儿童噬血细胞综合征
2018-09-14徐洪波黄婷芸田茂强
徐洪波,干 毅,黄婷芸,田茂强,路 健,陈 艳
(遵义医学院附属医院 小儿内二科, 贵州 遵义 563099)
噬血细胞淋巴组织细胞增生症(hemophagocytic lymphohistiocytosis,HLH),又称噬血细胞综合征(hemophagocytic syndrome,HPS),是一种罕见的、进展迅速的临床综合征,致死率高[1],通常使用激素、环孢素A及依托泊苷等综合免疫治疗[2]。然而,该治疗方法副作用大,且仍有部分患者难以奏效[3-4]。文献报道运用连续静-静脉血液滤过(continuous veno-venous hemofiltration,CVVH)在脓毒症治疗中取得了良好的效果[5-6]。少有报道连续性静-静脉血液透析滤过(continuous veno-venous hemodiafiltration,CVVHDF)或CVVH+PE治疗HLH的报道。因此,我们总结杂交血液净化技术成功治疗3例重症HLH患儿的临床资料,现报告如下。
1 资料和方法
1.1 临床资料 选取2015年6月至2017年6月遵义医学院附属医院收治的3例重症HLH患儿,诊断参考2004年国际组织细胞协会公布的HLH诊断及治疗指南[7]。收集患者性别、年龄、触发因素、临床症状、体征、实验室检查、基因检测结果和并发症情况。
1.2 血液净化的方式和时间
1.2.1 静脉置管部位选择 3例患儿均选择股静脉置管。
1.2.2 导管选择 Gambro Gamcath 导管GDK-612(7F)~GDK-1115(11F)单针双腔管,血液净化治疗及置管经家长同意签字。
1.2.3 机器、管路和滤器型号选择 采用PRISMA flex 血液净化系统(Gambro公司),PE采用TPE1000-2000膜式血浆分离器,CVVHDF或CVVH采用Gambro prisma 滤器M60或M100。
1.2.4 血液净化方法 血液净化前应用肝素盐水充分预冲管道,设置血流速3~5 mL/(kg·min)。PE置换泵速度300~500 mL/h,血浆置换量40~50 mL/(kg·次),两次PE间隔48 h。CVVHDF或CVVH置换液量和透析液量均为30~50 mL/(kg·h)。透析液采用Baxter公司生产的腹膜透析液(乳酸盐-G1.5%),2L/袋。置换液配方(复旦儿科):生理盐水2 000 mL+ 5%葡萄糖液125 mL+注射用水500 mL+10%氯化钙注射液 6 mL+25%硫酸镁2 mL+5%碳酸氢钠167 mL+10%氯化钾10 mL。根据电解质结果调整离子浓度,根据肾功能、水肿调整超滤量。
1.2.5 抗凝方法 选择普通肝素抗凝,首剂50~100 U/kg,然后5~15U/(kg·h)维持,使APTT维持在正常值的1.5~2倍。
1.3 观察病情转归 比较患者血液净化治疗前后临床症状及相关生化指标变化。出院后随访3例患儿的体温、血常规、铁蛋白、LDH等至2017年12月。
1.4 统计学方法 由于3例患儿病例数少,治疗前后的血生化指标直接采用均值表示。
2 结果
2.1 临床资料 3例患儿,最小10月,最大72月,1例为原发性HLH,另2例为继发性HLH,临床症状及体征有:发热、黄疸、肝脾肿大、三系下降、血清铁蛋白增高、纤维蛋白原降低和NK细胞活性下降等,见表1。
表中所涉及实验室数值均为峰值;Fib :纤维蛋白原;CRRT:持续血液净化;“-”:未见异常,“*”:基因突变见图1,“**”:噬血现象见图2。
2.2 基因检测(北京海斯特检验所) 病例1 UNC13D基因Exon14发现突变:c.1228A>C(p.Ile410Leu),见图1。其余两例未检出突变。
2.3 血液净化的时机、方法及时间 血液净化开始时间:化疗后48 h仍持续发热、三系进行下降、SF持续升高,或诊断时有合并症。血液净化治疗的终点:①临床症状好转,体温下降或正常,尿量达到2 mL/(kg·h)或以上,浮肿消退;②三系开始上升;③SF<500 μg/L,IL-6 <60 pg/mL;④脏器功能改善:sCr和BUN恢复正常范围、ALT<300 U/L,总胆红素(TBIL)<85 mmol/L,LDH<1 000 U/L。持续血液净化(CBP)的模式为CVVHDF(或CVVH),时间为56~136 h,血浆置换为2~3次,详见表1。

表1 3例患儿的基本临床资料

图中箭头所示为突变位点,c.1228A>C (p.Ile410Leu )。
2.4 病情转归及随访 3例患儿经化疗+血液净化辅助治疗后临床症状好转,体温正常,浮肿、黄疸消退,肝脾回缩,实验室指标显著改善,见表2,且未发现出血、凝血等并发症,最终好转出院。最后1次随访至2017年12月,病程分别为24、16及10个月,3例患者各项指标正常,均无复发,其中病例1为原发性HLH,等待干细胞移植中。
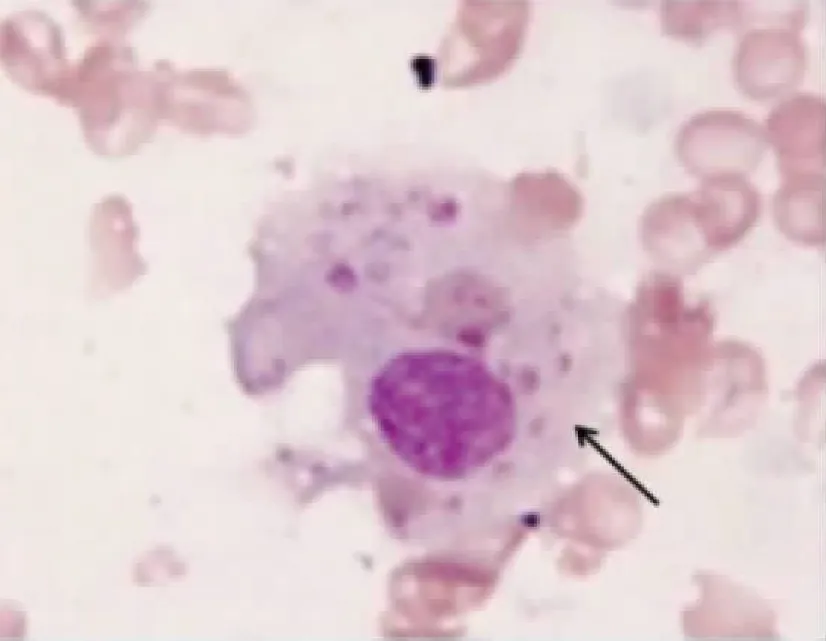
瑞氏染色,油镜,×100,箭头所示。

表2 血液净化治疗前后3 例患儿主要实验室检查指标均值的变化
3 讨论
HLH是一组由活化的淋巴细胞和组织细胞过度增生但免疫无效、引起多器官高炎症反应的临床综合征,分为原发性和继发性HLH,原发性多为家族性和免疫缺陷相关综合征,可能与某些基因突变相关,继发性则与感染、肿瘤及风湿性疾病相关[1-2]。本研究3例患者中病例1发现UNC13D基因杂合突变,为原发性HLH(FHL-3)常见突变位点,既往有类似报道[8]。原发性HLH为常染色体或性染色体隐性遗传,结合本例患者病情,考虑原发性HLH可能,但仍需进一步作父母基因突变验证明确。另2例未发现基因突变,诊断继发性HLH,3例均由感染(2例EB病毒)触发,与文献报道一致[9]。
HLH的发病机制不完全清楚,主要的机制有:①免疫清除功能障碍:NK细胞和细胞毒性T淋巴细胞(CTL)功能异常不能及时清除被病毒等感染的靶细胞;②免疫系统过度激活:持续存在的刺激使得CTL过度增殖活化,产生大量干扰素-γ(IFN-γ),刺激巨噬细胞过度增殖和活化;③细胞因子风暴:巨噬细胞产生白细胞介素(IL-1、IL-6、IL-10、IL-12)、肿瘤坏死因子α(TNF-α)等,IL-12又反过来刺激CTL增殖并产生IFN-γ,形成恶性循环,导致“细胞因子风暴”,从而引起发热、黄疸、肝脾肿大、血细胞减少及多脏器功能衰竭等一系列临床表现[1,10]。本研究3例患者均符合HLH的临床表现,3例患儿合并肝功能衰竭,2例合并肾功能衰竭,1例合并呼吸衰竭、神经系统损害,考虑与炎症细胞浸润及高浓度的细胞因子损伤有关[11]。
HLH理想的治疗方法是解除诱因,抑制细胞因子产生,快速清除细胞因子和早期死亡率相关的铁蛋白、LDH,脏器功能的支持,原发性HLH还需做异体基因干细胞移植。而目前由环孢素A、激素及依托泊苷组成的HLH-2004方案,仅能抑制细胞因子的产生,起效慢,无法快速清除已经释放入血的细胞因子,更起不到脏器支持作用,导致重症HLH患者治疗效果不理想。而CBP+PE技术既能清除大分子的铁蛋白,又能起到非生物型人工肝的作用,CBP清除中分子的细胞因子和小分子的水、BUN、sCr、LDH等,可弥补常规免疫治疗起效慢的缺点。本研究3例患儿明确诊断按HLH-2004方案治疗后持续发热,病情进行性加重,IL-6、SF、LDH持续升高,加用血液净化治疗后体温显著下降,病情好转,脏器功能改善,IL-6、SF、LDH明显降低,提示该方法治疗有效。
研究显示大量细胞因子中,IL-6作为内源性致热源之一,是引起HLH患儿发热主要的原因[1,12]。同时,高IL-6、IFN-γ、IL-10血症与病情的危重程度呈正相关,是导致HLH患者早期死亡的危险因素[1]。既往已经证实CBP能清除IL-6、IFN-γ、IL-10等细胞因子[13-14],3例患儿经血液净化治疗后体温下降、病情好转,考虑与大量细胞因子被清除有关。HLH患者最常见的实验室特征是血细胞减少,SF、LDH异常增高。SF水平与HPS严重程度、治疗后SF的下降反应与预后呈正相关[15-17]。LDH>3 707.5 U/L为HPS患者早期死亡的独立危险因素[1]。本研究3例患者均出现血细胞减少,SF、LDH异常增高,LDH均>8 000 U/L,病例2铁蛋白高达68 000 μg/L,经杂合血液净化技术治疗后血细胞较前显著上升,SF、LDH明显下降。结合IL-6水平变化分析,血细胞上升考虑与高浓度的细胞因子被清除,骨髓抑制减轻有关[18]。Gambro prisma 滤器膜吸附和血浆置换清除大分子的SF,CBP快速清除LDH,是SF、LDH迅速下降的主要原因。
综上,在HLH-2004方案化疗的基础上加用Hybrid血液净化技术,既能抑制细胞因子的产生,又能快速清除细胞因子、SF及LDH,同时还能起到肝肾替代的作用,且安全、起效快,是重症HLH患儿理想的治疗方法。Hybrid血液净化技术可给重症HLH患儿的治疗带来新的选择。
