脑卒中风险评估模型的研究进展
2018-09-14周德生邓奕辉葛金文
周 韩,周德生,邓奕辉,葛金文
脑卒中是由于脑部血管的突然破裂或血管内发生阻塞引起的以急性脑组织损伤为特点的一组脑血管疾病,其包括出血性脑卒中和缺血性脑卒中。脑卒中常具有发病率高、死亡率高和致残率高的特点,有调查显示,城乡合计脑卒中已位居我国目前死亡原因的第一位,并成为我国成年人残疾首要原因[1]。疾病风险评估模型是指应用统计学的方法对危险因素与疾病发病之间的关系进行模型拟合得到疾病发病危险预测模型,用所得到的预测模型对疾病发病危险进行量化并分级。脑血管疾病在发病前的早期预防意义远大于治疗,故早期应用风险评估模型来识别脑卒中的高危人群,明确脑卒中发生及复发的预防重点,早期干预,对于脑卒中一级和二级预防具有重要意义。国内外许多学者对脑卒中风险评估进行了大量的研究,其中已经建立了有效可行的评估模型和工具,并逐渐将其应用在预防实践。本文就近年来脑卒中风险评估模型的研究进展综述如下。
1 风险评估模型的起源
风险评估模型和工具在20世纪60年代首次建立,Truett等[2]在美国马萨诸塞州的Framingham心血管疾病队列研究的基础上建立了冠心病的风险模型,随后的大多数风险评估模型与工具都是基于Framingham的研究,随着研究的逐步深入,预测疾病从冠心病扩展到心脑血管疾病,此后进一步发展到评估冠心病与卒中分类。即脑卒中风险评估模型与工具是从心血管疾病风险评估工具演变而来,其研究方法、风险因素和研究人群与心血管疾病风险评估基本一致。心脑血管疾病的风险评估和预测一般分为两种方法,一种是建立在单因素与发病的基础上,一种建立在多因素与发病的基础上。单因素分析方法首先确定某种因素是预后因素,根据前瞻性研究中该因素与脑血管事件发病实际发病率的关系建立预测方程,以相对危险度表示强度,得到各相关因素的加权分数即为发病的危险性。而多因素分析方法是建立在多因素数理分析基础上,采用统计学的概率理论方法得到发病危险性与危险因素的关系模型,为了能包括更多的危险因素,提高预测的准确性,多因素分析方法近年来得到了发展。众多国内外学者做了大量的研究,主要建立的预测模型有基于Cox比例风险回归的Framingham模型[3]、基于Weibull accelarated falure time的Framingham模型[4]、基于Logistic回归的Whitehall积分模型[5]、PROCAM的神经网络模型[6]等,以使人群中心脑血管疾病的高危人群得到早期健康管理及健康干预。
2 国外主要的脑卒中风险评估模型
2.1 Framingham预测模型:此模型最早始于1967年,为研究心血管病发病危险的预测模型,用于个体发病危险的评估。其后又开发了各种基于不同预测模型的评估工具[7,8]。1991年Wolf等[9]结合Framingham子代研究开发了新的预测模型,此模型基于Cox比例风险回归模型,研究人群主要为来自美国马萨诸塞州弗明汉地区的5209名30~74岁的美国白人居民,根据吸烟、年龄、糖尿病史、心血管病病史、SBP、心房颤动及左心室肥厚共7项预测因子,并赋予分值权重,为每个受评的个体予以建立积分,然后计算出每个分值段的10年卒中发病率,建立卒中发病率与风险积分值对照表,最后风险综合评分被用来预测未来10年脑卒中发病的风险。由于抗血压治疗是影响卒中的重要因素,1994年,D′Agostino等[10]根据抗高血压药物的治疗情况,对危险积分规则进行调整,即对高血压患者的收缩压水平按照有无进行药物的治疗分别制定不同积分,建立了改良Framingham,提高了该量表对卒中风险的预测能力。1998年在之前的基础上,将Cox比例风险回归模型中的连续因变量转化为分类变量,纳入的危险因素包括年龄、性别、吸烟状况、收缩压、总胆固醇/高密度脂蛋白、饮酒、目前是否患有心血管疾病、是否绝经(女)及甘油三酯(女),运用Weibull accelerated falure_time模型,建立新Framingham模型[4],此模型更贴近于临床实际,目前在美国和世界其他国家被广泛应用,其样本人群来自35~74岁的美国白人。2001年,美国心肺血管研究所专门组织专家组[11],对美国的几项前瞻性研究资料进行了比较,得出结论:Framingham预测模型对中国人发病危险存在明显的低估,用于大多数美国成年人较好,而用于西班牙裔、亚裔、老年美国人误差较大。
2.2 卒中预后评定工具(Stroke Prognostic Instrument,SPI_Ⅰ和SPI_Ⅱ):SPI_Ⅰ量表为TIA患者一般在90天内首次发生卒中的预测模型,SPI_Ⅱ量表为TIA的患者2年内再次发生卒中或者死亡的风险预测模型。1991年,Keman等[12]制定了SPI_Ⅰ量表来评估卒中患者的远期复发风险,总分为11分,包括影响短暂性脑缺血发作后发生缺血性卒中或者死亡的5个因素,分别为糖尿病、年龄>65岁、本次事件为卒中而非TIA、重度高血压、冠心病,并赋予分值,再根据患者的得分情况分为3组:低危组、中危组、高危组,三组患者在90天内发生卒中或死亡的风险分别为10%、2l%和59%。SPI_Ⅰ量表推行之后,部分研究者认为样本量少且随访时间较短不够精确,于是,2000年,Keman等在SPI_Ⅰ量表的基础上制定了SPI_Ⅱ量表,该量表将年龄从65岁提到了70岁,且增加了充血性心力衰竭和卒中史2个危险因素,并将高血压降为了1分。根据SPI_Ⅱ量表评分进行风险分层分为3组,分别为低危组、中危组、高危组,三组患者2年内的死亡或卒中风险的不同风险级别相应为16%、24%及42%。SPI_Ⅱ量表较SPI_Ⅰ量表的样本量大且随访时间长,故评定TIA患者预后方面SPI_Ⅱ量表优于SPI_Ⅰ量表,见表1。

表1 卒中预后评定工具
注:重度高血压:收缩压≥180mmHg和(或)舒张压≥100mmHg;SPI_Ⅰ量表:0到2分为低危组,3到6分为中危组,7到11分为高危组;SPI_Ⅱ量表总分为15分,0到3分为低危组,4到7分为中危组,8到15分为高危组
2.3 ABCD评分系统:2005年,Rothwell等[13]对209例疑似或者确诊的TIA患者进行队列研究后提出了总分为6分ABCD评分法,以预测TIA后7d内卒中的风险。其中A表示年龄,<60岁为0分,≥60岁为1分;B表示血压,无高血压0分,有高血压1分;C表示临床特点,单侧无力2分,语言障碍但不伴无力1分,其他均为0分;D表示症状的持续时间,≥60min为2分,10~59min为1分,<10min为0分;而后研究发现,ABCD评分小于5分的患者发生TIA发作后7d内脑卒中发生率为0.4%,5分的患者为12.1%,而6分的患者则高达31.4%。但是,有研究发现,该评分模型的预测价值较有限,如Cucchiara[14]的研究显示,ABCD评分小于4分的患者仍有极大可能存在其他的高危因素或脑卒中的影像学证据。2007年,Johnston等[15]对4809例TIA患者进行了ABCD评分系统验证,提出ABCD2评分法,其将糖尿病史加入了ABCD评分系统中,形成包括年龄、高血压、临床表现、症状持续时间及糖尿病5个因素的评分模型,并且对脑卒中患者风险分层。该评分模型与ABCD评分系统相比(AUC 0.62),此评分法具有更高的预测价值(AUC 0.83),并在此后相关研究中得到验证,如Galvin等[16]对16项验证ABCD2评分有效性的研究(总样本量为6282388例卒中患者)进行了荟萃分析,其中14项研究对TIA后7d内的卒中发生风险进行了验证,11项研究对TIA发作后90d内的卒中风险进行了验证,结果显示ABCD2评分在TIA后7d内无论是对低、中、高危组的卒中风险都具有较好的预测价值。2010年,Merwick等[17]提出了ABCD3评分量表,其使用欧洲和北美的多中心数据库(共3886例患者,其中包括2654例推论人群及1232例验证人群),在ABCD2评分法基础上加入了7d内TIA病史,总分为9分。同年,Merwick等又在ABCD3评分模型基础上加上同侧颈动脉狭窄≥50%(2分)及DWI检查出高信号(2分),如此便形成了总分为13分的ABCD3I评分,进一步提高了TIA后脑卒中风险预测的准确性。张晓丹等[18]通过对186例TIA患者90d内卒中发生率随访后,采用接受者操作特性曲线(ROC曲线)对ABCD3、ABCD2和ABCD3I评分系统进行比较,结果显示ABCD2评分法、ABCD3评分法、ABCD3I评分法的AUC分别为0.608、0.796、0.860;阳性预测值分别为21.5%、59.1%、73%。该研究认为ABCD3I评分法在预测TIA进展为卒中的阳性率上,明显优于ABCD2评分法和ABCD3评分法,见表2。
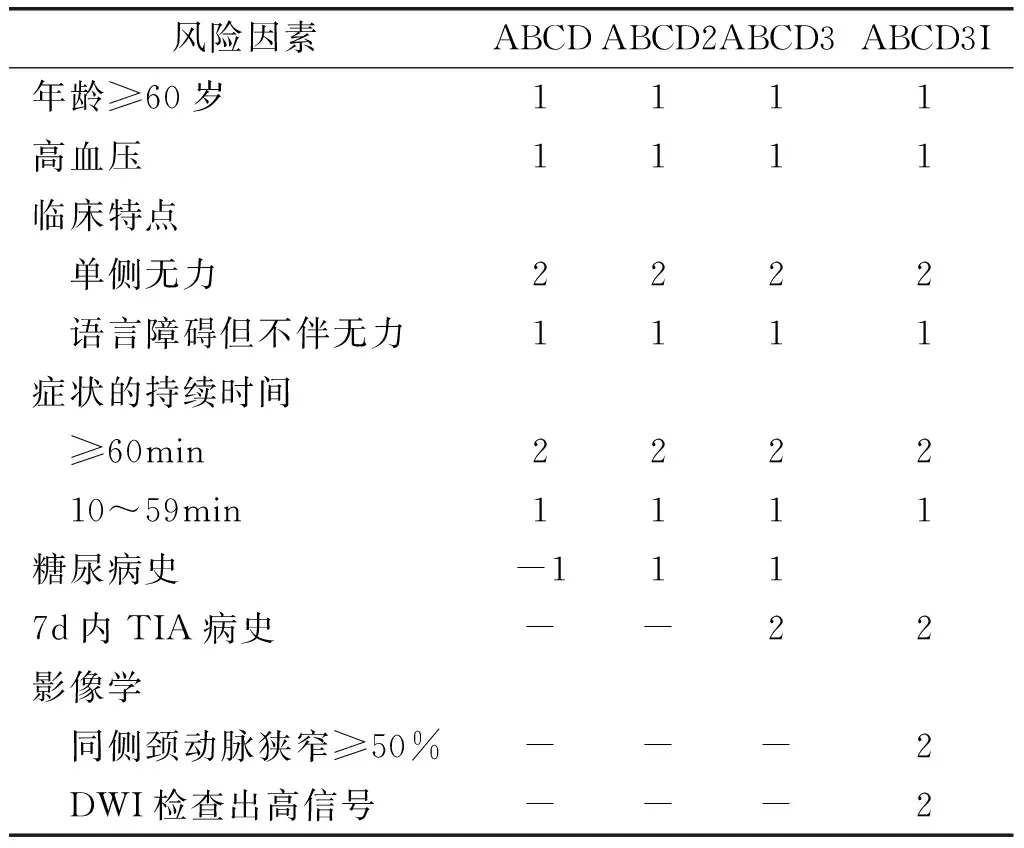
表2 ABCD评分系统
注:ABCD评分:总分为6分,≤3分为低危,>3分为高危;ABCD2评分:总分为7分,高危(6~7分)、中危(4~5分)和低危(0~3分);ABCD3评分:总分为9分,高危(7~9分)、中危(4~7分)和低危(0~3分);ABCD3I评分:总分为13分,高危(≥8分)、中危(4~7分)和低危(≤3分)。
2.4 心房颤动患者缺血性卒中发生风险与抗凝出血风险评估量表:见表3。该量表共包括两个评分系统,分别为传统的CHADS2评分及欧洲指南推荐使用的CHA2DS2_VASc评分。CHADS2评分量表是一种简单易行、操作性强、目前广泛应用于神经内科临床实践,对非瓣膜性心房颤动患者发生缺血性卒中风险进行评估和危险分层管理的评分量表。该量表于2001年由Gage等[19]根据既往数据,将美国卒中预防及心房颤动研究(Stroke Prevention in Atrial Fibrillation,SPAF)评分系统和心房颤动研究(Atrial Fibrillation Investigators,AFI)评分系统结合起来改良后提出,其可量化非瓣膜性心房颤动患者卒中的风险,并可以帮助选择抗凝药物治疗,此量表评分共计6分,包括5个危险因子,即年龄≥75岁、高血压病、糖尿病、心力衰竭以及既往有缺血性脑卒中或者TIA病史。2006年

表3 CHADS2评分系统
注:CHADS2评分:总分为6分,高危(≥2分)、中危(1分)和低危(0分);CHA2DS2_VASc评分:总分为9分,高危(≥2分)、中危(1分)和低危(0分)。
美国心脏病学会及欧洲心脏病学会心房颤动指南指出建议使用CHADS2评分量表对非瓣膜性心房颤动患者发生卒中风险进行分层。低危组建议可给予阿司匹林进行治疗或不予治疗;中危组建议给予阿司匹林或1种口服的抗凝药物治疗;高危组建议给予抗凝治疗。2009年,Lip等[20]在CHADS2评分量表基础上结合年龄65~74岁、血管疾病及女性这3个危险因素,提出了CHA2DS2_VASc评分,该量表共计9分。其将危险因素划分成了两大类,即主要危险因素与非主要危险因素,主要危险因素为卒中史及年龄≥75岁,并增加了卒中史评分的比重,且将年龄分成了两个档,而其余即为非主要危险因素。2012年欧洲心脏病学会(European Society of Cardiology,ESC)在《欧洲心脏杂志》发布了心房颤动管理指南推荐使用CHA2DS2_VASC量表,其提出评分为0者推荐不用药或者服用阿司匹林,评分为1分者;推荐口服阿司匹林或者抗凝药物,且推荐抗凝治疗;评分总分≥2者,推荐使用新型抗凝药或华法林。CHADS2评分量表操作简单易行,可筛选出需要进行抗凝治疗的对象,而CHA2DS2_VASC量表虽在临床操作中较为复杂,但却更能筛选出真正低危且不需要进行抗凝治疗的心房颤动患者。2018年,Chao等[21]使用CHA2DS2_VASc评分对台湾人群中310,039名未接受抗血栓治疗的低风险心房颤动患者进行了3种方法预测:即基线CHA2DS2_VASc评分、随访CHA2DS2_VASc评分及Delta CHA2DS2_VASc评分。并对基线,随访和Delta CHA2DS2_VASc评分在预测缺血性卒中方面的准确性进行了分析和比较,研究结果显示基线、随访及Delta CHA2DS2_VASc评分C指数分别为0.578、0.729和0.742,根据C指数和净重新分类指数评估,Delta CHA2DS2_VASc评分是缺血性卒中的显著预测指标,其表现优于基线或随访CHA2DS2_VASc评分。在这项队列研究中,研究者证实了CHA2DS2_VASc评分不是静态的,大多数心房颤动患者在出现缺血性卒中之前会发展≥1个新的卒中危险因素,反映了由于年龄的增长和事件并发症的增加,抗凝治疗心房颤动中卒中发生风险是一个动态的变化过程。
2.5 Essen卒中风险评分量表(ESRS):ESRS是一种简单且易于操作的9分量表,此量表来源于比较氯吡格雷和阿司匹林治疗高危缺血性事件患者的一项国际多中心随机双盲试验(CAPRIE研究),是针对非心源性缺血性脑卒中患者评估其复发风险的常用预测工具。CAPRIE研究入组19185例动脉粥样硬化疾病患者,其包括年龄、吸烟、心脏病、高血压、糖尿病、脑卒中或TIA病史等常见的危险因素,进行1~3年的随访,结果提示,随着Essen评分的增高,卒中的复发风险随之增加,Essen量表评分≥3分者,年卒中复发风险>4%,结论提示长期使用氯吡格雷降低脑卒中风险优于阿司匹林,而且就安全性而言,前者总体安全性与中等剂量阿司匹林相当[22,23]。目前许多研究表明,ESRS对急性缺血性脑卒中的远期(≥1年)复发风险具有较好的预测能力,国内有研究显示Essen卒中风险评估量表预测卒中复发的ROC曲线下面积为0.59(95%CI:0.58~0.60)[24]。孟霞等[25]研究表明,ESRS对TIA、缺血性脑卒中NIHSS评分≤3分、与>3分的1年复发风险预测的AUC分别为0.57、0.58、0.60。陈云霞等[26]研究表明,Essen卒中风险评分量表对缺血性脑卒中患者复发的预测的ROC曲线下面积为0.652(95%CI:0.574~0.731)。焉双梅等[27]研究表明,ESRS对AIS患者1年复发的预测ROC曲线下面积为0.587,提示ESRS对AIS患者1年复发风险具有一定的预测价值,与国内的研究基本相符,但ROC曲线下面积略低于国外研究。

表4 Essen卒中风险评分量表
注:0~3分为卒中复发低风险患者,3~6分为卒中复发高风险患者
2.6 RRE_90评分:RRE_90评分是2009年由美国神经病学学院的研究者基于回顾性研究提出的一个基于网络的评分量表,此量表最初制定的主要目的是用于预测首次缺血性卒中后90d内再发卒中的风险。2007年,Prabhakaran等[28]根据TIA患者的影像学表现将TIA患者分为2种类型:一为单纯TIA,一为短暂性症状伴梗塞(transient symptoms associated with infarction,TSI)。2009年基于组织学是否改变对TIA定义提出异议,认为无论TIA患者的临床症状持续时间多久,只要组织学出现改变就应当认为是卒中,但是研究者发现,TSI患者短期内发生缺血性卒中的风险大约比缺血性卒中患者再发卒中风险高15倍,如果将TSI等同于缺血性卒中,那么TSI作为缺血性卒中的高危预警就将被忽视,从而不能筛选出卒中的高危患者,将导致卒中的发生率增加。故2009年,美国神经病学学院的研究者制定了RRE_90网络评分量表,除明确的影像学等危险因素之外,还考虑了病因学分型,能够较准确地识别TSI患者潜在病因,其将TSI患者进行了分层,把RRE评分≤2者分为低危患者,其卒中风险≤1%,把RRE评分>2分者分为高危患者,其卒中风险>18%[29]。2016年,焉双梅[27]应用90d复发风险评估量表(RRE_90)和艾森脑卒中风险分层量表(Essen卒中风险评分量表ESRS)对483例急性缺血性脑卒中患者进行一项前瞻性队列研究,随访1年,结果发现RRE_90、ESRS评分预测AIS患者1年复发的ROC曲线下面积分别为0.588(95%CI:0.542~0.632)、0.587(95%CI:0.542~0.632),显示RRE_90与ESRS对AIS患者1年复发具有相同的预测效能。
2.7 TeleStroke Mimic(TM)评分:TM评分是在2014年由Ali等[30]提出的一个基于回顾性研究制定的用于预测远程脑卒中评估期间的缺血性脑卒中模拟(SM)的模型。其分析了来自2004年1月至2013年4月在新英格兰的合作伙伴远程脑卒中网络中的829名连续患者的衍生队列,以及332例内部验证,基于与SM状态无关的因素,包括年龄,心房纤颤、高血压、癫痫发作等病史及面部无力和NIHSS>14,使用逐步逻辑回归建立预测评分,并使用受试者(ROC)曲线分析评估其性能。结果显示TM评分在ROC曲线下面积分别为(推导组群AUC=0.75,内部验证AUC=0.71,外部验证AUC=0.77)。表示SM与缺血性脑血管病(ICVD)相比,SM平均年龄较低,血管危险因素较少,发作前癫痫发作频率较高,并有不同的症状表现。其认为TM评分可以帮助临床医生在复杂的时间关键性的脑卒中评估过程中考虑备选诊断并潜在地检测SM。2018年,Ali等[31]试图在更广泛的人群中外部验证TM评分,其利用来自3个不同的美国和欧洲的远程网络数据,评估了1930名犹他大学乔治亚州摄政大学的远程咨询和德国综合卒中护理网络TeleMedical项目的TM评分,用于之前推导的TM评分,其中较低的TM评分对应于较高的可能性是卒中模拟。结果显示,1930名患者中有630名(32.6%)为卒中模拟,ROC曲线下面积为0.72(95%CI:0.70~0.73)。结论提示,TM评分能够预测不同队列中的卒中模拟,TM评分这样的预测性工具可能有助于在复杂的、时间关键性的脑卒中评估过程中,突出卒中相似者与脑卒中患者之间的关键临床差异。
2.8 ABC_脑卒中评分(ABC_Stroke Score):ABC_脑卒中评分是Hijazi等[32]在2016年基于生物标志物开发的用于预测心房颤动患者发生卒中的风险评分,其包括年龄、心脏生物标志物N_末端片段B型利钠肽(NT_proBNP)、心肌肌钙蛋白高敏感性(cTn_hs)和既往卒中/TIA四个变量,此评分源于一项双盲双模拟随机临床试验(ARISOTLE试验)和一项国际性多中心双盲事件驱动试验(STABILITY试验),是针对于心房颤动患者预测卒中或全身性栓塞的预测工具。ARISOTLE试验入组18201例阵发性、持续性或永久性心房颤动或心房扑动患者,其包括年龄≥75岁、既往卒中、TIA或全身栓塞、心力衰竭、糖尿病或需要药物治疗的高血压等危险因素,随访1.9年,并外部验证1400名心房颤动或心房扑动(689位口服抗凝药物)的参与者和STABILITY试验中可用的生物标志物,结果提示生物标志物(NT_proBNP,cTn_hs)和临床变量(既往卒中/TIA)有助于预测卒中或系统性栓塞,结论提示ABC_脑卒中评分表现优于目前临床使用的风险评分,并可能改善AF的决策支持。2017年,Hijazi等[33]通过对4796例心房颤动患者调查心脏生物标志物的短期变异性,并评估ABC卒中风险评分是否能提供稳定的短期风险评估,根据8702人年随访和96次卒中/系统性栓塞事件,结果显示,2个月时的ABC评分达到0.70(95%CI,0.65~0.76)的相似C指数,结论提示2个月内生物标记物水平的平均变化很小,重复测量心脏生物标记物为死亡率提供了一些增加的预后价值,但与临床危险因素和生物标记物的基线水平相结合时,不提供对卒中的预后价值。同年,Rivera_Caravaca等[34]应用ABC_stroke评分与CHA2DS2_VASc评分对1125例心房颤动患者进行一项随机试验,随访6.5年,结果显示3.5年时ABC_卒中评分的C指数显著高于CHA2DS2_VASc(0.663:0.600,P=0.046),但两者的C指数在6.5年时无显著差异,结论表明在抗凝治疗的心房颤动患者中,与长期随访期间的CHA2DS2_VASc评分相比,新的ABC评分未提供明显更好的预测性能且CHA2DS2_VASc评分在识别低风险患者的方面较ABC评分好。
3 国内主要的脑卒中风险评估模型
3.1 国人缺血性心血管病10年发病危险评估(ischemic cardiovascular disease,ICVD )脑卒中风险评分量表,中美队列是运用在线计算器或手机软件(http://my.americanheart.org/evriskcalculator)来评估个体未来10年动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)的发生风险(致死性及非致死性心血管疾病及脑卒中)。1981年,由中国医学科学院阜外心血管病医院流行病学研究室负责的队列来自中美政府间合作项目“中美心肺疾病流行病学合作研究”(简称“中美队列”),该研究采用国际标准方法进行横断面研究和前瞻性研究,为我国首次进行的完全采用国际标准化方法的流行病学研究,其采用Cox比例风险回归模型,在1981年和1982年分别进行了数千人规模的预试验,于1993~1994年秋季在包括北京首都钢铁公司工人、北京石景山区农民、广州番禺县农民和广州造船厂工人的4个人群同时进行正式基线调查,纳入1993~1994年同年龄组独立样本人群中主要括年龄、性别、种族、收缩压、总胆固醇、高密度脂蛋白、糖尿病、吸烟及是否接受降压治疗等危险因素的均值,校正其回归系数,从而得到新的评估模型。结果显示其能较好地预测未来10年ASCVD的发生风险(AUC:男性0.713,女性0.818)。中国心脑血管病学多中心协作研究与“八五”攻关期间根据美国-中国心血管流行病学合作研究17年的随访数据应用Cox比例风险回归,进行的心脑血管病危险因素调查后续的队列人群随访资料对模型进行回代检验,同时因变量分类建立预测模型并开发相应的预测评分工具,该模型纳入的危险因素包括性别、年龄、收缩压、体重指数、血清总胆固醇,吸烟状况和糖尿病等,其结果显示Cox回归预测模型和简化的点评分模型对估计中国人10年综合心血管风险具有满意的预测能力,其中脑卒中是主要的心血管疾病[35]。
3.2 冠心病、脑卒中综合危险度评估及干预方案:我国的心脑血管疾病危险因素的流行病学特征与西方国家不同,为此国家开展了“十五”攻关课题,其依据中美心肺血管疾病流行病学合作研究队列随访资料,纳入包括年龄、性别、血压、血清总胆固醇、体重指数、吸烟等在内的主要危险因素,采用了数学模型拟合方法,得到最优预测模型,然后校正人群的危险因素在长期变化趋势中的影响,采用回代检验和计算ROC面积来检验该模型的预测能力,结果显示初步开发的ICVD事件10年发病危险预测模型和简易评估工具具有较为满意的预测能力,也能够较好地反映国人发生心血管病的综合危险[36]。而目前此工具在我国得到较为广泛的应用,成为较为适合我国人群心脑血管疾病综合风险的评估工具。
3.3 中医特色相关的脑卒中风险评估模型:中医“治未病”理论是我国中医现代预防医学领域的理论基础。《黄帝内经·素问》曰:“圣人不治已病治未病,不治已乱治未乱”,说明在此基础理论指导下的核心思想应为未病先防。现常将“治未病”这一理论分为三个方面,分别为未病先防、既病防变与病后防复。即在疾病出现预兆的初期予采取积极措施以防止疾病的发生,而在疾病发生之时通过积极的治疗以防止疾病的继续发展与传变,最后疾病倾愈之时予以调护避免病情加重反复,这与现代医学疾病的三级预防理念颇为相近,中医对脑卒中的防治积累了相当多的经验。在上述众多的脑卒中健康风险评估模型中,多是以现代医学中脑卒中的危险因素作为变量,我国传统医学方面从脑卒中的病因病机、症候类型、体质等与疾病的发生发展的关系入手亦做了大量研究。在1999年,吴大嵘等[37]就通过采用非条件和kli:k2i配对的条件Logistic回归的分析方法,对221例中风病人的临床中医证候特征进行比较分析,建立急性期中风病血瘀证的证候预测模型,并采用临床调查的结果对模型进行验证,结果显示Logistic回归模型的ROC曲线下面积为0.9738,说明该模型对急性期中风病血瘀证具有较好的预测作用。其后如李壮苗等[38]通过采用ABCD2评分,按分值分为低危组(0~3分)、中危组(4~5分)和高危组(6~7分),并用“中医体质量表”对患者进行体质判定分析不同体质的中风先兆证患者发生脑梗死的风险,结论显示不同体质的中风先兆证患者可能存在不同的脑梗死风险,痰湿质最高,其次是阴虚质,临床可针对患者体质开展中风先兆证的干预。董致郅等[39]通过探讨TIA早期风险预测工具(ABCD2)评分在评估中风先兆证患者发生中风转化中的价值,并分析ABCD2评分与中医证型的关系,结果显示中风先兆证中风痰内盛、瘀血阻络证有较高的发生中风病风险,故研究者认为实践中应将中医辨证与神经科量表评价结合起来,对中风先兆的高危人群进行准确识别,积极干预,防止发生中风转化。因此在中医“治未病”理论的指导下构建融合中医体质、证候、及危险因素等具备中医特色的风险评估系统,建立风险预测模型对指导脑卒中患者的一、二级预防具有深远意义。
4 小结
合理的风险评估有利于对脑卒中易患人群的管理,指导临床医生寻找更积极的预防策略,从而降低脑卒中的发生、复发风险。尽管目前的风险评估模型和工具繁多,但由于社会、文化、经济及人种等差异,导致其推广应用受到了限制,鉴于脑卒中的病因、发病机制及危险因素等的多样性,各种评估工具本身存在着一定局限性。现有的卒中风险评估模型常用的年龄、性别、吸烟状况、血压、血脂、血糖、饮酒、既往心血管病史等危险因素之间又具有极为复杂的相互作用,如患者年龄越大,累积的血压、血脂异常及心血管病等并发症亦越多,而在缺血性卒中风险预测时,大多评分模型都是基于基线风险因素计算的,结果在随访期后确定。然而,卒中风险并不是一成不变的,随着时间的推移,患者年龄越来越大,累积的合并症也越来越多,其发生中风的风险也加大,因此在风险评估模型的制定过程中应考虑基线及随访间的变化,使评估模型的准确性进一步提高。此外,随着影像学及临床医学检测技术的进一步发展和脑卒中亚临床标志物的深入研究,新的具有更准确的预警标志物也将会随之产生,故在危险因素研究的基础上,建立风险评估模型时能够增加脑血管病的影像学表现及亚临床识别标志,有望进一步提高风险评估模型的准确性与科学性。且现代中医在治未病理论的指导下,对防治脑卒中具有良好的优势和特色,将中医辨证、中医体质、证候及危险因素结合起来建立风险评估模型,有利于对卒中易患人群进行准确识别,防止发生中风转化。因此建立可融合中医特色的具有预测价值更高的且更适用于我国脑卒中易患人群的风险评估工具和模型是十分必要的,亦需要临床医生进一步的深入探索。未来随着影像学及临床医学检测技术的快速发展和卒中风险评估模型研究的深入,脑卒中风险评估模型必将得到进一步完善。
