二氧化钛—氧化石墨烯复合物去除水中有机污染物的性能研究
2018-09-11宋世举束传康王旭明
李 洋,梁 莹 ,刘 洋,宋世举,束传康,王旭明
(华东理工大学 理学院, 上海 200237)
1 研究背景
光催化降解技术可通过光催化剂将太阳能转化为化学能并驱动氧化还原反应实现对水中污染物的降解,具有节能、绿色、安全、价廉的优势,被认为是环境治理的理想方法。该技术的核心是光催化剂,目前研究和应用最广泛的是半导体光催化剂,TiO2作为其中的代表具有化学稳定性高、无毒、价廉、可大规模生产的优点。然而,由于TiO2属于宽禁带半导体,只能吸收紫外光,因此对太阳光的利用率不高,另外TiO2具有强吸水性,表面不易吸附有机污染物,严重影响了降解效率,这些缺陷使TiO2的应用受到极大限制。近些年,研究人员针对TiO2改性做了大量工作且取得一定进展。石墨烯的发现为TiO2光催化剂改性提供了新的途径。
石墨烯,一种由碳原子通过sp2杂化形成的单层二维蜂窝状结构,自2004年被发现以来就成为了研究焦点。石墨烯具有非常大的比表面积,极高的电子迁移率,优异的热传导性以及独特的力学性能,这些特性使其在很多领域展现出巨大的应用前景[1-4]。氧化石墨烯是石墨烯的一种衍生物,除了具有大的比表面积外,其单片层表面带有大量羧基、羟基、环氧化物等官能团,丰富的表面化学结构使GO在很多溶剂中,特别是水中具有良好的分散性,便于吸附水中的污染物,表面缺陷和褶皱结构等特性为表面化学反应提供了大量活性点位,有利于GO的功能化和污染物的降解。因此,在环境治理方面,氧化石墨烯(GO)[5-6]比石墨烯具有更大的应用价值。目前,针对GO改性光催化材料,以提高材料对污染物的吸附性能和降解效率为研究热点之一。在改性TiO2方面,大量研究表明,TiO2-GO复合物[7-10]中Ti-O-C化学键的形成会使TiO2的禁带宽度变窄,使其在可见光区表现出较大的光化学活性,GO可促进光生载流子的分离,提高光催化效率。但复合物中GO的比例不宜超过TiO2质量的10 %,否则,复合物的光催化活性会出现反转,即随着GO含量的增加复合物的光催化性能会下降[11-14]。因此,人们普遍将研究的重点集中在GO含量较低的情况,缺乏对高GO含量方面的科学探讨。污染物的去除是吸附和降解的协同作用,GO本身独特的表面性能使其表现出优异的吸附性,在去除污染物方面具有巨大的应用前景,它不仅可以用来改性TiO2,也可以作为主体被TiO2功能化。在这样的研究背景下,GO所占比重较大时(大于TiO2质量的10 %),其独特的吸附性和丰富的表面化学结构将对去除有机污染物产生显著影响,GO的环境净化作用会凸显出来,此时不再是TiO2基础上的改性,而是TiO2与GO彼此相互作用,GO会影响TiO2的光催化活性和机制,TiO2也会影响GO在水中的分散性以及对污染物的吸附性,其综合效果决定了复合物去除污染物的效率。鉴于此,本文在试验设计中将GO的质量分别调控为TiO2质量的10 %、20 %、30 %、40 %和50 %,采用水热法对二氧化钛-石墨烯复合物(TiO2-GO)进行了制备,并且对复合物的结构、形貌、光催化降解以及去除水中有机污染物的效率进行了研究。
2 试验设计
2.1 试验试剂
制备大片层氧化石墨烯所用原料为鳞片石墨(325目)、磷酸(分析纯)、98 %浓硫酸(分析纯)、高锰酸钾(分析纯)、30 %双氧水(分析纯);制备TiO2所用试剂为钛酸四丁酯(98.0%)、无水乙醇(≥ 99.7%);所用有机染料为罗丹明B(RhB,分析纯);试验用水均为实验室自制去离子水。
2.2 合成
2.2.1 TiO2-GO复合物的制备 采用改进Hummers法[15],在1 g鳞片石墨,6 g高锰酸钾的混合物中加入浓硫酸(120 mL)与浓磷酸(13 mL)的混合液,加热控制反应温度在50 ℃,反应12 h,冷却至室温,在冰水浴中加入1 mL 30 %双氧水,用去离子水洗涤、离心,配成浓度为4.26 mg/mL的GO水溶液。
将0.6807 g(2 mmol)钛酸四丁酯溶解在60 mL无水乙醇中,随后加入20 mL GO水溶液。其中GO含量分别为0.0160、0.0319、0.0479、0.0639和0.0799 g,对应的复合物分别为TiO2-10%GO、TiO2-20%GO、TiO2-30%GO、TiO2-40%GO和TiO2-50%GO。混合液磁力搅拌30 min后转入到100 mL聚四氟乙烯反应釜中,在170 ℃鼓风烘箱中反应24 h,自然冷却。反应后获得的深灰色粉末产物经去离子水、无水乙醇洗涤并离心收集后在60 ℃鼓风烘箱中干燥。
2.2.2 TiO2纳米粒子的制备 为了与TiO2-GO复合物去除污染物性能进行比较,采用相同的水热技术制备了单一TiO2纳米粒子:将0.6807 g(2 mmol)钛酸四丁酯溶解在60 mL无水乙醇中获得透明无色溶液,加入20 mL去离子水后变为白色溶胶,说明钛酸四丁酯发生了水解。将混合液移入到100 mL聚四氟乙烯反应釜中,在170 ℃鼓风烘箱中反应24 h,自然冷却。反应后获得白色粉末产物,经洗涤、离心收集后在60 ℃鼓风烘箱中干燥。
2.3 表征
X射线衍射技术(XRD)采用Rigaku D/MAX-2550衍射仪(铜靶Kα,5° ≤ 2θ≤ 80°,Δ2θ=0.02°)。透射电镜(TEM)和高分辨透射电镜(HRTEM)分别采用JEOL JEM-1400和JEOL JEM-2100电子显微镜。热重(TG)分析使用耐驰STA 409PC热分析仪,氮气气氛下,升温速率为10 ℃/min。固体紫外-可见吸收光度(UV-Vis)分析采用美国瓦里安公司的Cary 500紫外分光光度计。光催化降解试验所用光源为CEL-HXF300 氙灯光源系统(中国,中教金源),采用TU-1810 紫外可见分光光度计(中国,北京普析)测试罗丹明B的紫外-可见吸收光谱。
2.4 光催化降解测试
取20 mg催化剂分散于60 mL罗丹明B(20 ppm)溶液中,将悬浮液置于黑暗中进行磁力搅拌吸附30 min,接着在光照下(420~780 nm)磁力搅拌,每隔10 min收集4 mL液体,将液体在8000 r/min下离心30 min,取上清液测量其在200~800nm波段的吸收光谱。
3 结果与讨论
钛酸四丁酯(Ti(OC4H9)4)极易水解,作为前驱物在水热条件下可水解生成TiO2。为了与TiO2-GO复合物进行比较,试验中制备了单一TiO2。图1(a)为TiO2的XRD,其衍射峰均可指标为锐钛矿结构TiO2(JCPDS 21-1272),表明了产物的纯度和晶体结构类型。根据谢乐公式(特征衍射峰为2θ= 25.3° )近似计算其平均粒径为6.4 nm。透射电镜图片(图1(b))为形状规则、大小均一TiO2的纳米颗粒,粒径为几个纳米,且无团聚。
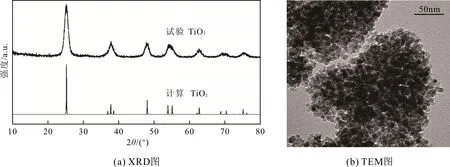
图1 TiO2纳米粒子的XRD图和TEM图
图2为制备的GO片和一系列TiO2-GO复合物(TiO2-10%GO、TiO2-20%GO、TiO2-30%GO、TiO2-40%GO和TiO2-50%GO)的XRD图,显示了样品的物相纯度和晶体结构类型。如图2所示,GO在2θ= 8.6°处的衍射峰对应其10.3Å的层间距,表明了GO的层状堆砌结构特点。对于TiO2-GO复合物,在2θ= 25.3°、37.8°、48.0°、53.9°、55.1°、62.7°、68.8°、70.3°和75.1°处的衍射峰分别对应锐钛矿型TiO2的 (101)、(004)、(200)、(105)、(211)、(204)、(116)、(220)和(215)晶面。利用谢乐公式(特征衍射峰为2θ= 25.3°)近似计算得到TiO2-GO复合物中TiO2粒子的平均粒径分别为7.2 nm(TiO2-10%GO)、6.8 nm (TiO2-20%GO)、6.7 nm (TiO2-30%GO)、6.5 nm(TiO2-40%GO)和6.5 nm(TiO2-50%GO),表明GO含量的变化不会影响TiO2的晶体结构类型和颗粒大小。
图3(a)为GO的HRTEM图片,从图3(a)中可观察到GO特有的片层结构。图3(b)为TiO2-30%GO复合物的HRTEM图片,图3(b)中大片层GO清晰可见,形状规则、大小均一的TiO2纳米粒子均匀分散在GO片层上,其粒径为几个纳米,与单一TiO2纳米粒子没有明显差异,说明GO的片层结构可作为TiO2纳米颗粒的良好载体,为TiO2晶核的生成和长大提供活性点位。GO的引入不但不会影响TiO2纳米颗粒的形貌和尺寸,且能使TiO2具有更好的分散性。拉曼光谱进一步给出了物相组分和结构的相关信息,图3(c)中,TiO2拉曼光谱在低频处的4个拉曼峰分别对应锐钛矿结构TiO2的E1g(148 cm-1),B1g(401 cm-1),A1g(519 cm-1) 和Eg(642 cm-1)振动模式。与TiO2纳米粒子相比,TiO2-30%GO复合物的E1g(150 cm-1)峰发生了红移,而B1g(399 cm-1),A1g(517 cm-1)和Eg(640 cm-1)拉曼峰略有蓝移(图3(c)中的小插图),表明GO的碳原子与TiO2之间存在强的相互作用。TiO2-30%GO复合物在1 342 cm-1和 1 606 cm-1处的拉曼峰分别对应GO上sp3杂化碳原子振动的特征峰(D带)和sp2杂化碳原子振动的特征峰(G带)[16],而单一TiO2没有这两个拉曼峰。TiO2-30%GO复合物的TG分析结果(图3(d))显示从室温到 80 ℃加热区间样品质量损失约为5 %,主要是由样品中吸附的水随温度升高挥发造成的,150~1000 ℃加热区间,样品质量损失约为22 %,归因于GO的分解。TG结果也进一步证明了该样品中GO的质量约为TiO2质量的30 %,与称量配比的理论计算结果一致,说明钛酸四丁酯全部水解生成TiO2,没有明显的原料损失。
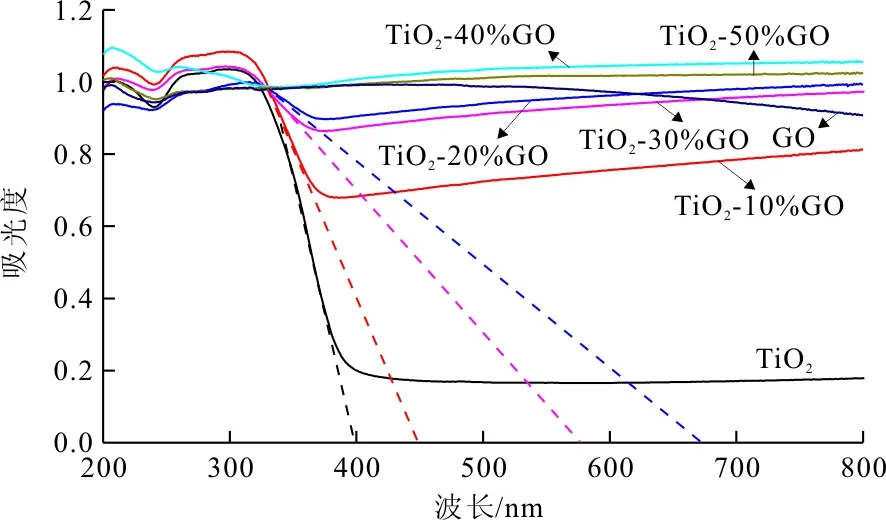
图4为TiO2纳米粒子,GO片层以及TiO2-GO复合物的紫外-可见吸收光谱。从图4中可以看到TiO2纳米粒子的吸收边在400 nm附近,主要吸收紫外光,对可见光的吸收能力非常弱。而GO在可见光区(400~800 nm)具有强的吸收,对应于它的表观颜色(黑色)。与单一TiO2纳米粒子相比,TiO2-GO复合物对可见光的吸收明显增强,并且吸收强度随GO含量的增加而提高,对应于样品的颜色逐渐加深。其中,TiO2-10%GO、TiO2-20%GO和TiO2-30%GO的吸收边分别在450 nm,575 nm和670 nm附近;而TiO2-40%GO和TiO2-50%GO在整个紫外-可见区域均有较强的吸收,没有明显的吸收边,结果表明TiO2与GO之间强相互作用会影响其光学性能。

图2 具有不同质量比的TiO2-GO复合物的XRD花样
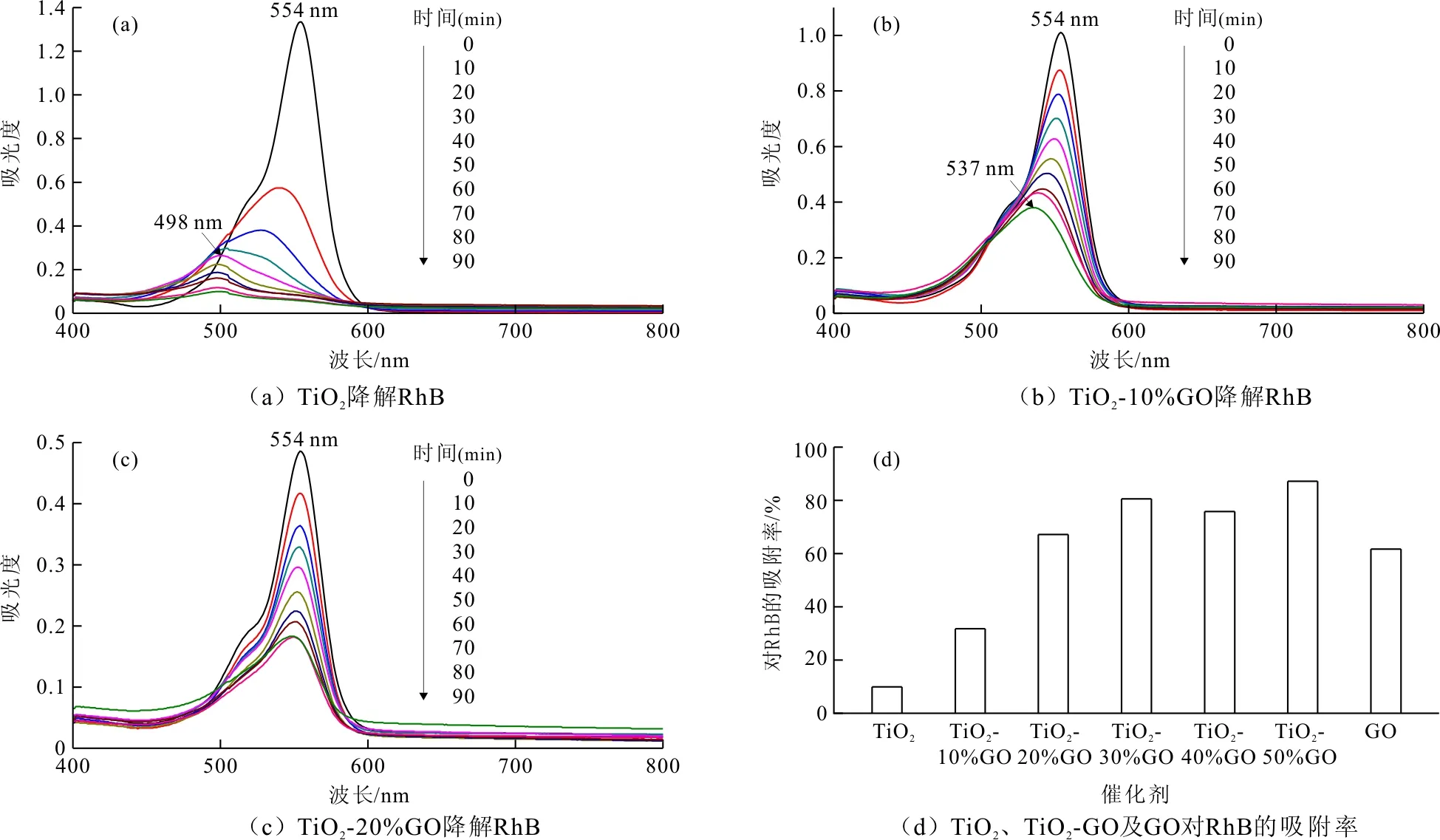
在去除水中有机污染物的过程中,TiO2纳米粒子和TiO2-GO复合物表现出不同的光催化降解机制和去除效率。图5(a)为TiO2纳米粒子在可见光(420~780 nm)照射下催化降解有机染料罗丹明B,在线监测的紫外-可见吸收光谱图。从图5(a)中可以看出,光照10 min后,罗丹明B在554 nm处的特征吸收峰明显减弱,光照40 min后,吸收峰蓝移到498 nm,这是罗丹明B在降解过程中产生的中间产物的特征吸收峰。随着光催化降解的继续进行,498 nm处的吸收峰逐渐减弱,光照90 min后,罗丹明B及其中间产物的吸收峰都基本消失,说明在TiO2光降解罗丹明B过程中,罗丹明B经中间产物后被进一步降解[17-18]。在试验中观察到罗丹明B溶液的颜色从粉红色逐渐变为黄绿色,最后变为无色,与其特征吸收峰的蓝移、减弱变化趋势对应。检测结果表明,虽然TiO2本身对可见光利用率极低,但易被有机染料敏化从而实现在可见光区对染料的有效降解。在TiO2-GO光催化降解体系中,罗丹明B溶液的颜色在降解过程中逐渐变浅,但没有观察到颜色的转变,说明TiO2-GO复合物与TiO2纳米粒子在降解罗丹明B时具有不同的反应机制,通过罗丹明B紫外-可见吸收谱的变化情况可以进一步证明这一点。如图5(b)所示,在TiO2-10%GO存在情况下,罗丹明B的特征吸收峰(554 nm)随时间逐渐减弱,光照90 min内只发生了微小的蓝移,从554 nm(0 min)移到537 nm(90 min)。当复合物中GO的含量进一步增加时则完全观察不到罗丹明B特征吸收峰蓝移的现象。如在TiO2-20%GO光催化降解体系,从图5(c)中只观察到554 nm处的吸收峰随光照时间逐渐减弱,但没有出现新的吸收峰,说明TiO2-20%GO直接将罗丹明B的发色基团进行分解,而没有经过复杂的中间产物[18]。
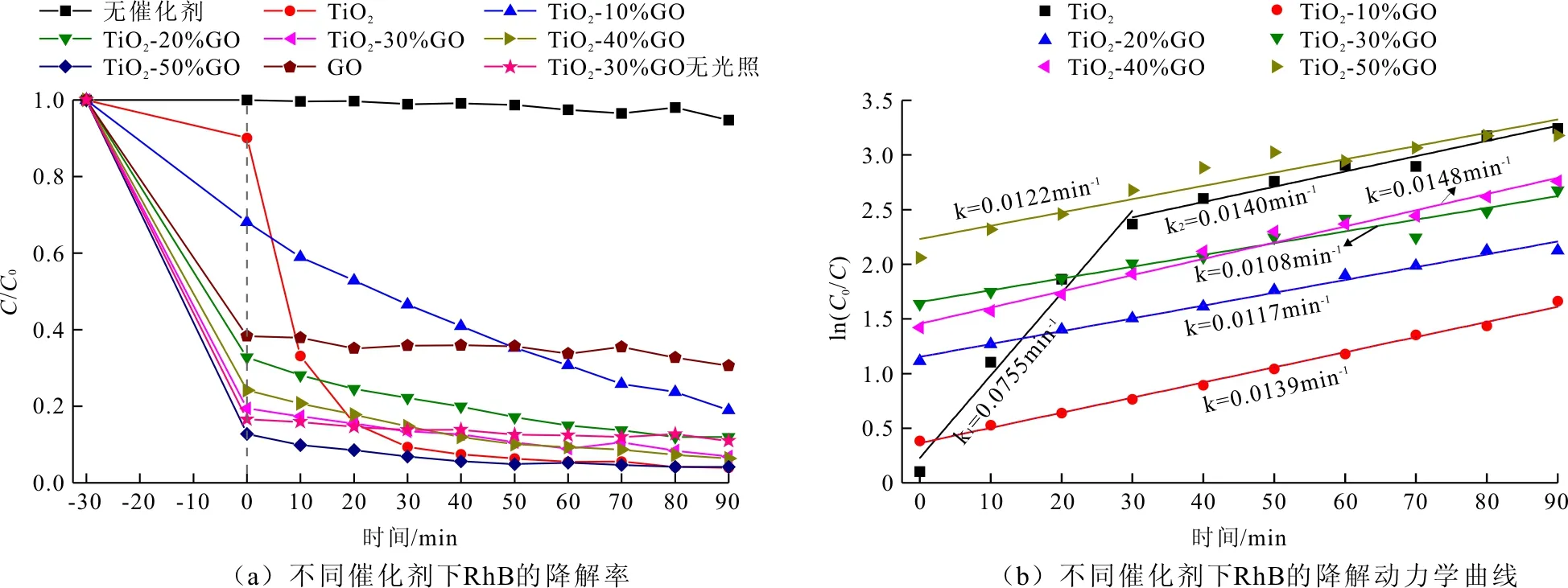
GO的引入不仅会改变TiO2降解水中有机污染物的机制,还会影响对污染物的吸附率。图5(d)为TiO2纳米粒子,GO片层以及TiO2-GO复合物(TiO2-10%GO、TiO2-20%GO、TiO2-30%GO、TiO2-40%GO和TiO2-50%GO)在光照前(即黑暗中搅拌30 min后)对罗丹明B的吸附率,从图5(d)中可以看到,TiO2-GO对罗丹明B的吸附率远远高于TiO2纳米粒子,这主要是由于GO丰富的表面化学结构和大的比表面积有利于吸附污染物。随GO含量的增加,TiO2-GO对罗丹明B的吸附率逐渐增加,但增加的幅度逐渐变小,而纯GO片层对罗丹明B的吸附率只高于TiO2-10%GO而低于TiO2-20%GO、TiO2-30%GO、TiO2-40%GO和TiO2-50%GO,吸附率由小到大的顺序为:TiO2纳米粒子 < TiO2-10%GO 图6(a)显示的是在光催化过程中,随着降解时间的延长,在不同催化剂(TiO2纳米粒子、GO片层以及一系列TiO2-GO复合物)存在下罗丹明B的降解效率。其中,C0代表罗丹明B的初始浓度,C为各个间隔时间段罗丹明B的浓度。两个对比实验分别为在没有催化剂存在下光照中罗丹明B的自降解以及在TiO2-30%GO体系中没有光照下罗丹明B的降解。从图6(a)中可以看到,在没有催化剂情况下,罗丹明B在90 min光照内浓度几乎不变,说明没有发生自降解。TiO2纳米粒子对罗丹明B的吸附性较差,但在光照下降解效率很高,60 min内几乎将溶液中的罗丹明B全部降解。GO对罗丹明B具有一定吸附性,当吸附量达到饱和时,光照下溶液中罗丹明B的浓度没有明显变化,说明GO本身没有光催化活性。 TiO2-GO复合物对罗丹明B具有较强的吸附性,在光照条件下对罗丹明B具有一定的降解效率,其中TiO2-50%GO在60 min内几乎将溶液中的罗丹明B全部去除。在TiO2-30%GO体系中,对比有、无光照两种情况,发现在光照下罗丹明B的浓度具有一定程度的降低,而无光照下罗丹明B浓度变化很小,进一步表明TiO2-GO复合物具有一定光催化活性。 TiO2纳米粒子和TiO2-GO复合物光催化降解罗丹明B的过程均符合一级动力学方程 ln(C0/C)=kt (1) 式中:k为动力学常数,t为反应时间。 图3 GO和TiO2-30%GO的HRTEM图,TiO2和TiO2-30%GO的拉曼光谱以及TiO2-30%GO的TGA曲线 图4 TiO2纳米粒子、GO片层以及一系列具有不同质量比的TiO2-GO复合物的紫外-可见吸收谱 图6(b)为可见光照射下,TiO2纳米粒子和TiO2-GO复合物降解罗丹明B的动力学曲线。其中,TiO2纳米粒子在光降解罗丹明B时有两个动力学过程,前30 min的动力学常数(k1= 0.0755 min-1)明显大于后60 min的动力学常数(k2=0.0140 min-1),说明在TiO2纳米粒子光降解罗丹明B过程中存在两个光催化降解机制,这与罗丹明B特征吸收峰随光照时间的变化趋势相对应。TiO2-GO复合物在光降解罗丹明B过程中只有一个动力学常数,分别为0.0139、0.0117、0.0108、0.0148和0.0122 min-1,与TiO2纳米粒子体系中的k2接近,并且几乎不受GO含量的影响,说明GO的含量可显著影响复合物对有机染料的吸附性和对可见光吸收但不会影响复合物的光催化活性。 图5 TiO2和TiO2-GO复合物降解罗丹明B在线监测的紫外-可见吸收光谱以及光照前对罗丹明B的吸附率 图6 TiO2和TiO2-GO复合物降解罗丹明B的动力学分析图 (1)采用水热法成功制备了TiO2-GO复合物,并对GO以不同的TiO2质量比进行了调控。 (2)研究发现在去除水中污染物方面,GO的引入大大提高了TiO2纳米粒子对水中有机污染物的吸附量;而TiO2纳米粒子存在于GO片层之间可有效抑制GO的团聚,从而保证随GO含量的增加,复合物的吸附性能逐渐增强。在光响应方面,GO的引入使TiO2-GO复合物对可见光的吸收显著增强,提高了材料对可见光的利用率。 (3)与单一成分相比,TiO2纳米粒子与GO片层复合后增强了材料对污染物吸附与光降解的协同作用,其综合效果大大提高了去除水中污染物的效率,在环境净化中具有巨大的应用前景。
4 结 论
