乳腺癌中GFRA1表达临床意义的生物信息学分析
2018-09-11
乳腺癌是女性肿瘤中最具侵袭性的恶性肿瘤,为女性肿瘤相关死亡的主要病因。2008年,中国约17万例女性患者被诊断为乳腺癌,占全世界的12.2%,预计到2021年,中国乳腺癌患者将高达250万例,女性发病率将从不到60例/10万增加到超过100例/10万[1]。2012年,我国约有52.2万例女性死于乳腺癌,其死亡人数约占全球癌症相关死亡人数的15%[2]。目前,乳腺癌是中国女性发病率最高的癌症,位居癌症死亡率第六。虽然乳腺癌的诊疗已取得较大进展,但乳腺癌的死亡率仍居高不下。因此,探讨可以作为乳腺癌诊断、治疗的靶点基因和蛋白具有重大临床价值。胶质细胞系源性神经营养因子受体 1(glial cell line derived neurotrophic factor α1,GFRA1)可以在乳腺癌导管和腺泡细胞质中检测到,与乳腺癌淋巴结转移、TNM分期和HER−2表达相关,与乳腺癌预后呈负相关[3]。通过GDNF体外刺激,GFRA1可显著促进乳腺癌细胞的增殖、存活和分散,可能是与炎性细胞因子TNF−α和IL−1β协同上调GDNF,活化GFRA1通路,促进乳腺癌的侵袭与转移有关[4]。目前缺少全面分析乳腺癌中GFRA1表达临床价值的研究,因此本研究旨在通过生物信息学分析GFRA1在乳腺癌组织中表达情况,及其预测乳腺癌治疗、预后的价值。
1 材料与方法
1.1 数据来源和方法
基于Oncomine数据库(https://www.oncomine.org/)分析GFRA1在乳腺癌组织中表达情况。以“GFRA1 and breast”在 GEO 数据库(https://www.ncbi.nlm.nih.gov/geoprofiles)进行检索。纳入GFRA1在乳腺癌组织、化疗及内分泌治疗耐药细胞株、敏感细胞株中表达水平的表达数据,以及GFRA1预测新辅助化疗中病理完全缓解(pathologic complete response,pCR)率的数据。
基于 TCGA(The Cancer Genome Atlas)数据库(https://cancergenome.nih.gov/)分析GFRA1在乳腺癌患者癌组织与健康人正常乳腺组织间、不同临床TNM分期、不同分子分型乳腺癌患者癌组织中的差异,分析GFRA1表达水平与ER、PR、HER−2、Ki−67表达水平的关系。
基于Kmplot数据库(http://kmplot.com/analysis/)分析GFRA1表达水平与乳腺癌总生存(overall survival,OS)率和无复发生存(recurrence free survival,RFS)率的关系,数据以危险比(hazards ratio,HR)和95%可信区间(95%confidence interval,95%CI)表示。
1.2 统计学分析
使用SPSS 21.0软件进行统计学分析。计量数据以均数±标准差(x±s)表示,采用t检验进行比较。统计检验均采用双侧检验,P<0.05为差异具有统计学意义。
2 结果
2.1 乳腺癌组织中GFRA1表达情况
基于Oncomine数据库,对6个研究[5−10]中乳腺癌患者癌组织中GFRA1表达水平进行分析,结果显示,不同病理类型乳腺癌(浸润性小叶癌、浸润性导管癌、导管原位癌)患者癌组织中均表达GFRA1,且显著高于健康人正常乳腺组织中GFRA1表达水平(P<0.05,表1)。
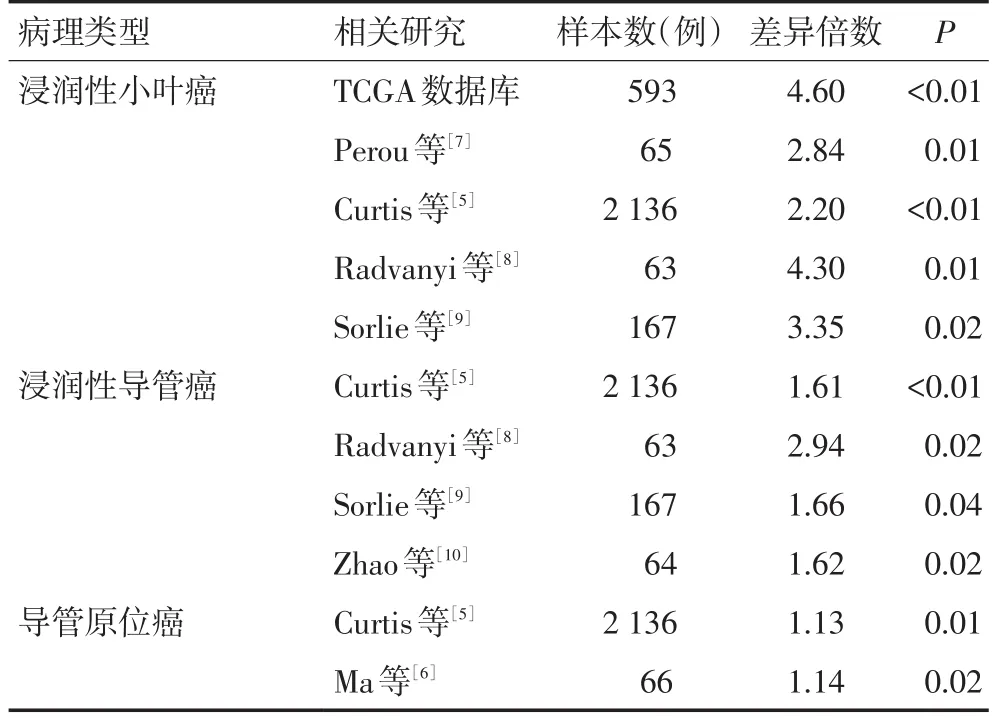
表1 不同病理类型乳腺癌组织与健康人乳腺正常组织中GFRA1表达差异
基于TCGA数据库进行分析,结果显示,乳腺癌患者癌组织中GFRA1表达水平明显高于健康人正常乳腺组织(P<0.05)。TNM临床分期中Ⅰ、Ⅱ、Ⅲ期乳腺癌患者癌组织中GFRA1表达水平显著高于健康人正常乳腺组织(P<0.05),Ⅳ期乳腺癌患者癌组织中GFRA1表达水平与健康人正常乳腺组织中的表达水平差异无明显统计学意义(P>0.05)。Luminal型乳腺癌患者癌组织中GFRA1表达水平显著高于健康人正常乳腺组织(P<0.05),HER−2过表达型、三阴性乳腺癌患者癌组织中GFRA1表达水平明显低于健康人正常乳腺组织(P<0.05,图1)。
基于GEO数据库进行分析,结果发现,ER阳性、PR阳性乳腺癌患者癌组织中GFRA1表达水平明显高于对应受体阴性者(P<0.05),但HER−2阳性乳腺癌患者癌组织中的GFRA1表达水平显著低于HER−2阴性者(P<0.05),GFRA1表达水平与淋巴结转移无相关性(P>0.05,表2)。
基于TCGA数据库分析结果显示,GFRA1表达水平与ER(r=0.66,P<0.05)、PR(r=0.22,P<0.05)表达水平呈正相关,与HER−2(r=−0.09,P<0.05)、Ki−67(r=−0.12,P<0.05)表达水平呈负相关。
2.2 GFRA1表达水平与pCR的关系
基于GEO数据库,对达到与未达到pCR的乳腺癌患者组织中GFRA1表达水平比较发现,大部分研究中两者差异无统计学意义(P>0.05),但GFRA1低表达的乳腺癌患者更易达到pCR。这说明GFRA1低表达乳腺癌患者可能对化疗高敏感(表3)。
2.3 GFRA1表达水平与化疗、内分泌治疗、靶向治疗耐药的关系
基于GEO数据库,对GFRA1表达水平与化疗、内分泌治疗、靶向治疗耐药关系进行分析,结果显示,多西他赛耐药细胞株与敏感细胞株中GFRA1表达水平差异无统计学意义(P>0.05),在拉帕替尼耐药细胞株与敏感细胞株中表达水平差异亦无统计学意义(P>0.05),但在他莫昔芬耐药细胞株和敏感细胞株中表达水平差异具有统计学意义(P<0.05),他莫昔芬耐药细胞株中GFRA1表达水平显著低于敏感细胞株(P<0.05)。多柔比星耐药细胞株中GFRA1表达水平(3.91±0.06)显著低于正常细胞株(9.47±0.23),两者表达水平比较差异具有统计学意义(P=0.01,表4)。
2.4 GFRA1表达水平与乳腺癌的预后关系
分析Kmplot数据库发现,1 402例乳腺癌患者有OS数据,626例患者有GFRA1表达水平数据,GFRA1基因片段205696_s_at(HR为0.69,95%CI为0.55~0.85)、227550_at(HR为0.58,95%CI为0.42~0.79)、230163_at(HR为0.53,95%CI为0.38~0.72)高表达水平的患者具有较高的OS(P<0.05)。3 955例乳腺癌患者有RFS数据,1 764例乳腺癌患者有GFRA1表达水平数据,统计分析发现,GFRA1基因片段205696_s_at(HR为0.71,95%CI为0.63~0.79)、227550_at(HR为0.56,95%CI为0.48~0.65)、230163_at(HR为0.56,95%CI为 0.48~0.66)高表达水平的患者具有较高的RFS(P<0.05,图2)。
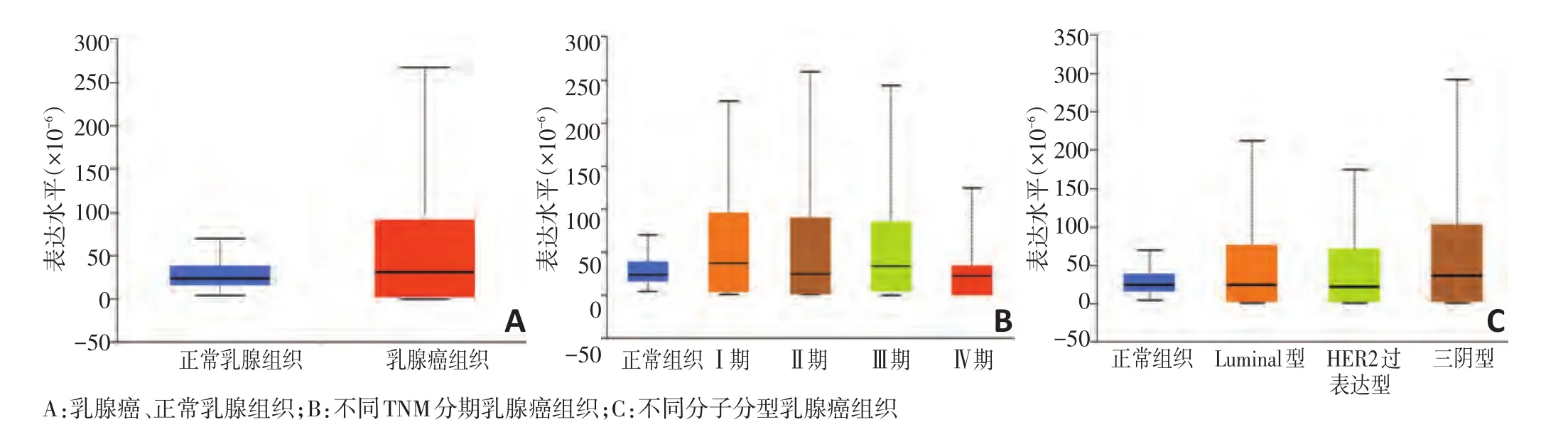
图1 基于TCGA数据库分析乳腺癌组织中GFRA1的表达
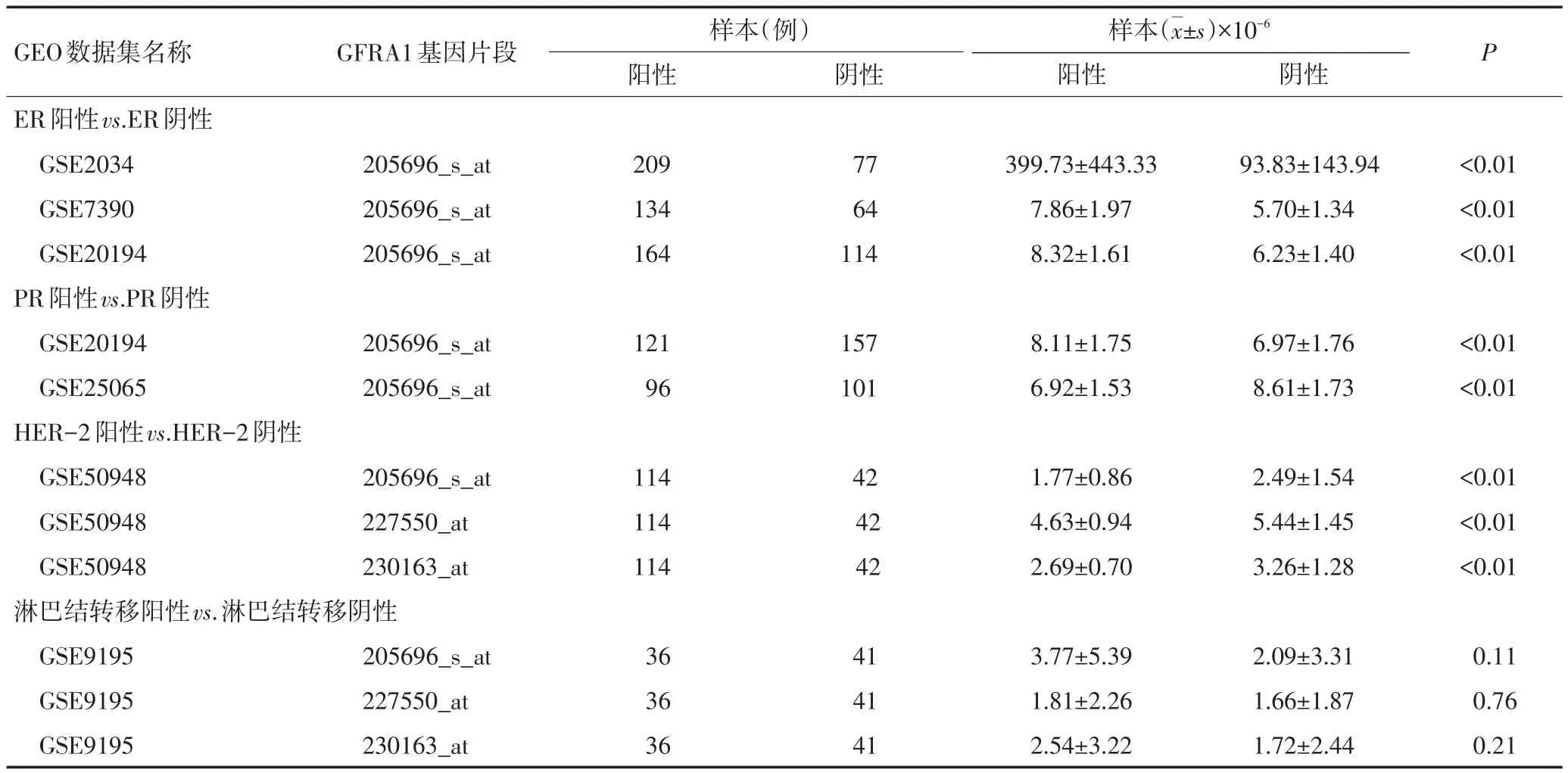
表2 不同受体与有无淋巴结转移乳腺癌患者癌组织中的GFRA1表达水平比较
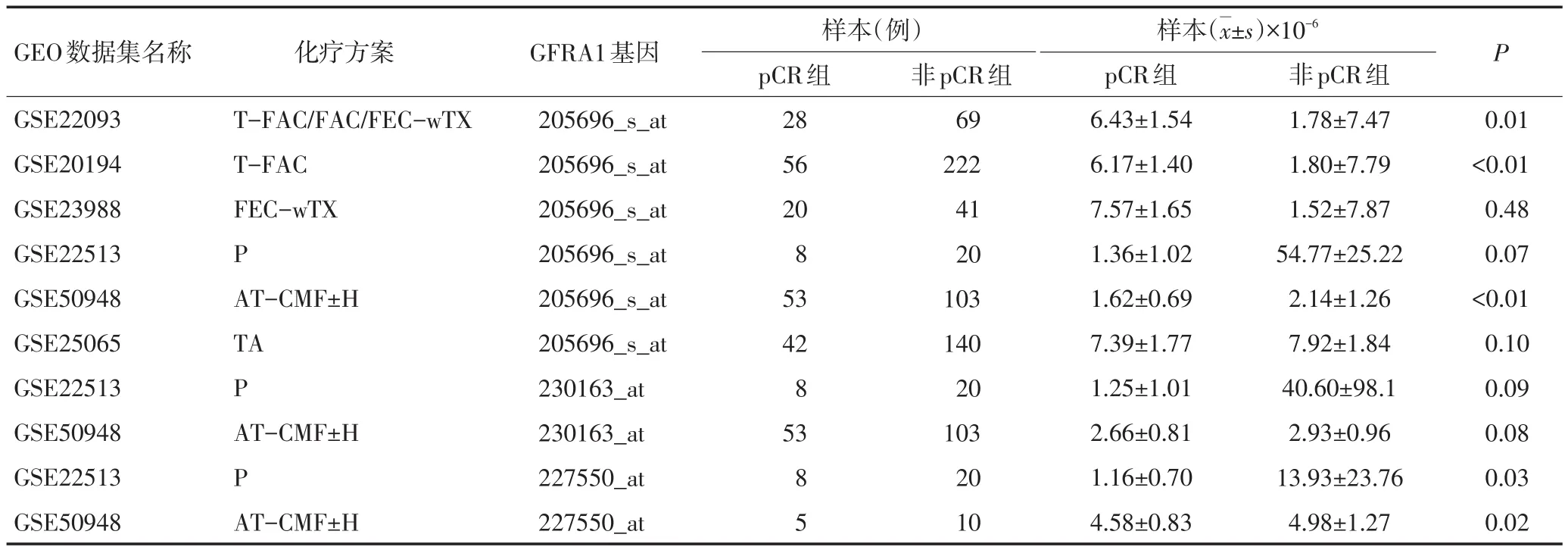
表3 GFRA1表达水平与pCR的关系
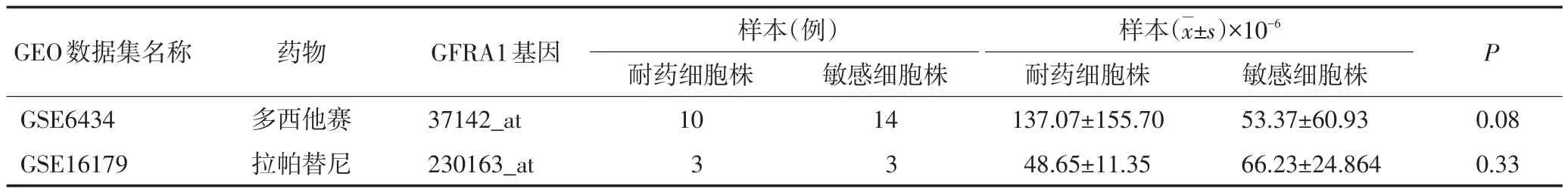
表4 GFRA1表达水平与化疗、内分泌治疗、靶向治疗耐药的关系
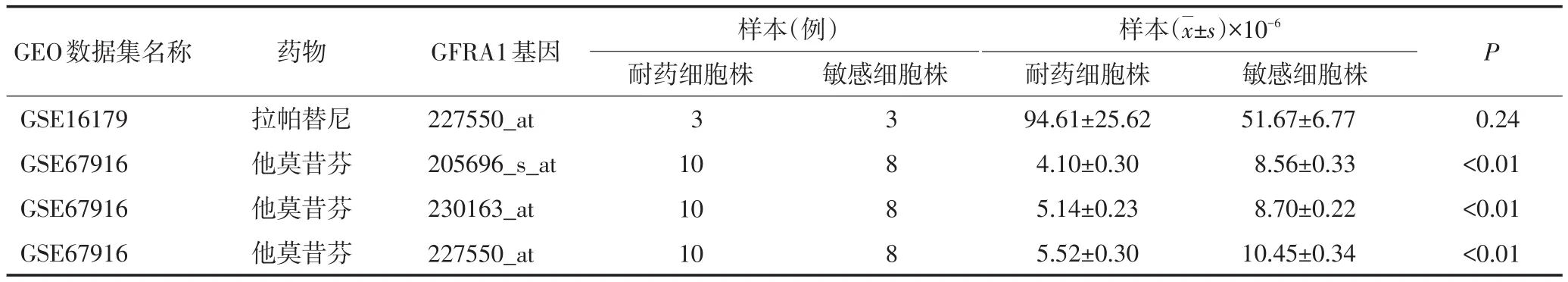
表4 GFRA1表达水平与化疗、内分泌治疗、靶向治疗耐药的关系(续表4)
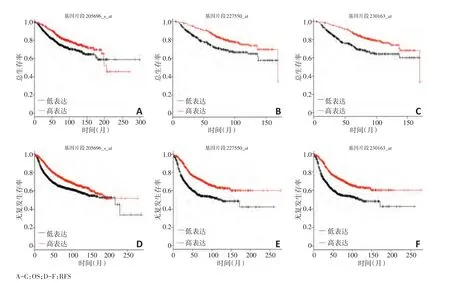
图2 GFRA1基因片段与乳腺癌预后的关系
3 讨论
本研究结果显示,GFRA1在乳腺浸润性导管癌、浸润性小叶癌、导管原位癌患者癌组织中高表达。GFRA1表达水平与ER、PR表达水平呈正相关,与HER−2、Ki−67表达水平呈负相关。Bhakta等[11]分析了113例乳腺癌组织发现,70%Luminal A型表达GFRA1,13%三阴性乳腺癌表达GFRA1,3.5%HER−2过表达型表达GFRA1。Wu等[3]分析了159例乳腺癌患者和26例良性乳腺疾病患者,结果显示GFRA1表达水平在乳腺癌组织中显著升高,与淋巴结转移、高临床分期、HER−2阳性状态相关。Esseghir等[4]发现乳腺癌组织中GFRA1高表达,在细胞膜上表达,GFRA1 mRNA与淋巴管浸润、淋巴结转移、ER、PR表达水平呈正相关,与EGFR、p53、MIB1表达水平呈负相关。
乳腺癌术后的治疗措施有化疗、内分泌治疗、放疗和靶向治疗,但这些治疗措施并不能避免复发和转移,只在一定程度上延缓疾病的复发和转移。化疗是乳腺癌主要治疗措施之一,GFRA1表达水平是否可以预测化疗疗效也是本研究的目的之一。Evans等[12]研究显示,GFRA1自身抗体可作为评估乳腺癌治疗效果的指标之一。基于新辅助化疗数据,GFRA1低表达乳腺癌患者易达到pCR,但是大部分研究差异无统计学意义,提示GFRA1表达水平预测pCR的价值存在争议。在多柔比星乳腺癌耐药细胞株中,GFRA1表达水平显著下调,说明GFRA1可能参与多柔比星的化疗耐药。
内分泌治疗是ER阳性乳腺癌患者的常用方案,主要包括卵巢功能抑制、抗雌激素药物(他莫昔芬、托瑞米芬)、孕激素、雄激素、芳香化酶抑制剂(aroma⁃tase inhibitors,AI)。本研究显示,他莫昔芬乳腺癌耐药细胞株中GFRA1低表达,说明GFRA1可能参与内分泌治疗耐药。AI耐药的细胞模型中GDNF信号显著增强,这可能是GDNF−RET信号通路的激活能促进AI耐药细胞的存活,并诱发AI敏感细胞的内分泌治疗抵抗[13]。因此,GFRA1可能参与乳腺癌内分泌治疗耐药。
GFRA1抗体与乳腺癌发生呈负相关,可作为乳腺癌筛选的标志物之一[14]。Bhakta等[11]研制出裂解缬氨酸瓜氨酸偶联的GFRA1抗体,可内化到溶酶体,发挥靶向杀伤肿瘤细胞的作用。70%Lumina A型乳腺癌表达GFRA1,裂解缬氨酸瓜氨酸偶联的GFRA1抗体是新型的靶向药物,可以靶向杀伤Luminal A型乳腺癌细胞,改善其预后。Wu等[3]分析了159例乳腺癌和26例良性乳腺疾病患者,结果显示GFRA1与乳腺癌预后呈负相关,GFRA1表达水平与ER、HER−2阳性乳腺癌患者的OS和RFS无关,与ER、HER−2阴性乳腺癌患者的OS和RFS呈负相关。本研究显示,GFRA1高表达患者的OS和RFS高于低表达患者。GFRA1表达水平与乳腺癌患者预后显著相关,可以作为预测乳腺癌预后的标志物之一。
本研究对GFRA1在乳腺癌诊断、治疗和预后判断中的价值进行全面系统评估,基于生物信息学和大数据全面详细分析GFRA1在乳腺癌中的临床价值。本研究仍存在以下局限性:1)本研究纳入的人群为乳腺癌患者,来自于不同的国家地区,存在一定的异质性。2)本研究仅分析GFRA1相关临床研究结果,未对结果进行合并,因此未进行批次校正,在一定程度上可能影响结果的准确性。3)基因芯片可能存在多个不同的基因片段,不同的基因片段的结果可能不一样。
综上所述,GFRA1在乳腺癌组织中高表达,在不同类型乳腺癌中表达存在差异。GFRA1低表达的乳腺癌患者对他莫昔芬和多柔比星可能耐药,且预后较差。GFRA1表达水平可以作为乳腺癌筛选、预后预测的标志物之一。
