足踝手术中超声引导腘窝坐骨神经阻滞最佳给药部位的临床研究
2018-09-10蔡光玉罗俊杰凌丹丹陈小瑞
张 娜, 蔡光玉, 罗俊杰, 凌丹丹, 陈小瑞, 余 斌
(同济大学附属同济医院麻醉科,上海 200065)
超声引导腘窝坐骨神经阻滞技术在足踝手术中现已广泛应用[1-2],有研究[3]表明,神经鞘膜下比神经旁鞘外注射局部麻醉药获得阻滞起效时间更短,阻滞成功率更高。但关于鞘膜下局部麻醉药的精准用量及术后镇痛效果的相关研究还未见报道。本研究对接受足踝手术的患者实施单侧连续腘窝坐骨神经阻滞,通过神经传导监测技术比较鞘膜下与鞘膜外注药坐骨神经传导达到完全阻滞所需时间、局部麻醉药的精准用量、术后镇痛效果、患者满意度及神经损伤等并发症,探讨足踝手术腘窝坐骨神经阻滞的最佳给药部位及局部麻醉药剂量,为今后临床应用提供参考。
1 资料与方法
1.1 一般资料
选择同济大学附属同济医院2016年5月—2017年4月择期行单侧足踝手术患者40例。本试验方案通过同济大学附属同济医院伦理委员会批准,患者同意参加本试验并签署知情同意书。入选标准: 美国麻醉医师协会(American Society of Anesthesiologists, ASA)分级Ⅰ~Ⅲ级,年龄18~65岁,男女不限。排除标准: 有严重心肺疾患的患者,有严重精神或神经系统疾病者,手术侧下肢肌肉、神经有病变者,糖尿病神经病变及穿刺部位有感染者。应用简单随机化分组将40例患者分为神经鞘膜外注药组(W组,n=20例)和神经鞘膜下注药组(X组,n=20例)。
1.2 实验方法
1.2.1 麻醉前准备 患者入室后监测血压、脉搏、血氧饱和度和心电图,给予吸氧、输液等辅助支持,静脉泵注右美托咪定镇静,首先给予负荷量0.8μg/kg,10min内注射完,然后改为0.3μg/(kg·h)维持泵注。
1.2.2 神经阻滞 两组患者均取患肢在上侧卧位,暴露腘窝,将超声探头短轴置于坐骨神经分为腓总神经和胫神经处。X组将新型连续神经阻滞套管针(20G,河南驼人集团)朝向足侧与皮肤约成30°~45°角从超声探头下方、腓总神经和胫神经之间进针,并在超声引导下将针尖放置于腓总神经和胫神经之间靠近底部。注射少量生理盐水观察针尖位置,可见神经无肿胀且生理盐水在鞘膜下扩散包裹在神经周围,则位置正确。然后退出针芯,外套管留置不动,回抽无血并注液无阻塞后使用贴膜固定。W组超声探头放置位置同上,但新型连续神经阻滞套管针紧靠坐骨神经外侧缘进针,角度朝向头侧,在超声图像中可观察针尖位置到达坐骨神经外侧缘,注射少量生理盐水可见其未在鞘膜下扩散包裹在神经周围,神经无肿胀,则位置正确。退出针芯,将外套管留置在坐骨神经外侧缘并贴膜固定。为减轻大腿止血带反应及某些涉及足踝内侧切口的止痛,对两组患者均实施股神经阻滞。
1.2.3 神经传导监测 实施神经传导监测(nerve conduction study, NCS)技术,在超声引导下,在神经阻滞点头端5cm处的坐骨神经上刺入两根针状刺激电极,针尖位于距离坐骨神经约2mm的正上方,记录电极采用贴片电极,分别放置于腓肠肌腹及肌腱处,参考电极置于刺激和记录电极之间。连接神经电生理监测设备,开启并调整刺激电流,记录诱发出的未给局部麻醉药时的最大肌肉动作电位波幅。然后单次推注负荷剂量1.5%利多卡因5mL快速包裹神经,8min后再次行神经传导检查,若此时肌肉动作电位波幅仍存在,通过留置的新型神经阻滞套管以30mL/h速度持续泵注1.5%利多卡因,并每2min 后再次进行神经传导检查,直至记录到的肌肉动作电位波幅为0~0.5mV且针刺足部皮肤痛觉消失,此时停止输注利多卡因,记录输注利多卡因剂量和输注开始到停止的时间。X组实验方法如图1所示,W组实验方法如图2所示。肌电图诱发电位仪和电极等购自上海诺诚电气有限公司,术中使用超声仪购自美国Sonosite公司。
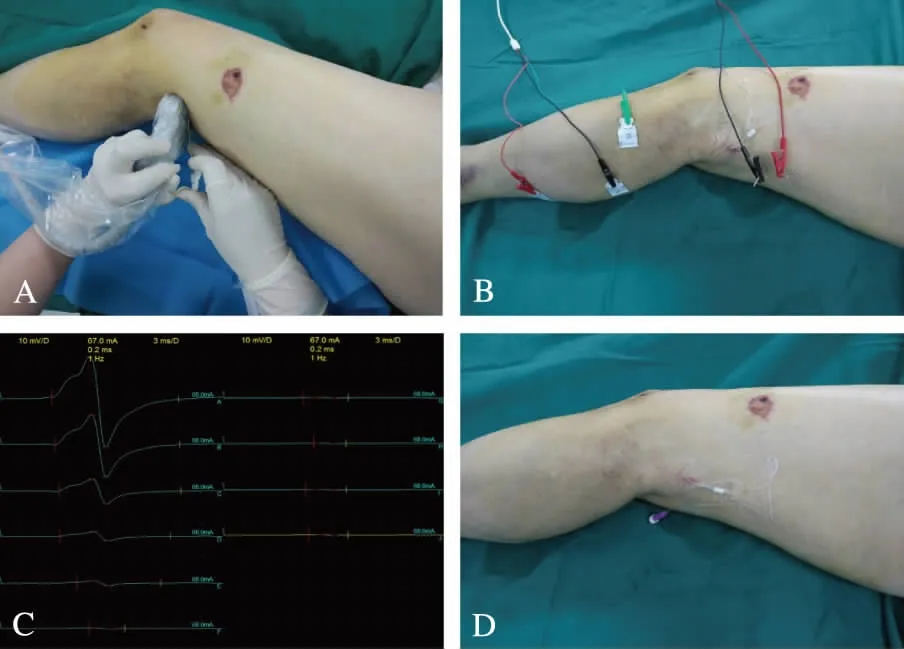
图1 神经鞘膜下入路穿刺置管Fig.1 The approach of subparaneural blockA: 超声引导下坐骨神经鞘膜下进针;B: 神经传导监测;C: 动作电位波幅变化;D: 留置神经阻滞导管并固定
停止输注后两组患者即开始消毒铺巾进行手术操作,患肢上止血带,压力250mmHg(1mmHg=0.133kPa),当手术时间较长而患者不能耐受止血带,可加大右美托咪定泵注速度和静脉泵注少量丙泊酚予镇静。手术结束后经留置的神经阻滞导管连接电子镇痛泵(ZZB-Ⅱ,南通爱普医疗器械有限公司)行患者自控镇痛(patient controlled analgesia, PCA),药物配方为0.2%罗哌卡因共300mL,参数调节: 首剂0mL,持续量5mL/h,单次3mL,锁时20min,最大量25mL/h,术后镇痛时间为48h。术后及随访时若出现留置导管堵塞可先用生理盐水疏通或调整留置导管位置,无效者可将留置导管拔出0.5~1cm,再无效者与患者沟通后予留置导管拔除并更换为其他镇痛方式并进行记录。患者术后感疼痛时,可按压镇痛泵,无效时可静注帕瑞昔布钠。
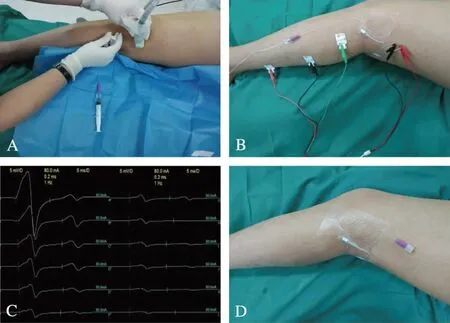
图2 神经鞘膜外入路穿刺置管Fig.2 The approach of extraparaneural blockA: 超声引导下坐骨神经鞘膜外进针;B: 神经传导监测;C: 动作电位波幅变化;D: 留置神经阻滞导管并固定
1.3 实验观察指标
两组患者坐骨神经传导完全阻滞时的局部麻醉药用量;腘窝分支处坐骨神经直径;神经传导完全阻滞所需时间;手术时间;术后镇痛效果(包括局部麻醉药用量、PCA次数、静止和活动时疼痛评分),术后并发症(导管渗漏、堵塞、滑出例数,恶心呕吐评分,0~24、24~48h使用止痛药例数),患者满意度评分。术后随访期间观察是否存在感觉运动异常等神经损伤。疼痛数字评分法(numerical rating scale, NRS)由0~10间隔相同的11个数字组成。0分: 无痛;1~3分: 轻度疼痛(疼痛不影响睡眠);4~6分: 中度疼痛;7~9分: 重度疼痛(不能入睡或睡眠中痛醒);10分: 剧痛。分别对静息时及肢体活动时进行NRS疼痛评分。患者满意度评分采用10分法: 0~10分,0分为最不满意,10分为最满意。
1.4 统计学处理
2 结 果
2.1 两组患者一般资料比较
两组患者一般资料,包括年龄、性别、身高、体质量、ASA分级比较,差异无统计学意义(P>0.05),见表1。

表1 两组患者一般资料Tab.1 General condition of patients
2.2 两组患者坐骨神经直径、局部麻醉药用量及神经完全阻滞所需时间比较
两组患者监测混合肌肉动作电位波幅下降0~0.5mV后开始消毒铺巾,手术均顺利完成,术毕通过腘窝处留置的连续神经阻滞导管镇痛。神经的直径影响局部麻醉药物在其中的扩散速度并直接影响到神经阻滞的效果。通过超声下测量,两组腘窝分支处坐骨神经直径分别如下表,差异无统计学意义(P>0.05)。X组与W组比较,完全阻滞所需局部麻醉药量[(10.9±1.7)mLvs(16.1±1.2)mL]和完全阻滞耗时[(19.9±3.5)minvs(30.3±2.5)min]差异有统计学意义(P<0.05)。两组手术时间比较差异无统计学意义(P>0.05),见表2。

表2 神经完全阻滞所需时间、局部麻醉药用量、手术时间及坐骨神经直径比较Tab.2 Comparison of the time of motor nerve block、Preoperative local anesthetics dosage、 time of operation and the diameter of sciatic nerve
与同时间点X组相比,*P<0.05
2.3 两组术后镇痛泵局部麻醉药用量、PCA按压次数及疼痛NRS评分比较
术后患者采用连续腘窝坐骨神经阻滞PCA镇痛方式。术后6、24、48h采用NRS量表记录静止和活动时的镇痛效果、PCA按压次数及镇痛泵中局部麻醉药平均累积剂量。其中静止NRS评分,W组术后6h高于X组(P<0.05),其他时间段两组间差异无统计学意义。活动NRS评分,X组除术后0h,其他时间段均显著低于W组(P<0.05);W组PCA按压次数明显多于X组(P<0.05);镇痛泵局部麻醉药平均累积剂量6、24、48h,W组明显高于X组(P<0.05),见表3。
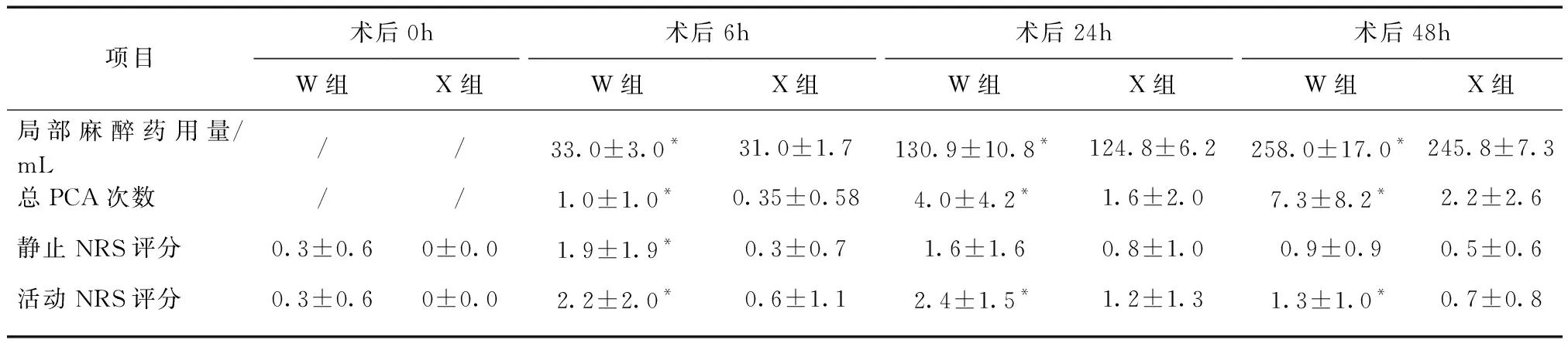
表3 两组术后镇痛泵局部麻醉药用量、PCA按压次数及NRS镇痛评分比较Tab.3 Comparison of postoperative analgesic pump local anesthetic dosage and PCA compression times and NRS analgesia score between the two groups
与同时间点X组相比,*P<0.05
2.4 两组患者不良反应、并发症及患者满意度比较
两组患者术后均未出现导管滑出及感觉运动异常等神经损伤并发症;导管堵塞、渗漏、恶心呕吐、使用止痛药物例数比较,差异无统计学意义。W组患者满意度评分低于X组(P<0.05),见表4。
表4两组患者导管留置期间其他随访项目及患者满意度比较
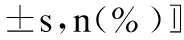
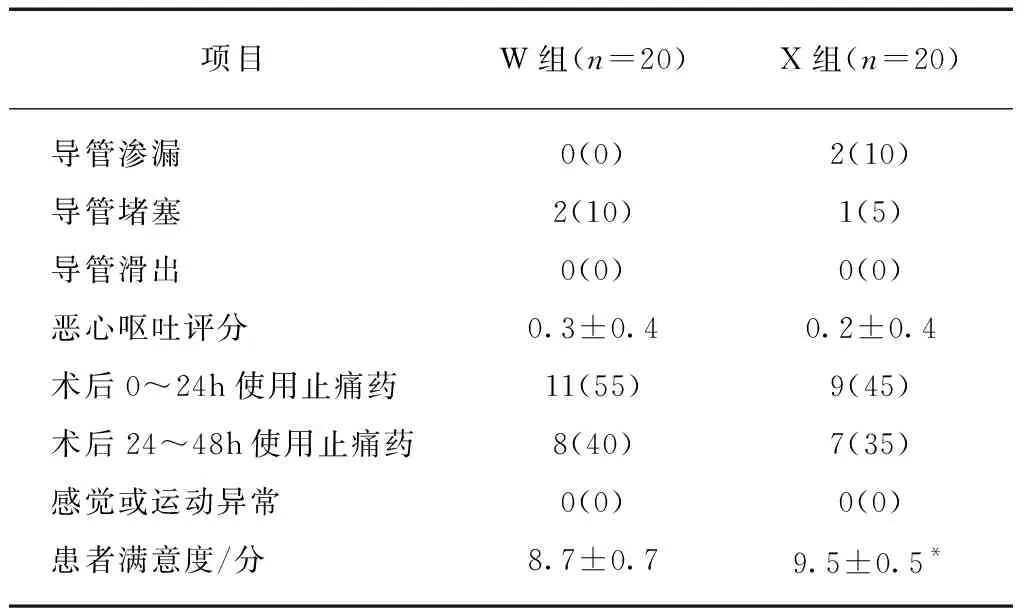
项目W组(n=20)X组(n=20)导管渗漏0(0)2(10)导管堵塞2(10)1(5)导管滑出0(0)0(0)恶心呕吐评分0.3±0.40.2±0.4术后0~24h使用止痛药11(55)9(45)术后24~48h使用止痛药8(40)7(35)感觉或运动异常0(0)0(0)患者满意度/分8.7±0.79.5±0.5*
与X组比较,*P<0.05
3 讨 论
周围神经由神经外膜、神经束膜及神经内膜包裹。动物研究表明在神经束膜内高压注射局部麻醉药可以导致神经束损伤和持久性神经功能缺陷[4]。而关于神经外膜下注射是否会引起神经损伤的争议也一直不断,神经外膜下注射可引起神经肿胀、神经面积增加,但不一定导致神经损伤[5];有研究称神经内注射时长斜面针更容易引起神经损伤[6]。而在腘窝坐骨神经分支处,Karmakar等[7]通过高分辨率超声分析腘窝坐骨神经周围的筋膜结构,认为神经鞘膜是位于坐骨神经外膜和周围肌肉肌外膜之间的高回声筋膜层;Perlas等[3]推荐神经鞘膜下注射是理想的腘窝坐骨神经阻滞点,而在腘窝坐骨神经分支处注射给药,针尖位置在腓总神经与胫神经之间,注射的局部麻醉药更容易进入神经鞘膜下直接包裹神经,由于神经鞘膜的阻隔作用,药液不易向外扩散,因此与神经鞘膜外注药相比,在获得相同麻醉镇痛效果的同时需要的局部麻醉药更少、术后镇痛效果更好。因为神经束膜内给药风险较大,本研究选择在神经鞘膜下给药。本研究在行连续腘窝坐骨神经鞘膜下阻滞时,神经阻滞针进入分叉处后,通过观察针尖位置及注射少量生理盐水,神经无肿胀且生理盐水在鞘膜下扩散包裹在神经周围,可确定针尖位于神经鞘膜下;患者在镇静下行神经阻滞,无异感报告,术后随访未发现感觉运动异常等神经损伤症状。本研究应用肌电诱发电位仪测定坐骨神经的CMAP波幅变化来判断坐骨神经阻滞的效果,若波幅降为初始值的一半,说明阻滞起效,若波幅降为0,说明完全阻滞[8]。本研究采用运动神经传导检查。神经传导检查能客观而准确地评价阻滞效果,但刺激电流增加了患者的不良体验,因此需在麻醉过程中泵注右美托咪定,产生镇静和镇痛作用,使患者完全能耐受麻醉过程。
下肢手术采用连续神经阻滞镇痛,效果好、副作用小而受到医生和患者欢迎[9-10],国内关于连续神经阻滞镇痛应用的报告也越来越多[11-12],由于进口连续神经针价格昂贵,置管成功率低、导管易渗漏移位等不足,国内应用受到一定的限制。新型连续外周神经阻滞针是国内专利转化产品,全新的针外导管设计操作方便,置管渗漏、移位少,在上、下肢创伤手术麻醉中已广泛应用,术后镇痛效果好,患者满意度高[13-16]。
足踝部除内侧感觉为股神经的隐神经支配外,其余均由坐骨神经支配,因此本试验采用腘窝坐骨神经阻滞可满足手术需求,手术涉及内侧切口时复合股神经或隐神经阻滞亦可获得良好的镇痛效果。本研究中,股神经阻滞采用1%利多卡因和0.25%罗哌卡因配伍使用,可阻滞大腿前部感觉与小腿、足踝内侧感觉,能提供手术所需麻醉镇痛效果和延长大腿处止血带耐受时间(术中约90min时,部分患者有止血带不适,可静脉予少量丙泊酚),同时也能为有内侧切口的患者提供一定时间的术后镇痛;术前腘窝坐骨神经阻滞采用1.5%利多卡因,起效时间短,便于监测运动神经传导的变化,同时为足踝手术提供一定肌松效果,术后运动阻滞时间短,利于早期活动与锻炼,在临床应用中,建议可以适当减少利多卡因的浓度以避免不必要的神经损伤并发症;术后镇痛的配方用0.2%罗哌卡因300mL,研究显示低浓度罗哌卡因可产生感觉阻滞而无运动阻滞效应[17],且对静止痛和运动痛都有效,镇痛的同时不影响术后早期活动与锻炼,但连续鞘膜下注药是否会对周围肌肉神经结构造成影响仍需在动物实验中进一步验证。
通过本研究发现,应用单次股神经阻滞+腘窝坐骨神经阻滞复合右美镇静技术可完成2h以内的足踝手术,术毕可采用在腘窝处留置导管实施连续神经阻滞镇痛。此种麻醉方法无需导尿,无需去枕平卧,术毕2h即可进食,符合目前快速康复外科理念,深受患者欢迎。对于腘窝处神经鞘膜下与神经鞘膜外注药两种给药方式,在坐骨神经直径无统计学差异情况下,鞘膜下注药满足手术所需要的局部麻醉药更少、麻醉起效时间更快、术后镇痛局部麻醉药更少,可以获得更好的术后镇痛效果、更高的患者满意度而不增加神经阻滞与置管操作的风险。在行单侧足踝手术时或多点神经阻滞时,尤其是老年患者神经阻滞中,可减少术中局部麻醉药用量和毒性反应。
由于采用神经肌肉混合动作电位监测神经传导,临床操作有一定难度,所收集的样本量较少,是本实验的不足之处。今后可扩大样本量继续深入研究。
