苦参碱通过P38通路调节H2AX磷酸化抑制宫颈癌细胞的增殖及迁移
2018-09-10赵淑婷程静新
赵淑婷, 雷 蕾, 程静新
(同济大学附属东方医院妇产科,上海 200120)
宫颈癌是女性中最常见的恶性肿瘤之一,且发病率逐年增高[1]。即使在早期宫颈癌根治性切除术后,仍大约有20%~30%的患者复发[2-3]。化疗广泛用于治疗复发或转移性疾病[4]。
苦参碱是一种从豆科槐属植物中提取的生物碱,具有利尿、抗病原体、抗肝炎病毒等作用,且无明显的毒性作用[5-7]。既往研究[8-10]表明,苦参碱可能是通过抑制癌细胞增殖、诱导细胞凋亡和细胞自噬而对胃癌、乳腺癌、非小细胞肺癌和胰腺癌等发挥抗肿瘤作用。其抗肿瘤作用极其复杂,涉及对细胞增殖、凋亡及周期的影响。本研究旨在探讨苦参碱对宫颈癌细胞生长和转移的抑制作用与H2AX是否相关。
1 材料与方法
1.1 主要试剂
苦参碱(分析纯)购自上海源叶公司,磷酸缓冲盐溶液(phosphate buffer saline, PBS)购自美国Corning公司;LipofectamineTM3000购自美国Invitrogen公司;Cell Counting Kit-8(CCK8)试剂盒购自日本同仁公司;Cell-Light EdU Apollo®567 In Vitro Imaging Kit购自广州锐博公司;细胞凋亡与坏死检测试剂盒购自上海碧云天生物技术有限公司,Annexin V-FITC试剂盒、Transwell小室购自美国BD公司;鼠单克隆抗体β-actin购自美国Proteintech公司;兔单克隆抗体H2AX、P38、抗鼠IgG及抗兔IgG二抗购自英国Abcam公司。
1.2 细胞系
人宫颈癌SiHa、C33A细胞购自中国科学院上海细胞库。SiHa细胞用含有10%血清的DMEM培养液培养;C33A细胞用含有10%血清的MEM培养液培养。以上细胞置于37℃,5% CO2饱和湿度下贴壁培养,根据细胞生长状况1~2d换液一次。
1.3 方法
1.3.1 CCK8试验 将对数生长期细胞按2×103/孔接种于96孔板,贴壁后更换不同浓度苦参碱(0~2mg/mL)培养基,于24、48、72h后按照CCK8说明书配制CCK8溶液,在培养箱中温育2h,用酶标仪测定450nm处吸光度值(A450)。
1.3.2 EdU法 将2×103个宫颈癌细胞接种于96孔板,贴壁后更换培养基,24h后按EdU试剂盒说明配置溶液,试剂A液孵育2h,4%多聚甲醛固定,甘氨酸脱色,渗透剂孵育。Apollo®反应溶液避光、室温、孵育后Hoechst33342反应液避光室温孵育,于荧光显微镜下观察。
1.3.3 流式细胞术 将细胞种于6孔板培养12h后,更换正常及含0.5mg/mL苦参碱的培养基,作用24h后的细胞,用预冷PBS充分洗涤细胞3次,按照Annexin V-FITC试剂盒说明书配置溶液,细胞用195μL 结合缓冲液和5μL Annexin V-FITC室温避光孵育10min,然后加入10μL碘化丙啶室温避光孵育10min,上机检测细胞凋亡率。
1.3.4 细胞凋亡与坏死检测 将5×103个宫颈癌细胞接种于6孔板,贴壁后更换不同浓度苦参碱培养基,作用24h后,先加入Hoechst33342染液4℃避光孵育30min,再加入碘化丙啶染液4℃避光孵育30min进行双标记染色,于荧光显微镜下观察。
1.3.5 细胞迁移试验 在Transwell小室中加入200μL(1×106个/mL)不同处理后的无血清细胞悬液,底部加入600μL含10%血清的培养液。置于37℃培养箱中孵育24h,将小室置于4%多聚甲醛溶液中固定后结晶紫染色,PBS轻轻冲洗小室,用棉棒将室顶细胞轻轻擦去,晾干后于倒置显微镜观察,随机取3个视野进行拍照,统计细胞迁移率。
1.3.6 划痕实验 将细胞以每孔1×106密度接种于6孔板中,待细胞贴壁长满后时用10μL枪头垂直划一条直线,PBS冲洗去除划下细胞,更换含(0、0.5mg/mL)苦参碱的无血清的培养基,放入37℃培养箱中培养,用倒置显微镜下分别在0、24h拍照。
1.3.7 Western印迹法检测 干预后的细胞经预冷PBS漂洗后,用RIPA裂解液处理后轻轻刮下细胞,冰上反应30min后超声并离心获得各组细胞总蛋白,BCA法检测蛋白浓度,与5×SDS蛋白上样缓冲溶液混合,100℃下变性8min。每孔上样30μg蛋白,SDS-PAGE分离并转膜后用5%脱脂牛奶封闭1h后加入相应一抗(1∶1000)4℃孵育过夜,随后加入二抗(1∶10000),室温孵育1h,进行ECL反应。利用Image J软件分析蛋白条带。
1.4 统计学处理
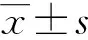
2 结 果
2.1 苦参碱对SiHa/C33A细胞增殖的影响
CCK8法检测0、0.25、0.5、1.0、2.0mg/mL苦参碱诱导24、48、72h后对宫颈癌细胞SiHa、C33A细胞增殖的影响。相同作用时间下,抑制作用随苦参碱浓度的升高而增强,相同浓度下,抑制作用随苦参碱作用时间的延长而增强,在苦参碱浓度高于0.5mg/mL时,差异有统计学意义(P<0.05)。EdU实验结果显示,1mg/mL苦参碱作用后细胞的增殖受到抑制,差异有统计学意义(P<0.05),见图1。
2.2 苦参碱对SiHa/C33A细胞凋亡的影响
通过细胞凋亡与坏死检测Hochest33342和碘化丙啶双染实验,评估苦参碱对宫颈癌细胞凋亡形态的影响,结果显示,苦参碱作用后的细胞密度明显降低,出现亮蓝色,核染色质固缩染色体碎裂、固缩的细胞被染成亮蓝色或淡红色。通过流式细胞术,检测结果显示,苦参碱诱导细胞凋亡率升高,差异有统计学意义(P<0.05),见图2。
2.3 苦参碱对SiHa/C33A细胞迁移的影响
通过Transwell实验与划痕实验检测苦参碱对宫颈癌迁移能力的影响。Transwell实验结果显示: 较正常对照组,苦参碱作用后的宫颈癌细胞的穿膜数量均减少,差异有统计学意义(P<0.05)。划痕实验结果显示: 处理24h时,正常对照组细胞划痕宽度大于苦参碱作用后的宫颈癌细胞,即迁移能力受到显著抑制,差异有统计学意义(P<0.05),见图3。
2.4 苦参碱对SiHa/C33A细胞H2AX、P38表达的影响
通过Western印迹法检测苦参碱对γH2AX、pP38蛋白水平的影响,结果显示苦参碱随着药物浓度增高,γH2AX、pP38的表达显著增高,即H2AX、P38磷酸化水平随着苦参碱浓度增高而增加,差异有统计学意义(P<0.05),见图4。
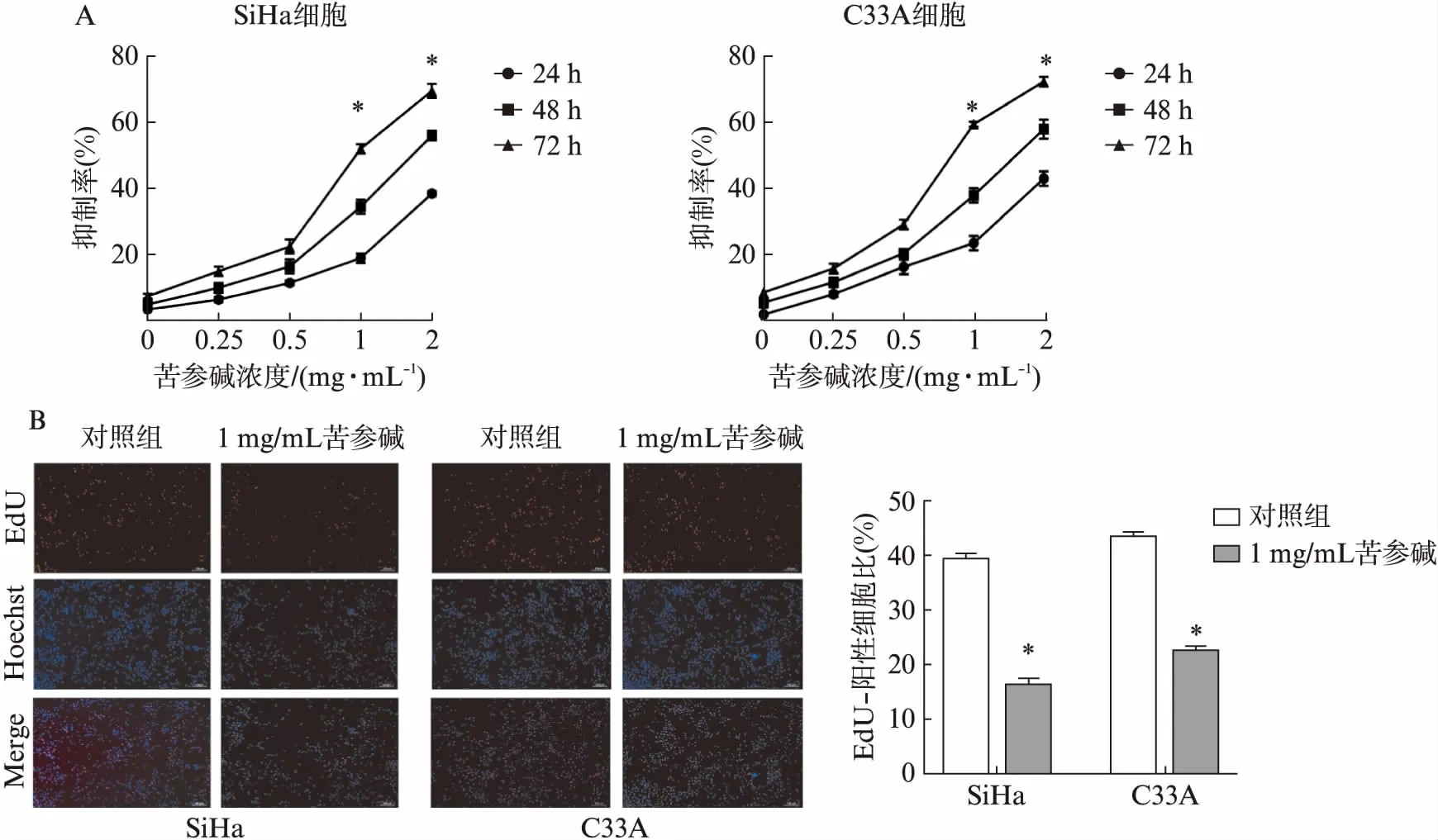
图1 苦参碱对宫颈癌细胞SiHa/C33A增殖的影响Fig.1 The effect of matrine on SiHa and C33A cell proliferationA: CCK8实验检测不同时间点、不同苦参碱对宫颈癌细胞增殖的影响;B: EdU法检测苦参碱对宫颈癌细胞增殖的影响;与对照组相比,*P<0.05

图2 苦参碱对宫颈癌细胞SiHa/C33A凋亡的影响Fig.2 The effect of matrine on SiHa and C33A cell apoptosisA: 细胞凋亡实验对宫颈癌细胞凋亡的检测;B: 流式细胞术对宫颈癌细胞凋亡的检测;与对照组相比,*P<0.05
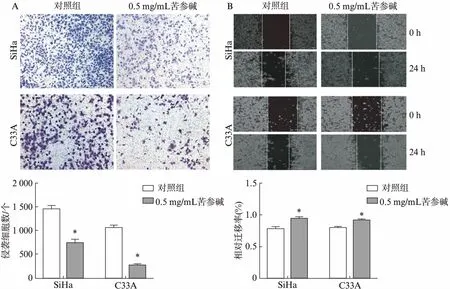
图3 苦参碱对宫颈癌细胞SiHa/C33A侵袭和迁移的影响Fig.3 The effect of matrine on invasion and migration of SiHa and C33A cellsA: 宫颈癌细胞侵袭能力;B: 宫颈癌细胞迁移能力;与对照组相比,*P<0.05
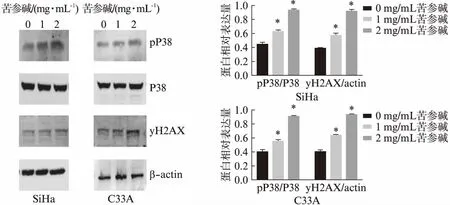
图4 苦参碱对宫颈癌细胞SiHa/C33A中H2AX基因表达的影响Fig.4 The effect of matrine on the expression of H2AX in cervical cancer cells与0mg/mL苦参碱组相比,*P<0.05
2.5 H2AX磷酸化对苦参碱作用的宫颈癌细胞增殖、迁移的影响
在宫颈癌细胞SiHa中稳转H2AX-wt和H2AX-139m(含有Ser139突变以阻断磷酸化)后加入苦参碱,检测H2AX的磷酸化不同对宫颈癌细胞增殖、迁移的影响。结果显示,与H2AX-wt组相比,苦参碱对H2AX-139m组宫颈癌细胞的增殖抑制程度减低,迁移率明显增强,即H2AX磷酸化的阻断可降低苦参碱对宫颈癌细胞的抑增殖、抑迁移的作用,差异有统计学意义(P<0.05),见图5。
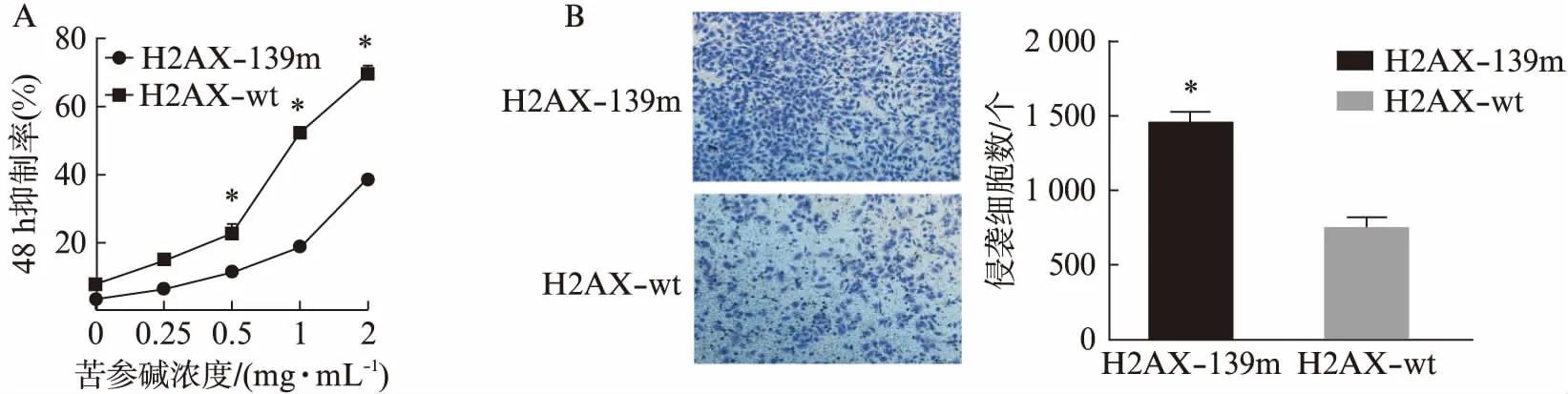
图5 H2AX磷酸化对苦参碱作用的宫颈癌细胞增殖、迁移的影响Fig.5 The effect of H2AX phosphorylation on proliferation and migration in cervical cancer cellsA: CCK8法检测苦参碱在H2AX不同磷酸化下对宫颈癌细胞48h增殖的抑制率的影响;B: Transwell实验检测苦参碱在H2AX不同磷酸化下对宫颈癌细胞迁移的影响;与H2AX-wt组相比,*P<0.05
2.6 苦参碱通过P38信号通路对宫颈癌细胞H2AX磷酸化的影响
在宫颈癌细胞SiHa中加入P38磷酸激酶抑制剂SB202190,通过Western印迹法检测P38磷酸化被抑制后对γH2AX、pP38表达的影响。结果显示,加入抑制剂后,P38信号磷酸化通路被抑制,同时H2AX磷酸化水平也随之降低,差异有统计学意义(P<0.05),见图6。

图6 苦参碱通过P38信号通路对宫颈癌细胞H2AX磷酸化的影响Fig.6 The effect of Matrine on the phosphorylation of H2AX in cervical cancer cells through P38 signaling pathway与苦参碱组相比,*P<0.05
3 讨 论
苦参碱对多种肿瘤有抑制作用,且毒副作用较小,是一种应用于临床的高效、低毒的新型抗肿瘤药。既往研究[8,11]表明,苦参碱在病毒性肝炎、心律失常、皮肤炎症等的治疗中广泛应用,且与标准疗法联合应用能显著改善癌症患者的生活质量和预后,显示其作为抗癌药物的潜力。然而,其对肿瘤抑制作用的具体机制目前还不明确,尤其是在宫颈癌中。在本实验中,探究不同浓度苦参碱对人宫颈癌细胞系SiHa和C33A细胞功能的影响,及与P38/H2AX基因表达的相关性,以期揭示苦参碱对宫颈癌抑癌作用的机制。
肿瘤细胞的增殖能力与肿瘤的恶性程度密切相关。本研究验证了苦参碱对宫颈癌细胞增殖的抑制,苦参碱对宫颈癌SiHa和C33A细胞的增殖显著抑制,且呈剂量依赖。肿瘤的发生、发展不仅与细胞的增殖分化有关,还与细胞的凋亡障碍有密切关系,细胞凋亡是维持机体自身稳态所必须的生理性细胞自杀过程,苦参碱在肝细胞癌中可通过凋亡诱导因子的核转位而产生的细胞凋亡,本研究发现在宫颈癌中,苦参碱可促进细胞凋亡。迁移和侵袭是评价宫颈癌预后的重要指标并提示治疗后效果,迁移能力强的细胞更具有复发和转移的潜能[12]。本实验通过Transwell实验和划痕实验检测苦参碱对宫颈癌细胞的迁移和侵袭能力的影响,发现苦参碱在宫颈癌中显著抑制细胞的迁移能力。这一结果与前列腺癌的低迁移率一致[5],进一步验证了苦参碱对宫颈癌细胞迁移的抑制作用[13];通过CCK8、EdU等实验技术,针对细胞的增殖、凋亡、转移等多角度综合证明苦参碱对宫颈癌的抑增殖、促凋亡、抑转移等抗肿瘤作用
关于苦参碱对肿瘤抑制作用的机制研究[14-15]认为,抑制作用可能与miR-21/PTEN/Akt通路、AKT/GSK3β/β-Catenin等通路相关。本研究通过苦参碱作用于宫颈癌细胞,证明苦参碱随浓度增加可梯度增加γH2AX、pP38的表达,提示苦参碱的抑癌作用可能与H2AX相关。H2AX属于编码组蛋白H2A家族,参与细胞的增殖和DNA的修复[16]。DNA损伤可导致增殖失控和驱动恶性肿瘤的形成H2AX在Ser139位点发生磷酸化进而调控细胞增殖、细胞凋亡、DNA的修复中起重要作用。在真核细胞中,生物、物理及化学因素等可使DNA损伤而形成γH2AX。在越来越多的证据[17]表明,γH2AX参与多种人类恶性肿瘤的凋亡过程中。H2AX磷酸化可由ATM、ATR和DNA-PKcs催化[18]。研究[19-20]报道,H2AX的磷酸化可通过P38丝裂原活化蛋白激酶途径调控细胞的凋亡。在本研究中发现,苦参碱抑制宫颈癌增殖、迁移时,γH2AX、pP38的表达增加,提示苦参碱可能是通过诱导H2AX磷酸化进而发挥作用。为证明H2AX是通过磷酸化激活发挥作用,通过抑制H2AX的磷酸化发现苦参碱对增殖、迁移的抑制作用解除。为探究γH2AX的作用通路,通过阻断H2AX上游基因P38的磷酸化,结果证实P38磷酸化的阻断可抑制γH2AX的表达。
综上所述,本研究发现苦参碱能够有效抑制宫颈癌SiHa/C33A细胞的增殖、迁移,诱导细胞凋亡,并证实苦参碱通过P38信号通路使H2AX(Ser139)位点磷酸化发挥抑增殖、抑迁移作用。本研究下一步将继续阐述苦参碱有无其他通路调控H2AX的表达,为宫颈癌辅助治疗的临床前和临床评价奠定基础。
