化学还原法原位制备石墨烯/纳米银复合粉体及其导电性能
2018-09-08支英甘卫平周健王晓庆
支英,甘卫平,周健,王晓庆
化学还原法原位制备石墨烯/纳米银复合粉体及其导电性能
支英1,甘卫平1,周健2,王晓庆1
(1. 中南大学 材料科学与工程学院,长沙 410083; 2. 宜春学院 江西省高校应用化学与化学生物学重点实验室,宜春 336000)
以水合肼为还原剂,PVP为分散剂,在反应温度为60 ℃,pH为6条件下同时还原氧化石墨烯和硝酸银,原位制备石墨烯/纳米银复合粉体。通过扫描电镜、X射线衍射、红外吸收光谱和拉曼光谱等手段研究溶液中硝酸银的质量浓度对石墨烯/纳米银复合粉体形貌与结构的影响。用石墨烯/纳米银复合粉体替代部分微米银粉制备低温固化导电浆料,对其导电性能进行研究。结果表明:银纳米粒子分布于石墨烯片层之间。当反应溶液中硝酸银的质量浓度为0.75 g/L,氧化石墨烯质量浓度为0.25 g/L时,获得分散性好,粒径均匀的石墨烯/纳米银复合粉体,且负载在石墨烯片层上的银纳米粒子的粒径集中在100 nm左右。用石墨烯/纳米银复合粉体替代4%微米银粉制备导电浆料,浆料的体积电阻率为1.8×10−5Ω·cm,与未添加石墨烯/纳米银复合粉体的导电浆料相比,电阻率降低61.7%。
石墨烯;水合肼;石墨烯/纳米银复合粉体;导电银浆
导电银浆由于其优异的导电性能、良好的抗氧化性能、优良的可焊性及合理的价格等吸引了广大研究者的注意[1]。纳米银粉比表面积大、导电性能良好,广泛应用于导电浆料、高性能电极材料等领域[2]。然而国内银粉制备工艺的不成熟导致纳米银粉粒度不均匀、易团聚[3],力学性能较差,用银粉与树脂匹配制备的浆料电阻率较高,导电稳定性较差。为了提高银粉的综合性能,研究人员发展了以银为基体的复合材料[4],即在银基体中加入增强体。石墨烯[5]是近年来开发的新型的碳质增强材料,具有高导电导热性能和超大的比表面积,以其作为支撑材料可供金属纳米颗粒循环反复的镶嵌和脱嵌。利用石墨烯与纳米银粒子各自的优异性能,通过杂化过程实现性能互补,可建立有效完善的导电网络,从而提高导电材料的导电性 能[6−7]。YOO等[8]将石墨烯应用于锂离子电池负极材料中,比容量达到540 (mA·h/g);WANG等[9]以柠檬酸作为稳定剂,硼氢化钠为还原剂,合成的石墨烯/纳米锡复合材料可用于锂电池的电极材料。尹奎波 等[10]以水合肼为还原剂制备石墨烯/纳米银复合粉体,氧化石墨烯与银离子均被还原,银纳米粒子较均匀地附着于石墨烯边缘和表面。虽然石墨烯/纳米银复合粉体的制备方法不断成熟,但石墨烯受层间分子吸引作用仍会出现堆叠现象,并且还未有人将这种复合粉体应用在导电银浆中。本文作者采用硝酸银和氧化石墨烯为前驱体,用水合肼作还原剂,通过化学还原法[11−12]原位制备石墨烯/银纳米颗粒复合粉体,在反应体系中加入适量PVP作为分散剂,使原料充分分散,并进一步提高还原后所得石墨烯和银颗粒的分散性。同时还采用石墨烯/纳米银复合粉体替代部分银粉制备导电银浆,研究复合粉体含量对银浆导电性能的影响,为制备用于导电银浆的石墨烯/纳米银复合粉体提供理论基础。
1 实验
1.1 原材料
硝酸银(AgNO3),分析纯(纯度99.8%),株洲集团贵金属部生产;无水乙醇,分析纯(纯度99%),天津市富宇精细化工有限公司生产;氨水,分析纯(25.0%),天津市致远化学试剂有限公司生产;聚乙烯吡咯烷酮(PVP,分子式K30([C6H9NO]n)),分析纯,天津大茂化学试剂厂生产;氧化石墨烯,苏州碳丰科技公司生产;水合肼(N2H4·H2O),分析纯,东北制药股份有限公司生产;片状银粉,平均粒径为5 μm,球磨自制;去离子水等。
1.2 石墨烯/银纳米复合粉体的制备
称取0,100,200,300和400 mg硝酸银(AgNO3),分别与100 mg氧化石墨烯(GO)混合分散在200 mL去离子水中,超声2 h。按(PVP)/(AgNO3)=0.5的比例称取PVP,将其加入到分散好的氧化石墨烯/硝酸银混合溶液中,用硝酸或氨水调节溶液pH为6,搅拌均匀,记为A液,得到5种不同AgNO3质量浓度的 A液。
称取一定量的水合肼溶解在200 mL去离子水中,制成B液。水合肼还原硝酸银的化学方程式为4Ag++ N2H4∙H2O®4Ag+4H++H2O+N2,水合肼与硝酸银的物质的量比(N2H4·H2O):(AgNO3)=1:4,为了确保硝酸银和氧化石墨烯反应完全,设置水合肼过量。将A液和B液分别在水浴锅中加热,待温度恒定60 ℃后,用滴管将B液缓慢滴加到A液中,溶液逐渐由黑色变成灰黑色。滴加完毕后,将混合溶液在一定温度下恒温搅拌约2 h,反应完全,得到灰色的悬浊液。将悬浊液静置一段时间,在7 800 r/min转速下离心分离15 min,去掉上层液体,然后再用去离子水和无水乙醇分别清洗3次,60 ℃下真空干燥12 h,得到石墨烯/银纳米复合粉体(即Ag/RGO)样品。
经过计算,由5种不同AgNO3质量浓度的A液与B液组成的反应体系中,AgNO3的质量浓度(AgNO3)分别为0,0.25,0.5,0.75和1.0 g/L,对应的 Ag/RGO复合粉体样品分别标记为RGO,Ag/RGO -1,Ag/RGO-2,Ag/RGO-3和Ag/RGO-4。
1.3 导电银浆的制备
在片状银粉中加入粒径均匀、分散性良好的石墨烯/银纳米复合粉体RGO/Ag-3一起作为导电相,复合粉的加入量(质量分数)分别为0,2%,4%,6%和8%。在导电相中加入15%环氧树脂、13%稀释剂和2%胺类固化剂,搅拌均匀,得到导电银浆。采用丝网印刷的方式将导电银浆印刷在经过乙醇洗涤并烘干的载玻片上,150 ℃温度下固化30 min,得到导电银浆固化膜。
1.4 测试与表征
采用D-MAX2500型X 射线衍射仪研究石墨烯/纳米银复合粉体的物相结构与粒度,Cu 靶Kα辐射,步进扫描,扫描速度为15 (°)/min;利用AVATAR 360 FT-IR,Nicelet 红外光谱仪和激光共焦拉曼光谱仪(LabRAM HR800,氦氖激光器,波长为632.8 nm)对样品进行结构分析;用MIRA 3 LMH/LMU 型高真空场发射扫描电镜观察石墨烯/纳米银复合粉体的形貌;用苏州华仪电讯科技公司生产的SZ-82数字式四探针测试仪测量银浆固化膜的体积电阻率。
2 结果与讨论
2.1 形貌
图1和2所示为在反应液中(N2H4·H2O)=0.0058 mol/L,(AgNO3)分别为0.25,0.5,0.75和1.0 g/L的条件下制备的 Ag/RGO复合粉体样品Ag/RGO-1,Ag/RGO-2,Ag/RGO-3和Ag/RGO-4的SEM形貌。从图1可以看出:随反应溶液中(AgNO3)增加,石墨烯表面银颗粒的致密性和均匀性提高,但当(AgNO3)为1 g/L时,由于化学反应速率大,石墨烯表面的银颗粒增多,颗粒发生团聚。当(AgNO3)=0.25 g/L时,银离子浓度低,银离子数量不足,因而氧化还原速率及银的析出率都较低,附着在石墨烯表面的银粒子较少且大小不均匀;(AgNO3)增加到0.75 g/L时,化学反应驱动力增大,银颗粒的数量增多,形成较致密均匀分布的石墨烯/纳米银复合粉体,负载在石墨烯片层上的银纳米粒子的粒径集中在100 nm左右。从图2看出:随(AgNO3)增加,石墨烯(RGO)片相互接触并叠加,形成RGO片层网络[14]。当(AgNO3)为0.25 g/L时,石墨烯片较平整,没有大的褶皱,(AgNO3)增加到1 g/L时,RGO片层堆叠现象较严重。因此较合理的(AgNO3)为0.75 g/L。

图1 石墨烯/纳米银复合粉体的SEM照片
(a) Ag/RGO-1; (b) Ag/RGO-2; (c) Ag/RGO-3; (d) Ag/RGO-4
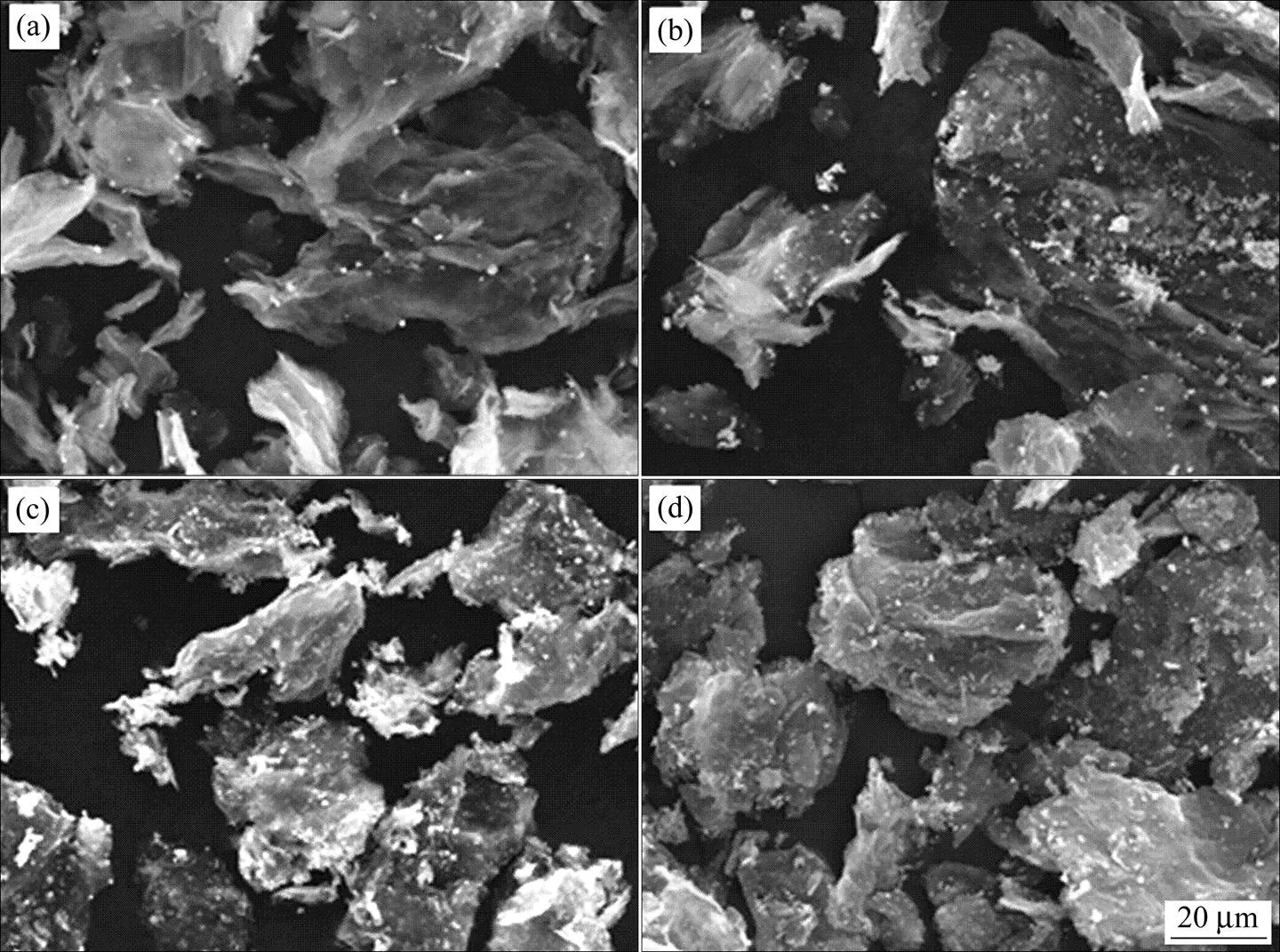
图2 石墨烯/纳米银复合粉体的SEM形貌
(a) Ag/RGO-1; (b) Ag/RGO-2; (c) Ag/RGO-3; (d) Ag/RGO-4
2.2 物相组成
图3所示为GO,RGO以及复合粉体样品Ag/ RGO-1和 Ag/RGO-3的XRD谱。从图3看出,氧化石墨烯原料在2=10.6°附近出现明显的(001)衍射 峰[13],还原后所得石墨烯在2=22.9°处出现其特征衍射峰[14]。根据布拉格衍射方程=2sin(式中:λ为射线的波长,=0.154 06 nm;为衍射角)计算出氧化石墨烯原料的片层间距为0.833 9 nm,石墨烯片层间距为0.388 nm,比氧化石墨烯的片层间距明显减小,说明氧化石墨烯经过还原后,其片层中的含氧集团被还原[15]。从图3看出,与石墨烯相比,石墨烯/纳米银复合粉体不同程度地出现尖锐的晶体特征峰形。在(AgNO3)分别为0.25与0.75 mg/mL条件下制备的复合粉体,2为38.096°,44.057°,64.406°和77.452°的位置,分别对应面心立方结构银的(111)、(200)、(220)和(311)晶面,与JCPDS 卡片04-0783 的数据吻合,说明氧化石墨烯和硝酸银同时被还原生成石墨烯/银复合粉体。

图3 氧化石墨烯,石墨烯和石墨烯/纳米银复合粉体的XRD谱
Fig.3 XRD patterns of graphene oxide, graphene and nano-silver/graphene composite powders
在Ag/RGO-1和Ag/RGO-3的衍射谱中没有出现氧化石墨烯的衍射峰,说明银粒子的产生破坏了氧化石墨烯有序的层状结构。在低浓度硝酸银条件下制备的Ag/RGO-1有相对较弱的银特征峰,随(AgNO3)增大,银的特征峰更明显。
2.3 分子结构
图4所示为GO,RGO以及Ag/RGO-1和 Ag/ RGO-3复合粉体的傅立叶变换红外吸收光谱。由图可知,GO的红外光谱中,3 384 cm−1处的吸收峰为O—H伸缩振动吸收峰,说明GO中存在大量羟基。1 755 cm−1处和1621 cm−1处的较强吸收峰为GO的羧基中的C=O伸缩振动吸收峰,1052 cm−1处的吸收峰对应的是C—O—C的伸缩振动,来源于氧化石墨烯表面的环氧基[16]。与GO相比,RGO的红外光谱中3 384 cm−1处的O—H伸缩振动吸收峰和1 052 cm−1处的C—O—C的伸缩振动吸收峰明显减弱,1 621 cm-1处的C=O伸缩振动吸收峰也略微减弱。这表明化学还原后,氧化石墨烯表面大量的含氧官能团被移除,这证实了在还原剂水合肼的作用下,氧化石墨烯被成功还原。由图4可知,与RGO相比,Ag/RGO复合粉体在3384 cm−1处的羟基伸缩振动峰和1 621 cm−1处的C=O伸缩振动吸收峰明显减弱,而且随银含量增多,减弱越明显,1755,1396,1222及1052 cm−1处的峰都逐渐消失。
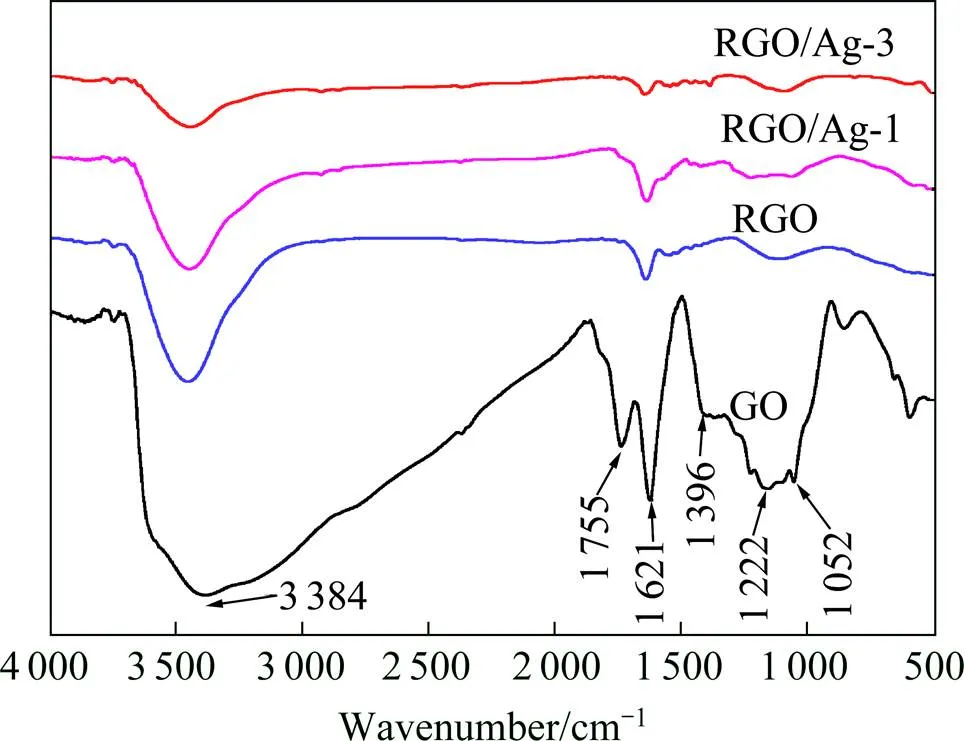
图4 氧化石墨烯,石墨烯和石墨烯/纳米银复合粉体的红外光谱图
图5所示为GO,RGO,Ag/RGO-1和Ag/RGO-3复合粉体的拉曼光谱[17]。拉曼光谱可以对碳材料结构、缺陷等进行简单快速的检测。在石墨的拉曼光谱上一般表现为2个峰,一个是相内振动的G峰,位于1 575 cm−1附近,该峰较窄,与sp2杂化碳原子的振动有关;另一个称为D峰,位于1 355 cm−1附近,该峰的出现是由于边缘、其它缺陷和不规则C(sp3)等所致。用D峰强度与G峰强度的比值(即D/G的值)来衡量碳材料的不规则度,是判断其有序性的重要指标,是验证石墨烯片层结构电子变化的证据之一。D/G越大,说明碳基材料中缺陷和不规则C(sp3)越多。由图可知,氧化石墨烯的D峰和G峰分别位于1 327 cm−1附近和1580 cm−1附近,D/G=1.03,表明该氧化石墨烯不规则,这是由于石墨经过氧化后,石墨片层间引入了大量的含氧官能团和悬挂键、导致大量缺陷的产生以及sp2碳杂化向sp3碳杂化的转变,破坏了石墨的结晶性能。氧化石墨烯被还原后所得的石墨烯也出现了D峰和G峰,峰的位置都没有发生明显偏移,D峰强度相比于氧化石墨烯增大了,D/G=1.41,这表明氧化石墨烯经过还原后sp3杂化的C原子数目增多,结构缺陷增多。RGO/Ag-1样品的D峰和G峰相比于RGO有明显的增强,约增加到原来的5倍,D/G=1.29,说明银对石墨材料具有很好的表面增强拉曼效应[18]。根据化学增强原理,石墨烯与银纳米粒子之间可产生转移电子的联合体,当光照射这些联合体时,位于激发态的频率吸收适当能量的光子而产生共振,而体系有效激活率明显提高,因此拉曼信号增强。当银含量增加时,峰强度及峰强度比值D/G相对于银含量较少的复合材料都有所降低,RGO/Ag-3样品的D/G=1.18,这表明银量增加对石墨烯的缺陷有一定的修饰作用。
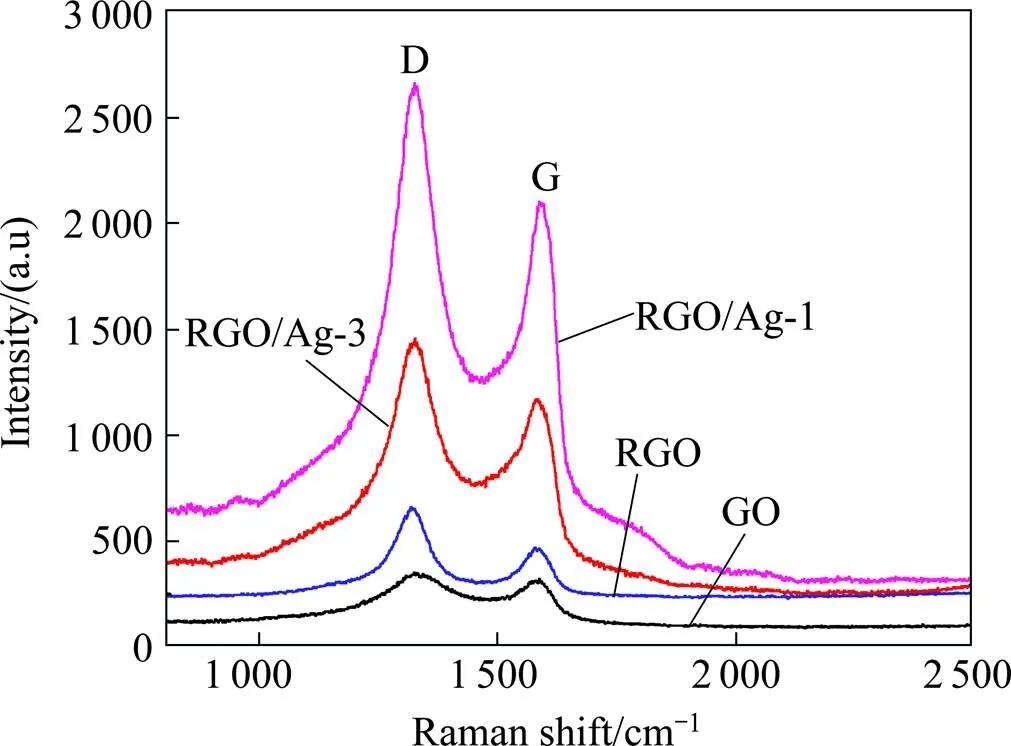
图5 氧化石墨烯,石墨烯和石墨烯/纳米银复合粉体的拉曼光谱图
2.5 导电性能
用粒径均匀,分散性良好的RGO/Ag-3替代0,2%,4%,6%和8%(质量分数)微米银粉制备导电银浆,并制成固化膜。图6所示为导电相中石墨烯/纳米银复合粉体的含量对银浆固化膜导电性能的影响。由图可知,当导电相中不含Ag/RGO-3时,固化膜的体积电阻率为4.7×10−5Ω·cm,银粉中加入Ag/ RGO-3后,固化膜的体积电阻率下降,当Ag/RGO-3含量增加到4%时,固化膜的体积电阻率达到最低值,为1.8×10−5Ω·cm,相比未添加石墨烯/纳米银复合粉体的导电浆料,其电阻率降低61.7%。当继续增加石墨烯/纳米银复合粉体时,体积电阻率反而增加,Ag/ RGO-3含量为8%时,固化膜的电阻率为3.1×10−5Ω·cm。这是由于当少量石墨烯/银纳米粒子填充到基体中时,一方面,片层结构的石墨烯基体可保证复合粉体与微米银粉之间的面接触;另一方面,复合粉末中的纳米银粒子可填充微米银粉之间的空隙,增加导电相之间的接触,使得导电相之间形成更加完善的导电网络,增加了电子的传导效率,从而提高导电浆料的导电性能。但当石墨烯/纳米银复合粉体增加到一定程度时,复合粉体发生团聚,难以在导电浆料中均匀分散,导致导电浆料的粘度增加,破坏导电通路,所以固化膜的体积电阻率增加。

图6 石墨烯/纳米银复合粉体含量对银浆固化膜导电性能的影响
3 结论
1) 以PVP为稳定剂,水合肼为还原剂,在温和的液相反应条件下,同时还原氧化石墨烯和硝酸银溶液中的银离子,得到分散性能良好、粒径均匀的石墨烯/纳米银复合粉体。
2) 随反应体系中硝酸银浓度增大,石墨烯表面的银颗粒致密性及均匀性提高,银颗粒的粒径先减小后增大,石墨烯/纳米银复合粉体团聚现象逐渐明显。当硝酸银质量浓度为0.75 mg/mL时,获得石墨烯片层分散性良好,纳米银颗粒表面光滑、粒径均匀细小(100 nm)的石墨烯/纳米银复合粉体。
3) 在微米级银粉中添加石墨烯/纳米银复合粉体,当石墨烯/纳米银复合粉体的含量不超过4%时,随含量增加,导电银浆电阻率逐渐降低,当石墨烯/纳米银复合粉体的含量为4%时,银浆的体积电阻率降至1.8×10−5Ω·cm,相比未添加石墨烯/纳米银复合粉体的导电银浆,其电阻率降低61.7%。
[1] WU Songping. Preparation of micron size flake silver powders for conductive thick films[J]. Journal of Materials Science: Materials in Electronics, 2006, 18(4): 447−52.
[2] 张文毓. 纳米银粉研究与应用[J]. 中国粉体工业, 2016(4): 7−11. ZHANG Wenyu. Research and application of nano silver powder[J]. China Powder Industry, 2016(4): 7−11.
[3] 赵德强, 马立斌, 杨君, 等. 银粉及电子浆料产品的现状及趋势[J]. 电子元件与材料, 2005, 24(6): 54−56. ZHAO Deqiang, MA Libin, YANG Jun, et al. Status and trend of silver powder and electronic slurry products[J]. Electronic Components and Materials, 2005, 24(6): 54−56.
[4] FENG Yi, YUAN Hailong, ZHANG Min. Fabrication and properties of silver-matrix composites reinforced by carbon nanotubes[J]. Materials Characterization, 2005, 55(3): 211−218.
[5] GEIM A K, NOVOSELOV K S. The rise of graphene[J]. Nature Materials, 2007, 6(3): 183−191.
[6] JIANG Lili, LU Xiong. Graphene applications in solar cells[J]. Journal of Inorganic Materials, 2013, 27(11): 1129−1137.
[7] XIE Yunfei, LI Yan, LI Niu, et al. A novel surface-enhanced Raman scattering sensor to detect prohibited colorants in food by graphene/silver nanocomposite[J]. Talanta, 2012, 100(20): 32− 37.
[8] YOO E, KIM J, HOSONO E, et al. Large reversible Li storage of graphene nanosheet families for use in rechargeable lithium ion batteries[J]. Nano Lett, 2008, 8(8): 2277−2282.
[9] WANG Guoxiu, WANG Bei, WANG Xianlong, et al. Sn/ graphene nanocomposite with 3D architecture for enhanced reversible lithium storage in lithium ion batteries[J]. Journal of Materials Chemistry, 2009, 19(44): 8378−8384.
[10] 尹奎波, 朱逸宇, 韩宇龙, 等. Ag-石墨烯纳米复合材料的室温制备及其结构分析[J]. 电子显微学报. 2011, 30(3): 187−90. YIN Kuibo, ZHU Yiyu, HAN Yulong, et al. Room-temperature synthesis and structure characterization of silver-graphene nanocomposites[J]. Journal of Chinese Electron Microscopy Society, 2011, 30(3): 187−90.
[11] HE Hongkun, GAO Chao, et al. Graphene nanosheets decorated with Pd, Pt, Au and Ag nanoparticles: Synthesis, characterization and catalysis applications[J]. Chinese Science: Chemistry, 2011, 54(2): 397−404.
[12] STANKOVICH S, DIKIN D A, PINER R D, et al. Synthesis of graphene-based nanosheets via chemical reduction of exfoliated graphite oxide[J]. Carbon, 2007, 45(7): 1558−1565.
[13] 周亚洲, 杨娟, 孙磊, 等. 石墨烯/银复合薄膜的制备及表征[J]. 无机化学学报, 2012, 28(1): 137−142. ZHOU Yazhou, YANG Juan, SUN Lei, et al. Synthesis and characterization of graphene/Ag composite films[J]. Chinese Journal of Inorganic Chemistry, 2012, 28(1): 137−142.
[14] JR W S H, OFFEMAN R E. Preparation of graphitic oxide[J]. Journal of the American Chemical Society, 1958, 80(6): 1339− 1339.
[15] LIU S, TIAN J, WANG L, et al. Stable aqueous dispersion of graphene nanosheets: Noncovalent functionalization by a polymeric reducing agent and their subsequent decoration with Ag nanoparticles for enzymeless hydrogen peroxide detection[J]. Macromolecules, 2010, 43(23): 10078−10083.
[16] PARK S, AN J, JUNG I, et al. Colloidal suspensions of highly reduced graphene oxide in a wide variety of organic solvents[J]. Nano Letters, 2009, 9(4): 1593−1597.
[17] 黄桥, 孙红娟, 杨勇辉. 氧化石墨的谱学表征及分析[J]. 无机化学学报, 2011, 27(9): 1721−1726. HUANG Qiao, SUN Xiaojuan, YANG Yonghui. Spectroscopy characterization and analysis of graphite oxide[J]. Chinese Journal of Inorganic Chemistry, 2011, 27(9): 1721−1726.
[18] SAITO R, HOFMANN M, DRESSELHAUS G. et al. Raman spectroscopy of graphene and carbon nanotubes[J]. Advances in Physics, 2011, 60(3): 413−550.
[19] CAO A, LIU Z, CHU S, et al. A facile one-step method to produce graphene-CdS quantum dot nanocomposites as promising optoelectronic materials[J]. Advanced Materials, 2010, 22(1): 103−106.
(编辑 汤金芝)
Fabrication and electrical properties of nano-silver/graphene composite powders prepared in-situ by chemical reduction
ZHI Ying1, GAN Weiping1, ZHOU Jian2, WANG Xiaoqing1
(1. School of Materials Science and Engineering, Central South University, Changsha 410083, China; 2. Key Laboratory of Jiangxi University for Applied Chemistry and Chemical Biology, Yichun University, Yichun 336000, China)
Nano-silver/graphene composite powders were prepared by chemical reduction method using hydrazine hydrate as reducing agent, PVP as dispersant, graphene oxide and silver nitrate as precursor at the reaction temperature of 60 ℃ and the pH of 6. The effects of silver nitrate concentration in solution on the morphology and structure of nano-silver/graphene composite powders were investigated by SEM, XRD, IR and RAMAN. Low temperature curing conductive silver paste was prepared by using graphene/nano-silver composite powder instead of some micron silver powder, and its conductive properties were studied. The results indicate that Ag nanoparticles uniformly distribute in the graphene sheets. Pherical silver particles with better dispersibility and uniform particle size can be obtained by using 0.75 g/L of silver nitrate, 0.25 g/L of graphene oxide. The size of Ag nanoparticles on the graphene sheets centralizes at 100 nm. When using graphene/nano-silver composite powder instead of 4% micron silver powder to prepare conductive paste, the volume resistivity of conductive paste is 1.8×10−5Ω·cm. Compared with the conductive paste without graphene/nano-silver composite powder, the resistivity decreases by 61.7%.
graphene; hydrazine hydrate; nano-silver/graphene composite powder; conductive silver paste
TG146.3+2
A
1673-0224(2018)04-433-06
2017−11−21;
2018−01−02
甘卫平,教授。电话:13707311733;E-mail: gwp@mail.csu.edu.cn
