基于DNA与单层二硫化钨的相互作用荧光法检测汞(Ⅱ)离子
2018-09-06关雅南李晓双连丽丽王希越高文秀娄大伟
关雅南,张 浩,李晓双,连丽丽,王希越,高文秀,祝 波,娄大伟
(吉林化工学院 化学与制药工程学院,吉林 吉林 132022)
汞是一种高毒性的重金属离子,在江河湖泊、工厂污水等环境中广泛存在.汞及其化合物是剧毒性的环境污染物[1],可对人类的身体健康构成不同程度的危害.因此,研究我们人类的饮用水中Hg2+离子的定性分析具有重要意义[2,3].目前,检测Hg2+离子的方法有很多,包括原子吸收光谱法[4]、电化学分析法[5,6]、比色法[7]、荧光法[8,9]等,其中,荧光法由于具有操作简单,分析检测时间短,成本低,选择性好等众多优点,受到了人们的广泛关注.因此,我们选择使用荧光法对Hg2+离子进行检测.近年来,随着石墨烯的强大发展与应用,二维类石墨烯物质也引起了人们的研究兴趣.目前,二维类石墨烯物质(包括过渡金属二硫化物,氧化物等)由于具有其独特的二维层状结构,在检测方面有很多应用.并且国内外研究者在检测应用方面也做出了很多报道.如Hao,Liling等人[10]报道了一种改进的基于RCA的CRET适体传感器,用于通过化学发光供体Co2+/ABEI-AuNFs和化学发光受体层状WS2纳米片之间的CRET过程来检测金黄色葡萄球菌.WS2是典型的层状结构材料,具有片层的堆叠,在层与层之间有较弱的范德华力,能够通过物理或化学方法得到少层或单层的片状结构[11].在本文中,我们提出了一种DNA与WS2相互作用检测Hg2+离子的新方法.通过研究WS2的浓度对实验反应的影响,确定最佳实验条件,从而对一系列的Hg2+离子浓度进行检测.
1 实验部分
1.1 试剂与仪器
DNA寡核苷酸是从上海生工生物工程技术有限公司购买的.DNA寡核苷酸序列为:3′-FAM-TTTCTTCTTGGGTTGTTGTTT-5′.
NaCl,MgCl2和Hg(NO3)2购自国药集团化学试剂有限公司,十二水合磷酸氢二钠(Na2HPO4·12H2O)和磷酸二氢钠(NaH2PO4·2H2O)均购自中国天津市永大化学试剂有限公司.自制40 mmol·L-1pH 7.4的PBS缓冲液(将7.16 g Na2HPO4·12H2O和3.12 g NaH2PO4·2H2O在1 L超纯水中溶解),在整个实验中使用.
荧光测量使用的是岛津RF-5301PC光谱荧光光度计.在520 nm激发波长处得到荧光光谱.pH值测量使用的是中国北京赛多利斯仪器有限公司生产的Sartorius PB-10 pH计.超纯水是使用Milli-Q试剂水系统(Millipore,Bedford,MA,USA)纯化的.
1.2 实验过程
将25 μmol·L-13 μL ssDNA、40 mmol·L-1150 μL PBS缓冲溶液、3 mol·L-110 μL NaCl和3 mol·L-110 μL MgCl2混合在一起,然后,将不同浓度的10 μL WS2加入到上述混合溶液中,在25 ℃下振荡反应30 min.最后,将一系列不同浓度的10 μL Hg2+离子加入到该混合溶液体系中,在25 ℃下振荡反应30 min,混合溶液的总体积为300 μL.所有实验均重复三次.
2 结果与讨论
2.1 该方法检测Hg2+离子可行性分析
为了验证该方法的可行性,我们分别对以下三种情况进行了测定:(a)不加WS2和待测物Hg2+离子;(b)加WS2,不加待测物Hg2+离子;(c)加WS2和待测物Hg2+离子.如图1所示,发现不加WS2和待测物Hg2+离子的a曲线的荧光强度最高;加WS2,不加待测物Hg2+离子的b曲线的荧光强度最低;加WS2和待测物Hg2+离子的c曲线的荧光强度与b曲线相比又增强.
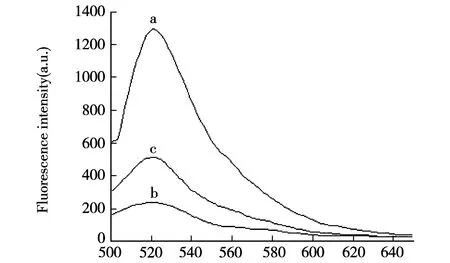
Wavelength/nm图1 不同条件下测得的荧光光谱图
这是由于DNA与WS2相互作用,当不存在待测物Hg2+离子时,被标记在ssDNA上的羧基荧光素(FAM)基团吸附在WS2上,由于发生荧光能量共振转移,导致荧光淬灭;当待测物Hg2+离子存在时,ssDNA中的胸腺嘧啶(T)与Hg2+离子形成T-Hg2+-T错配结构,其余部分根据碱基配对原则,杂交形成刚性的双链DNA(dsDNA),标记的FAM荧光基团不会吸附在WS2上,因此,体系的荧光强度增强.实验结果证明此方法检测Hg2+离子可行.
2.2 WS2的浓度对反应的影响
由于WS2在整个实验中起到了很重要的作用,并且WS2的浓度对实验反应也有一定的影响,因此,对WS2的一系列浓度进行了实验.如图2所示,其中,从a到f的WS2浓度分别为0 mg/ml;0.003 mg/ml;0.01 mg/ml;0.017 mg/ml;0.023 mg/ml;0.03 mg/ml.从图中可以看出,随着WS2的浓度增大,实验体系的荧光强度逐渐下降.为了满足实验的检测条件,将浓度为0.017 mg/ml的WS2,选择用于进行下面的实验.

Wavelength/nm图2 WS2的浓度对反应的影响图
2.3 Hg2+离子检测
基于确定了WS2的最佳浓度,因此,对一系列的Hg2+离子浓度进行了检测.如图3所示,其中,从a到e的Hg2+离子浓度分别为0 nmol·L-1;80 nmol·L-1;320 nmol·L-1;800 nmol·L-1;1 600 nmol·L-1.从图中可以明显看出,随着加入的Hg2+离子浓度越大,实验体系的荧光强度也随之增强.

Wavelength/nm图3 不同浓度的Hg2+离子检测图
2.4 Hg2+离子检测方法的选择性
为了证明检测Hg2+离子方法的选择性,把800 nmol·L-1的Hg2+离子替换成1 mol·L-1的其它金属离子(如Al3+,Zn2+,Mg2+,Fe3+,Fe2+,Ca2+,Mn2+,K+,Co2+),对其做了几组对照实验.实验过程与检测Hg2+离子的过程相同,如图4所示,在实验条件相同的情况下,只有Hg2+离子对体系的荧光强度有明显的影响.结果表明该实验对于Hg2+离子的检测具有良好的选择性.

图4 Hg2+离子检测方法的选择性图
2.5 Hg2+离子检测方法的抗干扰性
为验证该方法对Hg2+离子的特异性识别能力,考察了其它可能产生干扰的一系列金属离子的影响.如Al3+,Zn2+,Mg2+,Fe3+,Fe2+,Ca2+,Mn2+,K+,Co2+.将800 nmol·L-1的Hg2+离子和1 mol·L-1的其它金属离子加入到实验中,结果如图5所示,当Hg2+离子存在时,加入其它不同金属离子后,体系的荧光强度并无明显变化,这表明其它金属离子不会干扰对Hg2+离子的检测.

图5 Hg2+离子检测方法的抗干扰性图
3 结 论
总之,我们基于Hg2+离子特异性地与T碱基结合,进而ssDNA上剩余的碱基部分互相杂交形成刚性的dsDNA,被标记的FAM基团由于不会吸附在WS2上导致其荧光增强的原理,建立了一种检测Hg2+离子的荧光方法.实验结果表明该方法具有操作简单、成本低等优点.同时,检测体系对Hg2+离子表现出良好的选择性,而且常见的一些阳离子也不会干扰其测定.
