超高效液相色谱-串联质谱法快速测定地表水中联苯胺、苦味酸、甲萘威、阿特拉津和溴氰菊酯
2018-09-05唐访良徐建芬程新良王立群
张 明, 唐访良*, 徐建芬, 张 伟, 程新良, 王立群
(1. 杭州市环境监测中心站, 浙江 杭州 310007; 2. 淳安县环境保护监测站, 浙江 杭州 311700)
联苯胺(benzidine)是染料合成的中间体,在化工、印染和制药等工业生产中应用广泛,高毒且具有强烈的致癌作用[1];苦味酸(picric acid)是早期炸药的主要成分,同时大量用作杀菌剂、除霉剂及收敛剂等,属高毒类物质[2];甲萘威(carbaryl)主要用于粮食作物的病虫害防治,进入人体内可造成急性中毒症状,另外还被认为是潜在的内分泌干扰物[3];阿特拉津(atrazine)是目前应用最广泛的除草剂之一,适用于玉米、高粱等作物田及果园、林地等,具有内分泌干扰作用和潜在致癌性[4];溴氰菊酯(deltamethrin)是一类重要的合成杀虫剂,广泛应用于农业害虫、仓库害虫及卫生害虫等防治,具中等毒性[5]。通常,含有联苯胺、苦味酸、甲萘威、阿特拉津和溴氰菊酯等化合物的制成品在生产和使用过程中会不断地将这些化合物释放到环境中,并通过地表径流、大气干湿沉降等环境迁移行为进入地表水体,造成水环境污染,并对人体健康产生影响,进而影响整个生态系统。我国现行的地表水环境质量标准中,联苯胺、苦味酸、甲萘威、阿特拉津和溴氰菊酯均属于严格控制的特定项目[6],标准中规定了这5种有机污染物的相应检测方法,其中联苯胺、苦味酸、阿特拉津和溴氰菊酯分别采用气相色谱法,甲萘威则采用液相色谱法。这些方法灵敏度和特异性较差,易出现假阳性,而且均需通过液液萃取富集样品,使得整个检测过程操作繁琐且耗时很长。另外,大量具有毒副作用的有机试剂的使用导致方法的环境友好性较差,并潜在威胁操作人员的身体健康。
随着近年来频发的水污染事件和水资源供需矛盾的日益突出,环境健康研究领域受到了越来越多的关注,相关管理部门更是不断加大对水环境质量的监测力度,这也对环境监测技术的发展提出了新的要求。目前,具有高灵敏度和选择性的液相色谱-质谱联用技术越来越多地被应用于环境痕量有机污染物的分析,成为地表水中有机物残留快速筛查的有效分析方法之一[7-10]。现阶段,液相色谱-质谱联用检测地表水中联苯胺[11-13]、苦味酸[2,14]、甲萘威[15,16]、阿特拉津[17-19]和溴氰菊酯[20]的应用研究均取得了较大进展,但是目前绝大多数分析方法是将5种化合物分开检测,这就导致了实际检测过程中需要进行繁琐的方法切换,不仅降低了工作效率,大大增加了仪器设备的分析和维护成本,也严重影响到检测结果的时效性。因此亟须建立一批简单快速并能同时检测多种化合物的分析方法,以满足现阶段水质监测的要求。目前部分理化性质相近的化合物多组分同时检测的研究工作已逐步开展起来[3,21-25],但是地表水中不同性质的污染物多组分同时监测的分析方法还很缺乏。本文基于液相色谱-质谱联用技术,通过简化前处理程序,扩大检测范围,建立并验证了同时检测地表水中联苯胺、苦味酸、甲萘威、阿特拉津和溴氰菊酯5种有机污染物的超高效液相色谱-三重四极杆串联质谱(UPLC-MS/MS)方法。
1 实验部分
1.1 主要仪器
Acquity Ultra Performance LCTM超高效液相色谱仪-XEVO电喷雾串联四极杆质谱仪(美国Waters公司)。
1.2 主要材料与试剂
0.2 μm孔径聚四氟乙烯(PTFE)针式滤头(美国Waters公司)。甲醇(色谱纯,德国Merck公司);1 000 mg/L甲醇中联苯胺标准溶液、100 mg/L甲醇中苦味酸标准溶液和100 mg/L甲醇中甲萘威标准溶液(美国Accustandard公司)、100 mg/L甲醇中阿特拉津标准溶液(农业部环境保护科研监测所)、溴氰菊酯标准品(纯度99%,中国计量科学研究院)。实验用超纯水由Milli-Q Advantage A10系统(美国Millipore公司)制备。
1.3 标准溶液配制
准确称取溴氰菊酯标准品10.0 mg,用甲醇溶解并转移至10 mL棕色容量瓶中,甲醇定容制得1 000 mg/L的标准溶液,取1.00 mL该标准溶液至10 mL棕色容量瓶中,用甲醇定容制得100 mg/L的溴氰菊酯标准溶液;取1.00 mL联苯胺标准溶液至10 mL棕色容量瓶中,用甲醇定容制得100 mg/L的联苯胺标准溶液;分别取100 mg/L的5种化合物的标准溶液各1.00 mL,置于10 mL棕色容量瓶中,用甲醇稀释配制成质量浓度为10.0 mg/L的混合标准储备液,所有标准溶液和储备液均置于-20 ℃避光保存。实验中用超纯水将混合标准储备液稀释成系列浓度工作液,现用现配。
1.4 仪器分析条件
1.4.1色谱条件
Waters Acquity UPLC HSS T3色谱柱(100 mm×2.1 mm, 1.7 μm);流动相:2 mmol/L乙酸铵水溶液(A)和2 mmol/L乙酸铵甲醇溶液(B);梯度洗脱程序:0~0.6 min,45%B; 0.6~1.1 min,45%B~90%B; 1.1~3.4 min,90%B; 3.4~3.5 min,90%B~45%B; 3.5~4.0 min,45%B;柱温50 ℃;流速0.4 mL/min;进样量10 μL。
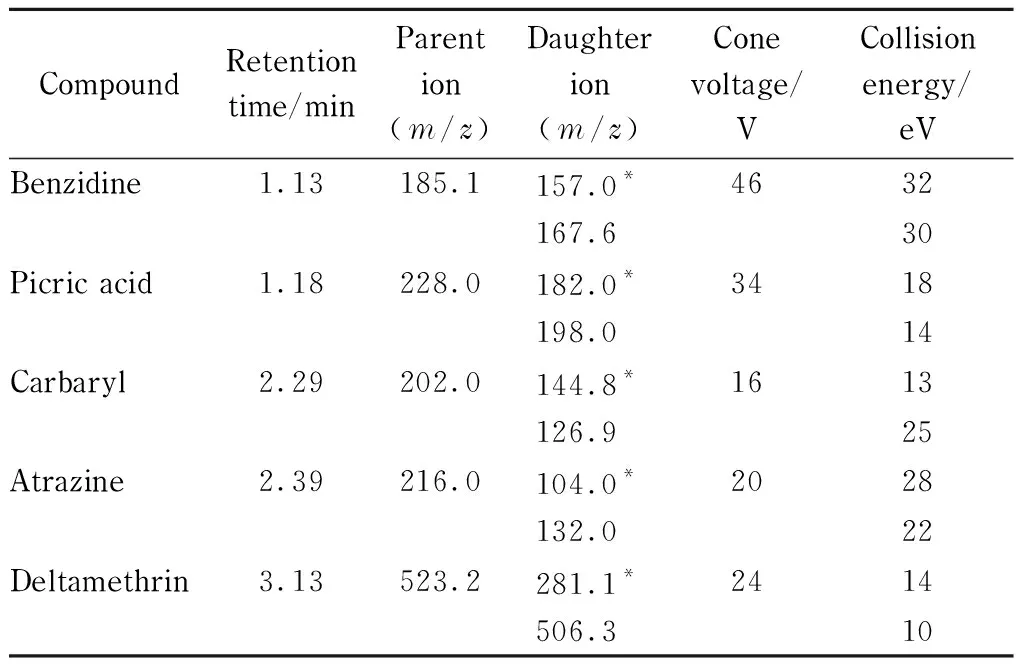
表 1 目标化合物的保留时间和优化的质谱参数
* Quantitative ion.
1.4.2质谱条件
电喷雾电离(ESI)源,正、负离子扫描切换;多反应监测(MRM)模式;毛细管电压:3.2 kV;离子源温度:150 ℃;脱溶剂气温度:550 ℃;脱溶剂气流速(氮气): 700 L/h;锥孔气流速(氮气): 30 L/h;碰撞气流速(氩气): 0.15 mL/min。在分析过程中,以离子对(母离子和两个子离子,见表1)信息比较和保留时间进行定性分析;以母离子和响应高的子离子通道进行定量分析。
1.5 实际样品采集和前处理
地表水样品采集前2天未下大雨,河流水采样点位于河流中垂线上,水库水采样点位于水库中间。水样采集后置于洁净的棕色玻璃瓶中,以锡箔纸包裹后用冰块保存,当天送回实验室,带回实验室的地表水样品经0.2 μm PTFE微孔滤膜过滤,待液相色谱-质谱联用仪分析。
2 结果与讨论
2.1 质谱条件的选择
根据目标化合物的结构特征,选择正、负离子扫描切换模式,其中联苯胺、甲萘威、阿特拉津和溴氰菊酯采用正离子模式,苦味酸采用负离子模式。采用流动注射泵进样,分别对5种目标化合物标准溶液进行一级质谱扫描,确定各待测化合物的准分子离子峰,并分别优化其锥孔电压。然后分别以其准分子离子为母离子,通过氩气碰撞产生碎片离子进行二级质谱扫描,同时优化碰撞能量,选择丰度较高的2种碎片离子作为定量与定性特征离子。为了保证每种化合物的灵敏度,采用分时段分别监测。优化后各目标化合物的定性、定量特征离子及质谱参数见表1。

图 1 脱溶剂气温度对质谱响应的影响Fig. 1 Influence of desolvation gas temperature on mass spectral response
ESI离子源的脱溶剂气温度对目标化合物的质谱响应有一定的影响,我们配制5种待测组分混合标准溶液(甲萘威和阿特拉津分别为5.00 μg/L;联苯胺、苦味酸和溴氰菊酯分别为50.0 μg/L)进样分析,对脱溶剂气温度进行优化。图1为不同脱溶剂气温度条件下各目标化合物的相对响应值变化趋势:脱溶剂气温度过低会抑制目标化合物的质谱响应,除了联苯胺在400 ℃脱溶剂气温度下质谱响应达到最高外,其余4种化合物响应值在300~500 ℃范围内随着脱溶剂气温度上升呈升高趋势;脱溶剂气温度在500~600 ℃时,各化合物质谱响应相差不大,当脱溶剂气温度大于550 ℃,除阿特拉津响应值略有升高外,其他化合物的响应值均有所下降。因此,方法的脱溶剂气温度设定为550 ℃。

图 3 5种目标化合物的MRM图Fig. 3 MRM chromatograms of the five target compounds
脱溶剂气流速同样直接影响目标化合物的质谱响应,我们试验了其他质谱条件不变的情况下不同脱溶剂气流速(300~1 000 L/h)对目标化合物质谱响应的影响,结果见图2。从图2可以看出:除了阿特拉津,其余各化合物在脱溶剂气流速低于500 L/h条件下响应值相对较低;过高的脱溶剂气流速同样对大部分目标化合物的质谱响应有抑制作用,当脱溶剂气流速大于800 L/h时,仅有苦味酸的响应值呈略微增长趋势。综合考虑5种化合物的响应值变化特征,确定方法的脱溶剂气流速为700 L/h。

图 2 脱溶剂气流速对质谱响应的影响Fig. 2 Influence of desolvation gas flow rate on mass spectral response
2.2 色谱条件的选择
色谱柱的选择对于样品分离非常重要,通常不同填料的色谱柱对同一样品有不同的保留时间。5种化合物均有使用常规C18色谱柱分离的文献报道,我们的实验结果表明甲萘威、阿特拉津和溴氰菊酯采用常规的反相C18色谱柱即能获得满意的分离效果,而强极性的亲水性化合物联苯胺和苦味酸在常规反相C18色谱柱中虽可以实现分离,但因与色谱柱的非极性固定相结合较弱而难以实现有效保留,通常会出现色谱峰拖尾或双峰的现象,苦味酸在常规C18色谱柱上的保留时间还会出现明显的漂移。采用亲水作用色谱柱可改善联苯胺[13]、苦味酸[2]的分离效果,但是该类色谱柱对甲萘威、阿特拉津和溴氰菊酯的分离效果并不理想。经过试验比较,我们选用一款极性化合物分析专用硅胶基体C18色谱柱,即T3色谱柱,用于5种目标化合物的分离,得到满意的分离效果。
在液相色谱-质谱联用仪的使用中,流动相的选择要兼顾各目标化合物的色谱分离效果以及质谱离子化效率,以获得最佳的分辨率和最高的灵敏度。经过考察,我们选择了甲醇-水作为流动相体系。在流动相中加入缓冲盐可调节系统的pH值,增加目标化合物在色谱柱上的保留并改善峰形,本文比较了添加不同缓冲盐(甲酸、氨水、乙酸铵)条件下目标物的离子化效率以及色谱峰形。实验中发现,氨水会抑制目标化合物的离子化效率;而选用甲酸则能增加联苯胺、甲萘威和阿特拉津等部分化合物的响应值,但是会导致联苯胺和溴氰菊酯的色谱峰变形,溴氰菊酯的响应值也会有所降低;选用乙酸铵作为缓冲盐,各目标化合物的离子化效率较佳且色谱峰形对称无拖尾。综合各方面因素,最终确定0.2 mmol/L乙酸铵水溶液和0.2 mmol/L乙酸铵甲醇溶液作为流动相,经过优化,得到1.4.1节的梯度洗脱条件,在该条件下,目标化合物分离良好。图3为混合标准溶液(甲萘威和阿特拉津分别为5.00 μg/L;联苯胺、苦味酸和溴氰菊酯分别为50.0 μg/L)按1.4节条件进样分析得到的MRM图。
2.3 样品过滤滤膜的选择
由于UPLC色谱柱填料孔径较小,地表水样品中的细小颗粒物容易造成色谱柱堵塞,因此样品需经过滤后才能进行仪器分析。研究选取PTFE、亲水性聚丙烯(GHP)、亲水尼龙(Nylon)、聚醚砜(PES)和亲水性聚偏二氟乙烯(PVDF)等5种常用材质滤膜过滤加标样品,统计回收率,结果见图4。

图 4 5种目标化合物过不同滤膜的回收率Fig. 4 Recoveries of the five target compounds through different filters PTFE: poly tetra fluoroethylene; GHP: hydrophilic polypropylene; PES: polyethersulfone; PVDF: polyvinylidene fluoride micro filters.
从图4可以看出,5种目标化合物经各种滤膜过滤后的回收率各不相同:联苯胺除了在PTFE滤膜上没有明显吸附效应外,经其余4种滤膜过滤后回收率均低于35%;苦味酸在Nylon滤膜上有明显吸附;阿特拉津则在GHP滤膜上吸附较高;甲萘威在试验的5种滤膜上均无明显吸附,经GHP和Nylon滤膜过滤后甚至有明显的增敏效应,回收率分别达到120%和118%;溴氰菊酯经PTFE和PVDF等2种材质滤膜过滤有较高的回收率,而在GHP和PES两种滤膜上表现出强烈的吸附效应。综合比较,采用PTFE滤膜过滤样品效果最佳,5种目标化合物的回收率在93.3%~102%之间,适合作为样品仪器分析前过滤使用。
2.4 上机溶液中有机相体积分数对响应值的影响
通常,HPLC特别是UPLC在色谱分离过程中有一定的“溶剂效应”,如果样品溶剂不合适,有可能会影响色谱保留而导致色谱峰形异常。我们在实验过程中也发现联苯胺和苦味酸的色谱峰随着样品溶剂中甲醇含量的增大而变宽,特别是当甲醇体积分数大于60%时,苦味酸的色谱峰出现双峰等严重变形现象。考虑到样品溶剂的成分同样会影响待测物在液相色谱-质谱联用仪中的电喷雾电离效果进而影响检测灵敏度,因此有必要考察样品溶剂中有机含量对目标化合物质谱响应的影响。分别以纯水、纯甲醇以及不同含量的甲醇水溶液作为溶剂,配制混合标准溶液进样分析,结果见图5。实验结果表明:苦味酸的质谱响应基本不受样品溶剂的影响;联苯胺的质谱响应随着样品溶剂中甲醇含量的增大而略有升高,但以纯甲醇为溶剂时其质谱响应出现明显降低;甲萘威和阿特拉津的质谱响应分别在以体积分数为40%、60%甲醇水溶液作为样品溶剂时最高,而以纯水为溶剂时均为最低,但变化不大。样品溶剂甲醇含量对溴氰菊酯的质谱响应影响较大,采用高甲醇含量的样品溶剂(体积分数≥80%)时其质谱响应比低甲醇含量时高了近一倍。充分考虑5种化合物的色谱分离效果和质谱响应,在能够满足地表水样品中各目标化合物的检测限值要求的前提下,本文选用水作为样品溶剂。这样虽然会降低部分化合物的灵敏度,但却大大提高了方法的检测便利性,可实现地表水样品直接进样快速分析。
2.5 方法的线性范围和检出限
以3倍和10倍信噪比(S/N)计算方法的检出限(LOD)和定量限(LOQ),结果见表2。可以看出,5种化合物的检出限在0.01~0.22 μg/L之间,检出限均低于我国地表水环境质量标准[6]中这些化合物的控制标准,能满足直接进样测定地表水样品中这些化合物的要求。实验中发现5种目标化合物的灵敏度各异且差别较大,因此,配制系列标准溶液的时候将5种目标组分分成2组,其中甲萘威和阿特拉津分别为0.10、0.20、0.50、1.00、5.00和10.0 μg/L;联苯胺、苦味酸和溴氰菊酯分别为1.00、2.00、5.00、10.0、50.0和100 μg/L。以目标组分响应值(Y)对相应的质量浓度(X, μg/L)绘制标准曲线。各种目标化合物的线性方程、相关系数(r)、线性范围见表2。

表 2 5种目标化合物的回归方程、相关系数、线性范围、检出限、定量限和标准限值
Y: peak area of the analyte;X: mass concentration, μg/L.
2.6 方法的回收率和精密度
选用不含5种待测组分的地表水样品,根据各化合物的线性范围添加一定浓度的标准溶液以制备低、中、高3个添加水平的加标水样,每个水平平行测定6次,计算回收率及其相对标准偏差(RSD),结果见表3。高、中、低3个添加水平的回收率在81.4%~113%之间,RSD为0.84%~14.0%,说明该方法有较好的回收率且具有较高的精密度,适合实际样品的检测分析。

表 3 目标分析物在实际样品中的加标回收率及其RSD(n=6)
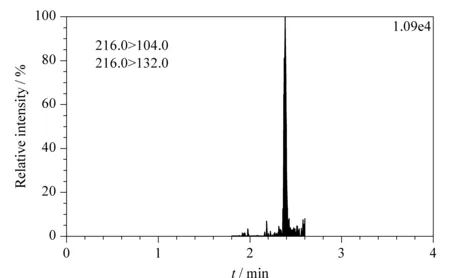
图 6 阳性地表水样品中阿特拉津的TIC色谱图Fig. 6 Total ion current (TIC) chromatogram of atrazine in a positive surface water sample
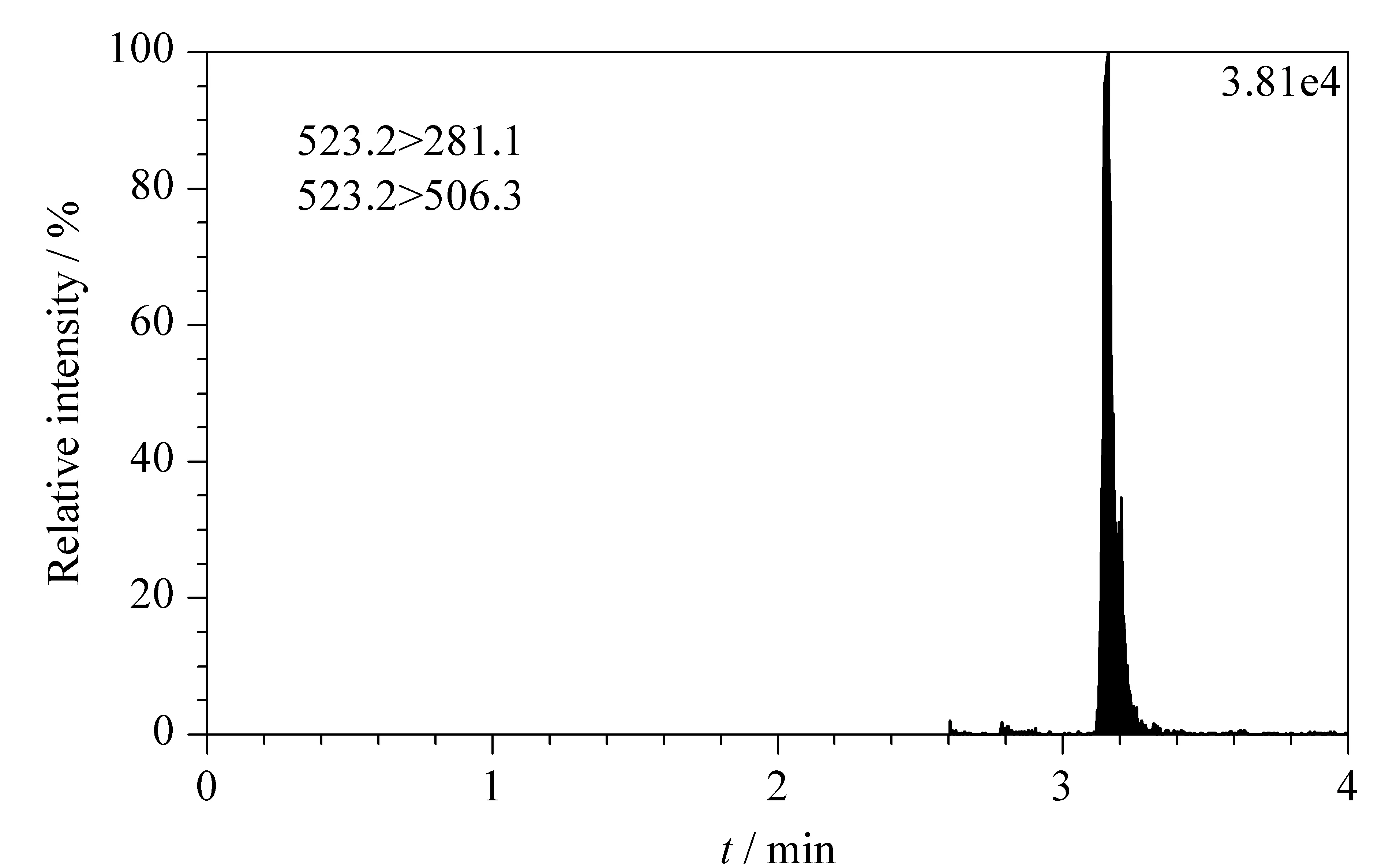
图 7 阳性地表水样品中溴氰菊酯的TIC色谱图Fig. 7 TIC chromatogram of deltamethrin in a positive surface water sample
2.7 实际样品检测
自2016年1月起,按照上述方法,对位于钱塘江、苕溪和千岛湖的杭州市集中式生活饮用水水源地水质进行每月一次的监测,部分水样中检出阿特拉津和溴氰菊酯。图6和图7分别为两个实际地表水样品中阿特拉津和溴氰菊酯的总离子流色谱图(TIC),其中图6水样检出阿特拉津(质量浓度为0.26 μg/L),图7水样检出溴氰菊酯(质量浓度为2.32 μg/L),检出化合物的质量浓度均远低于地表水环境质量标准规定的限值。
3 结论
本文建立了一种同时检测地表水中联苯胺、苦味酸、甲萘威、阿特拉津和溴氰菊酯的液相色谱-质谱联用方法。与原有的标准检测方法相比,灵敏度大大提高,仅需简单的超滤处理后直接进样检测,即可满足相关法规对地表水中这5项指标的控制标准要求,避免了烦冗的前处理程序,降低了实验人员因前处理过程中使用强毒性溶剂所面临的健康威胁,是一种高效、快速的适于实际水样中这5种目标化合物检测分析的方法。在杭州市地表水水质监测中,成功应用本方法对来自各个点位的水样进行了分析测定,部分水样中阿特拉津和溴氰菊酯有一定浓度的检出。
