荧光相关光谱法直接测定溶液中金纳米粒子浓度
2018-09-03刘芳超董朝青任吉存
刘芳超, 董朝青, 任吉存
(上海交通大学化学化工学院,上海 200240)
金纳米粒子(Gold Nanoparticles,AuNPs)由于具有强的表面等离子体共振等光学性质、稳定的物理化学性质、易于化学合成和表面修饰以及生物相容性好等优点,目前在生物传感[1 - 4]、基因或药物输送[5]、光动力学治疗[6]等领域具有重要的应用。AuNPs在这些生物应用过程中,如何准确测定其浓度是十分重要的。目前已经发展了多种AuNPs浓度的测定方法,如原子光谱/质谱-透射电镜测定法[7 - 8]、紫外-可见分光光度法[9]、流式细胞术计数法[10]、成像计数方法[11 - 12]、共振光散射相关光谱法[13]等。原子光谱/质谱-透射电镜测定法包括原子吸收光谱法、原子发射光谱法和质谱法等,是AuNPs浓度测定的经典方法。这类方法首先通过透射电镜测定AuNPs尺寸从而估计它所含Au原子数,同时将AuNPs消解后用原子光谱/质谱方法测定Au的浓度,从而计算AuNPs浓度。该方法测量结果准确,但步骤多,耗时长,其准确度受限于透射电镜法测定AuNPs中Au原子数,如AuNPs形貌的不规则等。紫外-可见光谱法是目前最简便的测定方法。在测定过程中采用其共振吸收峰处的吸光度值和相应的摩尔吸光系数值来计算。摩尔吸光系数值一般采用原子光谱/质谱-透射电镜测定法测得的数据,目前已有一些共振吸收峰波长与摩尔吸光系数值对应表[9]。但是,由于AuNPs的共振吸收峰位置随其尺寸变化的响应灵敏度较低,并易受表面配体的影响,这些都直接影响了该方法的准确应用。
近年来,Yan等人基于AuNPs在鞘流中形成的高信背比光子爆发信号,建立了流式细胞术测定AuNPs浓度的方法[10];Long等人建立了AuNPs成像计数分析方法[11];Ren等人建立了一种共振光散射相关光谱方法,实现了AuNPs浓度的测定[13]。这些方法主要利用了AuNPs的强共振散射光性质,对纳米颗粒进行直接测定。由于AuNPs在普通光源照射下激发产生的荧光很弱,甚少利用其荧光进行AuNPs的定量分析和成像分析。Ren等人发现,在激光照射下AuNPs能发出足够强的荧光信号,可被单光子检测器检测到信号,实现单颗粒分析[14]。
本文采用常见的柠檬酸三钠还原氯金酸的方法合成了多种不同粒径的AuNPs,利用激光激发AuNPs产生荧光信号,以实验室自主构建的荧光相关光谱(Fluorescence Correlation Spectroscopy,FCS)系统为检测仪器,通过优化光强等因素,建立了溶液中AuNPs摩尔浓度的直接测定方法,并与紫外-可见光谱法测得的浓度进行了比较。结果表明,建立的方法快速简便,可实现溶液中AuNPs摩尔浓度的直接测定。
1 实验部分
1.1 仪器与试剂
FCS系统[15]是在一台IX71倒置显微镜(日本,Olympus)基础上构建而成的,该系统使用561 nm的激光(德国,Coherent)作为激发光源。激光经过扩束镜扩束后由570DRLP双色镜(美国,Omega Optical)反射进入60×/NA1.2显微镜物镜(日本,Olympus),经物镜聚焦后激光照射到盖玻片上的样品溶液中。样品激发产生的荧光信号,经显微镜物镜收集后,透过双色镜和两片发射滤光片605DF50 和 BA590(美国,Omega Optical)滤除杂散光。通过的荧光经过35 μm针孔后由SPCM-AQR14单光子计数器(加拿大,Perkin-Elmer EG & G)收集。采集到的信号由Flex02-12D/C数字相关卡(深圳,Correlator.com)记录并自相关计算,得到FCS曲线。UV-3501紫外-可见分光光度计和WGY-10荧光光度计(天津市港东科技发展有限公司);JEM-2100透射电子显微镜(日本,电子)。
HAuCl4和柠檬酸三钠均购自国药集团化学试剂有限公司;叶酸、巯基聚乙二醇(分子量:5 000)、罗丹明 B (RB)购自美国Sigma-Aldrich公司。实验用水为超纯水。
1.2 AuNPs的合成及修饰
AuNPs采用经典的柠檬酸三钠还原HAuCl4的方法[15]制备。即油浴加热下在圆底烧瓶中加入98 mL超纯水和121 μL 0.2 mol/L HAuCl4,充分搅拌。待溶液沸腾后加入适量体积的0.01 g/mL 柠檬酸三钠溶液。反应溶液逐渐由黄色变为无色,再变成黑色,最终变成酒红色,之后继续加热15 min。将溶液冷却至室温,保存待用。通过改变加入柠檬酸三钠的体积,可以合成出不同尺寸的AuNPs。
表面修饰:将合成的1 mL AuNPs溶液,于4 000 r/min离心20 min后,弃去上清液;向其中加入10 μL 5 mmol/L的叶酸或者巯基聚乙二醇,混匀后室温下反应6 h,待用。
1.3 紫外-可见光谱法测定AuNPs浓度
先采用透射电镜测得AuNPs的平均粒径,然后根据文献查出其在共振吸收峰的摩尔吸光系数,再由紫外-可见分光光度计测定其在共振吸收峰的吸光度计算其浓度[9]。
1.4 荧光相关光谱法测定AuNPs浓度
测定前选用8 nmol/L罗丹明B为标准品对仪器系统进行校正,并测定荧光相关光谱系统的检测微区的体积。然后取用60 μL的AuNPs溶液或者修饰产物滴加在盖玻片上进行FCS测定,每次采样时间为120 s,平行测定3次。
2 结果与讨论
2.1 测定原理
荧光相关光谱中,激光通过聚焦物镜形成一个椭球形检测微区。溶液中AuNPs由于布朗运动不断进出该检测微区,从而在单光子计数器中生成荧光涨落信号,经数字相关卡对这些涨落信号进行自相关函数分析后,得到自相关曲线。根据分子/粒子自由扩散的自相关函数模型(公式1),曲线在纵轴上的截距(当τ=0时G(0))为检测微区内粒子数N的倒数值。
(1)
公式中,N为检测微区内平均分子或粒子数,τD为荧光分子或粒子的特征扩散时间,ω0和z0分别为椭圆形检测微区的轴向半径和纵向半径[17]。
检测微区体积的测定:采用已知扩散系数D的RB为标准品(温度在25 ℃下水溶液中的扩散系数约为2.8×10-6cm2/s)测定其FCS曲线,然后采用Origin 8.0 软件以公式1对获得的FCS曲线进行非线性最小二乘拟合,得到τD和S值,再采用公式(2)计算出检测微区体积。
(2)
其中,Veff为有效检测体积,S为检测体积的构型参数(S=z0/ω0),D为RB的扩散系数,τD为RB的特征扩散时间。
实验测得检测微区体积小于1.0 fL。因此在控制样品溶液不挥发的情况下,可以实现微小体积的样品检测,样品和试剂用量少。公式(3)为采用荧光相关光谱法测定浓度时的计算公式,其中NA为阿伏伽德罗常数。
(3)
2.2 AuNPs的表征
分别采用紫外-可见吸收光谱、荧光光谱和透射电镜对合成不同尺寸的AuNPs进行了表征。这些粒子的粒径分别为17.7 nm、 27.1 nm、37.8 nm和50.1 nm;共振吸收峰在520~530 nm之间;在630 nm处有荧光发射峰,可用于荧光检测。其中37.8 nm的AuNPs的透射电镜(TEM)图、紫外-可见光吸收光谱和荧光光谱如图1所示。
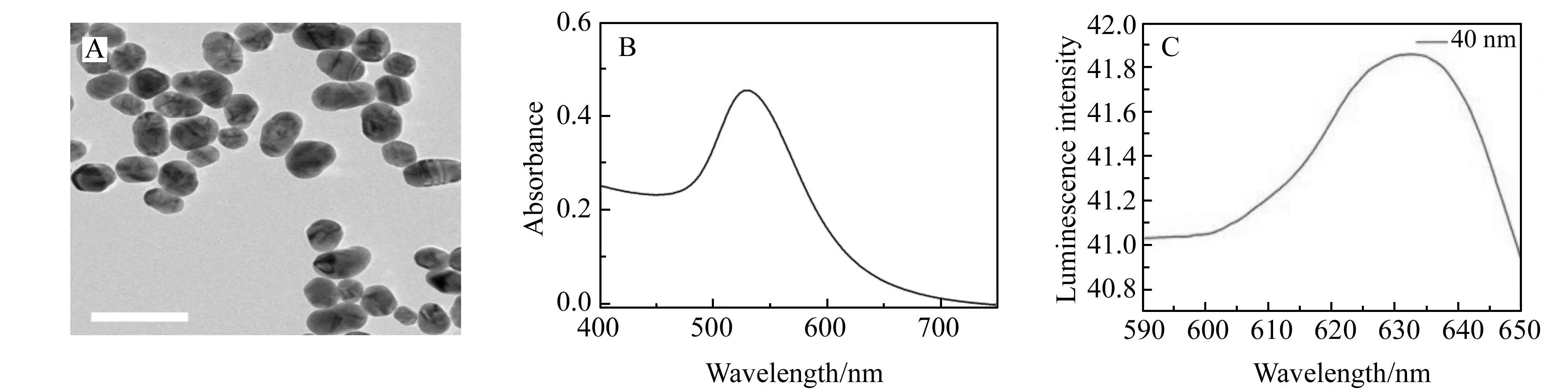
图1 AuNPs透射电镜(TEM)图(A)(标尺为100 nm)、紫外-可见(UV-Vis)吸收光谱(B)和荧光光谱(C)Fig.1 TEM image (A) (Scale bar is 100 nm),UV-Vis absorption spectrum (B) and fluoreescence spectrum(C) of AuNPs

图2 (A)在不同激光强度下测得的单颗粒荧光强度(BPP)柱状比较图;(B)在3.1 mW激发光强下测得的不同浓度AuNPs的荧光相关光谱(FCS)、拟合曲线、拟合残差分布曲线(内插图为测得AuNPs数目与浓度的线性关系曲线)Fig.2 (A) The histogram of brightness per particles(BPP) of AuNPs under different laser intensities;(B) The raw FCS,fitting,and residual curves of different concentration AuNPs under 3.1 mW of laser intensity(The inset is the linear relationship between the number and concentration)
2.3 检测条件优化
2.3.1激光光强对测定的影响AuNPs的荧光量子产率一般很低,在常规用于激发荧光小分子的激光光强(小于100 μW)下,其获得的微弱荧光信号无法用于荧光相关光谱单颗粒分析。图2A为激光强度分别为1.0 mW、3.1 mW、5.1 mW时AuNPs的单颗粒荧光强度;单颗粒荧光亮度随着激光强度增加而增强。这些单颗粒荧光亮度已足以用于单颗粒分析实验;同时,随着激光增强,背景噪音信号也逐步增加,将影响荧光相关光谱分析。因此系统研究了激光光强对金纳米粒子的荧光相关光谱曲线和浓度测定的影响。图2B为不同浓度的37.8 nm AuNPs在3.1 mW激光强度下的荧光相关光谱曲线。研究发现,采用三维自由扩散模型(公式1)拟合原始荧光相关光谱曲线得到的相关系数R2在0.914~0.998之间,残差介于±0.8之间,这说明AuNPs的三维自由扩散模型(公式1)可以很好地拟合荧光相关光谱曲线,并表明了粒子在水溶液中呈现布朗运动;另一方面,随着纳米粒子浓度的逐步减小,曲线的G(0)逐步增加(N值逐渐减小),证明获得的荧光相关光谱曲线确为AuNPs产生信号。内插图显示,测得的粒子数N与浓度具有良好的线性关系(相关系数为0.992),说明荧光相关光谱方法可以用于纳米粒子浓度的测定研究。
图3为不同激光激发强度下测得的浓度与紫外-可见光吸收光谱法测得浓度(c0)关系曲线。在三种不同的光强下,线性拟合的相关系数R2分别为0.988、0.996、0.993,线性相关性均较好,斜率分别为1.22、0.82和0.84。光强为3.1 mW和5.1 mW时,线性相关系数和斜率均较接近。但在1.0 mW和5.1 mW时每个数据点的标准偏差较大。因此选定优化后的激发光强为3.1 mW。

图3 不同激光激发强度下荧光相关光谱(FCS)法测得浓度与紫外-可见(UV-Vis)光谱法测得浓度(c0)关系曲线 Fig.3 The correlation of concentrations determined with FCS and UV-Vis methods A:1.0 mW;B:3.1 mW;C:5.1 mW.

图4 G(0)值随采样时间变化关系曲线Fig.4 The relationship between G(0) and the sampling time
2.3.2采样时间对测定的影响荧光相关光谱法测定AuNPs的重现性与检测时间有关,对检测时间进行了优化,如图4所示。图中误差棒为三次平行测定的标准偏差。随着采样时间延长,G(0)值波动逐渐减小,G(0)值的标准偏差逐步变小;采样时间超过60 s后,G(0)值基本不变;采样时间超过120 s后,标准偏差显著减小。因此,优化后的采样时间设置为120 s。
2.4 线性关系与检测限
在最优的检测条件下测定不同浓度AuNPs溶液,以测得的粒子数N为纵坐标,摩尔浓度为横坐标,得到它们的线性回归方程。17.7 nm:N=0.079+0.331c,线性范围为1~10 nmol/L,检测限为0.82 nmol/L。27.1 nm:N=0.095+0.090c,线性范围为0.2~7.9 nmol/L,检测限为0.17 nmol/L。37.8 nm:N=0.014+0.125c,线性范围为0.2~5.2 nmol/L,检测限为0.13 nmol/L。50.1 nm:N=0.003+0.283c,线性范围为0.2~1.2 nmol/L,检测限为0.10 nmol/L。
2.5 实际样品的测定
采用建立的分析方法对合成的不同尺寸、不同粒径的一系列AuNPs样品、巯基聚乙二醇和叶酸修饰的AuNPs样品进行了测定,并与紫外-可见光谱法进行对比,结果见表1。结果表明,27.1 nm和37.8 nm AuNPs样品测定中测定结果与紫外-可见光分光光度法结果接近。17.7 nm和50.1 nm AuNPs样品测定结果与紫外-可见光分光光度法结果偏差较大。但测量过程显示,荧光相关光谱测定过程中G(0)的变化仍与样品稀释倍数具有非常好的线性关系,因此这种偏差不应是样品的背景噪音造成的,可能与紫外-可见光分光光度法测定时引用的摩尔吸光系数数据偏差有关。说明该方法可以用于不同粒径、较宽的浓度范围内AuNPs浓度的准确测定。

表1 荧光相关光谱(FCS)和紫外-可见(UV-Vis)光谱法测定不同粒径AuNPs浓度的对比
aPEG -SH modified AuNPs;bFA modified AuNPs.
3 结论
利用AuNPs的荧光特性,采用荧光相关光谱建立了AuNPs摩尔浓度的测定方法,并成功用于合成的AuNPs溶液浓度测定。该方法在原理上与常用的原子光谱/质谱-透射电镜测定法、紫外-可见分光光度法和近年来提出的流式细胞术计数法、成像计数方法有显著不同。该方法快速简便,样品用量少,并对测定的样品无破坏,有望应用于活细胞内AuNPs浓度的实时原位测定。
