新生儿危重先天性心脏病的超声心动图诊断及外科治疗经验
2018-09-03孟红逄坤静王浩徐楠李守军闫军花中东王强
孟红,逄坤静,王浩,徐楠,李守军,闫军,花中东,王强
方法:回顾2012-01至2017-01来中国医学科学院阜外医院就诊的160例危重先心病新生儿资料,总结并分析这类患者的超声心动图诊断及外科治疗经验。危重先心病指:患有严重心内或大血管结构异常,容易导致难以纠正的低氧血症、酸中毒、呼吸道感染、心力衰竭等,只有通过外科或介入治疗才能生存。
结果:患儿术前超声心动图诊断包括完全性大动脉转位(50%)、室间隔完整型肺动脉闭锁或重度肺动脉瓣狭窄(17.5%)、单纯主动脉离断或弓缩窄(15%)、完全型肺静脉异位回流(10.6%)、共同动脉干或右肺动脉起源于升主动脉(3.8%)、合并室间隔缺损的肺动脉闭锁或重度法乐四联症(1.9%)、巨大室间隔缺损并发严重左心衰竭(0.6%)、右心房占位(0.6%)。共140例患儿接受手术治疗,其中134例接受一期根治手术,4例接受姑息手术,2例接受分期根治手术。院内死亡率为7.9%。129例患儿接受术后随诊,平均随访时间(16.8±18.2)个月。仅2例患儿接受二次手术,其余患儿均康复良好。
结论:有八类先心病需在新生儿期进行外科干预,既有紫绀型又有肺血多型。大部分危重先心病患儿经手术治疗可获得良好效果。
危重先天性心脏病(先心病)是指心脏大血管的严重解剖畸形,从而造成血液动力学严重异常,导致患儿出现难以纠正的低氧血症、酸中毒并呈进行性恶化,或反复出现呼吸道感染、心力衰竭,内科治疗难见成效。新生儿期危重先心病患儿表现尤其明显,只有通过外科或介入治疗才能生存[1]。新生儿期需要救治的危重先心病包括不同病种,其病理解剖、临床症状、手术方式也各有不同[2]。准确进行术前评估是制定最优手术方案、把握最佳治疗时机的前提[3]。本研究旨在回顾中国医学科学院阜外医院近5年救治的新生儿期危重先心病患儿资料,总结其病种分布、术前超声诊断要点及手术治疗情况。
1 资料与方法
本研究自2012-01至2017-01期间连续收集来中国医学科学院阜外医院就诊的新生儿期危重先心病患儿160例。危重先心病指:患有严重心内或大血管结构异常,容易导致难以纠正的低氧血症、酸中毒、呼吸道感染、心力衰竭等,只有通过外科或介入治疗才能生存。所有患儿在我院救治的临床资料齐全,均通过超声心动图明确诊断,其中28例行心血管造影或计算机断层摄影术(CT)补充或肯定超声心动图诊断。所有手术患儿于术后一周复查超声心动图。出院后患儿在门诊接受临床和超声心动图随访以及电话随访。
统计学方法:采用SPSS 19.0统计学分析软件处理所有数据,正态分布计量资料以均数±标准差表示,非正态分布计量资料以中位数及范围表示,计数资料以例(%)表示。
2 结果
160例患儿中,男113例,女47例,就诊时平均年龄(14.1±8.8)d。24例患儿术前经历抢救(表1)。
160例患儿涉及的先心病病种(图1):80例(50%)完全性大动脉转位(TGA);28例(17.5%)室间隔完整型肺动脉闭锁或重度肺动脉瓣狭窄;24例(15%)单纯主动脉弓离断或弓缩窄;17例(10.6%)完全型肺静脉异位回流(TAPVC);6例(3.8%)共同动脉干或右肺动脉起源于升主动脉;3例(1.9%)合并室间隔缺损(室缺)的肺动脉闭锁或重度法乐四联症;1例(0.6%)巨大室缺并发严重左心衰竭;1例(0.6%)右心房占位,梗阻三尖瓣口。
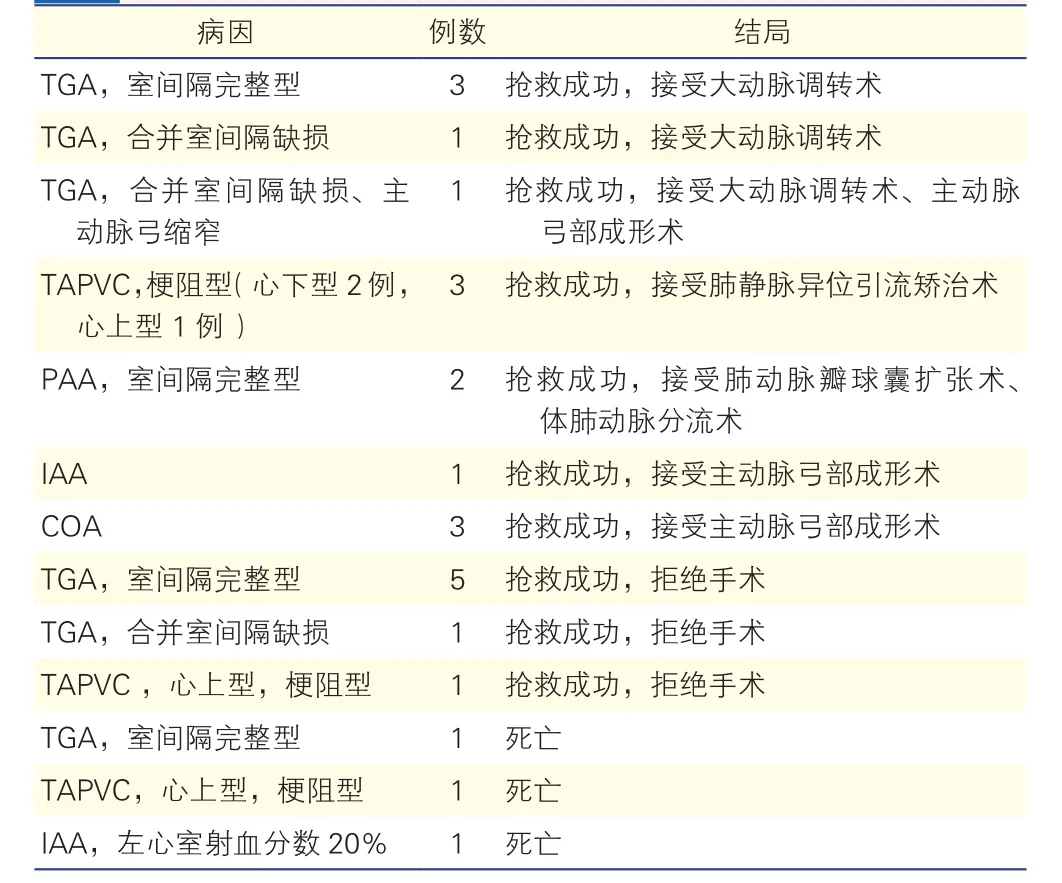
表1 住院期间术前经历抢救的24例先天性心脏病患儿情况

图1 160例新生儿期危重先天性心脏病病种分布
80例TGA患儿中,52例为室间隔完整型,平均经皮氧饱和度为67%(25%~90%);26例合并室缺,平均经皮氧饱和度为72%(45%~97%)。2例TGA患儿同时合并严重主动脉弓部病变(A型主动脉弓离断和重度主动脉弓缩窄),术前行CT检查肯定超声心动图对主动脉弓部病变的诊断。
17例TAPVC患儿中,8例心上型,5例心内型,3例心下型,1例混合型;12例共同肺静脉干回流途径存在梗阻或合并小房间隔缺损(≤4 mm),甚至仅为卵圆孔未闭(图2)。TAPVC患儿的平均经皮氧饱和度为77%(38%~89%)。术前7例患儿行CT检查明确肺静脉异常回流途径,与超声心动图检查结果均一致,无肺内静脉狭窄。
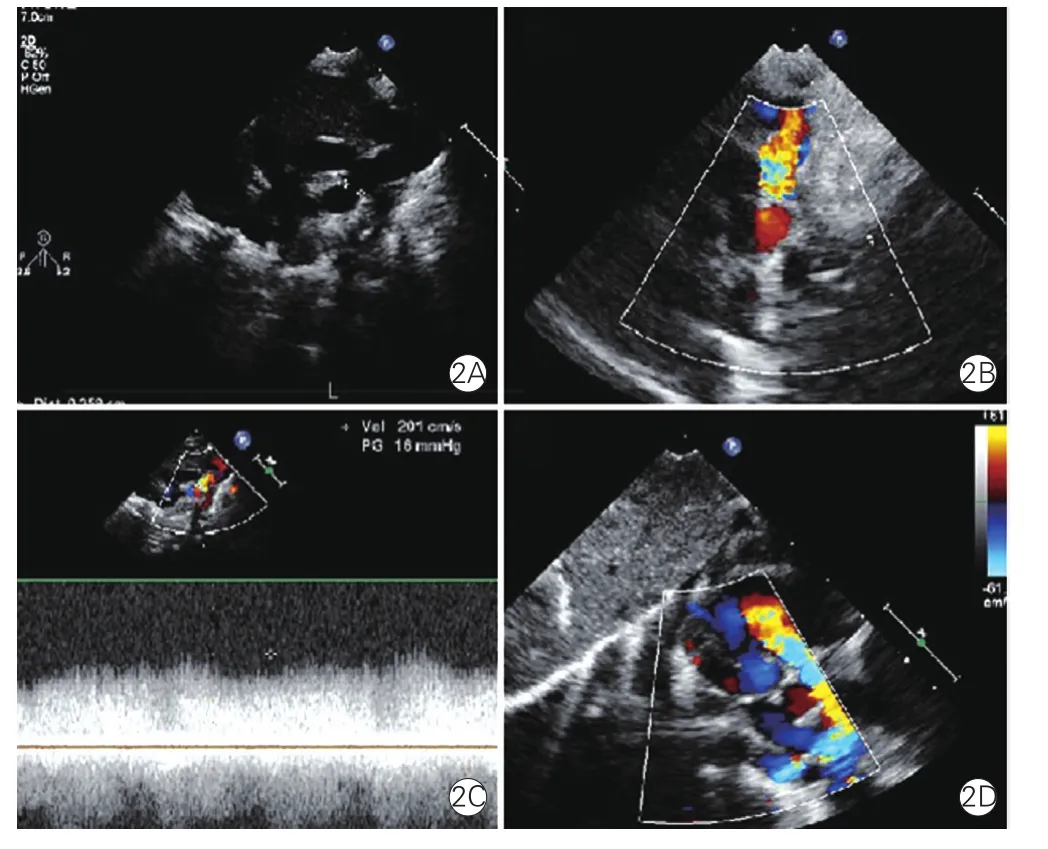
图2 完全型心上型肺静脉异位回流病例超声心动图结果
15例室间隔完整型肺动脉闭锁的患儿中,5例出现右心室发育不良;13例重度肺动脉瓣狭窄的患儿中,1例合并右心室发育不良(图3)。所有患儿均合并三尖瓣中度或以上程度反流,其中2例合并瓣叶发育不良、瓣叶狭窄或无启闭功能。患儿的平均经皮氧饱和度为73%(45%~94%)。
9例单纯主动脉弓离断患儿中,6例为A型,3例为B型[4],均合并室缺及动脉导管未闭;15例重度主动脉弓缩窄患儿,降主动脉最窄处内径2~4 mm,其中2例合并二尖瓣病变(伞型二尖瓣或瓣上狭窄)。患儿的平均经皮氧饱和度为93%(54%~100%)。14例患儿(5例主动脉弓离断,9例主动脉弓缩窄)术前行CT检查,与超声心动图检查结果一致。

图3 重度肺动脉瓣狭窄病例超声心动图结果
2例共同动脉干患儿,均为主肺动脉发自动脉干(Van Praaph A1型)[5],合并较大室缺(9 mm),均行CT检查肯定超声心动图诊断;4例右肺动脉起源于升主动脉,室间隔均完整且合并动脉导管未闭。患儿的平均经皮氧饱和度为92%(80%~92%)。
2例肺动脉闭锁和1例重度法乐四联症患儿,合并较大室缺,肺动脉发育极差。术前均行心血管造影,肯定超声心动图对肺动脉发育情况的诊断,左、右肺动脉内径 2~4 mm(Z值 -3~-7.2),患儿发育滞后,紫绀严重,平均经皮氧饱和度为78%(65%~86%)。
最终共140例患儿接受手术治疗(表2),其中非体外循环下手术26例,体外循环下手术114例。134例接受一期根治手术,4例接受姑息手术,2例接受分期根治手术。患儿手术时的平均年龄为(20.6±7.8)d(3~30 d),平均体重(3.5±0.6)kg(1.8~5.1 kg)。
11例(7.9%)接受手术的患儿院内死亡。129例(92.1%)患儿出院后接受临床及超声心动图随诊。平均随诊时间(16.8±18.2)个月(1~62个月)。仅2例患儿接受二次手术:一例主动脉弓缩窄成形术后患儿3个月超声心动图复查显示主动脉弓部再次狭窄,二次行主动脉弓部成形手术,术后随诊主动脉弓降部恢复通畅;另一例室间隔完整型TGA行大动脉调转术及肺动脉瓣成形术,术后18个月超声心动图复查发现肺动脉瓣再次狭窄,二次行肺动脉瓣球囊扩张术,术后肺动脉瓣口峰值压差下降。其余患儿康复良好。
表2 140例患儿术前诊断及手术情况(±s)
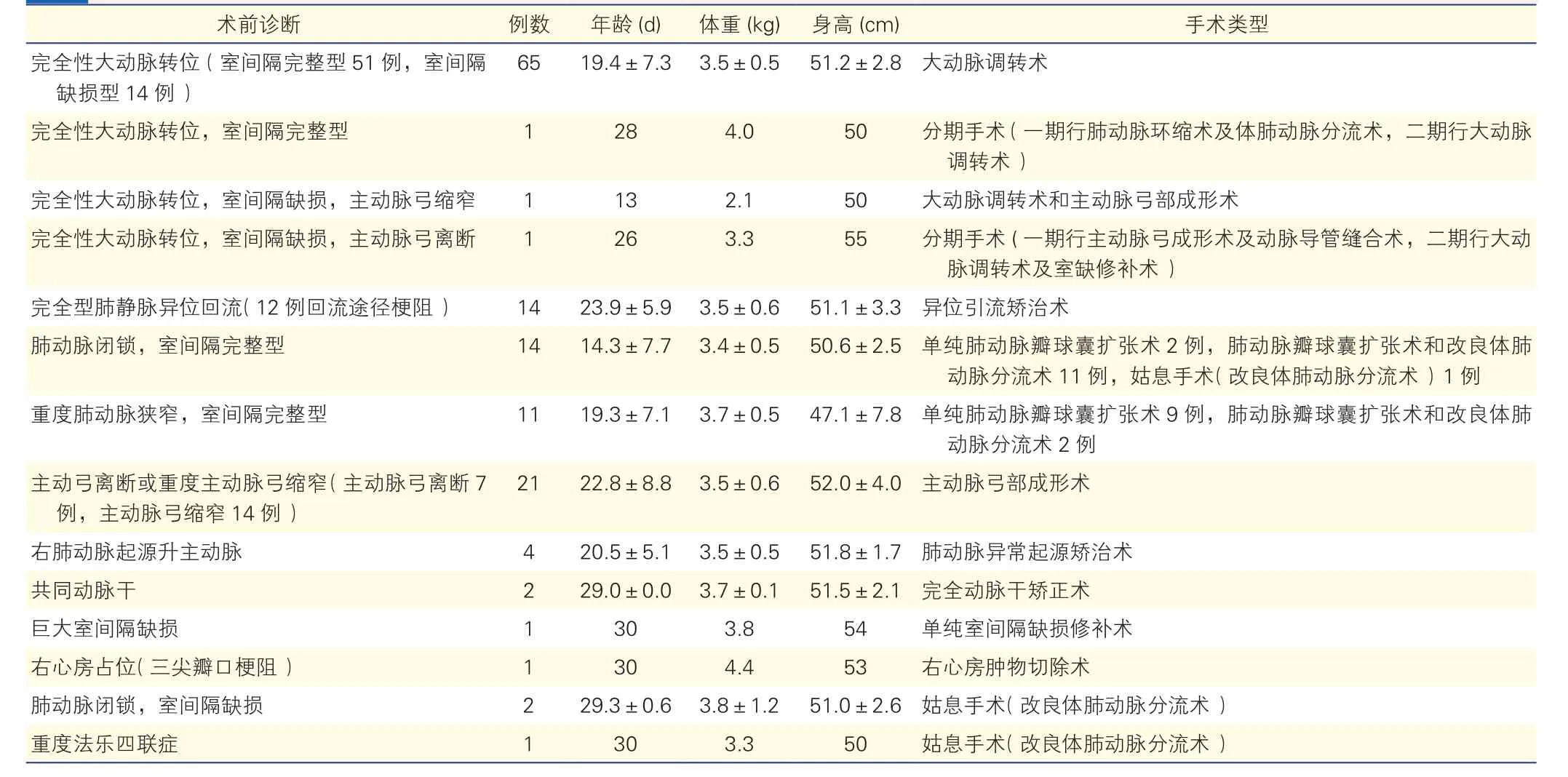
表2 140例患儿术前诊断及手术情况(±s)
术前诊断 例数 年龄(d) 体重(kg) 身高(cm) 手术类型完全性大动脉转位(室间隔完整型51例,室间隔缺损型14例)65 19.4±7.3 3.5±0.5 51.2±2.8 大动脉调转术完全性大动脉转位,室间隔完整型 1 28 4.0 50 分期手术(一期行肺动脉环缩术及体肺动脉分流术,二期行大动脉调转术)完全性大动脉转位,室间隔缺损,主动脉弓缩窄 1 13 2.1 50 大动脉调转术和主动脉弓部成形术完全性大动脉转位,室间隔缺损,主动脉弓离断 1 26 3.3 55 分期手术(一期行主动脉弓成形术及动脉导管缝合术,二期行大动脉调转术及室缺修补术)完全型肺静脉异位回流(12例回流途径梗阻) 14 23.9±5.9 3.5±0.6 51.1±3.3 异位引流矫治术肺动脉闭锁,室间隔完整型 14 14.3±7.7 3.4±0.5 50.6±2.5 单纯肺动脉瓣球囊扩张术2例,肺动脉瓣球囊扩张术和改良体肺动脉分流术11例,姑息手术(改良体肺动脉分流术)1例重度肺动脉狭窄,室间隔完整型 11 19.3±7.1 3.7±0.5 47.1±7.8 单纯肺动脉瓣球囊扩张术9例,肺动脉瓣球囊扩张术和改良体肺动脉分流术2例主动弓离断或重度主动脉弓缩窄(主动脉弓离断7例,主动脉弓缩窄14例)21 22.8±8.8 3.5±0.6 52.0±4.0 主动脉弓部成形术右肺动脉起源升主动脉 4 20.5±5.1 3.5±0.5 51.8±1.7 肺动脉异常起源矫治术共同动脉干 2 29.0±0.0 3.7±0.1 51.5±2.1 完全动脉干矫正术巨大室间隔缺损 1 30 3.8 54 单纯室间隔缺损修补术右心房占位(三尖瓣口梗阻) 1 30 4.4 53 右心房肿物切除术肺动脉闭锁,室间隔缺损 2 29.3±0.6 3.8±1.2 51.0±2.6 姑息手术(改良体肺动脉分流术)重度法乐四联症 1 30 3.3 50 姑息手术(改良体肺动脉分流术)
3 讨论
新生儿出生后动脉导管日趋变细、闭合,使部分先心病在新生儿期成为致死性疾病。虽然近50年来先心病的诊疗及围手术期管理水平显著提高,但新生儿各个脏器未完全发育成熟,复杂的心外科手术以及暴露于体外循环下激发的炎性反应均会导致新生儿期心外科手术风险增高。所以术前更需通过超声心动图鉴别出新生儿期危重先心病,准确把握诊断要点,选择手术时期,避免过早治疗,也避免延误治疗而危及生命。
本研究中,TGA占据新生儿期危重先心病的一半,是最常见的在新生儿期需要紧急救治的先心病。该疾病因心室、动脉连接不一致,患儿全身器官处于缺氧状态,所以动、静脉血液混合越多,患儿越安全。但动脉导管在新生儿期趋于闭合,虽静脉泵入前列腺素E1,但有时依然难以维持导管开放。当合并较大的室缺时,较多氧合血可以通过室水平分流进入主动脉,提高患儿混合血的氧合度;反之当室间隔完整时,患儿更危重。在本研究中,需要术前抢救的11例TGA患儿中,9例为室间隔完整型。所以术前超声诊断TGA时,尤其需要关注室间隔情况,完整型或仅合并小房室间隔缺损的TGA更危重,更需要及早救治。此外,室间隔完整型TGA患儿在出生后随着肺动脉阻力下降,与肺动脉相连的左心室内压力也下降,导致左心室无法承担动脉调转术后的体循环压,这种现象称为解剖左心室退化[6]。超声心动图表现为收缩期室间隔明显向左心室侧偏移,呈压低状态,提示解剖左心室内压力下降,还可测量二、三尖瓣反流速度,估算及比较解剖左、右心室收缩压,当双心室收缩压比值<60%时,需通过手术环缩主肺动脉,增加解剖左心室后负荷,纠正左心室退化,一般术后一周再次行超声心动图评估,当双心室收缩压比值>60%时,室间隔运动基本恢复正常,再行大动脉调转术。
排在新生儿期危重先心病第二位的为室间隔完整型肺动脉闭锁或重度肺动脉瓣狭窄,约占总病例数的17.5%。因为经肺动脉瓣口无或极少血流入肺氧合,所以患儿严重缺氧、紫绀,应尽早实施球囊扩张术,解除瓣膜闭锁或狭窄才是根本救治方法[7]。如果患儿合并右心室发育不良,单纯瓣膜成形术后氧饱和度多不满意,需加做改良体肺分流术,改善氧和[8]。术前超声心动图评估要点:(1)右心室的三部分腔室大小(流入部、流出部、心尖小梁部),心尖小梁部及流出部最易被异常肌束填充,严重发育不良病例超声心动图四腔心切面可观察到右心室长径远小于左心室长径,流入部变小,流出腔甚至呈缝隙样;(2)三尖瓣瓣环大小,超声心动图测量二、三尖瓣瓣环直径,同时计算Z值。正常情况三尖瓣瓣环应大于或至少等于二尖瓣瓣环,若所测值远小于二尖瓣环,则证明三尖瓣瓣环发育不良;(3)三尖瓣瓣叶发育情况,预测术后三尖瓣反流情况;(4)冠状动脉病变,尤其右心室依赖型冠状动脉循环,这种情况多发生在严重右心室发育不良,三尖瓣瓣环发育差(Z值大多<-5)的病例。合并室缺的肺动脉闭锁或法乐四联症多不在新生儿期行根治手术,只有在患儿频繁缺氧发作时,才实施改良体肺动脉分流术,以避免缺氧意外发生。
本研究中处于第三位的新生儿期危重先心病为主动脉弓离断或缩窄,约占患儿总数的15%。严重降主动脉病变会引发下肢及内脏缺血。所以本研究中2例主动脉弓离断和3例主动脉弓缩窄患儿术前出现呼吸急促、严重酸中毒而接受抢救。此外,严重主动脉弓部病变会引发左心功能减低、重度肺动脉高压,增加围手术期死亡风险。Kreutzer等[9]指出,主动脉弓离断患者合并发育小的主动脉瓣环或瓣叶畸形(如二瓣化)时,术后易出现左心室流出道狭窄,这与圆锥间隔病理性向后移位有关。所以术前超声诊断主动脉弓离断或缩窄时,观察重点包括主动脉弓部病变位置及累及长度、分支动脉是否在病变部位发出、心脏功能及主动脉瓣发育情况。术前可行CT检查明确主动脉弓部病变累及长度以及分支动脉情况。
另一种在新生儿期容易导致猝死、需急救的先心病为TAPVC,约占所有患儿的10.6%,回流途径存在梗阻时尤为危重。梗阻部位包括肺静脉总干、垂直引导静脉或限制性房水平分流(小缺损甚至卵圆孔未闭)。所以本研究中术前抢救的5例患儿都是梗阻型TAPVC。Seale等[10]指出,术前严重的肺静脉梗阻是术后肺静脉狭窄发生及死亡的独立危险因素,这可能和长时间的回流途径梗阻导致肺静脉分支发育不良有关。所以术前超声心动图需仔细追踪检查回流途径中是否存在梗阻,房水平分流情况,术前可行CT检查明确肺内静脉发育情况。
其他类型先心病包括共同动脉干、右肺动脉起源于升主动脉、巨大室间隔缺损等会诱发少数患儿出现药物难以纠正的心力衰竭,所以可选择在新生儿期手术矫治。在行超声心动图检查时,需结合临床表现找出心力衰竭的病因,为临床治疗提供及时、准确的信息。
本研究中提到的八种先心病均为新生儿期致死性先心病,必须予以及时、准确的救治。术前超声心动图诊断至关重要,明确每一种危重先心病的术前诊断要点,才能提供合理的术前建议,制定最优的手术方式,从而提高新生儿期危重先心病的救治效果。
特别感谢盘锦市中心医院李剑白医师参与电话随访工作。
