血管超声对颈部动脉夹层的临床诊断价值
2018-08-30沈德娟夏炳兰
沈德娟,夏炳兰*,孙 骏
1.江苏省苏北人民医院超声科,扬州 225001 2.江苏省苏北人民医院医学影像科,扬州 225001
颈部动脉夹层(cervical artery dissection, CAD)临床表现缺乏特异性,诊断主要依靠影像学手段[1-2]。数字减影血管造影(digital subtraction angiography, DSA)是评价CAD的金标准,但其具有创伤性、操作繁琐、耗时、设备要求高和费用高等缺点,限制了其普及应用[3]。近年来,无创性超声血管成像技术发展迅速,被越来越多地应用于颈部动脉疾病的诊断[4]。因此,本研究重点分析CAD的血管超声影像学特征,并探讨血管超声对CAD的诊断价值。
1 资料与方法
1.1 一般资料 选择2016年1月至2017年3月于江苏省苏北人民医院就诊怀疑CAD的32例患者作为研究对象,对其影像学资料进行回顾性分析。其中,男性21例,女性11例,年龄36~80岁,中位年龄43.6岁。患者临床诊断为急性缺血性脑卒中,表现为局灶性神经功能缺损,伴颈部疼痛6例,明确外伤史2例。患者首先接受颈动脉超声检查,均在48 h内完成高分辨率MRI(HR-MRI)检查,其中12例行DSA检查。
1.2 检查方法
1.2.1 血管超声检查 GE Logiq E9型彩色超声仪及线阵与凸阵探头联合应用,沿双侧颈总动脉、颈内动脉及椎动脉走行,先横切面后纵切面扫查,重点观察动脉管腔二维形态及管径、内中膜厚度、斑块大小及回声强度、彩色血流状况,记录血管频谱形态、收缩期峰值血流速度、舒张期末血流速度、血管阻力指数等指标。所有患者的超声检查及诊断均由2名有10年以上颈部血管超声诊断经验的医师共同完成。
1.2.2 磁共振检查 应用GE Discovery MR750W 3.0 T超导型MRI扫描仪,头颈部相控阵线圈。(1)冠状位脂肪抑制CUBE T1WI:重复时间(repetition time, TR)/回波时间(echo time, TE): 575/15 ms,层厚0.8 mm,视野(field of view, FOV)200 mm×180 mm,矩阵 320×256。(2)轴位3D TOF血管成像:TR/TE 30 ms/min,层厚1.8 mm,FOV 200 mm×176 mm,矩阵256×192。
1.2.3 DSA检查 采用GE Innove 3100 DSA造影机、改良Seldinger法,经股动脉穿刺,分别行主动脉弓上血管及全脑血管造影。
1.3 图像分析 参考相关文献[5-6],拟定CAD如下诊断标准:(1)DSA或MRI检查至少发现特征性表现,线样狭窄、夹层动脉瘤、内膜瓣、“鼠尾征”、“火焰征”、“双腔征”中的1种;(2)磁共振T1抑脂序列见血管壁内血肿呈显著高信号。各由1名高年资神经影像诊断医师和神经介入医师进行盲法阅片,分析其影像学表现,意见不一致时协商解决。
1.4 统计学处理 采用SPSS 16.0统计软件进行数据处理。绘制受试者工作特征(ROC)曲线,计算曲线下面积,计算血管超声诊断CAD的敏感度、特异度及准确度。采用Kappa一致性检验分析血管超声与HR-MRI评估CAD的一致性。
2 结 果
2.1 CAD的血管超声特征 32例患者共发现血管病变42处。其中,19例患者共23处动脉夹层病变,包括5处椎动脉夹层(图1)、18处颈内动脉夹层(图2)。血管超声直接征象表现为壁内血肿14处(图1A)、双腔5处(图2A)、瘤样扩张3处、瓣膜漂浮1处。间接征象包括夹层位于非粥样硬化好发部位,共17处;夹层近段或远段阻力指数的改变,共16处;夹层与对侧正常血流速度的差异超过50%,共12处。余13例为动脉粥样斑块所致动脉狭窄共19处,其中3处斑块内见出血。

图1 右侧椎动脉夹层血管超声及MRI影像
A:血管超声示椎动脉椎间孔段(V2段)低回声充填,箭头处为壁内血肿;B:MRI-T1加权脂肪抑制示高信号影环绕受压的真腔(箭头)
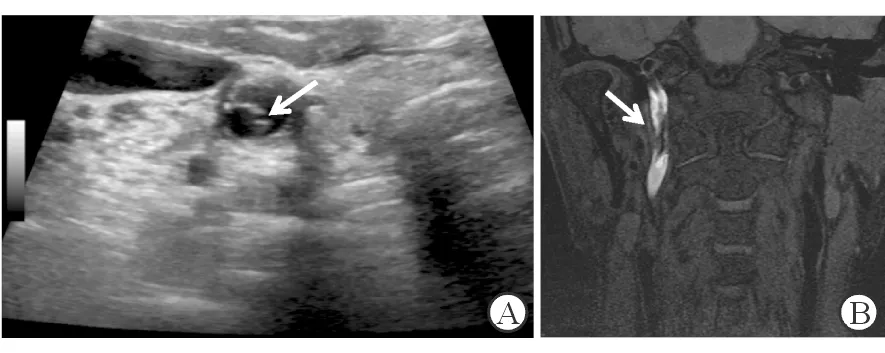
图2 右侧颈内动脉夹层血管超声及MRI影像
A:血管超声显示右侧颈内动脉颈段内膜破口(箭头),内膜瓣分隔呈双腔结构;B:MRI-T1加权脂肪抑制示高信号影环绕受压的真腔(箭头)
2.2 血管超声对CAD的诊断价值 血管超声将2处颈部动脉斑块合并出血误诊为CAD,2处CAD漏诊。结果(表1)表明:以DSA和(或)MRI检查结果为标准,血管超声诊断CAD的敏感度为91.3%(21/23),特异度为89.5%(17/19),准确度为90.5%(38/42);ROC曲线下面积为0.904,将其与HR-MRI行一致性检验,Kappa值为0.808。
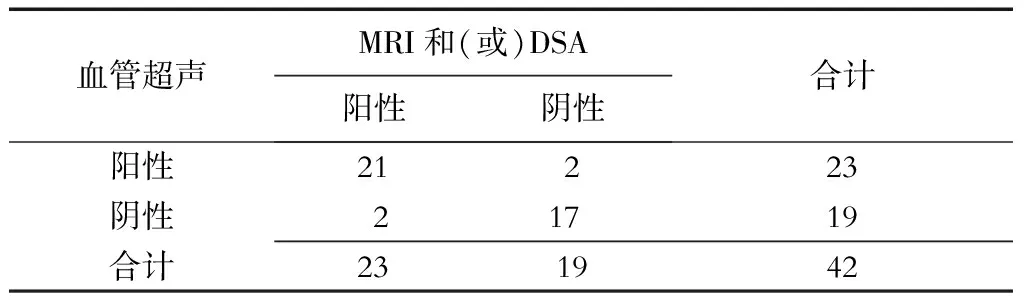
表1 血管超声与MRI和(或)DSA诊断CAD结果对比 n
3 讨 论
CAD 是青壮年缺血性卒中的重要原因,占青壮年缺血性卒中的15%~20%[7]。CAD的临床表现多样化,影像学检查是诊断CAD的重要手段。长期以来,DSA一直是被认为是诊断CAD的金标准,但仅能发现不到10%的“双腔征”和内膜瓣,对“鼠尾征”“线样征”“火焰征”和动脉瘤具有诊断价值,但非特异性[2,8]。而且,因其具有创伤性、电离辐射、操作繁琐、费用高等缺点,目前DSA诊断CAD有被其他影像学方法取代的趋势[3]。有研究[9]以MRI-T1加权脂肪抑制结合MRA作为诊断标准,该方法可以直观显示内膜血肿,最具特征性的征象是扩张的动脉中可见新月形高信号环绕受压的真腔,真腔通常是偏心的流空低信号。本研究中,MRI检查采用CUBE T1扫描技术能实现快速采集高分辨率各向同性的数据[10],并实现任意角度重建,有利于评估颈部血管解剖结构和病变。而用颈动脉超声不仅可以直接观察动脉管壁情况,还能观察血流方向、测量血流速度等血流动力学参数,并可以观察到夹层破口,对MRI所显示直观静止的影像是很好的补充[1,11]。同时,颈部血管超声检查具有无创、费用低、操作简便快捷、床旁实时反复动态观察病情等优点。因此,本研究着重分析CAD的超声影像学特征,探讨血管超声对CAD的诊断价值。
本研究对32例临床怀疑CAD的脑卒中患者进行超声检查和分析,以MRI和(或)DSA为诊断标准,血管超声诊断CAD的敏感度为91.3%、特异度为89.5%、准确度为90.5%,ROC曲线下面积为0.904,与Nebelsieck等[12]研究结果基本相符。本研究中,CAD主要血管超声表现为壁内血肿,二维超声显示低回声物质充填导致管腔不同程度狭窄或闭塞,占60.9%(14/23);显示内膜破口血流信号,内膜瓣分隔呈双腔结构,真腔与假腔内见“红蓝”血流信号,占21.7%(5/23);少数可呈现瘤样扩张及瓣膜漂浮。本研究中,间接征象包括夹层位于非粥样硬化好发部位(73.9%,17/23),多普勒显示夹层近段或远段阻力指数改变(69.6%,16/23),夹层与对侧正常血流速度的差异超过50%(52.2%,12/23)。本研究结果同时对超声和MRI行一致性检验,Kappa 值为0.808,说明血管超声诊断CAD与MRI一致性良好,存在较好的诊断价值,加之血管超声具有价格便宜、对患者依从性要求低等优点,相比MRI更易于被患者接受。
此外,2处假阴性CAD发生于颈内动脉颅内段,位置偏高,单用线阵探头,检查长度受限,MRI未能探及异常血流动力学变化,应联合应用凸阵式探头。此外,CAD随时间变化,其病理形态学及血流动力学都会发生改变,可实时反复动态观察。2处假阳性CAD是由颈动脉斑块所致管腔重度狭窄,狭窄段血流速度显著增快,超声探测到红蓝相杂的湍流信号,因而误诊。受仪器分辨率、操作者经验等因素的影响,CAD易误诊、漏诊,应结合患者的临床特征,全面扫查。
综上所述,血管超声能清晰显示CAD血管腔及管壁的多种影像学征象,可以较准确地诊断CAD,且敏感度、特异度较高,是诊断CAD快速而有效的影像学方法,值得推广应用。
