Bi/TiO2复合催化剂制备及其用于降解罗丹明B研究
2018-08-29
(四川大学化学工程学院,四川成都,610065)
由于工业和生活废水的排放,大量的有机污染物进入淡水中,这些有机废水生物毒性大、涉及面广、有机污染物种类复杂,单一的物理或生物治理方法很难将其完全净化。因此,研究开发一种高降解活性且降解有机物种类多的新型污水治理方法已迫在眉睫。其中光催化以其利用能源清洁、制备工艺成本低、降解彻底以及底物无选择性等优点从众多新型污水治理方法中脱颖而出,受到广泛关注。二氧钛以其催化活性好、来源广泛、价格便宜、环境友好等一系列优点被认为是最有发展潜力的光催化剂[1]。但由于TiO2光生载流子利用率较低,绝大多数载流子在参与光催化反应之前便已经发生了复合[2]。因此,为了提高TiO2的载流子利用率,本文采用光沉积法,在TiO2纳米片表面沉积Bi金属颗粒,通过调节沉积时间来优化Bi/TiO2的催化活性,使其达到最优催化效果。采用罗丹明B模拟有机污染物,对所得样品光催化活性进行测试,实验结果表明:当沉积时间为1h时,样品TiO2-1H活性最好,此时TiO2表面Bi颗粒大小为6 nm,根据Langmuir-Hinshelwood公式拟合结果显示此时反应速率常数k1值为0.471 min-1,相比于空白样品k0值的0.0144 min-1提高了32倍。
1 实验
1.1 催化剂制备
TiO2纳米片采用一步水热法合成,在搅拌状态下向10 ml钛酸丁酯(TBOT)中滴加1.2 ml氢氟酸,待混匀后转移至高压水热釜中,置于180 ℃烘箱内反应24 h[3],反应结束后,冷却至室温,经0.1 M氢氧化钠溶液和无水乙醇分别润洗3次后干燥即得TiO2。
Bi/TiO2复合催化剂采用光沉积法合成,称取0.36 g五水硝酸铋溶解至100 ml的0.1 M硝酸溶液中,然后向溶液中加入0.2 g上述TiO2纳米片,置于汞灯下进行光沉积,沉积完毕后经离心、洗涤、干燥即得样品,沉积时间为0.5 h、1 h、2 h样品编号分别为TiO2-0.5H、TiO2-1H、TiO2-2H。
1.2 催化剂表征
XRD测试仪器为EMPYREAN(荷兰帕纳科公司)X射线衍射仪,测试管电压为40 KV、管电流为40 mA,扫描步长为0.026°,扫描角度2θ为15°-80°;TEM以及元素Mapping测试仪器为FEI Titan G2 60-300(AC-TEM)。
1.3 活性评价
取100 mL 15 mg/L的RhB水溶液模拟污染物,然后称取50.0 mg催化剂均匀分散于溶液中,置于遮光处搅拌30 min,待催化剂表面RhB吸附平衡后置于汞灯下进行催化反应,每3min取样一次,离心后采用紫外-可见分光光度计检测上层清液吸光度,由标准曲线得出此时RhB剩余浓度,最后根据Langmuir-Hinshelwood模型得出各样品反应速率常数[4]。
2 结果与讨论
2.1 XRD测试
XRD测试结果如图1所示,根据PDF 21-1272和PDF 26-0214可知,图中25.3°、37.8°、48.1°、53.9°、55.1°、70.3°分别为锐钛型TiO2的特征衍射峰,32.0°为Bi金属单质特征衍射峰[5],从图中可以看出Bi的衍射峰较宽且峰强较弱,说明Bi颗粒分散性较好且尺寸较小,这种小尺寸的Bi颗粒可以有效汇集TiO2表面电子,促进内部电子向表面扩散,从而提高载流子利用率[6];但如果Bi颗粒过大,则会促进载流子复合,使得催化剂活性降低[7]。
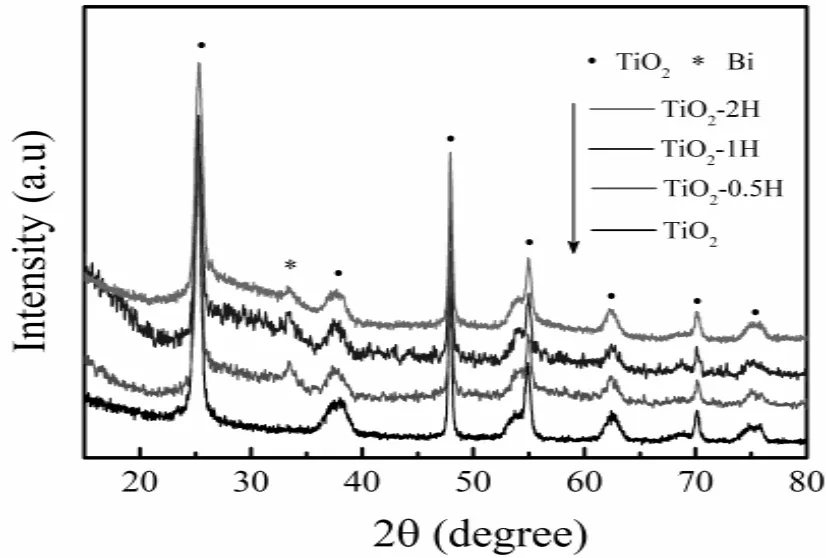
图1 样品XRD衍射图谱
2.2 活性测试
样品的RhB降解曲线如图2所示,催化剂活性采用L-H模型进行评价,k值如图3所示。从图中可以看出Bi/TiO2复合催化剂活性均高于TiO2,这是由于在光催反应过程中,TiO2体相产生的光生载流子未能及时转移至催化剂表面,导致其内部载流子浓度过大,增加载流子复合概率,因此活性较低;而Bi/TiO2复合催化剂表面的Bi金属颗粒可以有效的汇集TiO2表面的光生载流子,促进内部载流子向表面扩散,增加载流子利用率,因此活性较高[8]。且随着沉积时间的增加,催化剂的活性先增加后减小,其中TiO2-1H活性最好,其反应速率常数k1值为0.471 min-1,相比于空白样品k0值0.0144 min-1提高了32倍。这是因为在沉积时间较短时,随着沉积时间的增加,TiO2纳米片表面的Bi颗粒尺寸增大,有利于搜集更多的表面载流子,促进更多的内部载流子向表面扩散,而当沉积时间过长时,Bi/TiO2表面Bi颗粒尺寸过大,则会促进载流子复合,导致催化活性开始下降。
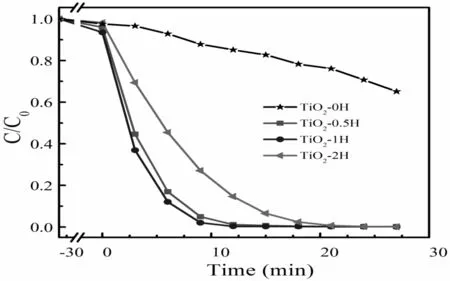
图2 催化剂活性降解图
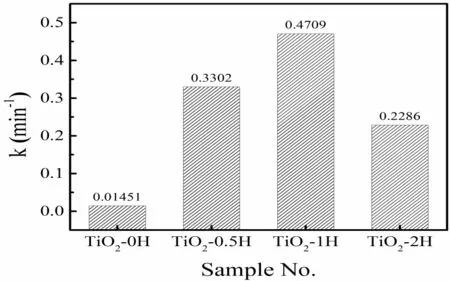
图3 催化剂速率常数计算结果
2.3 TEM测试
图4为样品的TEM图,其中a、b分别是TiO2、TiO2-1H的低倍TEM图,c、d分别是图4b中椭圆区域的电子衍射斑和HR-TEM图。从图4a中可以看出水热法制备的TiO2纳米片形貌规整,尺寸分布较窄,边长均在50 nm - 80 nm之间。从图4b中可以看出,TiO2-1H表面附着许多大小均一的金属颗粒,由图4c电子衍射斑可以确定该金属颗粒为Bi,从图4d中可以得出Bi金属颗粒大小为6 nm,且此时Bi金属颗粒已经将TiO2表面基本覆盖。若继续延长沉积时间,Bi颗粒将会继续增大,而过大的Bi金属颗粒会成为载流子的复合中心,降低载流子利用率,使得催化剂活性开始下降。

图4 催化剂微观形貌:(a)TiO2的TEM,(b) TiO2-1H的TEM,(c) TiO2-1H的HR-TEM,(d) TiO2-1H的电子衍射斑
2.4 元素Mapping
采用元素Mapping对TiO2-1H表面元素分布情况进行分析,测试结果如图5所示,其中图5a是TiO2-1H的HAADF图,图5b、c、d分别为图5a中的Bi、Ti、O元素Mapping图。从图5a中可以发现,TiO2-1H为纳米片堆叠的球状,其中单片形貌见于图4b。图5b表明催化剂表面沉积着大量的Bi金属,且分散性较好,粒径分布窄,这在XRD和TEM测试中也得到证实。表面Bi金属颗粒可以促进内部载流子向表面迁移,提高载流子利用率,使得催化剂的降解活性得到提高[6,9]。
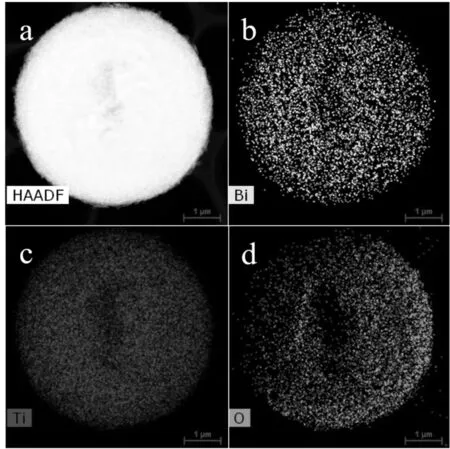
图5 TiO2-1H元素Mapping:(a)HAADF,(b)Bi,(c)Ti,(d)O
3 结论
采用光沉积制备出Bi/TiO2复合催化剂,其中TiO2纳米片颗粒大小为50 nm - 80 nm,Bi颗粒为6 nm。当沉积时间低于1 h时,随着沉积时间增加,Bi颗粒大小逐渐增加,所汇集的光生载流子数增加,促使更多TiO2内部的载流子向表面迁移,提高载流子利用率;但若光沉积时间继续增加,TiO2表面的Bi颗粒将会因尺寸过大而成为载流子复合中心,使得载流子利用率下降。综上所述,当沉积时间为1 h时,TiO2-1H载流子利用率最高,活性最好,其反应速率常数k1值为0.471 min-1,相比于空白样品k0值的0.0144 min-1提高了32倍。
