多指标综合评分-正交试验法优化五味清肺固本胶囊的提取工艺
2018-08-27
1.兰州市肺科医院,甘肃 兰州 730000;2. 兰州现代职业学院,甘肃 兰州 730000;3.兰州市第二人民医院,甘肃 兰州 730000;4.甘肃省高校中(藏)药化学与质量研究省级重点实验室,甘肃 兰州 730000
五味清肺固本胶囊是兰州市肺科医院传统制剂,处方由白及、百部、冬虫夏草等5味中药组成,具有滋肺益肾、止咳化痰、消肿生肌的功效。方中百部的主要活性成分为百部生物碱,是百部科植物所特有的吡咯或吡啶并氮杂薁母核结构的生物碱,有杀虫、镇咳平喘、抗肿瘤和抗菌等药理作用[1];白及的主要活性成分为多糖类,有收敛、止血、消肿生肌等作用[2]。五味清肺固本胶囊是在散剂的基础上经过剂型改造发展而来,原制剂服用量大而患者的依存性较差,对制剂的临床使用有一定的影响。研究采用L9(34)正交试验设计,依据中药复方药理作用的整体性,中药成分和作用机制复杂性的作用特点,主要对制剂生产中的总生物碱、总多糖的转移率进行考察,并在制备过程中采用精制除杂,可以减少制剂的服用量,同时符合中药现代化的要求。以多指标综合评分法优选提取工艺条件的实验研究,也为该制剂的质量标准提升提供了基础[3]。
1 仪器与材料
1.1 仪器 UV-2450紫外分光光度计(岛津);FA2004B电子天平(北京赛多利斯仪器公司);RE 5298A旋转蒸发仪(上海亚荣生化仪器厂)。
1.2 材料 药材均购自兰州安泰堂中药饮片有限公司,经杨怀武高级工程师鉴定均符合《中国药典》2015 年版一部相关项下规定;三批样品为我院实验中心自制,批号分别为20171210、20171211、20171212;D-无水葡萄糖对照品(批号:110833-201205,中国食品药品鉴定研究所);对叶百部碱对照品(批号:6879-01-2,上海源叶生物科技有限公司);纯化水;其它试剂均为分析纯。
2 方法与结果
2.1 干膏得率的测定 按照L9(34)正交表安排进行提取操作,100目筛趁热过滤,合并提取液,浓缩后定容到250 mL量瓶中,精密量取50 mL,置干燥恒重的蒸发皿中,在水浴上蒸干后,于105 ℃干燥3 h,取出至干燥器中冷却30 min、迅速精密称定,计算干膏得率。
2.2 总多糖含量的测定[4-8]
2.2.1 供试品溶液的配制 精密称取正交试验6号样品浸膏粉约0.15 g,置于10 mL容量瓶中,加水充分溶解并定容至刻线,摇匀,转移至离心管中,以3500 r·min-1的转速离心5 min,精密吸取上清液1 mL于离心管中,加入无水乙醇9 mL,至刻以3500 r·min-1的转速离心10 min,倾去上清液,沉淀用无水乙醇洗涤3次后,加水溶解并转移至25 mL容量瓶中,定容至刻线,摇匀即得。
2.2.2 对照品溶液的配制 精密称取D-无水葡萄糖对照品11 mg,置于50 mL容量瓶中,加水溶解并定容至刻线,摇匀即得浓度为0.22 mg·mL-1的D-无水葡萄糖对照品溶液。
2.2.3 检测波长的选择 分别精密吸取供试品溶液和D-无水葡萄糖对照品溶液适量于10 mL具塞试管中,加水至2 mL,分别加入5%苯酚溶液1 mL和浓硫酸5 mL,摇匀后于60 ℃水浴保温30 min,取出,放至室温,以水为空白,按照紫外—可见分光光度法在200~800 nm进行扫描,结果D-无水葡萄糖对照品溶液和供试品溶液的最大吸收波长均为490 nm,故选择490 nm为检测波长。
2.2.4 线性关系的考察 精密吸取0.22 mg·mL-1的D-无水葡萄糖对照品溶液5 mL于10 mL容量瓶中,加水定容至刻线,摇匀,即得浓度为0.11 mg·mL-1的D-无水葡萄糖对照品溶液。分别取0.2、0.4、0.6、0.8、1.0 mL,按“2.1.3”项下的方法处理后,在波长490 nm处测定吸光度。以质量浓度(x,μg·mL-1)横坐标、吸光度(y)为纵坐标,得回归方程为y=0.0574x+0.0101(r2=0.9980)。结果表明D-无水葡萄糖在2.75~13.75 μg·mL-1呈良好的线性关系。
2.2.5 精密度试验 分别精密吸取D-无水葡萄糖对照品溶液0.3 mL于6支具塞试管中,加水至2 mL,按“2.2.3”项下的方法处理后,在波长490 nm处测定吸光度并计算RSD。结果RSD=1.55%(n=6),表明该方法精密度良好。
2.2.6 稳定性试验 精密吸取“2.2.1” 项下供试品溶液,按“2.2.3”项下的方法处理后,分别在0、15、30、45、60、90、120 min测定其吸光度并计算RSD。结果RSD=0.17%(n=7),表明该方法处理后的溶液在120 min内稳定性良好。
2.2.7 重复性试验 精密吸取“2.2.1” 项下供试品溶液,按“2.2.3”项下的方法处理后,在波长490 nm处测定吸光度,并计算样品中总多糖含量的RSD。结果RSD=2.56%(n=6),表明该方法重复性良好。
2.2.8 加样回收试验 精密称取已知含量的样品适量,按“2.2.1”项下的方法制备后,分精密吸取0.5 mL于具塞试管中,共9份,分别精密加入0.22 mg·mL-1的D-无水葡萄糖对照品溶液0.8、1.0、1.2 mL,加水至2 mL,按“2.2.3”项下的方法处理后,在波长490 nm处测定吸光度并计算总多糖含量及加样回收率,结果见表1。结果平均加样回收率为101.16%,RSD=1.88%(n=9),表明该方法准确性良好。见表1。
2.2.9 样品中总多糖含量的测定 精密称取L9(34)正交试验样品适量,按“2.2.1”项下的方法制备并按“2.2.3”项下的方法处理后,在波长490 nm处测定吸光度,计算样品中总多糖含量。
2.3 总生物碱含量的测定[9-10]
2.3.1 供试品溶液的制备 精密称取正交试验6号样品浸膏粉约1 g于锥形瓶中,加甲醇25 mL,超声处理30 min,过滤,滤液定容于25 mL容量瓶中,即得。
2.3.2 对照品溶液的制备 精密称取对叶百部碱对照品19.5 mg于25 mL容量瓶中,加甲醇定容至刻线,摇匀,即得0.78 mg·mL-1的对叶百部碱对照品溶液。
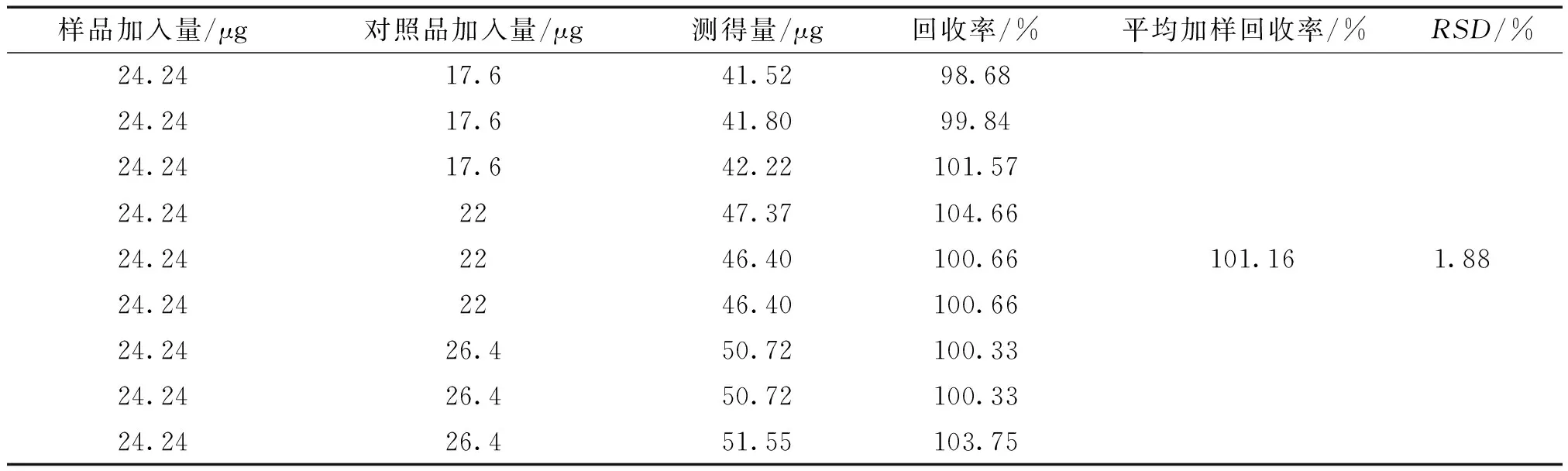
表1 加样回收率试验
2.3.3 检测波长的选择 分别精密吸取供试品溶液和对照品溶液适量于分液漏斗中,加入pH 6.6磷酸盐缓冲液5 mL和溴百里香酚蓝试液3 mL,摇匀,用氯仿萃取2次,每次10 mL,取下层液于25 mL容量瓶中,用氯仿定容至刻线,摇匀。以甲醇为空白试剂,按照紫外—可见分光光度法在200~800 nm进行扫描,结果对叶百部碱对照品溶液和供试品溶液的最大吸收波长均为412 nm,故选择412 nm为检测波长。
2.3.4 线性关系的考察 精密吸取对叶百部碱对照溶液1 mL,按“2.3.3”项下的方法处理,分别取2、4、6、8、10 mL于具塞试管中,加氯仿至10 mL,摇匀,以甲醇为空白试剂,于412 nm处测定吸光度。以质量浓度(x,μg·mL-1)横坐标、吸光度(y)为纵坐标,得回归方程为y=0.0262x-0.1001(r2=0.9987)。结果表明对叶百部碱在6.24~31.2 μg·mL-1呈良好的线性关系。
2.3.5 精密度试验 精密吸取对叶百部碱对照溶液1 mL于分液漏斗中,共6份,按“2.3.4”项下的方法处理后,在波长412 nm处测定吸光度并计算RSD。结果RSD=1.20%(n=6),表明该方法精密度良好。
2.3.6 稳定性试验 精密吸取供试品溶液1 mL于分液漏斗中,按“2.3.4”项下的方法处理后,分别在0、10、20、30、40、60、90 min测定其吸光度并计算RSD。结果RSD=0.24%(n=7),表明该方法处理后的溶液在90 min内稳定性良好。
2.3.7 重复性试验 精密吸取“2.3.1”项下的方法制备的供试品1 mL,共6份,按“2.3.4”项下的方法处理后,测定吸光度并计算样品中总生物碱含量的RSD。结果RSD=1.10%(n=6),表明该方法重复性良好。
2.3.8 加样回收率试验 精密吸取“2.3.1”项下的方法制备的供试品0.5 mL,共9份。分别精密加入0.78 mg·mL-1的对叶百部碱对照品溶液0.28、0.35、0.42 mL,按“2.2.4”项下的方法处理后,测定吸光度并计算总生物碱含量及加样回收率,结果见表2。结果平均加样回收率为101.60%,RSD=2.13%(n=9),表明该方法准确性良好。见表2。
2.3.9 样品中总生物碱含量的测定 精密称取L9(34)正交试验样品适量,按“2.3.1”项下的方法制备并按“2.3.3”项下的方法处理后,在波长412 nm处测定吸光度,计算样品中总生物碱含量。
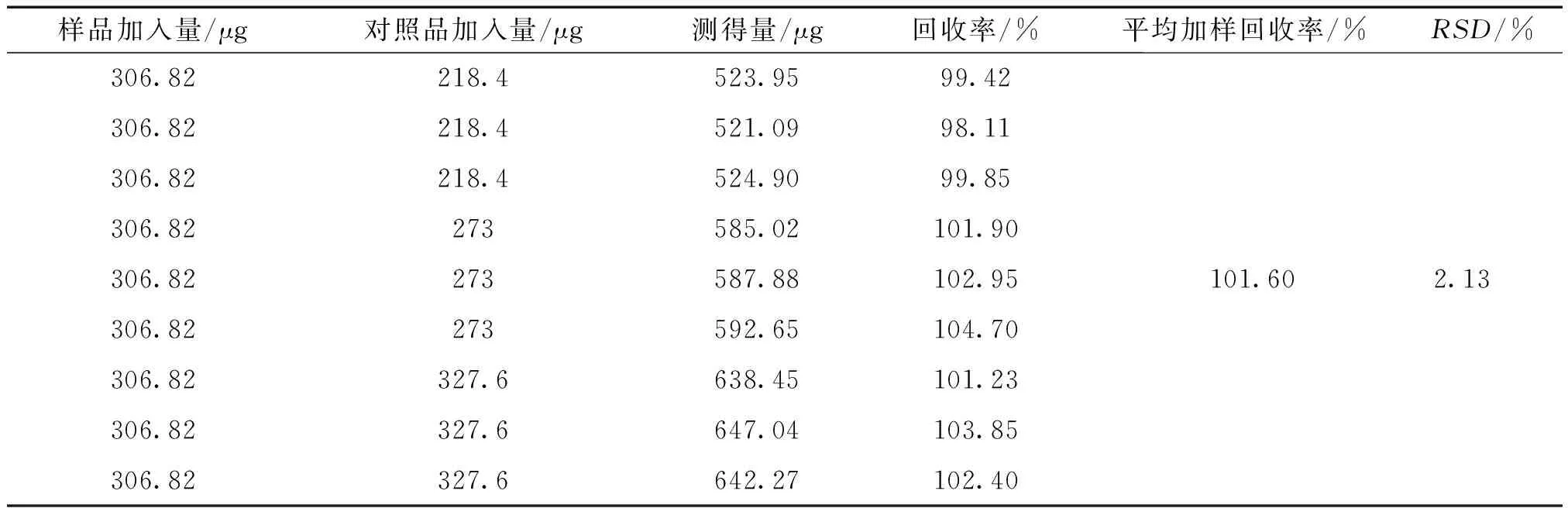
表2 加样回收率试验
2.4 正交试验优选提取工艺及结果 依据前期实验,确定本组方药效成分为水溶性成分,因此设计提取溶剂为水。按处方比例称取百部、白及等药材共94.5 g(除冬虫夏草),共9份。选用L9(34)正交设计进行试验,根据处方中药材有效成分的作用,以浸泡时间、加水总倍数、提取总时间和提取次数作为考察因素,以总多糖提取率、总生物碱提取率和干膏得率作为考察指标,因素与水平(见表3)。利用SPSS 19.0对正交试验结果进行分析(见表4、5)。由极差分析结果可知,各因素对综合评分的影响大小顺序为C>D>B>A;由方差分析可知,因素C、D对综合评分具有极显著性影响(P<0.01),因素B对综合评分具有显著性影响(P<0.05),因素A对综合评分无显著性影响(P>0.05)。综合分析得出最优提取工艺为A1B3C3D3,即总加水32倍,浸泡0.5 h,提取3次,提取总时间为3 h。

表3 因素水平表
注:提取2次时每次的加水倍数分别为:加水总倍数/2+1、加水总倍数/2-1;提取3次时每次的加水倍数分别为:(加水总倍数-2)/3+2、(加水总倍数-2)/3、(加水总倍数-2)/3;每次的提取时间为:提取总时间/提取次数。
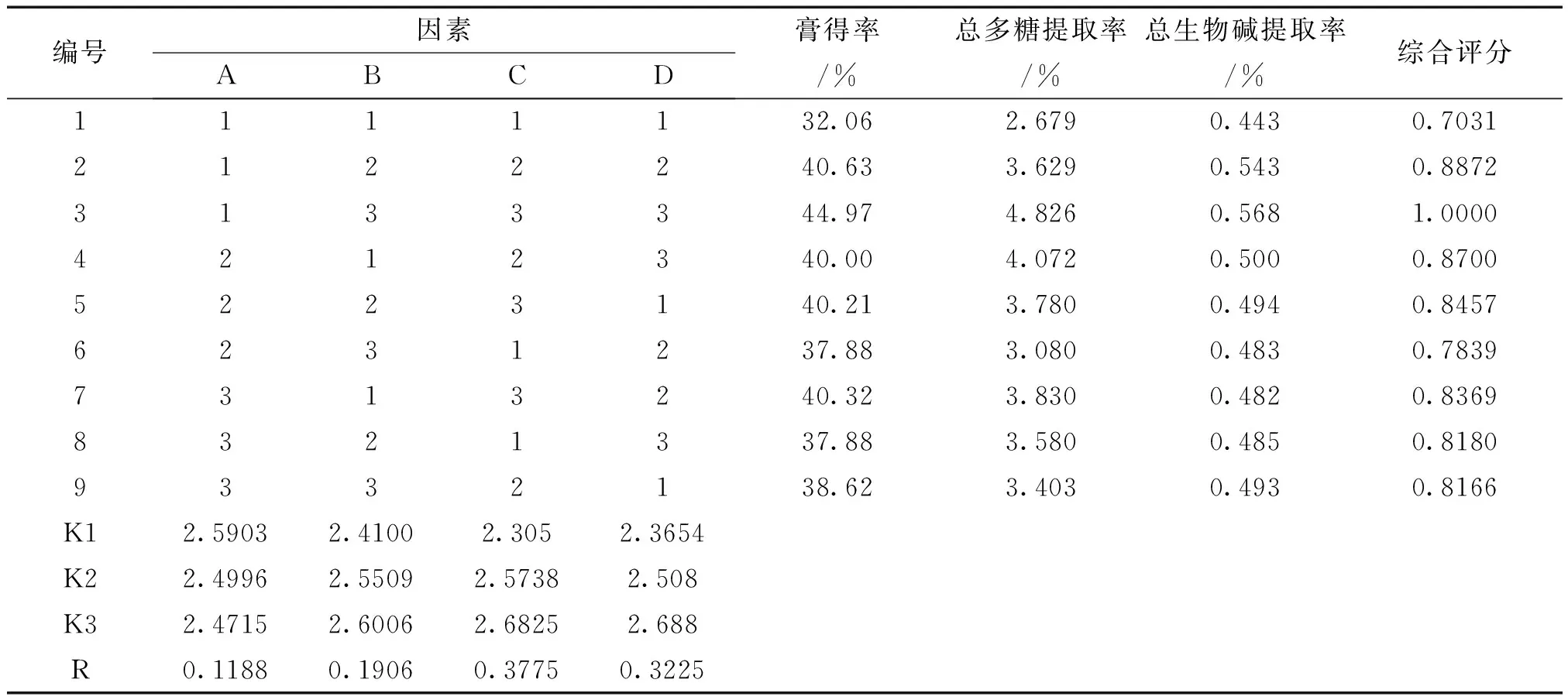
表4 正交试验结果
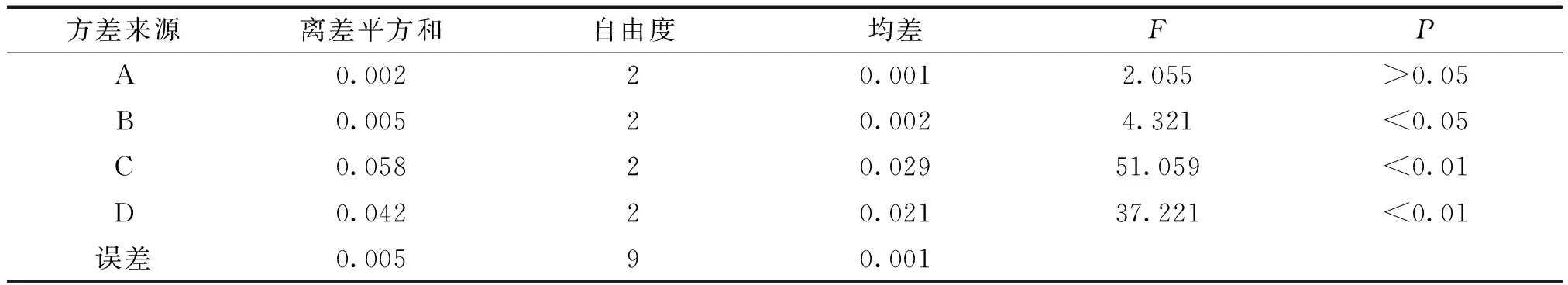
表5 综合评分方差分析结果
2.5 权重系数及综合评分公式的确定[11-12]采用层次分析法(Analytic Hierarchy Process,AHP)并综合考虑五味清肺固本胶囊的现代药理研究,得到总生物碱、总多糖和出膏率的AHP法权重系数分别为0.5815、0.3090、0.1095,经一致性检验,其一致性比率(CR)=CI/RI =0.0036/0.58=0.0062 < 0.1,表明指标优先比较判断阵距具有一致性,权重系数合理、有效。最终得到的综合评分=总生物碱提取率/最大总生物碱提取率×0.5815+总多糖提取率/最大总多糖提取率×0.3090+出膏率/最大出膏率×0.1095。
2.6 提取工艺验证试验 按比例称取同一批百部、白及等药材适量,平行3份,按照最优工艺进行提取。结果平均出膏率为43.91%,RSD为1.50%;平均总多糖提取率为4.96%,RSD为2.10%;平均总生物碱提取率为0.50%,RSD为0.90%;平均综合评分0.9338,RSD为1.08%,表明该工艺稳定可行。见表6。
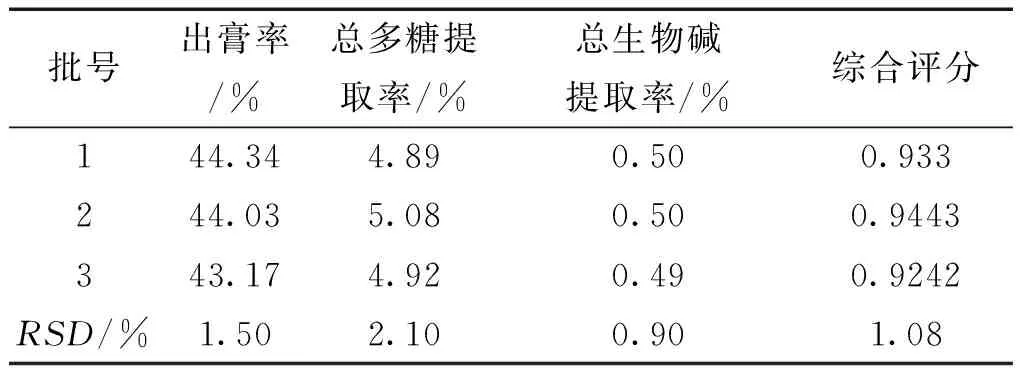
表6 验证试验结果
3 讨论
3.1 有效部位的确定和多指标综合评分 五味清肺固本胶囊由白及、百部、冬虫夏草等5味中药组成,药效成分主要为生物碱、多糖等成分。本提取工艺的优化设计是建立在中药药效学和复方制剂药效的整体性、多靶点、多途径特点的基础上,贯穿质量源于设计的思路,充分考虑五味清肺固本胶囊中百部、白及等药材的药效部位,如抑菌、止咳平喘、止血等成分的理化性质与提取溶剂、提取方法的关系,以总生物碱、总多糖和干膏得率为评价目标,结合层次分析法确定各指标权重,采用多指标综合评分法分析优选提取工艺。
3.2 制备工艺和检测方法的优化 本实验在五味清肺固本胶囊的制备中采用传统的溶剂提取法,在提取液多糖的制备过程中,利用多糖溶于水而不溶于无水乙醇的性质,采用两步离心法结合醇沉法,第一步对提取液的离心可以较大程度的除去其中的蛋白质、糊化淀粉、油脂等杂质;第二步是用90%的醇沉后离心,以此降低多糖纯化成本,也可以减少多糖类成分的损失;在总多糖含量测定方法的选择上,选用简便、灵敏度高的苯酚-硫酸法,进一步避免了复方提取液中蛋白质等成分对含量测定的影响。选用酸性染料比色法测定百部总生物碱的含量,该方法是离子对萃取比色法中比较经典方法,以溴百里香酚蓝为酸性染料亦最大程度地减少对检测结果干扰。
3.3 工艺优选对临床应用和制剂质量的影响 五味清肺固本胶囊是在散剂的基础上通过剂型改造发展而来,采用L9(34)正交设计试验优选的提取工艺最大限度的保证了药材中药效部位提取程度,也保证了制剂的临床疗效。同时,经过精制除杂过程,除去了提取液中的一些蛋白类、淀粉等物质,较原制剂减少了服用量,提高患者的用药依存性。通过对提取工艺的研究,在制剂的生产过程中,可以用总多糖和总生物碱作为中间品控制的定量指标,进一步提升制剂的质量。
