磷尾矿循环酸浸试验的研究
2018-08-17潘志权张华丽
杨 成,李 防,潘志权,张华丽*
1.武汉工程大学化学与环境工程学院,湖北 武汉 430205;2.湖北兴发化工集团股份有限公司,湖北 宜昌 443000
我国磷矿资源储量丰富,但约80%以上为中低品位磷矿[1],为了满足优质磷酸和浓度高的磷肥生产需求,必须经过选矿富集后才能加以利用[2]。浮选工艺原理表明,磷矿经浮选后会产生大量的尾矿,其中质量分数w(MgO)≥15%,w(P2O5)≤10%[3]。目前这些尾矿的随意堆放,不仅会浪费资源,并且会造成环境污染[4],因此,对磷矿资源的二次开发综合利用极其重要[5]。综合开发利用磷尾矿中的有用成分不仅能改善生态环境和可持续利用资源,而且能产生巨大的经济和社会效益[6]。
黄芳等[7]对磷矿浮选尾矿在硫酸中的酸解行为进行了研究。黄芳等[8]对磷尾矿的酸解动力学过程介微观现象进行了研究,解释了硫酸酸解过程的反应机理。赵琦[9]以高镁磷尾矿为研究对象,对其进行新药剂再浮选,得到了品位为19.06%、回收率为91.19%的镁精矿。吴梦[10]以磷尾矿为原料,采用氨水沉淀法制备纳米氢氧化镁,团聚现象明显,可作为添加型高效抑烟阻燃剂应用于塑料、橡胶等领域。马会娟等[11]以磷尾矿为原料,采用工业盐酸分解高镁磷尾矿并制备硫酸镁产品,制得的七水硫酸镁产品符合国家行业一等品标准。马会娟等[12]以磷尾矿为原料,采用循环酸浸-复盐结晶法制备磷酸二铵,制得的磷酸二铵产品符合国家标准优等品的要求。高金锋等[13]以改性后的铁矿尾矿为原料,采用干压成型方法制备出蒸压砖;罗力等[14]以铁尾矿、石灰石为原料制备出硅酸盐水泥熟料;Onuaguluchi等[15]利用铜尾矿制备混凝土;Shettima等[16]对采用铁尾矿作为细料制备混凝土的可行性进行了研究;张龙等[17]针对沙柳木粉对添加造孔剂法制备粉煤灰基多孔陶瓷的影响进行了研究等。
试验选取湖北某地高镁磷尾矿作为原料,对此尾矿进行物相及化学全元素分析后发现,该尾矿的主要物相为白云石[CaMg(CO3)2]和氟磷灰石[Ca5(PO4)3F],其中P2O5质量分数为8.0%,MgO为14.6%,而CaO为33.2%,可看作高镁磷尾矿。
试验采用工业盐酸对高镁磷尾矿进行酸解预处理,得到酸解滤液和渣相,对得到的渣相进行水洗,水洗液与酸解滤液混合后产生固体1,再对其固液分离后的液体进行酸化处理,酸化滤液进行浓缩产生固体2,浓缩滤液通过循环酸解使滤液中的磷和镁得到富集[18]。
1 实验部分
1.1 实验原料
该磷尾矿来自于湖北某选矿企业,化学成分分析(质量分数,%)CaO,49.506;MgO,19.498;P2O5,15.992;SiO2,7.654;Al2O3,1.797;K2O,0.420;TiO2,0.186;MnO,0.110;Fe2O3,0.957;Na2O,0.116;SrO4,0.039。
用X射线衍射(X-ray diffraction,XRD)对尾矿进行物相分析,XRD检测结果见图1。
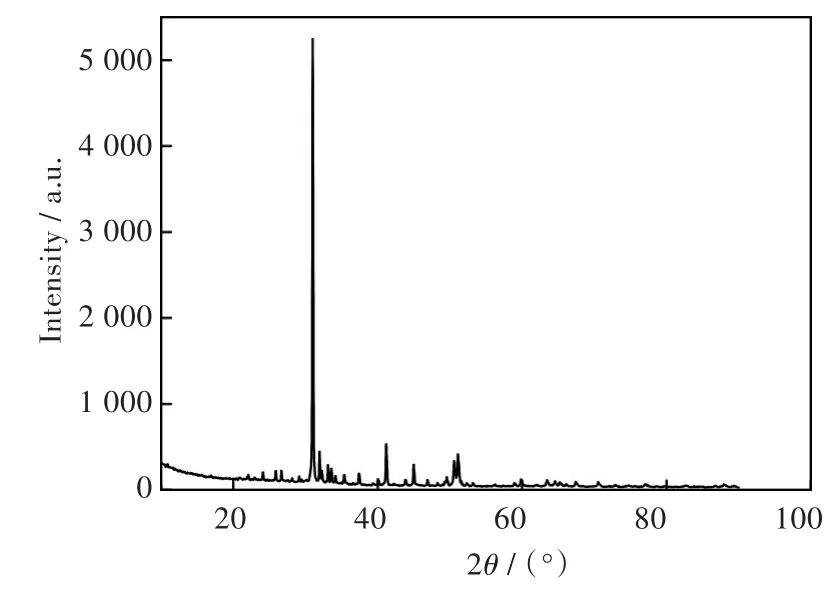
图1 尾矿XRD图谱Fig.1 XRD pattern of phosphate tailing
经图1分析可知,该磷矿尾矿主要以白云石[CaMg(CO3)2]和氟磷灰石[Ca5(PO4)3F]等矿相组成,其质量分数分别为93.53%、6.47%。
1.2 实验方法
取适量工业盐酸倒入3000 mL圆底烧瓶中,系统升温至某一温度,用加料漏斗连续性加入一定量的磷尾矿。待加完毕反应一段时间后停止搅拌,保温抽滤,滤饼为未参加反应的硅渣,用适量的水连续分别洗涤3次,烘干,测定硅渣的质量及其CaO,MgO和P2O5含量,计算其分解率[18]。所得滤液为酸解液,将其与矿渣一次水洗液均匀混合静置,次日离心过滤,离心滤液测定钙镁磷含量后转入2000 mL烧杯,用恒压滴液漏斗连续缓慢滴加与钙离子等摩尔的浓硫酸进行酸化除钙,待浓硫酸滴加完毕后继续反应一段时间使硫酸钙熟化完全,停止反应静置陈化。次日抽滤,用适量的水连续分别洗涤滤饼3次,测定石膏的质量及其CaO,MgO和P2O5质量分数,计算其夹带率[12]。所得滤液为酸化液,与石膏一次水洗液混合后进行水平衡,过滤,测定滤液中CaO,MgO和P2O5含量,以及滤液的酸度。测量其体积,转入3000 mL三口烧瓶中,补加工业盐酸使混酸的氢离子总物质的量与起初酸解磷尾矿所加工业盐酸氢离子总物质的量相等,如此循环分解,流程图如图2。
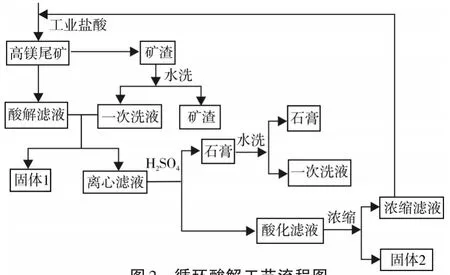
图2 循环酸解工艺流程图Fig.2 Process flowchart of multicyclical acid immersion
2 结果与讨论
2.1 循环次数对CaO、MgO、P2O5分解率的影响
循环次数对CaO、MgO和P2O5分解率的影响的实验结果如图3(a)所示。
由图3(a)可知,MgO分解率随着循环次数的增加基本保持不变,CaO、P2O5分解率均随着循环次数的增加先有所降低,循环到第9次后有所增加,这是因为在前8次循环的酸化过程中加入的酸的量都是根据钙的总摩尔量加入等摩尔的浓硫酸,当钙以硫酸钙的形式沉淀下来后,酸化滤液中仍有部分游离的硫酸根及微溶硫酸钙返回到下一次分解过程中,在酸解过程中,有大量的钙离子产生,于是硫酸根与钙离子反应产生的硫酸钙沉淀包裹在未来的及与工业盐酸反应的尾矿上,影响其分解过程的进行,随着循环次数增加,镁离子逐渐富集,浓度增加,所以每次进行下一次循环之前系统中游离的硫酸根越来越多,在酸解过程中产生的硫酸钙沉淀也越来越多,故包裹效应越来越严重,因此前8次矿渣的分解率随着循环次数的增加逐渐降低;而后进行的循环分解率又有所增加是因为在循环过程中,随着循环的次数不断增加,杂质含量不断的累积,致使在第9次循环分解时,进行水平衡浓缩出来的固体最多,而导致部分硫酸钙沉淀被带出,硫酸钙的包裹现象减弱[12]。总体来说,MgO分解率均达到了99%以上,循环分解效果比较好。
2.2 循环次数对酸解滤液及一次水洗液中CaO、MgO、P2O5浓度的影响
循环次数对酸解滤液及一次水洗液中CaO、MgO、P2O5浓度的影响的实验结果如图3(b)。
从图3(b)中可以看出,随着循环次数的增加,酸解滤液加一次水洗液混合液中MgO、P2O5浓度是逐渐升高的,因为高镁磷尾矿中的CaMg(CO3)2和(Ca5(PO4)3F)随着每次循环酸解的进行被分解,有效成分磷、镁在酸解滤液中得到了有效富集,故检测到P2O5、MgO浓度是逐渐升高的。酸解滤液中的CaO浓度是逐渐降低且趋于平衡的,这是因为在酸化过程中每次加入的浓硫酸的量都是根据钙的总摩尔量加入等摩尔的浓硫酸,除钙是彻底的,每次分解的氟磷灰石也是一定的,因此测得的CaO浓度趋于平衡。这说明循环酸浸能够有效富集有效元素磷、镁,硫酸除钙彻底。
2.3 循环次数对酸化滤液及一次水洗液中CaO、MgO和P2O5浓度的影响
循环次数对酸化滤液及一次水洗液中CaO、MgO、P2O5浓度的影响的实验结果如图3(c)所示。

图3 循环次数对(a)分解率,(b)酸解滤液浓度,(c)酸化滤液浓度,(d)石膏中CaO,MgO和P2O5含量的影响Fig.3 Effect of cycles on(a)decomposition rate,(b)concentration of acid solution,(c)concentration of acidizing fluid,(d)content of CaO,MgO and P2O5in gypsum
从图3(c)可以看出,随着循环次数的增加,酸化滤液中MgO、P2O5浓度均是逐渐增加的,并且进行第6次循环后增加的程度明显大于前面5次循环过程增加的程度,这是因为前5次循环未加石膏一次水洗液,6次~12次循环加了石膏一次水洗液;第6次循环后,随着循环次数的增加,增加的幅度便不大,是因为随着循环次数的增加,酸化滤液中P2O5、MgO浓度都随着增加,进行水平衡操作时,则会有大量的磷、镁析出,因此后面的循环浓度增加幅度不大。CaO浓度随着循环次数的增加,均保持在较低浓度的平衡状态,说明在酸化除钙过程中,除钙操作稳定彻底。
2.4 循环次数对石膏中CaO、MgO、P2O5含量的影响
循环次数对石膏中CaO、MgO、P2O5含量的影响的实验结果如图3(d)。
从图3(d)可以看出,在循环过程中,石膏中MgO、P2O5的含量随着循环次数的增加而逐渐趋于最低平衡状态,在第5次循环过程中,MgO、P2O5的含量突然降低,是因为前4次循环过程中未水洗石膏,在随后的循环过程中,均水洗石膏,致使石膏中夹带的MgO、P2O5被水洗出来,因此,石膏中的MgO、P2O5下降并趋于平衡。说明水洗石膏是必要的,可以大大降低损失。
2.5 产品的检测
所得固体经XRD物相分析,XRD检测结果见图4。
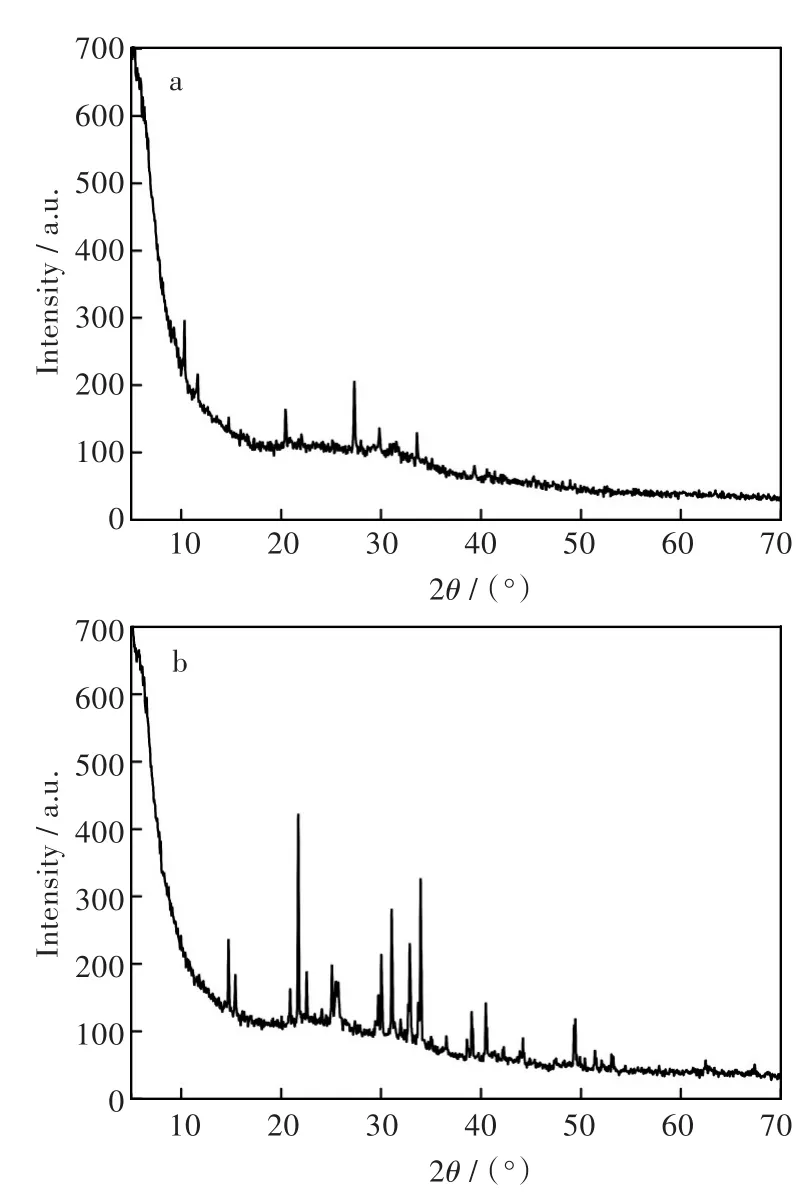
图4 (a)固体1,(b)固体2的XRD图谱Fig.4 XRD patterns of solids:(a)No.1,(b)No.2
所得固体经XRF全元素分析,XRF检测结果见表1。

表1 固体化学成分分析Tab.1 Chemical compositions of solid
经图4和表1可知,该固体1的主要物质为CaClH2PO4·H2O和 CaSO4·2H2O。固体 2的主要物质为 MgCl2和 Ca(PO3)2,还含部分 CaSO4·2H2O,MgSO4和 FeCl2等。
3 结 语
分别利用XRD、XRF对高镁磷尾矿进行分析可知:该尾矿的主要物相为白云石[CaMg(CO3)2]和氟磷灰石[Ca5(PO4)3F],其中P2O5质量分数为8.0%,MgO为14.6%,而CaO为33.2%,可看做高镁磷尾矿。
循环酸浸能够有效富集有效元素磷、镁,酸解循环过程中,酸解液加一次水洗液中MgO和P2O5分别可达到116.07 g/L和49.99 g/L,酸化液加一次水洗液中MgO和P2O5分别可达到170.37 g/L和72.06 g/L,且这些数据基本保持稳定。
固体1主要物质为CaClH2PO4·H2O以及CaSO4·2H2O,固体 2主要物质为 MgCl2和 Ca(PO3)2,此两种物质可作为生产磷镁肥原料或制备高端镁系材料的原材料。
