小剂量与标准剂量静脉阿替普酶治疗国人急性缺血性脑卒中疗效与安全性Meta分析
2018-08-13葛淑瑜于妍婷陆绪亮应茵葛卫红
葛淑瑜 于妍婷 陆绪亮 应茵 葛卫红
据国家第三次全国死因调查显示,脑卒中已经成为我国居民死亡的第一位病因[1]。其中,急性缺血性卒中(acute ischemic stroke,AIS)为临床最常见的卒中类型,其致残率、复发率和病死率均较高,严重影响患者的生存质量,同时给患者家庭和社会带来沉重的负担。阿替普酶作为一种重组组织型的纤溶酶原激活剂,为当前仅有的被批准用于AIS患者实施治疗的药物[2]。美国和欧洲的缺血性卒中治疗指南均建议以0.9mg/kg为标准剂量,但由于中国人与欧美人在种族、体质和血管危险因素等方面存在较大差异,因此中国AIS患者是否完全适合标准剂量治疗仍存在较大争议[3-6]。另外,目前仍缺乏适合中国AIS患者的阿替普酶给药剂量的大样本、多中心、前瞻性、随机对照临床试验。本研究通过Meta分析的方法,探讨小剂量与标准剂量阿替普酶静脉溶栓治疗中国AIS患者的临床疗效和安全性,旨在为中国AIS患者提供参考。
1 资料和方法
1.1 检索策略 计算机检索建库至2017年3月维普网、万方数据库、中国知网、中国生物医学文献以及美国国立医学图书馆(PubMed)等数据库。中文以“阿替普酶”“重组组织型纤溶酶原激活”“剂量”“tPA”“rt-PA”作为检索词;英文以“alteplase”“tPA”“rt-PA”“dose”作为检索词。逐一查阅检索到的文献,获取可能符合纳入标准的参考文献。文献语种仅限于中文和英文。
1.2 纳入、排除标准及结局指标 纳入标准:(1)中、英文文献(;2)队列研究;(3)符合《中国急性缺血性脑卒中诊治指南2010版》缺血性卒中静脉阿替普酶治疗入选与排除标准的中国(含港澳台)患者;(4)小剂量组为接受小剂量(<0.9mg/kg)阿替普酶治疗的急性脑卒中患者,标准为接受标准剂量(0.9mg/kg)阿替普酶治疗的急性脑卒中患者;(5)结局指标:①记录有小剂量组和标准同期神经功能缺损评分量表(NIHSS)评分,或改良Rankin量表(mRS)评分,或颅内出血(如脑出血、脑血肿、出血性卒中、卒中的出血性转变、颅内血肿、蛛网膜下腔出血)发生率(按照美国国立神经疾病与卒中研究所定义的颅内出血),或病死率;②NIHSS评分和mRS评分核心数据为连续型变量数据(以表示)。排除标准:(1)非临床试验研究;(2)试验设计不严谨的研究,如小剂量组与标准比例严重失衡等;(3)综述性、数据不完整及重复数据的文献。
1.3 资料筛选和提取 由2位研究者独立提取记录相关数据资料,若有异议,由两者达成共识后再行提取。提取数据按照以下形式列出:第一作者、文献发表时间、小剂量组和观察组等相关信息。
1.4 统计学处理 采用RevMan 5.2软件,如各组间异质性过大,则采用描述性分析。二分类变量采用比数比(OR),连续性变量采用标准化均数差(SMD),两者均以95%CI表示。对各研究结果采用I2检验进行异质性检验。当I2<50%时,表明各研究具有同质性,采用固定效应模型进行合并统计分析;当I2≥50%时,表明各研究间具有异质性,采用随机效应模型进行合并统计分析。若存在异质性风险,采用灵敏度分析等方法对产生异质性的原因进行分析,并进行亚组分析。使用漏斗图法、Begg法、Egger法或失安全系数对Meta分析进行发表偏倚分析。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果及纳入文献的基本特征 根据检索策略,共检索到中英文文献6 457篇,其中中文文献3 133篇:中国知网745篇,维普网515篇,万方数据库1 214篇,中国生物医学文献数据库659篇;英文文献3 324篇:Pubmed 3 324篇。纳入研究的基本参数资料详见图1。本研究共纳入符合条件的文献28篇,均为队列研究,包括研究对象4 914例,其中小剂量组2 659例,标准2 255例。对纳入文献进行Newcastle-Ottawa质量评价,2篇文献质量评价得分8分,5篇7分,15篇6分,6篇 5分(表1)[7-34]。
2.2 Meta分析结果
2.2.1 治疗24h后NIHSS评分 12个研究均研究了两组治疗前和24h的NIHSS评分,共纳入患者989例,其中小剂量组 471 例,观察组 518 例[8,11-18,28-30]。各项研究具有同质性(I2=0,P>0.05;图 2),采用固定效应模型进行统计分析。结果显示,小剂量组和标准剂量组在治疗24h后NIHSS评分改善方面的差异无统计学意义(总体效应SMD=-0.08,95%CI:-0.20~0.05,P>0.05;图 2)。Pr>|Z|=0.488>0.05,说明无统计学意义,即本研究不存在明显的发表偏倚。
2.2.2 治疗90d后NIHSS评分 7个研究均研究了两组治疗前和90d的NIHSS评分,共纳入患者785例,其中小剂量组 379 例,观察组 406 例[8,11,15,17,22,24,29]。各项研究具有同质性(I2=32%,P>0.05;图 3),采用固定效应模型进行统计分析。结果显示,小剂量组和标准剂量组在治疗90d后NIHSS评分改善方面的差异无统计学意义(总体效应SMD=0.04,95%CI:-0.10~0.18,P>0.05;图 3)。Pr>|Z|=0.592>0.05,说明无统计学意义,即本研究不存在明显的发表偏倚。
2.2.3 mRS评分 9项研究均研究了两组治疗前和90d后的mRS评分,共纳入患者694例,其中小剂量组 321 例,观察组 373 例[7,10,12-18]。各项研究之间存在异质性(I2=91%,P<0.01;图 4),采用随机效应模型进行统计分析。结果显示,小剂量组和标准剂量组在改良Rankin量表评分上的差异无统计学意义 (总体效应 SMD=-0.35,95%CI:-0.18~0.87,P>0.05;图 4)。

图1 文献检索策略
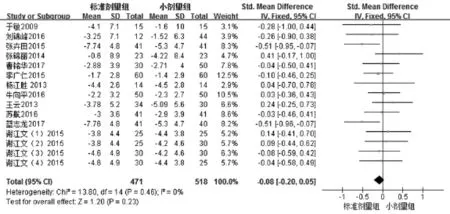
图2 两组患者治疗24h前后NIHSS评分变化值比较的Meta分析
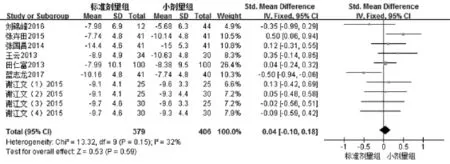
图3 两组患者治疗90d前后NIHSS评分变化值比较的Meta分析
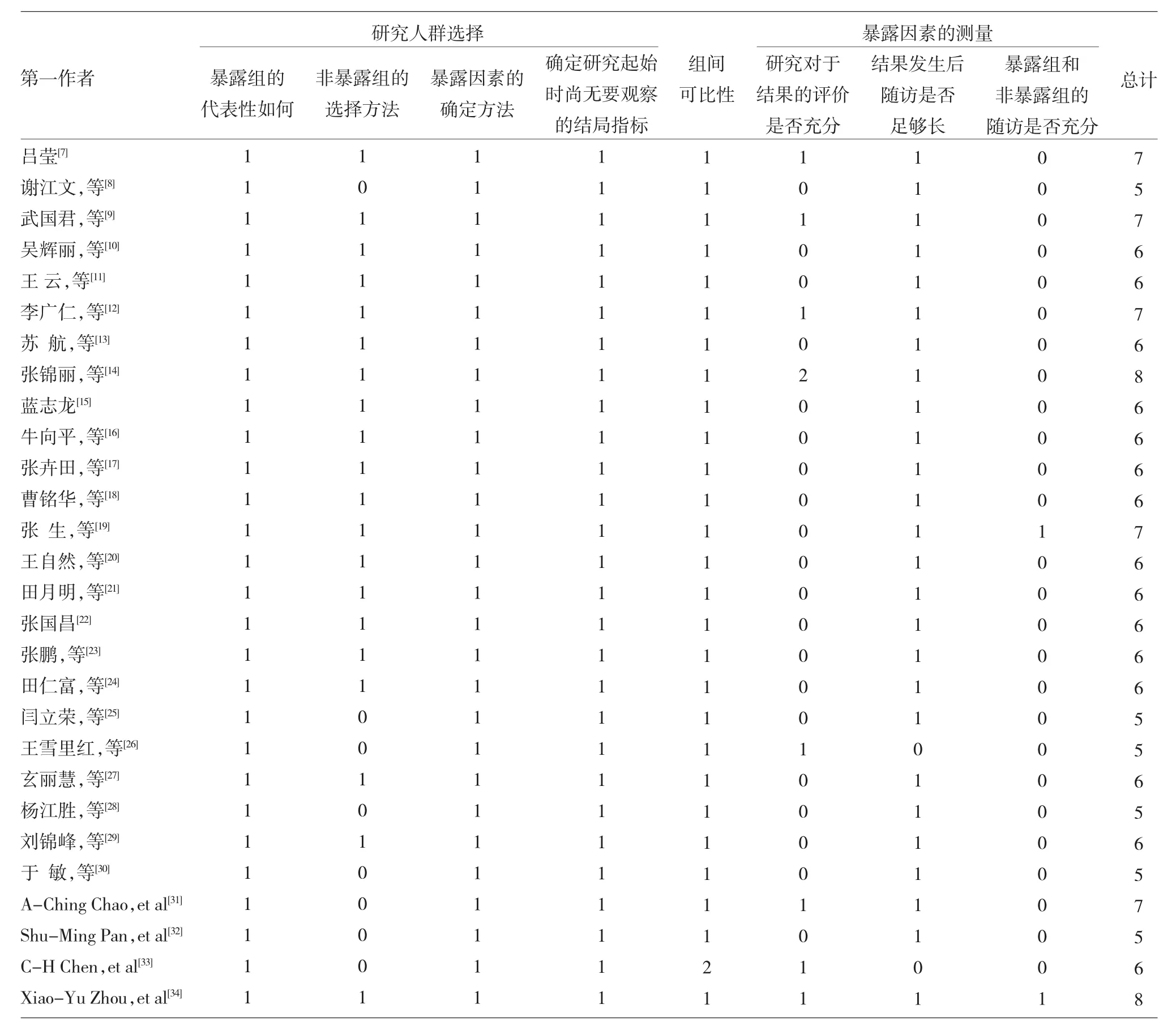
表1 纳入研究的质量评价(Newcastle-Ottawa量表评分)

图4 两组患者治疗90d后mRS评分变化值比较的Meta分析
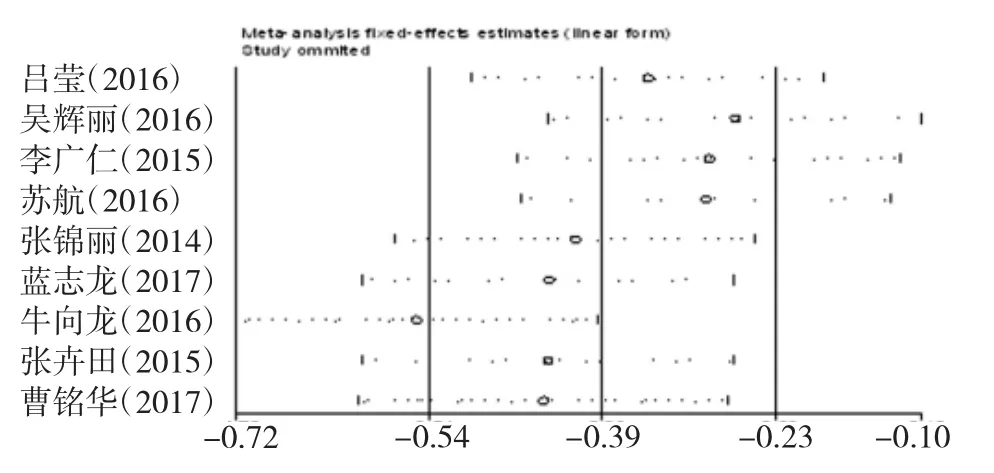
图5 灵敏度分析
由于各项研究之间存在异质性,使用Stata12.0统计软件对Meta分析进行灵敏度分析,结果显示(图5)仅有一个研究在上限和下限之外[12],即研究的SMD总体趋势不一致,该研究可能为异质性来源。根据灵敏度分析结果是否在上限和下限之内分为两个亚组,分别为在上限和下限之内组和上限和下限之外组。亚组分析显示,在上限和下限之内组 (I2=81%,P<0.01)较整体(I2=91%,P<0.01)异质性风险明显降低(图6),标准剂量组在改良Rankin量表评分方面优于小剂量组(总体效应SMD=-0.57,95%CI:-0.95~-0.18,<0.01;图 6)。使用 Stata12.0统计软件进行Begg法检验,结果显示,Pr>|Z|=0.754>0.05,说明无统计学意义,即本研究不存在明显的发表偏倚。经计算本研究的失安全系数(Nfs)0.05 为 144.28(P=0.05)[31],即需加入约 144 个阴性结果的研究才能逆转标准剂量组在改良Rankin量表评分优于小剂量组的结论。
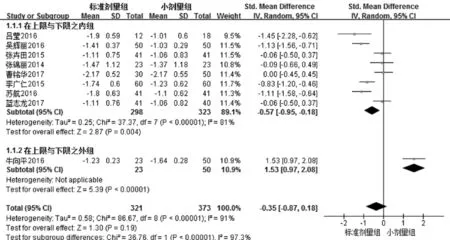
图6 两组患者治疗90d后mRS评分变化值比较的亚组分析结果
2.2.4 颅内出血发生率 19个研究均研究了两组治疗后颅内出血发生率,共纳入患者6 032例,其中小剂量组 2 398 例,观察组 3 634 例[8-9,11-12,15,18,20-34]。各项研究具有同质性(I2=0,P>0.05;图 7),采用固定效应模型进行统计分析。结果显示,标准剂量组治疗后颅内出血发生率大于小剂量组(总体效应SMD=1.54,95%CI:1.19~1.99,P<0.01;图 7)。使用Stata 12.0统计软件进行Begg法检验,结果显示,Pr>|Z|=0.359>0.05,说明无统计学意义,即本研究不存在明显的发表偏倚。
2.2.5 治疗后90d内病死率 19个研究均研究了两组治疗后90d内病死率,共纳入患者4 491例,其中小剂量组 2 099 例,观察组 2 392 例[8,10-12,15-21,26,28-34]。各项研究具有同质性(I2=0,P>0.05;图 8),采用固定效应模型进行统计分析。结果显示,小剂量组治疗后90d内病死率与标准剂量组无统计学差异(总体效应 SMD=0.93,95%CI:0.74~1.16,P>0.05;图 8)。使用Stata 12.0统计软件进行Begg法检验,结果显示,Pr>|Z|=0.133>0.05,说明无统计学意义,即本研究不存在明显的发表偏倚。
3 讨论
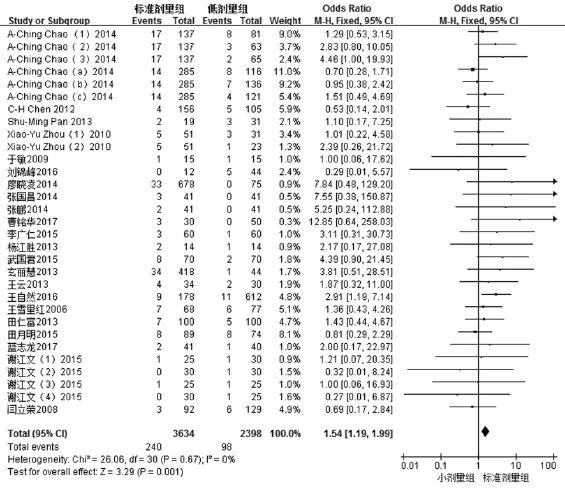
图7 两组患者治疗后颅内出血发生率的Meta分析
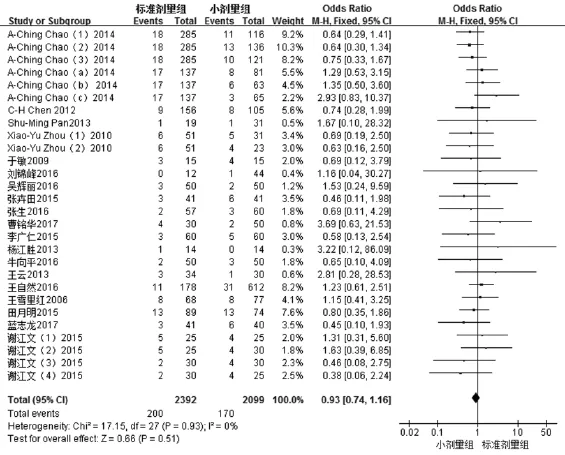
图8 两组患者治疗后90d内病死率的Meta分析
阿替普酶是一种具有纤维蛋白特异性的溶栓制剂,对纤维蛋白有高亲和力,即仅与血栓中的纤维蛋白结合,对血液中的纤维蛋白原无明显的纤溶作用,对全身纤溶系统影响不大,不产生全身纤溶状态,故有选择性局部溶栓作用[35],为目前唯一被批准用于治疗AIS的药物,但其价格昂贵,限制了临床使用的普及。关于阿替普酶量效关系一直存在较大的争议,美国及欧洲国家对急性脑梗死治疗指南建议0.9mg/kg为静脉溶栓常规标准剂量,而日本对急性脑梗死治疗指南建议0.6mg/kg为最佳剂量[3,36]。但针对中国AIS人群何种剂量具有更好的疗效及安全性,一直缺少相关大规模循证医学研究。本研究比较了小剂量与标准剂量静脉阿替普酶治疗中国AIS患者的临床治疗效果和安全性。结果显示,临床疗效比较上,小剂量组与标准剂量组治疗后24h和90d NIHSS评分较治疗前明显降低,但两组差异均无统计学意义,90d改良Rankin量表评分两组间差异有统计学意义,标准剂量组溶栓后90d神经功能恢复优于小剂量组;安全性比较上,小剂量组与标准剂量治疗后90d病死率差异无统计学意义,而颅内出血发生率两组间差异有统计学意义,即标准剂量组溶栓后颅内出血发生率高于小剂量组。
发表性偏倚是影响Meta分析质量的重要因素之一,评价Meta分析发表偏倚的方法有很多,包括漏斗图法、Begg法、Egger法和失安全系数法等。目前最常用的偏倚检测方法有倒漏斗图法和失安全系数法,但两者不能对发表偏倚进行量化检测。而Begg法和Egger法则可对偏倚进行量化检测[37],可更加客观的判断是否存在发表性偏倚,故使用Begg法进行量化检测。异质性评价是Meta分析中必须要进行的一项工作,对于保证Meta分析的质量具有重要意义[38]。本研究采用灵敏度分析和亚组分析对Meta分析进行异质性评价,异质性分析结果显示,部分研究组Meta分析存在较大的异质性,根据灵敏度分析结果进行亚组分析后,各研究之间异质性明显降低,提示改良Rankin量表评分结果可能与入组患者年龄或纳入文献质量有关,更准确及全面的结论有待于进一步研究。
综上所述,标准剂量较小剂量阿替普酶静脉溶栓治疗AIS患者临床疗效更佳,但颅内出血风险同时增加,临床使用应权衡其获益与风险。