高考新宠——表格型实验题
2018-08-06宁夏王开山
宁夏 王开山
实验是化学的重要组成部分,一直以来是高考考查的重点内容。纵观高考试卷,近几年表格型实验选择题因其结构简单、信息明确、知识覆盖面广以及兼顾基础和能力的综合考查等特点而成为高考新宠。
文章结合近几年高考试题,总结了表格型实验题的主要类型、考点及解答要点,现做如下分析。
类型一、基本操作判断型
化学实验基本操作是进行化学实验时必须掌握的基本技能。化学实验基本技能也是进行科学探究的基础。
考点:常用化学仪器的洗涤、安装、气密性检验及使用;化学试剂的取用、称量、加热;混合物的过滤、蒸发、结晶、萃取、分液、蒸馏、渗析;气体的除杂、干燥、收集;一定浓度溶液的配制等。
例1.下列实验操作正确且能达到相应实验目的的是( )
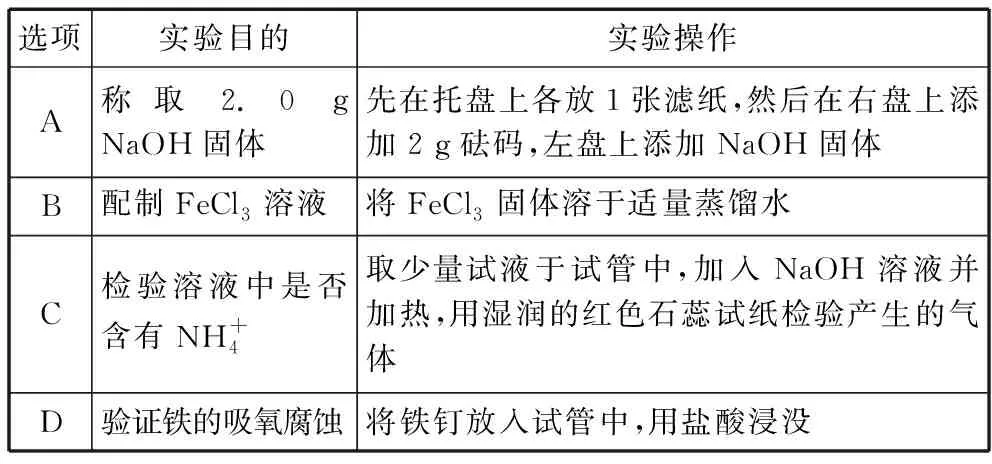
选项实验目的实验操作A称取2.0 g NaOH固体先在托盘上各放1张滤纸,然后在右盘上添加2 g砝码,左盘上添加NaOH固体B配制FeCl3溶液将FeCl3固体溶于适量蒸馏水C检验溶液中是否含有NH+4取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体D验证铁的吸氧腐蚀将铁钉放入试管中,用盐酸浸没
解析:A选项考点为药品的称量。物质称量过程中要考虑固体物质的物理、化学性质,如是否易潮解、易腐蚀、易变质等。因为NaOH具有腐蚀性,不能直接放在托盘上称量,要放在烧杯中称量,A错误。B选项考点为溶液的配制。溶液的配制要注意溶质的性质,如是否水解、是否易发生反应等。FeCl3溶液中铁离子容易发生水解反应,配制前应先将FeCl3固体溶解在一定浓度的盐酸中,然后加水稀释到所需要的浓度,B错误。C选项考点为离子检验操作。离子检验要注意检验试剂的选择、添加顺序、其他离子的干扰等。D选项考点为物质性质实验具体操作。物质性质实验要考虑具体的实验条件等。验证铁的吸氧腐蚀需要在中性或者碱性条件下,不能用盐酸浸没(发生析氢腐蚀),D错误。
答案:C
解答策略:基本操作判断型表格实验题重在考查具体物质的性质。要以具体物质性质为基础熟练掌握每一个化学实验基本操作原理、步骤和规范要求。尽可能走进实验室,带领学生亲自做实验,体会操作要领,达到融会贯通。
类型二、因果关系判断型
元素化合物知识和基本实验原理结合的因果关系判断型试题不仅要求学生熟练掌握元素化合物知识和基本实验原理,还要求学生具备一定的分析、判断能力和逻辑思维能力,较“基本操作判断型”试题有了一定的综合性。
考点:元素化合物知识(物理性质、化学性质、特性等);基本实验原理(离子检验、混合物分离提纯、溶液配制等)。
例2.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
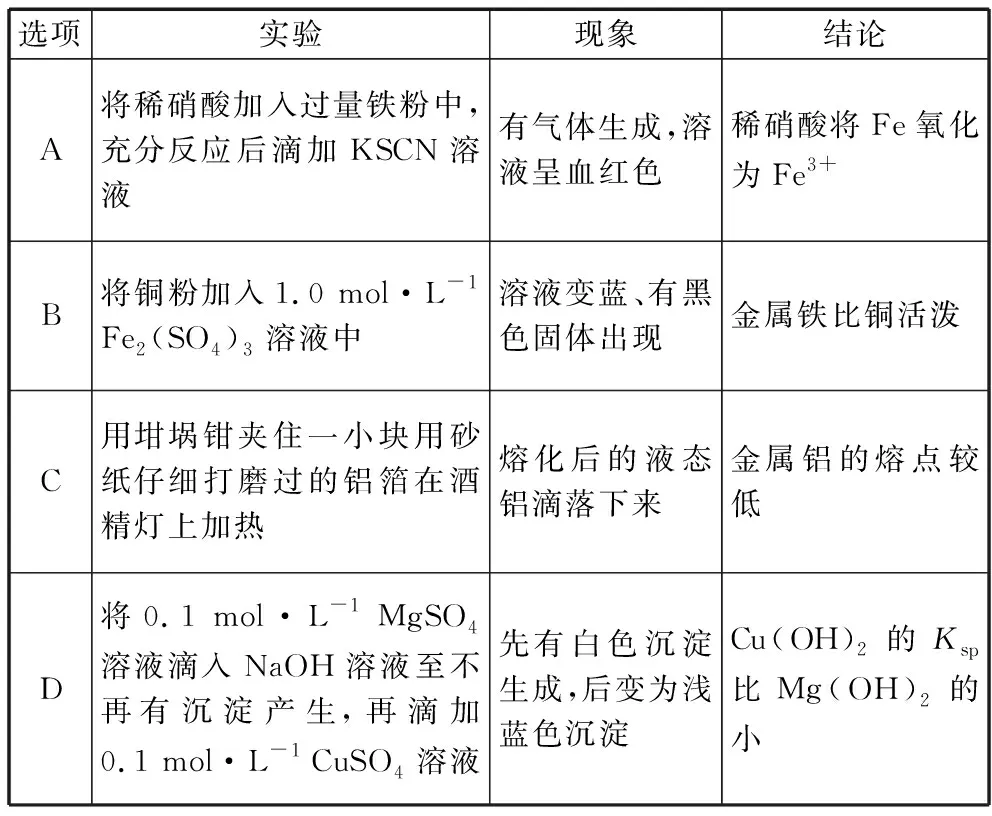
选项实验现象结论A将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液有气体生成,溶液呈血红色稀硝酸将Fe氧化为Fe3+B将铜粉加入1.0 mol·L-1 Fe2(SO4)3溶液中溶液变蓝、有黑色固体出现金属铁比铜活泼C用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热熔化后的液态铝滴落下来金属铝的熔点较低D将0.1 mol·L-1 MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1 mol·L-1 CuSO4溶液先有白色沉淀生成,后变为浅蓝色沉淀Cu(OH)2的Ksp比Mg(OH)2的小
解析:A选项考点为硝酸和Fe3+的性质。主要考查硝酸和Fe3+的氧化性。稀硝酸与过量的Fe充分反应生成硝酸亚铁、NO和水,无三价铁离子生成,所以加入KSCN溶液后,不变红色,A错误。B选项考点为Fe3+的氧化性,Fe3+会与常见金属反应生成Fe2+。Cu与硫酸铁发生氧化还原反应,生成硫酸铜和硫酸亚铁,无黑色固体出现,B错误。C选项考点为金属铝和氧化铝的物理性质(熔点)。铝在空气中加热生成的氧化铝的熔点较高,所以内部熔化的铝不会滴落,C错误。D选项考点为沉淀的转化,Cu(OH)2的Ksp比Mg(OH)2小,随着CuSO4溶液加入,Mg(OH)2沉淀逐渐溶解生成Cu(OH)2沉淀。 D正确。
答案:D
解答策略:1.熟练掌握物质的重要性质(物理性质、化学性质、特性等)和常见化学实验基本操作的原理(混合物的分离、提纯,物质检验,溶液配制等);2.判断物质性质和具体操作之间的逻辑关系时,要综合考虑具体操作的原理是否与物质的性质有因果关系。
类型三、实验方案评价型
评价意味着要进行全方位综合考虑。实验方案评价在化学中属于层次能力要求,能很好地考查学生的推理判断能力、综合分析能力以及知识的迁移能力等。体现着新课程、新教材的特点,引领着高考改革。
考点:物质鉴别方案评价,溶液配制方案评价,离子检验方案评价,物质性质验证方案评价。
例3.以下实验设计能达到实验目的的是( )
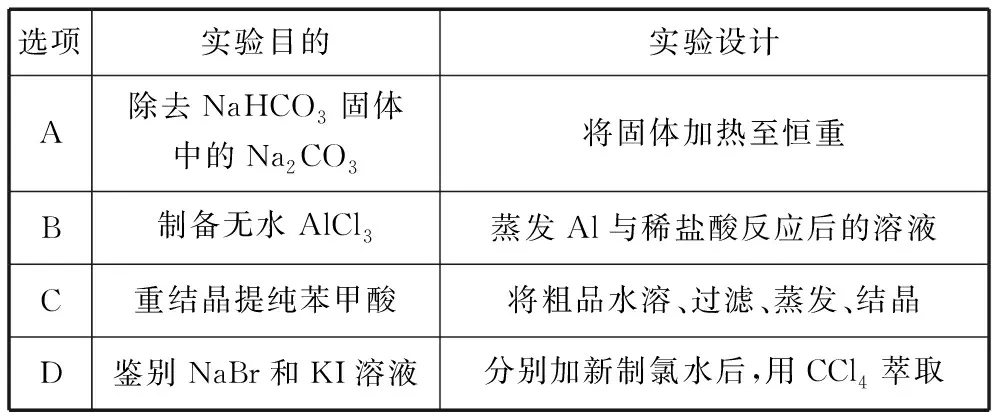
选项实验目的实验设计A除去NaHCO3固体中的Na2CO3将固体加热至恒重B制备无水AlCl3蒸发Al与稀盐酸反应后的溶液C重结晶提纯苯甲酸将粗品水溶、过滤、蒸发、结晶D鉴别NaBr和KI溶液分别加新制氯水后,用CCl4萃取
解析:A选项考点为物质除杂,物质除杂的要点主要是利用混合物各组分的特殊性质进行除杂。加热碳酸氢钠分解生成了碳酸钠,不能达到实验目的,A错误。B选项考点为物质的制备,直接蒸发Al与稀盐酸反应后的AlCl3溶液,会促进Al3+发生水解生成Al(OH)3,不能达到实验目的,B错误。C选项考点为物质提纯,物质提纯要注意提纯物质的性质,如溶解性等。重结晶法提纯苯甲酸的方法是将粗品溶解,趁热过滤,滤液冷却结晶即可,C错误。D选项考点为物质鉴别,物质鉴别主要是利用不同物质的不同性质进行鉴别。Br2溶于CCl4溶液为橙红色,I2溶于CCl4为紫红色。
答案:D
解答策略:1.实验方案评价的基础是元素化合物知识、实验基本操作和基本原理。熟练掌握上述内容是解答该类型试题的前提。2.对实验方案进行评价要仔细审题,针对题意,全方位综合考虑。如方案是否科学、合理、严密;操作是否正确、安全、规范;用药是否节约、环保等。

