高考中电化学试题的常见题型与命题预测
2018-08-06黑龙江栾厚福
黑龙江 栾厚福
从近几年全国各地的高考试题来看,电化学部分是历年高考必考内容,属于高考的“常客”,在高考中分值一般占6~10分。这部分试题主要以选择题形式出现,在非选择题中偶尔结合其他情境信息、知识等综合考查。试题考查的核心素养是宏观辨识与微观探析。本文通过对近三年高考真题和模拟、联考题的研究,综合高考信息等,归纳总结电化学试题的常见题型并预测2018年高考命题趋势,希望对高考备考具有借鉴和指导意义。
一、高考常见题型
电化学试题几乎都是结合图示装置给出,如根据对新型化学电源和燃料电池考查原电池原理的理解和应用;结合具体事实或实验等考查电解原理的应用等。近几年高考中主要出现了如下五种常见题型,结合具体例题分析说明。
题型一 常规原电池原理的应用
这类题型所给出的装置中含盐桥或离子交换膜等。主要考查正负电极的判断与电极反应式的书写,电子(或电流)和溶液中离子移动方向等,偶尔涉及简单计算,如计算溶液质量变化或产生气体在标准状况下的体积、判断溶液pH变化等,试题难度较小。
例1(2015·天津卷·4题)锌铜原电池装置如图所
示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )

A.铜电极上发生氧化反应
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡

【答案】C
【解题策略】根据图示装置和电极材料等判断正负电极,需注意原电池中的“三个方向”:①电子转移方向:负极→导线→正极,②电流方向:正极→负极,③离子移动方向:阳离子→正极,阴离子→负极;写出电极反应式并根据电路中转移电子数目相等可计算电极质量变化或生成气体在标准状况下的体积等。
题型二 新型化学电源
化学电源是高考中考查频率较高的题型,且80%以上试题都是考查新型化学电源的工作原理,融入新的情境、科技前沿信息等命题,综合考查考生接受信息、处理信息和综合作答的思维能力,试题中信息较多,从中提取有用信息,根据总反应式或图示装置等判断出正负电极名称,结合电解质特点分析电极反应式。同样选项中也涉及电极反应式书写、简单计算,以及电极材料的选择等内容的考查,试题难度较大。



B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中Li2S2的量越多

【答案】D
【解题策略】解答新型化学电源试题需明确:①根据总反应方程式和元素化合价变化,可判断出电极材料或写出电极反应式;②二次电池中“放电”时相当于原电池,“充电”时相当于电解池;③燃料电池中通入燃料的电极为负极,通入空气或O2的电极为正极;④装置中阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过,注意离子交换膜的存在,对书写电极反应式的影响;⑤书写电极反应式要注意不同电解质环境(酸性、碱性、熔融碳酸盐、熔融氧化物等)的影响;⑥根据电路中转移电子数目相等,找到关系式可进行相关计算。
题型三 电解原理的应用
近几年的高考试题中,关于电解原理及其应用的试题考查相对较多,这类试题对教材内容考查很少,但侧重运用教材电解原理的理论知识解答具体的实际问题。大多数试题以结合图象的形式给出,一来很多信息都出现在图象中,二来能增加区分度。要做好这类试题,就要读懂题中关键信息,准确判断电极,结合图象信息等分阶段写出电极反应式并进行分析与计算,同时还要注意离子交换膜对离子移动的影响等。试题综合性较强,略有难度。


(1)电解一段时间后,c(OH-)降低的区域在__________(填“阴极室”或“阳极室”)。
(2)电解过程中,须将阴极产生的气体及时排出,其原因为__________。
(3)c(Na2FeO4)随初始c(NaOH)的变化如图b,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:____________________。

(2)根据题意Na2FeO4只在强碱性条件下稳定,易被H2还原。由于阴极产生H2,为防止Na2FeO4与H2反应使产率降低,即电解过程中,须将阴极产生的气体及时排出。
(3)根据题意Na2FeO4只在强碱性条件下稳定,在M点c(OH-)低,Na2FeO4稳定性差,且反应慢;在N点c(OH-)过高,铁电极上有Fe(OH)3(或Fe2O3)生成,使Na2FeO4产率降低。
【答案】(1)阳极室 (2)防止Na2FeO4与H2反应使产率降低 (3)M点c(OH-)低,Na2FeO4稳定性差,且反应慢[或N点c(OH-)过高,铁电极上有Fe(OH)3(或Fe2O3)生成,使Na2FeO4产率降低]
【解题策略】(1)注意电极名称的判断:①与电源正极相连的为电解池的阳极,反之为阴极;②电解池工作时阳离子向阴极移动,阴离子向阳极移动,据此可判断电极名称。
(2)电极反应式的书写,阳极反应式书写时要注意:①金属电极:金属失电子发生氧化反应;②惰性电极(Pt、Au、石墨)离子放电顺序:S2->I->Br->Cl->OH->含氧酸根。阴极反应式书写时要注意阳离子被还原,其放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+。
(3)掌握电解原理在氯碱工业、粗铜电解精炼、电镀、电冶金中的具体应用,如电极名称、电解质溶液、电极反应式等。
(4)根据图示装置能正确书写电极反应式,结合图象等做到具体问题具体分析,并能善于运用题中信息。
(5)电化学计算的方法:
电化学计算主要包括两极产物的定量计算、溶液pH、相对原子质量和NA测定、产物的量与电量互算等。不论哪类计算,均可概括为三种方法:
①电子守恒法:用于串联电路,阴阳两极产物、正负极产物、相同电量等类型的计算;
②总反应式法:先写出电极反应式,根据电极反应式写出总反应式,根据总反应式列比例式计算;


题型四 电化学与金属腐蚀
近两年高考中与金属腐蚀有关的试题出现的频率较高,无论是全国卷还是单独命题的省份都出现过,一般结合特定情境考查金属腐蚀的原理和金属腐蚀的电化学防护措施等。要使活泼金属不被腐蚀,该金属应人为控制使其作原电池的正极或电解池的阴极,试题相对简单。
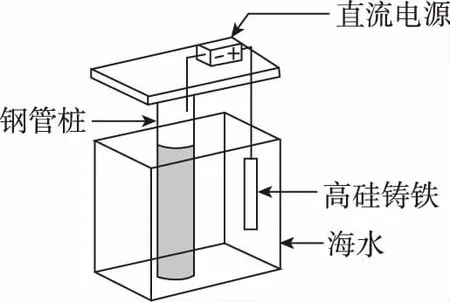
例4(2017·全国卷Ⅰ·11题)支持海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
【分析解答】钢管表面不失电子,几乎无腐蚀电流,A项正确;外电路中,电子从高硅铸铁流向电源正极,从电源负极流向钢管桩,B项正确;高硅铸铁为惰性辅助电极,不被损耗,C项错误;保护电流应根据环境(如pH、离子浓度、温度)变化进行调整,D项正确。
【答案】C
【解题策略】(1)由图示装置和介质的性质等判断金属腐蚀的类型,如酸性条件为析氢腐蚀,弱酸性或中性为吸氧腐蚀。
(2)金属的电化学防护措施:①牺牲阳极的阴极保护法;②外加电源的阴极保护法,结合具体情境掌握两种电化学防护措施的实际应用。
题型五 电化学与实验
高考中有时以探究实验为载体考查电化学知识的灵活运用。这类试题结合图示给出,根据实验现象等分析电极反应式或实验原理等。试题比较新颖,难度也不大,是北京卷常考题型,也代表新的命题方向和趋势。
例5(2016·北京卷·12题)用石墨电极完成如图所示电解实验。下列对实验现象的解释或推测不合理的是( )

实验一实验二装置现象a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化两个石墨电极附近有气泡产生;n处有气泡产生……



D.根据实验一的原理,实验二中m处能析出铜

【答案】B
【解题策略】解答这类试题需根据图示中有无外接电源,可判断是原电池还是电解池;再根据图示正确判断电极名称,结合电解质溶液和实验现象正确书写电极反应式进行分析。尤其是电解池要根据实验现象的不断变化,分阶段写出电极反应式并进行分析。
上述重点分析了近三年高考电化学试题的常见题型与考查方式,不难看出原电池原理、新型化学电源和电解原理及其应用是重点考查的内容,也是高考命题的热点。仔细研究还会发现近三年的高考真题中对电解原理及其应用、金属的腐蚀与防护的考查有所升温,较以往比对原电池原理的考查有所减少。
从近三年高考试题和最近全国各地的模拟、联考题来看,原电池原理、新型化学电源、电解原理及应用、金属的腐蚀与防护仍然是2018年高考命题的重点与热点,而且考查形式灵活新颖,如试题设置不同的电极室、离子交换膜等,会增加试题的新颖度,要避免受定式思维的影响。多数试题仍以选择题形式考查为主,同时也有很多试题结合其他知识以非选择题的形式进行综合命题,如2017年天津卷、2015年山东卷等。
高考中除了上述常见题型外,还可能出现原电池与电解池串联的试题,结合工艺流程的形式等考查电化学知识的综合运用等。现结合具体例题分析这两种可能的命题形式及解题策略。
二、高考命题预测
预测一 原电池与电解池串联
近五年各地高考中几乎没有出现原电池与电解池串联的试题,但是各地模拟、联考卷中原电池与电解池串联的试题较多,尤其以燃料电池与电解池串联的居多,这也代表一种命题趋势。所以这种题型要引起注意,选项设置仍以电极反应式书写、离子移动方向、简单化学计算等为主,试题难度较高。
例6(2018·石家庄质检·12题)NaBH4燃料电池具有理论电压高、能量密度大等优点。以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是( )

A.离子交换膜应为阳离子交换膜,Na+由左极室向右极室迁移
C.电解池中的电解质溶液可以选择CuSO4溶液
D.每消耗2.24 L O2(标准状况)时,A电极的质量减轻12.8 g

【答案】D
【解题策略】解答原电池与电解池串联的试题需注意:①根据图示装置可以正确判断原电池和电解池装置,若均为惰性电极很可能是电解池、活动性不同的电极很可能是原电池。②结合图示信息能正确判断电极名称,如图示通入O2的电极为原电池的正极,由此可确定原电池的负极、电解池的阴极和阳极。③根据图示能正确写出电极反应式,根据电路中转移电子数目相等,进行简单的化学计算。④注意离子交换膜对离子移动方向和电极反应式的影响等。
预测二 电化学与工艺流程
工艺流程题是近年来非常流行的一类试题,具有信息量大、结合生产实际等特点,备受命题教师青睐,电化学知识也可能结合化工流程形式考查,试题综合性较强。要结合具体情境和操作目的分析有关的电极反应和进行计算等。在以往高考中也出现过,这种命题形式也要引起重视。
例7(2017·江苏卷·16题)铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为__________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH__________(填“增大”“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是__________。
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为__________,阴极产生的物质A的化学式为__________。

(5)铝粉在1 000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是__________。


【解题策略】工艺流程题是将生产流程用框图形式表示出来,并根据生产流程中有关的化学知识步步设问,是无机框图的创新。解答这类试题要求考生依据流程图分析原理,紧扣信息,能找出有用信息,抓住关键,并能结合题干信息,正确分析过程,根据图示措施推理其用意。

