胰腺术后迟发性出血的介入治疗
2018-07-30祖庆泉周春高施海彬
左 鹏, 祖庆泉, 周春高, 施海彬
术后出血是胰腺外科术后少见而严重的并发症,据报道其发生率为 1%~17.8%,死亡率为10%~38%[1]。根据国际胰腺外科研究小组(International Study Group of Pancreatic Surgery,ISGPS)的标准,术后24 h作为早期出血和迟发出血的分界[2]。胰腺术后早期出血多与手术操作或技术熟练程度有关,如术中胰腺残端和吻合口止血不彻底等,需要再次行剖腹手术,且往往有较好的止血率。而迟发性出血,多由胰漏、胆漏、腹腔感染等术后并发症腐蚀组织血管或动脉骨骼化等导致假性动脉瘤形成所致[3]。
以往治疗迟发性出血主要行外科剖腹探查,研究认为迟发性出血患者腹腔粘连重、组织脆性高,手术难度及风险较大,且伴发较高的术后并发症及死亡风险[4]。介入治疗方法因其创伤小、安全性较高,达到80%以上的确切止血率,近年已逐步成为胰腺术后迟发性出血的首选治疗方法[5-7]。
既往研究多局限于少量病例探讨介入治疗胰腺术后迟发性出血的有效性及安全性,且对介入术后再出血部位鲜有报道。本研究旨在回顾性探究血管内介入治疗胰腺术后迟发性出血的安全性和有效性,分析再出血部位及再次介入治疗成功率,为临床治疗提供参考。
1 材料与方法
1.1 一般资料
回顾2010年1月至2017年6月在我院因胰腺术后迟发性出血行血管造影检查的61例患者,其中男50例,女11例,平均年龄59岁(28~82)。61例患者的病理类型为胰腺癌35例(57.4%),壶腹部癌16例,胆总管下端癌4例,十二指肠间质瘤4例,慢性胰腺炎2例。手术方式为胰十二指肠切除术49例(80.4%),胰体尾切除术7例,胰腺部分切除术5例。
根据ISGPS定义,本组病例均为迟发性出血(>24 h),出血时间为外科术后1~60 d,中位时间14.0 d。患者表现为腹腔出血47例(腹腔引流管引出血性液体),消化道出血14例(表现为呕血、血便、胃管引流出血性液体),其中11例(18.0%)合并表现为失血性休克。22例(36.1%)有前哨出血,即发生在大量出血之前腹腔引流管或消化道的少量出血。28 例(45.9%)合并胰漏,17 例(27.9%)合并腹腔脓肿。患者的一般基线资料详见表1。
1.2 方法
1.2.1 介入诊疗技术
1.2.1.1 血管造影:局部麻醉后,Seldinger 技术经股动脉穿刺插管造影,常规行腹腔动脉、肠系膜上动脉、肠系膜下动脉造影,发现可疑血管病变,则超选至靶血管进一步造影确认。如不能明确出血部位,则进一步超选择性插管造影:胃十二指肠动脉、脾动脉、肝动脉、胰腺动脉、肠系膜动脉分支等。阳性造影表现定义为对比剂外溢和或假性动脉瘤。
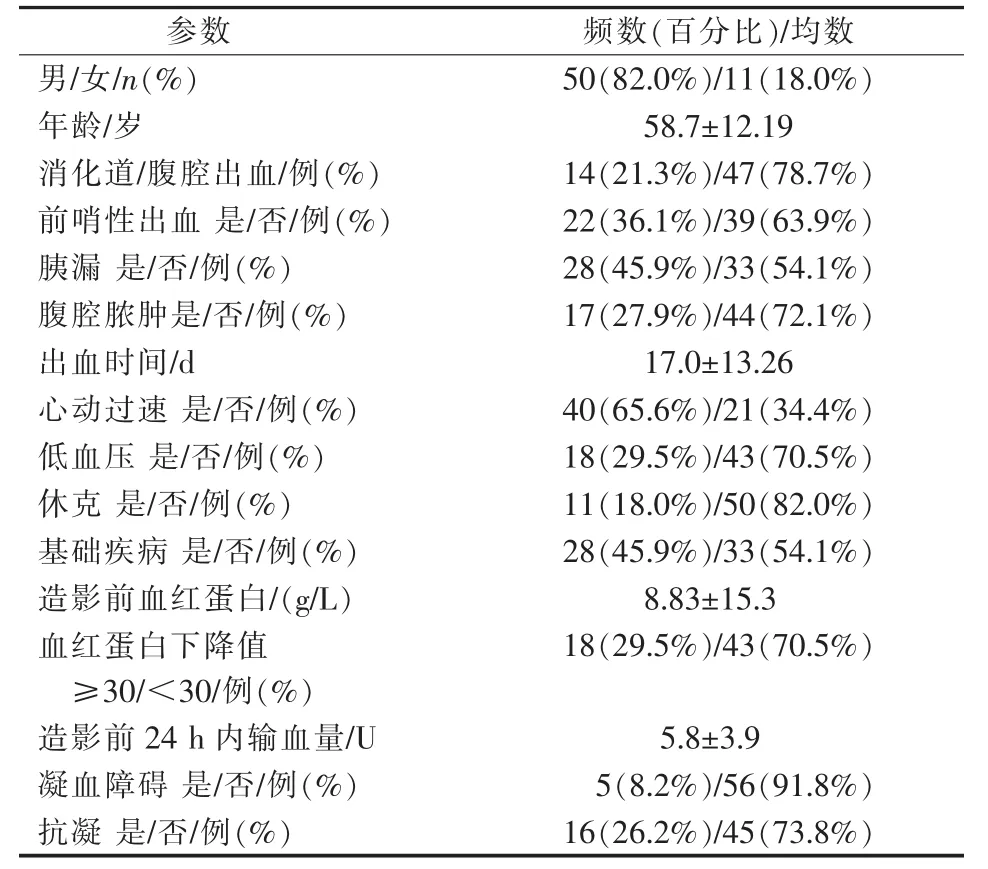
表1 患者的一般基线资料
1.2.1.2 血管栓塞:明确出血动脉后,使用 2.7 F 微导管(Progreat,Terumo,Japan)超选择插至出血动脉远端、近端充分栓塞靶血管,栓塞后常规复查造影确认靶血管是否完全闭塞。栓塞材料主要有微弹簧圈(Tornado,Cook,USA)、明胶海绵颗粒及生物胶(Glubran,Brown,Italy)。 对于栓塞靶血管后可致严重缺血并发症的患者,可行覆膜支架(Graftmaster,Abbott Vascular,Belgium)治疗。具体栓塞材料的选择及治疗方式由具有15年以上经验的术者根据患者临床及术中造影表现抉择。
1.2.2 术后观察及随访 术后常规行止血、抗感染等对症支持治疗,密切观察腹腔及消化道引流液情况,监测血常规、肝肾功能、血清及引流管淀粉酶等指标。住院期间及术后1个月内常规随访,记录患者有无再次出血、再出血时间、处理措施及死亡原因。
1.2.3 定义 技术成功定义为介入治疗后造影见靶血管完全闭塞,无再出血造影表现。临床成功定义为单纯介入治疗术后30 d内无再出血表现。再出血定义为介入术后30 d内再发出血表现,且需要即刻的液体复苏、内镜、介入或外科干预。30 d死亡定义为住院期间或首次介入治疗后30 d内发生的死亡。
1.3 统计学方法
采用SPSS 20.0软件进行统计学分析,计量资料视具体情况用均数±标准差、中位数(范围)或百分比表示,计量资料采用t检验,等级资料应用秩和检验,计数资料应用卡方检验或Fisher精确概率法。P<0.05为差异有统计学意义。
2 结果
2.1 血管造影表现
61例患者行选择性血管造影检查,其中造影显示出血血管为47例(77.0%)。责任血管为胃十二指肠动脉11例(23.4%)、肝总动脉及分支9例(19.1%)、肠系膜上动脉及分支8例(17.0%)、胃十二指肠动脉残端7例(14.9%)、胰腺动脉4例(8.5%)、脾动脉4例(8.5%)、胃短动脉3例(6.4%)、右肾上腺动脉1例(2.1%)。血管造影表现为单纯假性动脉瘤35例(74.5%),对比剂外溢11例(23.4%),假性动脉瘤伴对比剂外溢1例(2.1%)。
2.2 首次介入疗效
造影阳性患者均行介入治疗,其中30例(63.8%)单纯行弹簧圈栓塞治疗,15例(31.9%)行弹簧圈联合明胶海绵颗粒栓塞,2例(4.3%)行覆膜支架植入,支架植入部位为肠系膜上动脉主干和肝总动脉各1例。1例患者首次造影表现为胃十二指肠动脉假性动脉瘤,行弹簧圈成功栓塞出血动脉后,再造影见多支细小吻合动脉参与供血,无法再次行栓塞治疗,但患者术后出血停止。综上,介入治疗的技术成功率为97.9%(46/47)。首次介入术后13例(27.7%)发生再出血,临床成功率为72.3%(34/37)。
2.3 再出血及治疗结局
首次介入术后13例发生再出血,其中位时间为2(0~30)d。再出血患者中8例行造影检查,其中造影显示出血血管5例,行栓塞治疗后3例成功止血;3例造影阴性患者中2例行单纯内科保守治疗后未再出血,再次介入治疗的临床成功率为5/8。另5例行剖腹探查术,其中4例发现责任血管,行外科治疗后2例成功止血。再出血患者行介入和外科治疗的临床成功率差异无统计学意义(P=0.592)。综上,单纯介入治疗的临床成功率为83.0%(首次介入后止血成功34例,再出血行二次介入成功止血5例)。再出血部位为原栓塞动脉7例(53.8%)、不明部位4例(3例造影阴性、1例剖腹探查阴性)、新发出血动脉2例(其中1例合并门静脉出血)。再出血患者的详细资料见表2。

表2 再出血患者的一般资料
2.4 并发症及死亡
首次介入术后3例出现并发症,其中2例为肝脏缺血性损伤,表现为肝转氨酶异常升高(小于10倍正常值),经保守治疗后均恢复正常;另1例行脾动脉栓塞后复查CT提示部分脾脏梗死,患者无明显临床症状;所有患者未出现肠道或肝脏缺血坏死等严重并发症。介入术后30 d死亡4例(8.5%,4/47),其中3例死于术后再出血,死亡病因2例为失血性休克,另1例为弥散性血管内凝血(DIC)。
3 讨论
早期诊断和合理治疗是降低胰腺术后出血死亡率的关键所在。CT常作为胰腺术后出血的一线检查方法[8]。然而,相比较CT检查,尤其对怀疑出血是由假性动脉瘤所致或血流动力学不稳定的患者,血管造影有其独特的优势,因为造影不仅是一种诊断方法,更是一种治疗手段。本研究中对所有可疑出血动脉均进行超选择插管。对造影阴性患者,药物诱发造影没有常规实施,因为其不适用血流动力学不稳定患者,且担心增加患者再出血风险。既往研究认为前哨性出血是假性动脉瘤严重出血的前兆表现,尽管前哨性出血有较低的造影阳性率,仍推荐对所有前哨性出血患者常规行血管造影检查[9]。本研究造影阳性率为77.0%,既往研究报道的阳性率为79%~83%[9-10]。造影阴性可能因消化道出血的间歇性,且造影对静脉及组织创面渗血的敏感性较低所致。
本研究中首次行介入治疗后,72.3%患者成功止血,结果与Zhou等[11]报道的72.4%临床止血率相仿。单纯使用弹簧圈或联合明胶海绵颗粒栓塞出血动脉是治疗胰腺术后出血的主要方式,其安全性及疗效已得到文献广泛证实[12],这也是本研究主要治疗手段。近年来生物胶在治疗消化道出血上受到广泛重视,在伴有凝血功能障碍患者上,生物胶相比微弹簧圈显示出更大的优势,但在使用时要重视反流、异位栓塞、粘管等严重并发症[13]。本研究中1例胰背动脉假性动脉瘤行弹簧圈栓塞后1 d再发出血,予以组织胶栓塞后成功止血(见图1)。相比单纯弹簧圈栓塞,覆膜支架可以保留组织正常血供,降低脏器缺血坏死风险,因而近年来已成为肝总动脉等内脏动脉主干出血的首选治疗方式[14]。本研究中2例行覆膜支架植入患者,术后30 d随访均未发生再出血及支架闭塞等相关并发症,但其长期通畅性有待进一步研究。
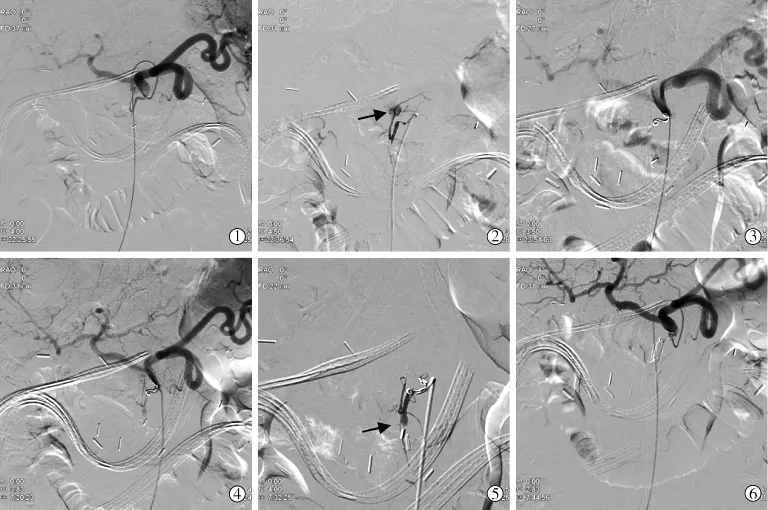
图1 男,48岁,壶腹部癌,胰十二指肠切除术后4 d腹腔引流管出血
本研究中27.7%患者首次介入治疗后发生再出血,文献报道的再出血率为20%~30%[9]。以往剖腹探查常作为介入治疗失败后的补救治疗方式[15]。本组病例中再出血行介入和外科治疗的止血率成功率相仿,因此,二次介入可能同样适用于介入术后出血复发的患者。本研究中再出血部位主要为原栓塞动脉,这可能由于动脉壁在首次出血后相对脆弱,且外科术后并发症如胰瘘、腹腔脓肿等继续破坏原栓塞血管导致再出血。然而,结论不同于Ching等[16]报道的 28例行介入治疗后,再出血中8例(80%,8/10)为新出血动脉。我们认为可以从以下两个方面解释结论的不同:①本研究中所有患者在全面评估临床资料后均进行超选择插管造影以明确出血部位,这有助于降低造影假阴性率;②本研究仅对造影阳性患者进行介入治疗,对造影可疑及阴性患者未行经验性栓塞治疗,从而降低栓塞的盲目性。本研究再出血中位时间为2 d(0~30 d),结果强调介入术后早期严密监测患者引流液变化的重要性,这可及时发现并处理再出血,降低术后死亡风险。
消化道出血行栓塞治疗后最严重的并发症为肠道等脏器缺血坏死。由于肝脏、上消化道的多重血供特性,往往认为对其出血行栓塞治疗是安全的[17-18]。本组病例中2例行肝固有动脉栓塞后出现肝缺血性损伤表现,经内科治疗后均恢复正常。研究认为肝脏缺乏异位肝动脉供血,伴发门静脉狭窄或阻塞是肝动脉栓塞术后并发肝脏缺血坏死的主要危险因素[19]。因此,肝动脉栓塞术前充分行肝脏供血动脉造影,准确评估门静脉通畅程度是必不可少的步骤。对于门静脉回流不畅的患者,可选择覆膜支架植入治疗。本研究介入治疗后30 d总体死亡率为8.9%,结论与文献报道的胰周动脉出血行栓塞治疗后总体死亡率(9%~20%)相仿[20]。研究认为胰瘘、凝血功能障碍和再出血是术后30 d死亡的主要危险因素[1]。本组病例中3例死于再出血。因此,降低术后再出血率,积极且有效地处理围手术期并发症是降低术后死亡风险的关键所在。
除了这是一项单中心回顾性研究外,本研究还存在以下不足:研究仅包含首次造影阳性并行栓塞治疗的患者,对有可疑出血动脉及造影阴性患者未行经验性栓塞治疗,这可能导致病例选择偏倚。
总之,血管内介入是治疗胰腺术后迟发性出血一种安全、有效的方法,大部分患者通过单纯介入治疗可成功止血。