纳米磁颗粒电磁探测及成像技术研究进展
2018-07-19朱健健杨文晖魏树峰
朱健健 杨文晖 魏树峰 王 铮 吕 行*
1(中国科学院电工研究所,北京 100190)2(中国科学院大学电气电子与通信工程学院,北京 100049)
引言
近年来,磁性纳米颗粒(magnetic nanoparticle, MNP)已经越来越多地应用于生物医学和生物科技的相关研究中,包括靶向给药、肿瘤磁过热疗法、MRI的对比增强、生物传感器、环境生物学的快速分离以及特异靶点(如细菌、白细胞、蛋白质)的浓度示踪等[1]。
磁纳米颗粒成像(magnetic particle imaging, MPI)作为一项新型的断层成像技术首次由学者Gleich 与 Weizenecker于2005年提出并设计研制首个静态扫描仪[2]。2009年,Weizenecker 等第一次呈现了老鼠体内心脏的3D的实时图像[3]。在过去的12年里,磁纳米颗粒成像技术经历了一维的原型设计发展到三维的商业化的成像系统。在生物医学领域,磁纳米颗粒成像技术显示了的巨大应用潜力,诸如血管造影术[4-6]、细胞跟踪[7]、炎症成像[8]、靶向纳米粒子成像[9-10]和靶向磁热疗[11]等。由于MPI高灵敏度、高分辨率的优点,它还可以很好地用于分子影像中, 比如利用超顺磁氧化纳米颗粒(superparamagnetic iron oxide nanoparticles,SPIONs)标记头部和颈部的鳞状癌细胞,来可视化癌细胞的迁移过程[10]。
1 基于磁纳米颗粒的分子成像与诊疗
磁性纳米粒子(magnetic nanoparticles, MNP) 是一种纳米级的颗粒,一般由铁、钴、镍等金属氧化物组成的磁性内核及包裹在磁性内核外的高分子聚合物/硅/羟基磷灰石壳层组成。它既具有纳米材料所特有的性质,又具有超顺磁性,且在外加磁场下实现定向移动,在交变磁场下吸收电磁波产热。基于以上优良的特性,磁纳米颗粒被广泛应用于生物医学领域,包括核磁共振成像(MRI)、肿瘤的分子医学影像、肿瘤磁热疗、药物的靶向治疗等。
分子影像是指将小的结构(如细胞、受体甚至药剂)可视化。以前已经有学者将超顺磁性氧化铁分子的纳米颗粒应用于磁共振分子影像,但它的局限在于磁共振成像灵敏度非常低,因而找到一个合适的方法非常重要。磁纳米颗粒成像由于高灵敏度、高分辨率和特异性,故而可以很好地用于分子影像中。Bulte 等早些年已证实了细胞水平的MPI的适用性,并且将磁纳米颗粒成像的技术应用于干细胞的探测中[12-13]。2015年,Bulte等将不同数目的嵌入磁性纳米粒子的干细胞植入小鼠大脑的两个半球,且用临床前的MPI扫描仪进行断层成像,发现可以定量化不同干细胞的MPI信号的差异[14]。将磁颗粒嵌入间充质干细胞(mesenchymal stem cells, MSCs)是实现磁纳米颗粒靶向成像的一个很好的方案,因为MSCs可以在很多组织类型中被发现,而且可用于各种疾病的治疗,比如中风、心肌梗塞、外创性大脑损伤和癌症。其中,Zheng等分别于2015、2016年首次展示了在小鼠体内嵌入纳米磁颗粒的干细胞的体内影像[15-16]。关于嵌入MNP的干细胞的图像重建,Them等于2016年发表文章介绍了更多的细节[17],基于系统矩阵的图像重建,在干细胞的条件下需要严格要求磁纳米颗粒的流动性。
通过静脉注射,磁纳米颗粒作为跟踪剂可以在血管系统中停留一段时间,直到在网状内皮组织中堆积,然后转移到正常的体内代谢中。因此,磁纳米颗粒非常适合用于心脏或大型组织的动态血管造影中或者脑和心肌的灌注研究中。故而在诊断方面,由于磁纳米颗粒不含辐射和允许使用可跟踪装置的优势,其在心血管诊断方面也能有很好的应用,包括大血管的诊断、冠状动脉评估,以及心肌灌注到介入手术。各种各样专用的纳米磁颗粒都已经用于主动或被动的定位或药物输送[18-20]。
在肿瘤的磁热疗领域,磁纳米颗粒由于交变磁场下磁颗粒的产热特性,在靶向热疗方面也有广阔的应用前景。实际上,早在20世纪50年代末,Gilchrist等就提出了磁靶向热疗的概念,但由于材料、温度测定方法、磁场等条件的限制,研究结果与临床应用有很大差距[21]。随着纳米技术的飞速发展,20世纪90年代初,Jordan等发现,磁性氧化铁纳米颗粒具有很高的热效应,在临床允许的磁场强度和频率范围内,其热效应比微米级的磁性粒子高得多[22]。磁纳米颗粒的靶向热疗是一种通过直接注射、静脉注射或者介入等方式使MNP聚集到病变区域、并在交变磁场下发生磁致热效应的靶向治疗手段。当肿瘤组织被靶区磁介质感应加热到40~70℃时,热效应将破坏肿瘤细胞促使其凋亡,而非热区的健康细胞不受影响,从而达到细胞水平的精准靶向治疗的目的[23-25]。
2015年,Muraser等发现,磁纳米颗粒对于预测磁热疗的治疗效果确实有用,因为在肿瘤组织中MPI相关的特性与温度升高有着重要的关系[26]。2016年,又有众多学者用实验表明,MPI可以用在定量评估磁热疗中肿瘤的早期反应[27-28]。最近几年的研究发展,比如用于MPI导向的磁热疗的新的表现很好的氧化金属颗粒[29]、多维谱MPI的温度场成像[30]、靶向磁热疗等,均表明MPI在磁热疗方面的巨大的医学应用潜能[31]。
另外,作为一种新的缓释靶向给药系统,磁性纳米铁颗粒在肿瘤靶向治疗方面的研究飞速发展,成为国内外抗癌药物剂型研究的重点和热点[32]。
2 磁纳米颗粒的电磁探测
当外加时变磁场做输入时,磁流体(互不影响的超顺磁性纳米粒子组成)的磁化曲线成Langevin方程分布,可通过测量其磁感应强度来检测相关磁响应变化。通过检测接收线圈中的电压即可检测磁感应强度变化,由此进一步表征磁颗粒的浓度来代表MPI信号。用傅里叶变换将时域的电压信号转换为频域,即可得到信号的频谱。
基于上述原理,Biederer等提出了能测量磁纳米颗粒的交变磁场下感应出的频谱的磁谱仪,并通过建立颗粒模型,表明可以用磁谱仪来探测纳米颗粒[33]。2012年,Erbel等已经提出了商业化的磁谱仪,并准备推向市场[34]。
有研究表明,除了磁颗粒的溶液黏度、温度和颗粒黏合物的状态,磁颗粒的尺寸和材料特性比如各向异性均会影响颗粒的动力学特性[35],从而影响检测信号和磁颗粒浓度之间的关系。这就表明,磁颗粒电磁探测的信号会包含一些可以提取的功能信息。故而可以利用磁颗粒电磁探测的频谱来估计温度、黏性、颗粒黏合物的组分[36-38]。
2009年,Weaver等提出一种直接对MNP进行温度测量的方法,根据MNP的非线性磁化响应与其温度之间存在一定的单调特性来进行MNP本身的温度测量[36]。John等参照Gleich等提出的磁颗粒非线性响应波谱检测装置[2],证明利用这种方法可精确获得至0.3 K的温度测量结果。在国内,刘文中团队也对磁纳米颗粒的温度电磁探测方法进行深入研究,不断提高温度测量精度,从理论和实验上进行了在交变磁场或恒定磁场下的磁纳米颗粒的温度探测[39-40]。刘文中团队研究了一维空间上磁纳米颗粒温度成像,结果显示一维空间上颗粒浓度的变化越剧烈,颗粒浓度分布对温度测量的影响越大[41]。在温度成像方面,国内已有人得到了很好的一维成像效果,故而实现多维的温度成像有待进一步研究。2016年,Stehning 等实现了多维谱MPI的温度成像[30],他们提出了磁颗粒分布的同步成像和采用“多色”重建方法的温度测绘,为图像介入治疗比如磁靶向间质热疗的温度实时监控提供了可能,在MPI领域具有里程碑式的意义。
3 磁纳米颗粒的电磁成像
磁纳米成像(magnetic particle imaging, MPI)是磁纳米颗粒的重要应用领域,MPI 装置中激励频率通常低于25 kHz,这相当于在身体的波长约1 km。另外,MPI分辨率精细程度可以超过身体的波长6个数量级,单位达到毫米级别。这种技术不使用电离辐射。人体是逆磁性的,所以组织不会产生MPI信号。人体组织对MPI中使用的低频磁场来说完全透明,因此MPI对于无背景纳米颗粒造影剂的检测十分理想,它具有高灵敏度和高分辨率的优点。
2003年,Gleich提出了一种全新的基于示踪剂的成像方式-磁纳米颗粒成像[42]。它利用交变磁场下的超顺磁纳米颗粒的非线性磁化响应,通过检测磁纳米粒子的浓度分布进行成像。为了得到磁颗粒分布的图像,整个样品需要置于一个能产生零磁场点(field-free point,FFP)或零磁场线(field-free line,FFL)的梯度磁场。梯度磁场把除了FFP或FFL之外的所有粒子都磁化饱和,从而起到定位的功能。驱动线圈产生交变磁场,通过一系列的接收线圈检测纳米粒子产生的电压信号,通过傅里叶变换检测到的信号包含的高阶谐波即用于成像功能。MPI装置的原理如图1所示。
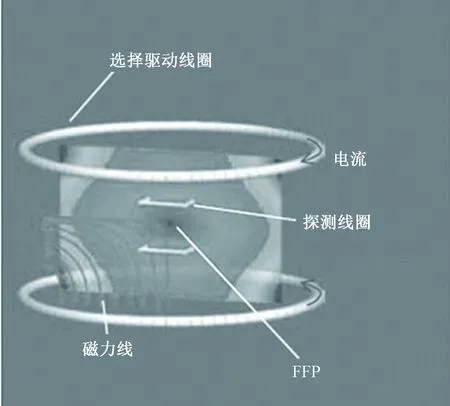
图1 MPI 装置原理[2]Fig.1 Schematic structure of MPI[2]
3.1 磁纳米颗粒成像扫描仪的研制
2005年,Gleich在飞利浦实验室研制成功了首个MPI静态扫描仪[2],但是基于该装置的基本的点成像原理,它需要已知浓度的磁颗粒作为实验参考来求系统矩阵。由于在视场下零磁场点的移动需要磁颗粒样品的机械移动,故而整个成像过程需要几分钟的较长的信号采集时间。2007年,Weizenecker 等发表了关MPI敏感度和空间分辨率的仿真论文[43]。为了提高数据采集时间,2008年Gleich等扩展了二维Lissajous轨迹的扫描仪,帧速可以达到25帧/s,并且第一次建立了动态的二维图像[44]。为了提高 MPI 的灵敏度,同年 Weizenecker 等提出了新的编码方案,该方案使用“零场线”[45],其扫描仪的结构和FFL的轨迹如图2所示,32个小的线圈产生旋转的零磁场线,FFL沿着驱动线圈磁场矢量移动即FFL的方向垂直于驱动线圈磁场矢量。使用FFL的断层成像需要零场线旋转起来,Erbe等介绍了第一个旋转FFL的原型[46],且Konk等[47]和Bente等[48]都展示了相关的成像实验。
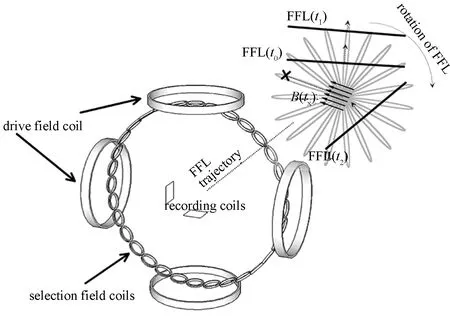
图2 扫描仪的结构和FFL的轨迹[45]Fig.2 Schematic setup of the simulated scanner geometry and the path of the FFL [45]
2009年, Weizenecker 等建立了三维实时成像,第一次展示了MPI 体内成像数据,揭示了小鼠的心跳特性(示踪剂的浓度经过了临床验证,且证明MPI能实现高实时分辨率(46帧/s)的四维成像)[3],如图3所示为飞利浦研究团队的小鼠MPI扫描仪。

图3 飞利浦研究团队的小鼠MPI扫描仪[3]Fig.3 Picture of the MPI mice scanner developed at Philips Research[3]
以上扫描仪的视场均处于一个对称的线圈装置中,这样一来会限制里面放置样品的尺寸,为了解决这个问题,2009年,Sattel 等发明了单边MPI扫描仪(见图4),并且展示了动态的一维成像[49]。如图4(a)所示,单边MPI扫描仪由两个同轴的驱动线圈(浅灰色)和一个单独的接受线圈(深灰色)组成,由图中箭头表示的相反方向的电流叠加产生选择梯度场。
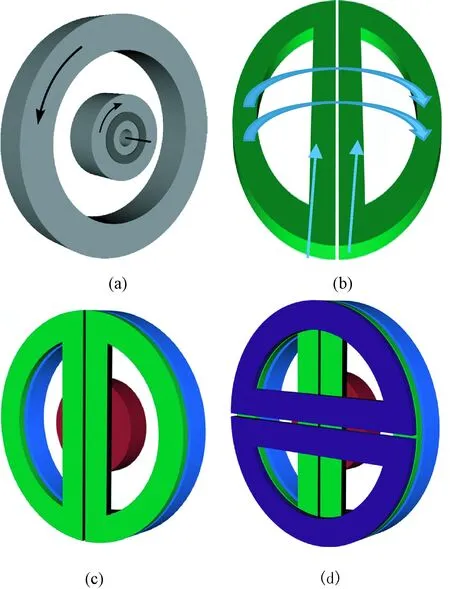
图4 单边MPI扫描仪结构[49-50]。(a)一维单边MPI线圈结构;(b)D形状线圈产生垂直磁场的原理;(c)二维单边MPI线圈结构;(d)三维单边MPI线圈结构Fig.4 Setup of a single-sided MPI scanner[49-50]. (a) Coil assembly of 1 d single-sided MPI scanner; (b) Principle of generating an orthogonal magnetic field using a pair of D-shaped coils;(c) Coil assembly of 2 d single-sided MPI scanner; (d) Coil assembly of 3 d single-sided MPI scanner
从图4中可以看出,轴线方向的信号传输和信号接收是通过环形线圈来实现,D形状的线圈对可用于多维成像的单边MPI扫描仪与轴线垂直方向的磁场部分的建立[50]。后来Sattel和Gräfe及其合作者建立了能实现多维成像的单边的MPI扫描器[51-52]。但是这种单边的MPI扫描仪与最初的扫描器设计相比,单边线圈拓扑结构扫描仪的空间分辨率表现出强烈的非均匀性,它随着距离的增加而减小。不同于在这之前所有提出的磁颗粒成像的图像重建一套理论,2010年,Goodwill等提出了一种基于x-space投影的MPI的图像重建方法,并且建立了第一个基于x-space投影的MPI扫描器,如图5所示[53-55]。图中NdFeB磁铁产生y轴方向的零磁场线(FFL),FFL缓慢移动磁铁,其电磁场的变化使FFL能沿x轴方向移动,激励驱动线圈xmit使FFL在z轴上快速移动。
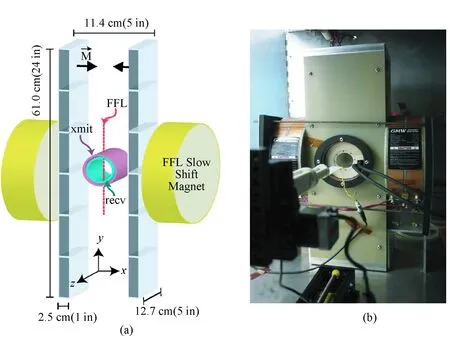
图5 第一个基于四极磁铁的投影MPI扫描装置[55]。(a)Berkeley研究团队的基于FFL扫描仪原理;(b)投影MPI 扫描仪Fig.5 First projection MPI scanner based on a quadrupole magnet [55].(a)Diagram showing all the magnets in the Berkeley FFL scanner; (b) Completed projection MPI scanner
3.2 磁纳米颗粒成像的图像重建
关于磁颗粒成像的图像重建,大体上可以分为代数的重建方法和分析重建方法。代数的重建方法也叫harmonic-space的重建方法,其原理是建立磁纳米颗粒的空间分布与频率空间电压信号关系的系统方程,然后将方程离散化通过矩阵求逆的方法来求磁颗粒的浓度,有
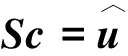
(1)
式中,S为M×N的系统矩阵,M为电压信号傅里叶变化后的谐波次数,N为磁纳米颗粒的样品的编码个数,c为N×1的浓度向量,为M×1的电压信号谐波的向量。
系统矩阵可以通过基于样品校正方法、基于模型的方法或者压缩感知的方法得到。基于样品的校准的方法即在每个体元网格的位置放置已知浓度的磁纳米颗粒的示例样品来测量相应的电压信号的频谱。这种方法的缺点在于当系统矩阵较大时对于大的运算很复杂,且基于样品校正的重建方法很耗时间。2010年,Knopp 等提出建立一个合适的信号链的模型来仿真整个MPI的系统,从而得到与校正法类似的图像重建效果。为了省去这种基于样品校正方法的采集时间,Knopp和Weber首次将压缩感知概念引入MPI系统矩阵,结果发现在二维成像中仅需求出系统矩阵的1/4[56-58]。
分析重建方法的思想是做出确定的假设得到明确的算法,目前有基于x-space的重建和Chebyshev 重建方法。基于x-space投影的MPI的前提假设是均匀磁场和线性时不变系统以及顺磁性纳米颗粒的Langevin的理论,它直接建立起零磁场点与电压信号的关系,即
(2)
式中,Hsat为激励磁场,s(t)为检测的电压信号,m为磁颗粒的磁矩,G为选择场梯度,B1为检测线圈的灵敏度,xs(t)为零磁场点(FFP)的瞬时位置,h(x)为零磁场点的路径传播方程。
由此,由已知的磁颗粒的位置,得到电压信号后进行零磁场点运动的速度补偿和网格化接受信号后直接进行图像重建。
基于x-space的重建方法比于上面求系统矩阵的harmonic-space的重建方法有很多优点:它可以产生线性时不变的图像且达到实时成像的速度,因为其每个像素点的重建相对简单;再者,它没有harmonic-space的重建方法的去卷积运算,不用考虑去卷积运算对提高分辨率的影响,而且避免了去卷积运算所带来的噪声增益。后来Rahmer 等提出,可以用加权Chebyshev转换的系数代表频率空间的信号[59]。Grüttner 等发现,基于x-space的重建和Chebyshev 重建方法在数学上是等同的,所以会得到同样的结果[60]。2010年,Knopp 等又引入了基于零场线(FFL)的重建方法[61-63]。
不过目前为止,在图像重建领域,仍然存在一个主要挑战:对成像过程中复杂的磁化动力学还没有完全理解。如果关于MPI有一个完全精确的模型,会加深对成像过程的理解,从而更好地分析设计硬件系统、FFP或者FFL的运动轨迹、磁颗粒和重建算法。
3.3 混合MRI/MPI的扫描器
由于磁纳米颗粒的检测缺少形态学的信息,故而使得对真实器官结构的氧化铁颗粒(superparamagnetic iron oxide,SPIO)的空间分布的确定变得困难。所以,Franke等提出了一种将磁纳米颗粒成像和磁共振成像(magnetic resonance imaging,MRI)相结合的高度集成的系统,它将基于MPI得到的有关SPIO分布的时间分辨率的测量和基于MRI得到的形态学和功能性信息相结合从而得到高的空间精度。2013 年,Franke等展示了第一台能连续数据采样的MPI-MRI混合扫描器的设计[64-65]。2014年,Vogel等研制了第一台试验性的混合MRI/MPI的扫描器[66],他们用嵌入行波MPI的欲极化的低场MRI系统得到二维混合图像[66]。2015年,Franke等基于MPI-MRI混合系统得到初始的三维混合图像[67],他们于2016年制造了第一台集成系统,其中MPI/MRI扫描器使用同一线圈系统来产生MRI的静态磁场B0和MPI的选择场[68],且得到三维时间分辨率的MPI数据和0.662×1.25 m3空间分辨率的三维MRI数据,且不需要样品的重置。这些初步的影像学研究表明了此高度集成化的MPI-MRI系统适用于多模态的体内临床研究,且在MRI数据的基础上提供了MPI精确的视场设计特征。
4 展望
由于氧化超顺磁磁性纳米粒子的优良特性,被用于分子影像、心脏或大型组织的动态血管造影、脑和心肌的灌注研究、心血管诊断、药物输送、肿瘤的磁热疗和靶向治疗这些重要的医学应用上。令人振奋的是,从最近几年的发展来看,MPI在干细胞示踪[14-16]、红细胞长期监测[9]、肺部影像[69]等方面也有着巨大的应用前景。
关于磁纳米颗粒的电磁探测,研究发现磁颗粒的信号和温度变化存在一定的关系,这就表明在未来有可能进一步发展磁纳米颗粒功能影像和磁热疗。2015年,Rahmer等提出在MPI领域具有里程碑意义的彩色或多维MPI技术[70],它能够提供更多的功能信息,比如区别不同的MPI示踪剂或者决定环境中的温度或者介质的黏度。2016年,Stehning 等实现了多维MPI的温度成像[30],他们提出了磁颗粒分布的同步成像和采用“多色”重建方法的温度测绘。不过此方法还应该试图研究在体内的没有溶解或者血液悬浮的颗粒的情况,例如在肝脏。此外,需要进一步通过测量或模拟评估产生与温度相关的信号变化的机制,如改变粒子的磁化斜率或磁滞。利用附加的线圈加热磁颗粒来诊断和治疗的高热装置已于2016年问世,应用MPI的磁热疗将成为MPI相关医学应用上的重要体现。
目前,磁纳米颗粒的一个重要的应用领域即磁纳米颗粒成像。自从MPI被发明以来,科学家们致力于发展提高其分辨率和灵敏度。在大部分研究工作中,使用的MPI分辨率已达到1~5 mm。尽管磁纳米颗粒成像的分辨率随颗粒的增大而增大,但相应也会增加纳米颗粒的弛豫效应,因而造成成像的模糊。为了达到能与MRI或CT竞争的空间分辨率,必须能合成最佳的超顺磁性氧化铁颗粒。为MPI量身定做SPIOs能显著改善其空间分辨率,故而为MPI研发合成专门的超顺磁性氧化铁颗粒已成为研究的一个新兴领域[71-74]。目前表现最好的MPI示踪剂之一已于2015年由Ferguson等发明,它由外面包裹着聚乙二醇的高分散性的金属磁颗粒组成[75]。
围绕MPI扫描仪的线圈拓扑结构也很多,各种拓扑结构设计除了追求分辨率和灵敏度比如提高选择场梯度,将MPI扫描器的尺寸提高到满足人体的要求也是研究趋势之一。对比核磁共振成像,MPI的扫描器可以从临床前小鼠尺寸扩大到人体适用的尺寸。2008年,Gleich等展示的扫描仪有32 mm的孔径[44],到2010年他们展示的扫描仪原型的孔径能达到12 cm[76]。以人的尺寸设计的梯度场肯定是可行的。例如,市售的3T的MRI扫描仪外面的孔具有7.2 T/m的最大空间梯度。发展和扩大针对基于人体的大小的扫描仪的MPI技术需要解决诸如安全、功耗、图像重建的时间和造影剂生产的问题。为了得到较大的激励磁场的需要由输出功率较大的功率放大器去驱动线圈,为了使背景场得到较高的梯度需要功率较大的电源。若采用麦克斯韦线圈对达到1.3 T/m的梯度需要功率大约900 W的直流电源,如果更大的磁场梯度即需要更大的功率。研究表明若考虑安全因素,在交变磁场频率为25 kHz的情况下约20 mT的磁场对于适用人体的装置来说太高了。许多研究小组正在开发一些临床前成像扫描仪。2011~2015年间飞利浦公司的团队一直致力于第一款人类MPI扫描仪,并在2016年的IWMPI会议上进行了展示。相关临床前成像扫描仪的实现反过来可以让专家进一步深入探究MPI潜在的医学应用。
关于磁纳米颗粒图像重建方法,其研究目标在于追求高的信噪比和短的采集时间。Kaczmarz算法作为一种重要的代数重建技术由于其快速的收敛性和易于实现的优点,它可以被视为解决有关MPI系统矩阵的重建方法的黄金方法。代数的图像重建方法的局限在于储存系统矩阵的内存需求,比如一个三维的 MPI包含323个位置,所有测量频率的系统矩阵需要大约20 GB,故可以进一步考虑将问题转化为稀疏矩阵进行压缩。
目前国外已有两家独立的厂商(Bruker Biospin MRI GmbH 2014, Magnetic Insight, Inc. 2017)生产出有商业化的临床MPI装置,而国内对MPI技术的研究几乎还处于空白阶段。磁纳米颗粒的检测缺少形态学的信息,使得其成像对真实器官结构的氧化铁颗粒的空间分布的确定变得困难,所以有人提出将MRI(或者其他影像手段)和MPI相结合实现多模态成像。在未来也许会建立类似于PET/CT和 PET/MRI的MPI/MRI的混合系统,在相邻的空间内有两种模态的影像。不过如果将MPI运用到需要高的实时分辨率的应用上,比如呼吸和心跳上就会存在问题,因为静态的背景图像只是真实背景的近似。所以混合MRI/MPI的扫描器所面临的挑战在于在MRI背景数据的基础上还要考虑MPI动态数据,从而设计出相应的解决方案。
