氧化铁/氧化锰复合负极材料的制备及其电化学性能的研究1
2018-07-13刁贵强郭娴梓封科军解芳陈晓宇廖文华邓妍芝
刁贵强,郭娴梓,封科军,解芳,陈晓宇,廖文华,邓妍芝
(惠州学院 化学与材料工程学院,广东 惠州 516007)
近年来,化石燃料的过度消耗和低效使用引发了一系列的环境问题,寻找可循环利用的绿色新能源变得尤为重要.化学电源作为一种新能源形式已引起人们的高度重视,其中,锂离子电池作为第三代化学电源,被称为“绿色电池”,它具有比容量高、充放电电压平稳、无记忆效应、循环寿命长及对环境污染小等优点,被广泛应用于手机、笔记本电脑[1-2]等便携式电子设备.
锂离子电池的负极材料是影响电池性能的关键因素之一.目前锂离子电池的负极材料主要为有碳基材料、硅基材料、锡基材料、氮化物、过渡金属氧化物等[3].其中,过渡金属氧化物作为负极材料具有理论比容量高(铁氧化物和锰氧化物的理论比容量均大于700 mAh/g)、放电平台低(MnO2:约0.4V,Fe2O3:0.8 V)、体积效应较小、成本低廉、对环境友好、制备工艺简单和产能较高的优点,是一类应用前景很好的锂离子电池负极材料[4-5].然而,过渡金属氧化物中,铁基氧化物和锰基氧化物存在电子导电性差、充放电过程中结构不稳定、材料体积变化大等缺陷,其实际比容量较小,并且循环稳定性差[3].
Tarascon研究小组[6]于2000年在Nature上首次报道了一种新型负极材料——金属氧化物MO(M:Co、Ni、Fe、Cu).其中,FeO 作为负极材料具有高达 600 mAh/g的容量,经过100次循环,仍有较好的稳定性.2013年,丁朋等人[7]发现MnO作为负极材料组装成扣式电池时,发现在充放电电流密度升高到141.1 mA/g时,循环充放电50次之后,发现其容量保持率高达99.5%.李静等人[8]发现MnFe2O4首次放电比容量为1 309 mAh/g,100次循环后放电比容量稳定在160 m Ah/g.这些研究结果显示了铁氧化物/锰氧化物有望成为一种高性能的锂离子电池候选负极材料.
当前研究者的研究方向是对其进行改性,例如通过改变制备方法、掺杂以及碳包覆等手段来提高锂离子电池的电化学性能[9].文章主要通过简便快捷的制备过程可控合成出不同结构的氧化铁/氧化锰复合材料,考察在空气气氛中,不同焙烧温度对氧化铁/氧化锰复合负极材料的电化学性能的影响.
1 实验部分
1.1 可控合成纳米氧化铁/氧化锰复合负极材料
将 0.78g Fe(NH4)2·(SO4)2·6H2O 溶解于 20 mL 纯水中,配制成淡绿色溶液;再加入1g NaOH、10 mL无水乙醇、10 mL油酸于60℃下搅拌2 h,得到棕褐色浊液A.另取0.99g KMnO4溶于150 mL纯水中,缓慢滴加浊液A于60℃下搅拌2 h,得到棕褐色浊液B.将棕褐色浊液B离心,用纯水和无水乙醇分别洗涤3次,放入烘箱中干燥,并在空气气氛中,分别在温度400℃、500℃、600℃、700℃、800℃、900℃、1000℃下焙烧2 h后得到一系列氧化铁/氧化锰复合材料.
1.2 电池组装
将活性物质、炭黑和羧甲基纤维素(CMC)按质量比为80:10:10混合研磨,然后滴加适量N-甲基吡咯烷酮溶液(NMP),搅拌使其成粘稠状,涂覆到铜箔上得到电极片于真空干燥箱进行干燥后,经辊压裁片后放入充满氮气的手套箱中组装成CR2025纽扣电池.其中对电极为金属锂片,隔膜为Celgard 2400多孔聚丙烯膜,电解液为1mol/LLiPF6,EC:DEC(1:1).
1.3 纳米氧化铁/氧化锰复合材料的表征及性能测试
1.3.1热重(TG)分析
在德国NETZSCH TG 209F1 Libra热重分析仪下进行热重分析:吹扫气为O2(流量20 mL/min)、保护气为N2(流量10mL/min)、升温速度为10℃/min,升温区间为30℃~950℃.
1.3.2X-ray衍射仪(XRD)测试
在德国布鲁克AXS公司D8-Aavance X–ray衍射仪下对材料进行结构表征:射线源为Cu-Kα,以Ni作为过滤片(λ =1.54056 Å),工作电压、电流分别为为40kV、40mA,扫描区间为2θ =10°~90°.
1.3.3红外光谱法(IR)测试
采用德国Bruker Tensor 27红外光谱仪进行红外测试,以KBr压片,记录样品在4000-400cm-1波数范围内的吸收峰,其分辨率为4 cm-1,样品和背景的扫描时间均为16s.
1.3.4电化学性能测试
交流阻抗(AC)测试在CHI660D电化学工作站进行,工作条件:振幅为5mV,频率范围为0.01Hz-100kHz,静止2s.在CT2001A蓝电电池测试系统中对其进行不同倍率的恒流充放电测试,工作条件:恒温23℃、电压区间0.01V-3.0 V.
2 结果与分析
2.1 热重(TG)分析
图1是干燥后未焙烧的氧化铁/氧化锰前驱体的TG曲线.由图可以看到,随温度的升高,样品的质量逐渐减少,在室温~325℃时样品质量减少对应自由水的蒸发和结晶水的脱去,失重率为17%;因油酸的分解温度在360℃,故在360℃~460℃对应油酸的分解失重,失重率约为20%,这与文献[10]报道一致;彭文等人[11]认为,MnO2在空气中高温烧结时容易失去晶格氧,Mn4+转变成Mn3+,因此,在460℃~800℃区间内样品缓慢失重,该过程应为氧化铁/氧化锰中氧化锰受热不稳定逐渐分解(MnO2→Mn2O3)引起的,其失重率为14%;而升温至800℃后样品质量有所增加,其2%的增重率可能是在高温条件下,样品与空气气氛中的氧气反应生成新物质导致的,这与图2XRD分析的结果观察到900oC下的产物出现强度较弱的MnO2衍射峰,说明更高温度下,Mn3+会与空气气氛中的O2发生反应生成Mn4+氧化物.

图1 氧化铁/氧化锰复合材料的前驱体空气气氛热重分析图
2.2 X-ray衍射仪(XRD)分析
在空气气氛中,对前驱体在400℃~900℃下进行焙烧后,由XRD对材料结构进行表征,结果如图2所示.
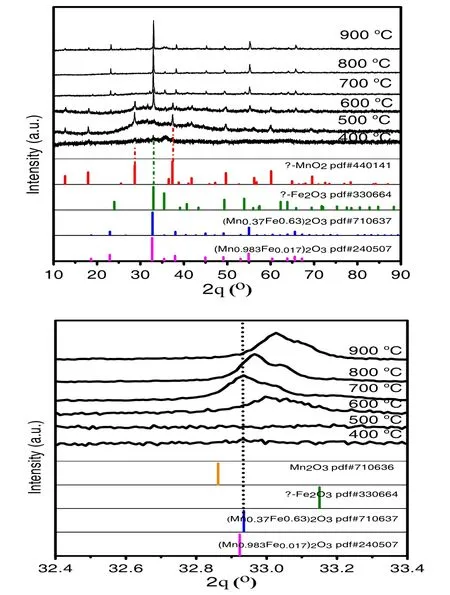
图2 (a)不同温度下焙烧的产物的XRD谱图(b)XRD衍射图谱局部放大图(2θ=32.4°-33.4°)
由图2可见在不同的焙烧温度下合成的氧化铁/氧化锰复合材料结构不同.400℃焙烧后得到的产物在XRD谱图中同时出现了多个强度较弱的衍射峰,这些衍射峰分别与 α-MnO2(PDF#:440141)和 α-Fe2O3(PDF#:330664)的特征衍射峰相对应,说明400℃焙烧的产物为结晶度较小、平均颗粒尺寸小的α-MnO2和α-Fe2O3的混合物,结合TG结果(图1)分析,这可能是由于在较低焙烧温度下,油酸分解不完全造成的;当焙烧温度升至500℃时,产物在2θ=28.8°、37.5°等处衍射峰变得更为尖锐,对应α-MnO2的特征衍射峰强度增大,说明500℃焙烧后,α-MnO2的结晶度变好,平均颗粒尺寸变大;将焙烧温度升高至600℃,产物α-MnO2的衍射峰强度减弱,且在2θ=33.0°处出现了衍射峰强度较大衍射峰,将2θ=32.4°-33.4°XRD衍射图谱局部放大(图2 b)可见该衍射峰位置相较于α-Fe2O3的特征衍射峰的位置向低角度偏移;这种现象随着温度进一步升高更为明显,当温度为700℃时,产物的衍射峰与(Mn0.37Fe0.63)2O3(PDF#71-0637)的特征衍射峰相符,说明随着温度的升高,α-Fe2O3的结晶程度增大、MnO2→Mn2O3转换,Mn3+(r=0.0645nm)和 Fe3+(r=0.0645nm)发生同晶替代逐渐生成了(Mn0.37Fe0.63)2O3复合氧化物,将温度上升至800℃或900℃,2θ=32.9处衍射峰逐渐向右移动,结合(Mn0.983Fe0.017)2O3(PDF#240507)的衍射峰位置分析,特征衍射峰向右偏移,这可能是产物(MnxFey)2O3复合物中Fe3+形成的氧化物结晶度增大,含量增加,而Mn3+的氧化物含量减少.另外,在900oC也可观察到强度较弱的MnO2衍射峰,说明更高温度下,Mn3+也会与空气气氛中的O2发生反应生成Mn4+氧化物,这与根据TG分析900℃观察到的2%增重结果相吻合.
综上,本论文制备的氧化铁/氧化锰复合物的前驱体在空气气氛中,通过调节不同焙烧温度可生成不同结构的产物(如表1所示),即,在400oC下首先生成了α-MnO2和α-Fe2O3混合物,随着焙烧温度的增加,α-Fe2O3的结晶度增大,MnO2的含量减少,在焙烧温度高于600℃时可生成组成为(MnxFe1-x)2O3的复合氧化物,并且随着焙烧温度的不同,x逐渐减小,即Mn3+氧化物成分逐渐减少.

表1 不同焙烧温度下的XRD产物表

(续表1)
2.3 红外光谱(IR)分析
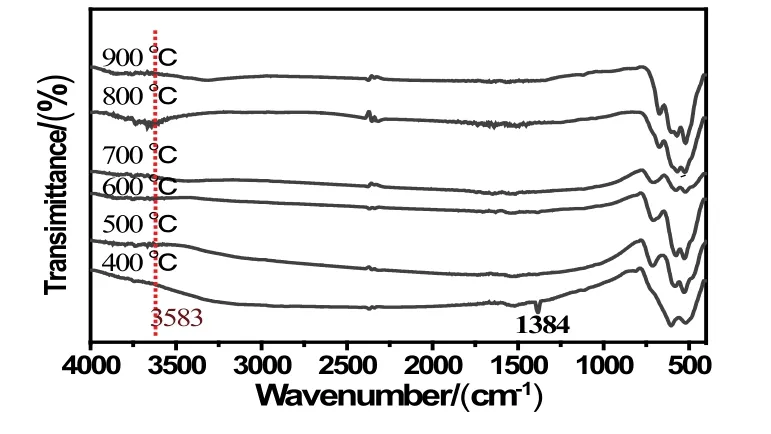
图3 不同温度下焙烧的产物的IR谱图

图4(图3局部放大图)
图3为氧化铁/氧化锰复合材料在不同焙烧温度(400℃~900℃)下的IR图.3583 cm-1附近的吸收峰是由样品中O-H的弯曲振动造成的,对应O-H和H2O分子缔合的特征峰[12].而400℃的曲线在1384 cm-1处显示一个吸收峰,可能是由未被完全分解的油酸中的C-O伸缩振动产生.根据文献[12-15]可知,在528.52 cm-1、579.66 cm-1、716 cm-1处的吸收峰为 MnO2的特征吸收峰;670 cm-1,611 cm-1,576 cm-1为 Mn2O3的特征吸收峰.而568 cm-1和583 cm-1处的吸收峰是因为Fe-O的伸缩振动,482 cm-1和595 cm-1则归属于Mn-O的弯曲振动.图3中样品的吸收峰大多分布在500~750 cm-1处,说明在不同温度下焙烧后的产物的结构中存在Mn-O和Fe-O.图4是图3在400~1000 cm-1区间内的局部放大图.由图4可见:400℃曲线中在521 cm-1和604 cm-1处有吸收峰,这与XRD分析结果中400℃时产物为α-MnO2和α-Fe2O3相吻合.当焙烧温度为500℃、600℃和700℃时,随温度升高,581 cm-1处的吸收峰向短波长区方向偏移,而577 cm-1和575cm-1处的吸收峰为Mn2O3的特征吸收峰;结合XRD谱图的分析:随着温度升高,α-Fe2O3的结晶度增大,其含量的增多而MnO2含量减少的情况相符.这也说明在更高温度下焙烧,即 700℃ 下 ,MnO2→Mn2O3转 换 、或 者 Mn3+(r=0.0645nm)和 Fe3+(r=0.0645nm)发生同晶替换生成(Mn0.37Fe0.63)2O3复合物.另外,当焙烧温度为800℃和900℃时,吸收峰的峰位向短波长区方向偏移,主要在673 cm-1,570 cm-1,520 cm-1处,同时存在Mn-O和Fe-O的吸收峰,这与XRD分析得出产物为铁/锰复合氧化物(MnxFe1-x)2O3相符.当焙烧温度继续升高至900℃时,在670 cm-1,602 cm-1,513 cm-1处可观测到吸收峰,这也说明其焙烧后的产物除铁/锰氧化物(MnxFe1-x)2O3外还含有少量MnO2.
结合TG、XRD和IR的分析可以表明,在不同焙烧温度下合成的氧化铁/氧化锰复合材料有三种,分别是Fe2O3和Mn2O3的混合物氧化铁/氧化锰复合物(MnxFe1-x)2O3(O<x<1)及(MnxFe1-x)2O3与MnO2的混合物.
2.4 电化学性能分析
2.4.1倍率性能
将不同结构的产物作为负极材料组装成扣式电池,对其进行恒流充放电测试,如图5和图6为不同温度下制得的电极材料分别在200、400、800、1600、3200和200mA/g下的倍率性能图.
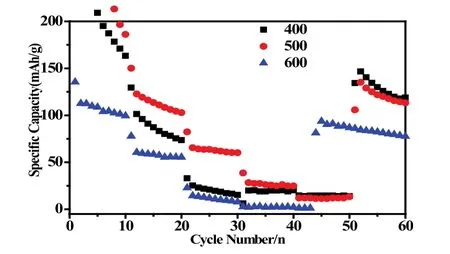
图5 (400~600℃的倍率性能图)

图6 (700~900℃的倍率性能图)
由图可见:所有样品在低电流密度下比容量衰减较快,随着电流密度的增大,电池的比容量进一步减少,这可能是由于氧化铁/氧化锰复合材料在充放电过程中存在体积变化大的缺点,造成该材料实际比容量较低和倍率性能较差.结合XRD(表1)和IR结果,400~500℃的产物为Fe2O3和MnO2的混合物,600℃时产物 为(MnxFe1-x)2O3x>0.37和 MnO2,700℃ 的 产 物 为(Mn0.37Fe0.63)2O3复 合 物 ;800℃ ~900oC 时 为(MnxFe1-x)2O3复合物,x<0.37,且含少量的MnO2.而在图6中,700℃~900℃曲线的倍率性能趋势与图5的趋势相同,随着温度升高,产物的比容量逐渐减少.对比图5和图6,可观察到700℃~900℃的倍率性能较400~500℃的样品好.其中,700℃下制得的的(Mn0.37Fe0.63)2O3倍率性能最优,当电流密度回到200 mA/g时,电池的比容量有较大幅度回升.这可能是由于铁氧化物和锰氧化物的复合,产生协同效应,能够在彼此充放电时作为缓冲介质,削弱体积变化的负面效应.同时,含少量MnO2的样品(900℃)倍率性能相对较差,这与文献[12]报道的一致.
2.4.2充放电曲线
由上述倍率性能可见700℃下制得的的(Mn0.37Fe0.63)2O3倍率性能最优,因而进一步分析200 mA/g的电流密度下电压及充放电比容量的关系,结果如图7:
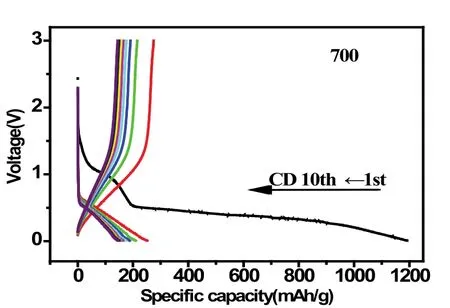
图7 电流密度为200 mA/g时,700℃下不同充放电次数的充放电曲线图
由图7可见:700℃下制得的(Mn0.37Fe0.63)2O3在第一次充放电曲线中,样品的放电平台较低(0.5V),初始放电比容量达1200 mAh/g,介于Fe2O3和MnO2的理论比容量之间(Fe2O3负极材料的理论比容量为1007 mAh/g,MnO2负极材料的理论比容量为1232 mAh/g),但其首次充电比容量较低(275mAh/g),初始库伦效率约为23%.这与文献[8]报道的铁锰复合氧化物氧化物的MnFe2O4类似,MnFe2O4比容量在30次左右循环后趋于稳定,为160 mAh/g[8].(Mn0.37Fe0.63)2O3在 2到10圈的充放电曲线中,样品比容量减少量较少,趋于稳定,说明随着循环次数的增多,样品的稳定性较好.
2.4.3交流阻抗
在0.01~105频率范围条件下对所得电池负极材料进行交流阻抗测试,结果如图8.
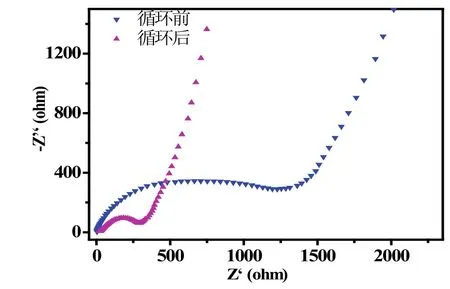
图8 700oC焙烧的产物充放电循环前与循环后阻抗谱图
700℃制得的样品,交流阻抗谱图由高中频区(103-104Hz)半圆与在低频区的斜线组成,半圆的半径大小代表电极/电解液界面的电荷转移阻抗(半圆越大,电阻越大),而低频区(10-3-103Hz)斜线反映电极活性物质孔道中电解液的离子扩散阻抗,又叫Warburg阻抗(斜率越大,电容性能越好)[16].在经过100次循环后半圆明显减小,说明在经过循环后电池的传导速度和扩散速度较大,电池性能较好,这与其倍率性能结果相吻合.
2.4.4循环性能
进一步探究700℃制得的样品的寿命循环性能,待电池循环100次后对其进行分析,结果如图9.
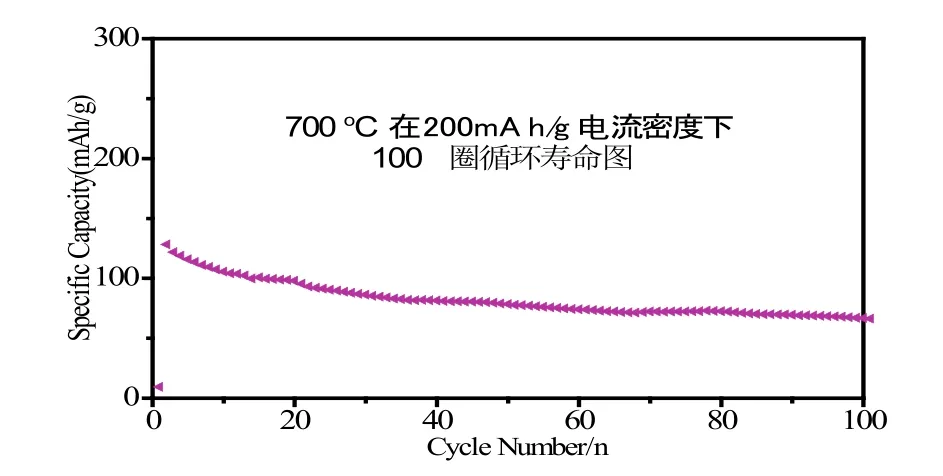
图9 700℃下循环100圈的倍率性能图
由图9可见:样品在100次循环后,其比容量衰减速度减缓,最终基本保持在70 mAh/g左右,其库伦效率为99%.说明样品循环稳定性较好,有利于增长电池的使用寿命,但其实际比容量较低.该结果与MnFe2O4类似[8],随着循环次数的增加,样品的充放电比容量均有所减少,充放电比容量趋于稳定.
3 结论
采用氧化还原沉淀法在空气气氛下,不同的焙烧温度可控合成了氧化铁/氧化锰复合负极材料,通过X-ray衍射(XRD)、红外光谱(IR)表征其结构,利用倍率性能、交流阻抗等测试测定其电化学性能.结果表明:本论文采取的方法可合成三种氧化铁/氧化锰复合负极材料:在400℃~500℃时为α-MnO2和α-Fe2O3混合物;700℃时为(Mn0.37Fe0.63)2O3复合氧化物;800℃~900℃时为(MnxFe1-x)2O3复合氧化物和二氧化锰的混合物.其中,700℃ 下合成的(Mn0.37Fe0.63)2O3作为负极材料时,其电化学性能优于其它结构的氧化物材料.
