碳纸负载纳米结构钴、镍及其合金薄膜催化剂的研制及其催化硼氢化钠水解制氢研究
2018-07-13冯裕发廖锦云
冯裕发,廖锦云*,季 山
(1.惠州学院 化学与材料工程学院,广东 惠州 516007;2.嘉兴学院 生物与化学工程学院,浙江 嘉兴 314001)
由于可开采利用石油资源的逐渐减少和环境污染问题[1-3]的日渐严峻,开发和利用新能源资源成为人类重要的课题.氢气作为高热值的能源[4],越来越受到人们的关注.氢气的热值为120 MJ·kg-1,是石油热值的3倍,且燃烧后产物为水,是最清洁的能源[5-7].氢气是一种易燃易爆的物质,储存和运输成为了制约其开发利用的重要因素[8-9].近年来,储氢材料和储氢技术受到广泛关注和研究.储氢材料主要有化学氢化物[10]、吸附储氢材料[11]和金属氢化物[12].金属氢化物由于储氢容量大,通过简单的水解反应即可制备出高纯度的氢气,因而具有其他材料无法比拟的优势[13].硼氢化钠催化水解制氢气是一种实用、方便且能有效制备高纯度氢气的新型制氢技术[14].硼氢化钠水解制氢多采用贵金属催化剂[15-18],其催化活性虽然较高,但由于其价格昂贵以及催化剂无法循环利用[19],限制了其应用.因此开发一种非贵金属且可循环利用的催化剂[20-21]成为了金属氢化物储氢制氢技术研究的重点.
本文通过制备一系列碳纸负载纳米结构钴、镍及其合金薄膜催化剂,并对其催化硼氢化钠水解制氢性能进行了研究,得出了反应的最佳工艺条件.
1 实验部分
1.1 碳纸负载纳米结构钴、镍及其合金薄膜的合成
使用的试剂均为分析纯,未做进一步纯化处理,实验用水为二次蒸馏水.
剪取一定面积(5×12 cm)的基体材料(碳纸),用蒸馏水和乙醇溶液反复清洗后放入反应釜.称取一定物质的量比的前驱物(NiCl2·6H2O与CoCl2·6H2O),加入20 mL蒸馏水搅拌至溶解,加入一定量的络合剂搅拌至溶解,称取一定量的NaOH,溶解后缓慢滴加至上述溶液体系中,加入一定量的表面活性剂,用移液管量取10 mL水合肼加入体系中,再加入约40 mL左右的无水乙醇,控制体系溶液约为80 mL,充分搅拌后,将溶液转移到反应釜中.在120℃下,反应釜加磁场反应8 h.反应结束后冷却至室温,取出碳纸,用蒸馏水和乙醇溶液喷洗2~3次,自然风干得到碳纸负载纳米结构钴、镍及其合金薄膜催化剂,用以各种测试.合成了8组纳米结构钴、镍及其合金薄膜,合成配比见表1.
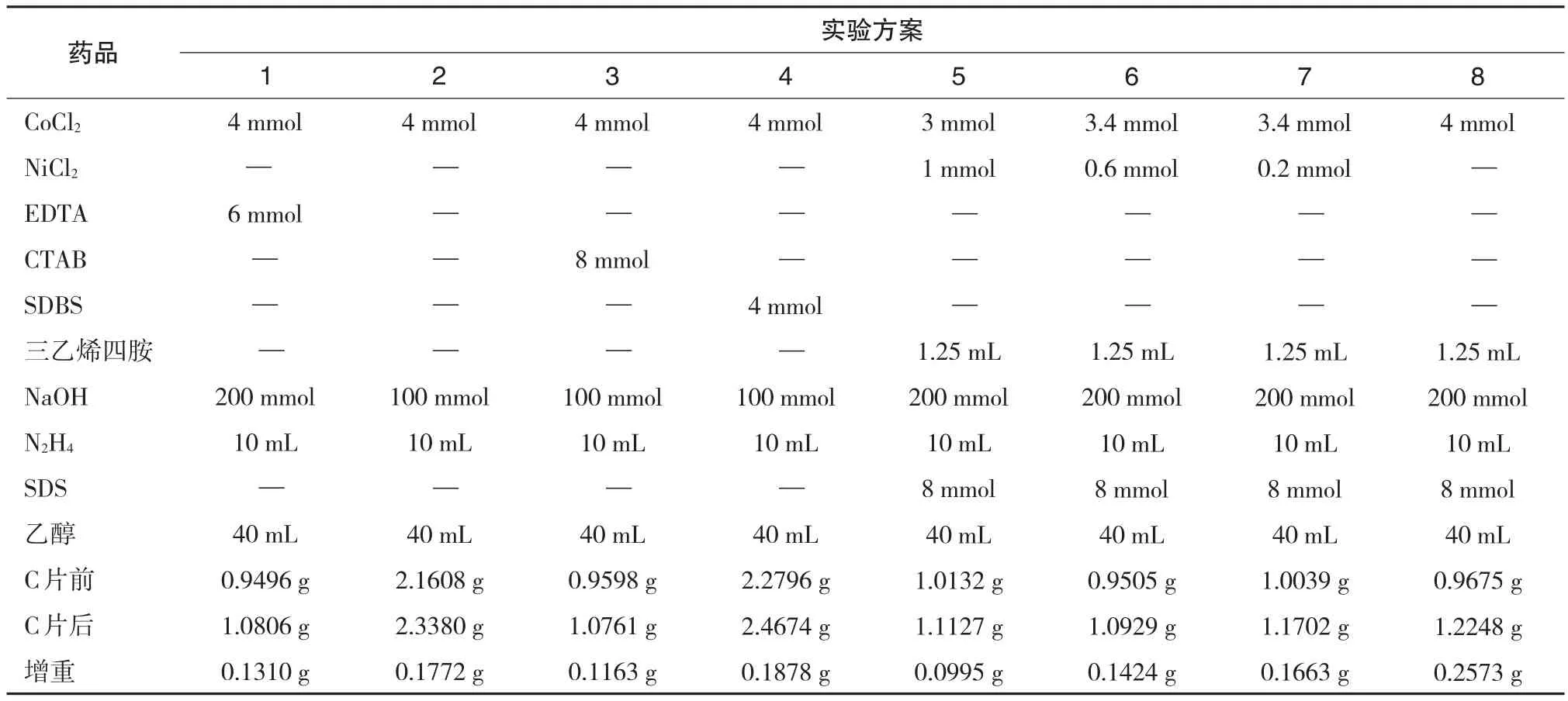
表1 8组催化剂合成配比
1.2 样品表征
使用日本日立公司的Hitachi-S4800型扫描电子显微镜分析样品的微观形貌.采用日本岛津公司的XD-3A型X射线衍射仪对样品进行晶型分析.测试条件为:Cu靶、Ni滤波,射线波长为0.15418 nm,管电压35 kV,管电流为30 mA.
1.3 催化性能表征
配制0.2 mol/L的硼氢化钠和0.4 mol/L的氢氧化钠溶液,分别取出25 mL加在圆底烧瓶中,裁剪一片催化剂(2.5×3 cm)加入混合溶液中,测定其产氢速率.
35℃水浴恒温,每5 min记录量产氢体积,共记录60 min.
硼氢化钠水解反应如下:

在没有加入催化剂,硼氢化钠在水溶液中,仍然会发生水解反应,碱性环境会抑制其水解.Kreevoy[22]等人提出了经验公式:
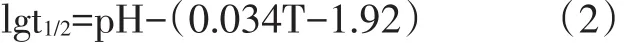
式中lgt1/2是NaBH4半衰期(单位为min),T是绝对温度(单位为K).即使在25℃下,NaBH4与水混合也会发生一定程度水解,因此,为了使NaBH4制氢能够得到实际应用,必须将其保持在强碱性溶液中.在25℃和pH值为14的情况下,根据式(2)计算出硼氢化钠溶液的半衰期约为421d,可满足实际应用要求.
本实验通过加入氢氧化钠,调节溶液pH值,在没有加入催化剂之前,抑制NaBH4水解,从而更精准地考察催化剂的活性.
2 结果与讨论
2.1 纳米薄膜SEM表征结果
图1为纳米薄膜催化剂SEM照片.图1a为未负载催化剂的基体材料碳纸的SEM照片,图1b为负载了钴的1号催化剂SEM照片,从图1b可以发现1号催化剂为片状结构,分散均匀,表面蓬松,从图1c可以看出该催化剂纳米片宽度为300~400 nm,纳米片的厚度仅为10 nm左右.李浩等人[23]认为EDTA在该体系中与钴源络合为稳定的[Co(EDTA)]2-,并起到以下作用:(1)改变了反应的前驱体;(2)降低溶液中自由钴离子的浓度,减缓了还原反应的速率.当络合剂与金属离子形成稳定的络合物后,络合剂可以作为形貌导向剂选择性地吸附在晶体的不同晶面控制晶体生长.(3)通过络合的形式对金属离子进行储存,并控制金属离子的释放速率,使其在特定的环境中得到一些具有特殊形貌的纳米材料.


图1 催化剂SEM照片
2.2 纳米薄膜XRD表征结果
图2为催化剂的XRD谱图.2θ在26.4°和54.5°出现的衍射峰为C纸的特征峰对应的是六方密堆积结构碳的(002)、(004)晶面的衍射峰(PDF#41-1487),将2θ在 40°~70°局部放大,可以发现,2θ在 41.7°、44.3°和47.0°出现的衍射峰对应的是六方密堆积结构钴的(100)、(002)和(101)晶面的衍射峰(PDF#05-0727).
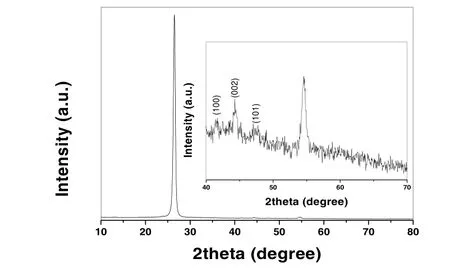
图2 催化剂XRD谱图
2.3 不同催化剂催化性能比较
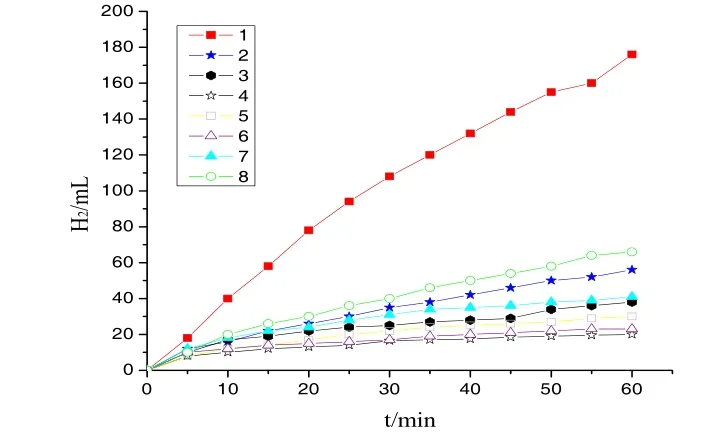
图3 不同催化剂催化性能比较
由图3可以看出,1号样品的活性比其他样品的活性高,60 min后能产生176 mL的氢气,且产氢速率明显高于其他样品,而活性最差的4号样品60 min后只产生了20 mL的氢气,其他样品产生的氢气也不多,各样品采用不同的表面活性剂和不同配比的药品,导致样品活性有差别.结合表1可以看出,加入EDTA络合剂的1号样品催化活性比加入三乙烯四胺络合剂的8号样品催化活性更高,这可能是因为EDTA的空间位阻大于三乙烯四胺的空间位阻,导致了以EDTA为络合剂合成的纳米薄膜催化剂活性位数量要多于以三乙烯四胺为络合剂合成的薄膜催化剂.明显可以看出,没有加入络合剂的2号样,活性比1号样和8号样活性差.说明络合剂作为形貌导向剂,调控了催化剂的形貌,进而增加了催化剂的活性位数量.另外,通过对比加入CTAB的3号样品和加入SDSB的4号样品,可以发现加入阳离子表面活性剂合成的薄膜催化剂活性优于加入阴离子表面活性剂合成的薄膜催化剂.
2.4 反应条件对纳米薄膜催化性能的影响
选取1号催化剂,考察了反应温度、反应物浓度和催化剂用量对催化剂性能的影响.


图4反应条件对催化性能影响
图4a为反应温度对催化活性的影响.可以发现随着温度的提高,催化制氢的速率逐渐提高,55℃时能放出440 mL的氢气,并且反应时间只要40 min,而在25℃时60 min只放出52 mL氢气.这是因为随着反应温度的提高,反应物分子的能量增加,使一部分能量较低的分子变成活化分子,增加了分子的碰撞次数,从而增加了反应速率.
图4b为反应物浓度对催化活性的影响.对比了反应物浓度为0.2 mol/L的硼氢化钠和0.4 mol/L的硼氢化钠水解制氢的性能.结果表明硼氢化钠浓度为0.4 mol/L制氢速率较好.这是因为随着反应物浓度的增加,分子间碰撞的几率增大,从而加快了反应速率.
图4c为催化剂用量对催化活性的影响.可以发现,当催化剂用量为2片、3片和4片时,60 min后,系统产出的氢气体积均能达到445 mL,与理论产氢量448 mL非常接近.当催化剂用量为1片时,系统产氢量为176 mL,与理论产氢量相差较大.从图4c还可以发现放氢速率随着催化剂用量的增加而增加.这是由于催化剂用量的增加,使活性位数量增加,反应变得更容易.
3 结论
采用溶剂热法合成了一系列碳纸负载纳米结构钴、镍及其合金薄膜催化剂并通过催化硼氢化钠水解制氢考察了其催化活性,研究表明在EDTA做络合剂,钴做前驱物的条件下合成的催化剂的活性最高,在35℃条件下反应1 h,放氢量可达176 mL.同时考察了不同反应温度和不同反应物浓度对催化剂活性的影响,得出了较高的反应温度、较高的反应物浓度和较多的催化剂用量有助于提高催化剂活性.
