腹腔镜肝切除的临床应用研究
2018-07-13游锦华廖锦岐段进东邱金伦
游锦华 袁 波 廖锦岐 段进东 廖 方 邱金伦
广东省惠州市第一人民医院肝胆外科,广东惠州 516003
微创手术将成为未来手术的趋势,所以腹腔镜作为微创手术的一部分,在未来肯定会被越来越广泛运用。腹腔镜肝切除术一直以来被视为高难度、高风险的腔镜手术,曾经是微创技术的相对禁区,但近年来该项技术在国内外发展迅速,成为微创技术在肝胆外科领域的重大突破。1991年Reich等[1]首先报道2例腹腔镜肝切除术,拉开了腹腔镜手术的序幕。经过20多年的发展,目前国内各大型医疗中心已积累较多手术病例,其中部分术式如腹腔镜肝左外叶切除已有望成为治疗肝左外叶肿瘤的标准术式,腹腔镜肝切除术与传统开腹手术相比具有手术创伤小、全身反应轻及术后恢复快等优点[2-4],同时也能达到同开腹手术相同的疗效,本研究旨在通过对已有病例的总结及新病例的积累,从术式规范、手术经验总结及与传统开腹手术各项指标对比等方面着手进行研究。本研究选取2016年1月~2017年12月我院已完成的54例肝切除患者为研究对象,现报道如下。
1 资料与方法
1.1 一般资料
选取2016年1月~2017年12月完成的54例肝切除患者。手术方式根据患者意愿而非随机选择。其LH组31例,男18例,女13例,年龄28~82岁,平均(53.6±10.2)岁,肝功能Child-Pugh评分;A级20例,B级11例;术后病理诊断(肝癌21例,肝内胆管结石10例),病变位置:Ⅱ段20例,Ⅲ段11例;肝脏占位性病变直径约(6.4±2.6)cm,;OH组23例,男14例,女9例,年龄31岁~78岁,平均(52.2±9.6)岁,肝功能Child-Pugh评分;A级15例,B级8例,术后病理诊断(肝癌15例,肝内胆管结石8例),病变位置:Ⅱ段15例,Ⅲ段6例,Ⅴ段2例;肝脏占位性病变直径(5.6±3.1)cm。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。
表1 两组患者手术相关资料比较(±s)
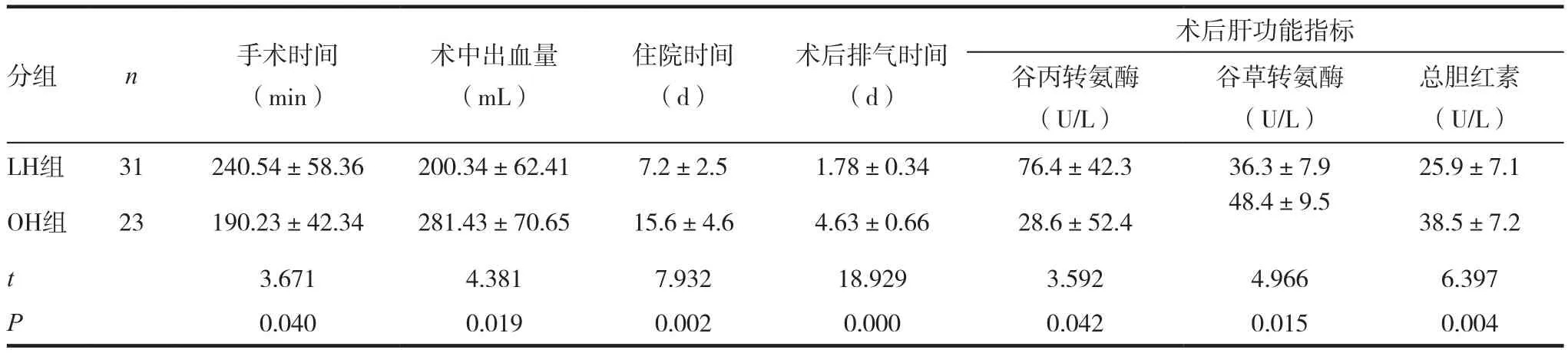
表1 两组患者手术相关资料比较(±s)
分组 n 手术时间(min)总胆红素(U/L)LH组 31 240.54±58.36 200.34±62.41 7.2±2.5 1.78±0.34 76.4±42.3 36.3±7.9 25.9±7.1 OH组 23 190.23±42.34 281.43±70.65 15.6±4.6 4.63±0.66 28.6±52.4 48.4±9.5 38.5±7.2术中出血量(mL)住院时间(d)术后排气时间(d)术后肝功能指标谷丙转氨酶(U/L)谷草转氨酶(U/L)t 3.671 4.381 7.932 18.929 3.592 4.966 6.397 P 0.040 0.019 0.002 0.000 0.042 0.015 0.004

表2 两组患者术后并发症比较
1.2 手术方法
1.2.1 LH组 患者气管插管,全身麻醉,常规外科手术消毒。于脐周1cm做个切口,穿刺建立气腹。成功建立后,置10mm的Trocar导入腹部,置入腹腔镜,一般采用4孔或5孔法进行操作 ,操作孔位置根据具体肝脏病变位置而定。手术步骤 :(1)先全面探查腹腔,再探查肝脏及邻近器官,根据肝脏占位性病变大小、位置及局部血供,综合评估决定手术切除范围和具体术式。(2)根据肿瘤位置,Ⅱ、Ⅲ段采用肝左叶外切除,切断相应肝周韧带,游离肝脏以充分显露肿瘤,解剖肝门,并夹闭且切断左肝动脉及肝左外叶段门静脉属支。游离右半肝时应注意小心处理肝短静脉。若Ⅴ段肝脏病变,解剖第一肝门,沿门静脉右后支游离肿物下缘。(3)应用超声刀切开肝脏,遇到显露段血管应用闭合夹夹闭,防止出血。(4)观察肝断面是然后出血或胆汁漏后用止血纱布覆盖断面。留置引流管,切除肿瘤装入标本袋方便做病理,确认肿瘤是否完整切除。
1.2.2 OH组 患者气管插管,全身麻醉,常规外科手术消毒,选取正中或肋缘下切口。手术步骤:(1)依次探查腹腔、肝脏和邻近器官,根据占位性病变的大小、位置及局部血供决定手术切除范围和具体术式。(2)切除前解剖第一和第二肝门,预留止血带预防出血,用电刀在肝表面标记肝切线,沿标记线旁开占位性病变处2cm行钝性切除术,逐一钳夹切断断面管道并结扎,将病变处完整切除。后续操作同LH组[5]。
1.3 观察指标
比较分析两组在手术时间、术中出血量、住院天数、肛门排气时间、围手术期并发症(胆漏、肠漏、出血、腹腔感染、伤口感染)等情况,并增加远期随访指标(半年复发率、一年复发率、两年复发率、无瘤生存)。
1.4 随访
所有患者采用电话和门诊随访。定期复查,复查内容包括肝功能、彩色多普勒超声等影像学检查,恶性肿瘤复查内容包括肝功能、AFP、CT或彩色多普勒超声等影像学检查。
1.5 统计学处理
采用统计学软件SPSS19.0版对数据进行统计分析,计量资料以(±s)表示,采用t检验,计数资料以百分数(%)表示,采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 手术情况
LH组手术时间、术中出血量、住院时间、术后排气时间和术后肝功能指标均低于OH组,差异均有统计学意义(P<0.05)。术后并发症方面,LH组术后1例发生胆漏,2例腹水,抗炎治疗后效果明显,4例术后少量出血,给予止血,输入冷沉淀凝血因子及充分引流后愈合,没有发生感染,无死亡患者。OH组2例胆漏,对症处理,7例发生少量出血,给予止血后痊愈;2例切口感染,给予勤换药对症处理后愈合;无死亡患者。LH组术后并发症发生率低于OH组,差异有统计学意义(P<0.05)。见表1~ 2。
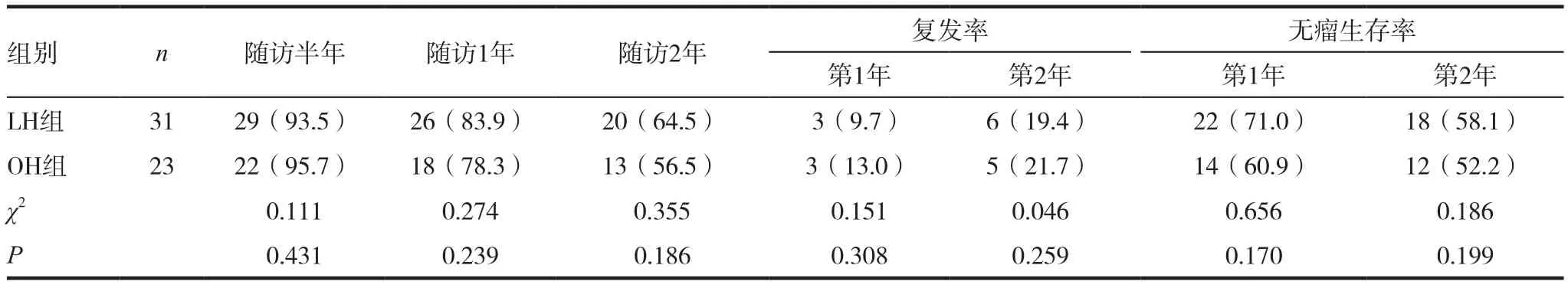
表3 两组患者术后随访情况[n(%)]
2.2 随访
术后随访1.0~2.0年,出院后半年行AFP,CT检查,每6个月复查一次。随访满半年段患者,腹腔镜组有29例(94%),开放手术组有22例(96%);随访满一年的患者,腹腔镜组26例(84%),开放组18例(78%);随访满2年的患者,腹腔镜组有20例(65%),开放组有13例(56%)。患者在1、2年复发率和无瘤生存率比较差异无统计学意义(P>0.05)。见表3。
3 讨论
我国是肝肿瘤和肝内胆管结石发生率较高的国家,腹腔镜切除术与传统开腹手术相比具有手术创伤小、全身反应轻及术后恢复快等优点[6-9],本研究得到了同样的研究结果,在住院时间、进食时间、手术出血这几项指标中,腹腔镜手术具有明显的优势,值得推广和研究。在随后的随访中,第1、2年的复发率和无瘤生存率没有太多差别,与开腹手术相当[10]。根据手术切除方式 ,可将腹腔镜肝切除术分为腹腔镜解剖性肝切除与非解剖性肝切除。根据肿瘤占位的大小、位置等,选择相应的最佳手术方式。就病变部位而言,不同术式的腔镜肝切除手术能否成功开展与术者及腹腔镜技术水平及所在单位整体技术和设备水平有关。已有共识,(1)(Couinaud 1I、Ⅲ、IVb、V、VI段)[11]病变是腹腔镜肝切除的较好适应证。(2)病变未侵及第一、第二肝门及下腔静脉;(3)良性病变直径≤15 cm,恶性肿瘤直径≤10 cm;(4)患者肝功能应在Child—Pugh评分为A级或B级;(5)无其他脏器严重器质性病变及凝血功能障碍,剩余肝脏能够满足患者的生理需要[12]。
然而腹腔镜手术仍然有很大难题,肝脏血运复杂,解剖结构很复杂,因此有很多禁忌症[13],(1)开腹切除术禁忌症;(2)肝癌合并肝内转移、门静脉癌栓、肝门淋巴结转移或肿瘤边界不清;(3)有上腹部手术史且腹腔内粘连严重、严重肝硬变、门静脉高压者;(4)肝功能分级 Child C 级或合并其他重要脏器功能不全者;(5)病变较大,第一、二肝门无法进行显露和分离,或病变需要大范围淋巴清扫。还有就是如何控制腹腔镜手术下的大出血问题,仍然需要攻克。杨刚等[14]报道,合适的病例、Trocar布置、观察角度、术前充分评估、三围重建模拟切除、术中对肝内外管道的精细解剖及多种方式的止血手段,会大大降低手术意外出血的风险,并极大提高手术成功率。有效的预防和控制出血是腹腔镜手术的成功关键。本研究为了减少手术出血,降低风险,在手术团队,术野暴露,医疗器械都有严格的要求。手术是否实用与治疗费用关系密切。LH 手术结合使用Ligasure、金属Trocar,减少了直线切割器等,一次性耗材的使用,更具费用效益[15]。同时腹腔镜手术相对手术拓展小,避免了腹部脏器段直接暴露,对胃肠刺激弱,所以肠道功能损害小。而且腹腔镜手术相对精细,减少因为输血而增加肿瘤复发但因素,术后痛苦小,可以早期活动,也减少了下肢静脉血栓的发生。
