掺杂型ZnAgInS2量子点的制备、表征及其在铜离子检测中的应用
2018-07-04许效龄王艺凝
赵 丹,伦 嘉,许效龄,王艺凝,张 蕊
(中南民族大学 药学院,武汉 430074)
近年来,荧光纳米材料在光电设备、分析检测、生物成像、控释给药等领域均展现出巨大的应用前景[1],荧光纳米材料的合成及应用开发成为众多研究者关注的重点.为避免有害物质在人体内的富集及对环境的破坏,含有汞、铅、镉等元素的量子点(QDs)逐渐被抛弃,研究转向生物相容性更好的新型水溶性量子点,如金、银、硅以及Ⅰ-Ⅲ-Ⅵ族(AgMX2,CuMX2;M=Al,Ga,In;X=S,Se)量子点等.
水热法[2]合成的量子点无需相转移直接可应用于生物体系,且操作简单、设备廉价、利于技术推广.水相合成法制备单元素金、银、硅量子点时难以实现波长的调节[3].而Ⅰ-Ⅲ-Ⅵ族量子点的水热法合成则可通过控制元素比例、反应温度和时间、反应原料、表面修饰和元素掺杂条件等实现波长的调节,但存在量子点不够稳定且量子产率较低的问题[4,5],可通过包壳和元素掺杂解决.例如,水热法合成AgInS2和CuInS2量子点的量子产率仅为1%,在其表面包覆一层ZnS的壳后量子产率可达到20%[5,6],Zn掺杂得到的Zn-Ag-In-S四元量子点的量子产率可达到20%~30%[7].由于包壳操作繁琐,条件难控导致重复性不佳,而元素掺杂作为直接合成法无需后续处理,已合成了Zn掺杂的Zn-Ag-In-S[7,8]和Zn-Ag-In-Se[9]量子点,其稳定性及产率均大大提高.
Cu2+既是有毒的重金属离子同时也是人体必需的微量元素之一,过多的Cu2+富集会导致人体代谢紊乱,严重影响健康.已有如CdSe/CdS QDs[10]、CdTe QDs[11]、石墨烯QDs[12]实现了对Cu2+检测.而与毒性较大的荧光探针相比,生物相容性更好的ZnAgInS2QDs对Cu2+的检测更具研究价值.
本文首次以N-乙酰-L半胱氨酸为配体,利用水热法一步合成了ZnAgInS2四元量子点,详细讨论了pH值、元素比例、反应温度和时间等因素对合成的影响,并进一步考察了该量子点的稳定性、光学性质和形貌等,最后以所合成的ZnAgInS2量子点作为荧光探针完成了对水溶液中Cu2+的检测.
1 实验部分
1.1 仪器与试剂
硝酸银(中国上海试剂一厂,纯度99.95%~100.05%),醋酸铟(Strem Chemicals,纯度99.99%),硫化钠(上海统亚化工,分析纯AR),N-乙酰-L-半胱氨酸(Aladdin,纯度99%),罗丹明6 G(Aladdin,分析纯AR),实用水均为超纯水(Milli-Q-RO4水净化系统,Millipore),高纯N2(四川天一).
傅里叶变换红外光谱仪(Nicolet 6700型,英国),透射电镜(Tecnai G2 20型,美国FEI),X射线能谱仪(Ametek型,美国EDAX Gensis),紫外可见分光光度计(Lambda-35型,美国),荧光分光光度计(LS55型,美国),电子天平(CP214型,上海奥豪斯),pH计(PHS-3C型,雷磁公司),集热式恒温磁力搅拌器(DF-101D型,巩义市予华仪器),电热恒温鼓风干燥箱(DHG-9030型,上海一恒),暗箱式自动紫外分析仪(ZF-20C,上海宝山顾村电光仪器厂).
1.2 ZnAgInS2 QDs的合成
按反应物摩尔比r[Zn(Ac)2∶In(Ac)2∶AgNO3∶NAC] = 0.2∶1∶0.25∶9配制反应前驱液,其中c(In(Ac)2)= 2 mmol·L-1, 调节pH值至9.5.在N2保护下加入Na2S溶液,其中r(In3+∶S2-)=1∶1.8.将反应液转移至高压反应釜中190 ℃反应3.5 h后取出,即得ZnAgInS2QDs.
1.3 ZnAgInS2 QDs的表征
采用红外、TEM、X射线能谱仪、荧光分光光度计对量子点进行表征,所制备ZnAgInS2QDs的相对量子产率是以罗丹明6G(乙醇为溶剂,QY=95%)为基准测得,所有光谱图数据均在室温下测得.
1.4 Cu2+的检测
依次移取适量QDs,Cu2+溶液,PBS(50 mmol·L-1,pH = 7.8)共1 mL到荧光比色皿,混匀,避光反应5 min后测定体系的荧光.
2 结果与讨论
2.1 ZnAgInS2 QDs的合成
2.1.1 醋酸锌浓度对ZnAgInS2QDs的影响
由于反应物摩尔比、前驱溶液pH值、反应时间、温度均能极大地影响量子点的荧光性能,为了获得高质量的量子点,必须严格控制实验条件.在pH=9.5,θ=190 ℃,t=3.5 h,c(In2+)=2 mmol·L-1条件下,固定反应物摩尔比r[In(Ac)2∶AgNO3∶Na2S∶NAC]=1: 0.25: 1.8: 9,仅改变Zn的添加量,在r(In∶Zn) = 1∶0,1∶0.05,1∶0.1,1∶0.2,1∶0.3,1∶0.4条件下合成ZnAgInS2QDs,结果如图1所示.
图1中当r(In∶Zn)的摩尔比由1∶0升至1∶0.2时,量子点荧光强度上升了83.54%.由于掺杂进入体系的锌离子导致体系的能带隙发生改变并完善量子点的晶体结构[13],锌元素的掺杂使ZnAgInS2QDs的发射峰位置由593 nm蓝移至550 nm.当r(In∶Zn) >1∶0.2时,量子点的荧光强度不再升高,因此In/Zn最佳摩尔比为1∶0.2.

图1 不同Zn/In摩尔比下所合成的ZnAgInS2 QDs的荧光图谱Fig.1 Fluorescence spectra of the ZnAgInS2 QDs prepared at different Zn/In molar ratios
2.1.2 硝酸银浓度对ZnAgInS2QDs的影响
其他条件不变,只改变Ag添加量,考察r(In∶Ag) = 1∶0.05,1∶0.15,1∶0.25,1∶0.35,1∶0.45时合成的ZnAgInS2QDs的荧光性能,结果见图2.如图2所示:在一定范围内随着Ag含量增加,ZnAgInS2QDs的荧光强度不断增强,由于随着In/Ag比例的变化,量子点能带隙发生了改变.在r(In∶Ag) = 1∶0.25时荧光强度达到最大,继续增加Ag的配比,荧光强度不再增加反而出现明显的降低,故In/Ag最佳摩尔比为1∶0.25.

图2 不同Ag/In摩尔比所合成ZnAgInS2 QDs的荧光图谱Fig.2 Fluorescence spectra of ZnAgInS2 QDs prepared at different Ag/In molar ratios
2.1.3 NAC浓度对ZnAgInS2QDs的影响
配体的用量也会在一定程度上对量子点的荧光光谱产生影响,改变NAC用量来探究配体用量对ZnAgInS2QDs的荧光性能的影响,其余条件不变,考察在r(In∶NAC) = 1∶5,1∶8,1∶9,1∶10,1∶11的条件下合成的ZnAgInS2QDs的荧光强度变化,结果见图3.如图3所示:当r(In∶NAC)的摩尔比从1∶5升至1∶9时,其荧光强度上升了132.7%,r(In∶NAC)=1∶9时,ZnAgInS2QDs的荧光强度达到最大值,故In/NAC最佳摩尔比为1∶9.

图3 不同NAC/In摩尔比所合成的ZnAgInS2 QDs的荧光图谱Fig.3 Fluorescence spectra of ZnAgInS2 QDs prepared at different NAC/In molar ratios
2.1.4 硫化钠浓度对ZnAgInS2QDs的影响
在其他条件最佳的条件下,只改变S2-的投入量,分别考察r(In∶S) = 1∶1,1∶1.5,1∶1.8,1∶2,1∶2.5时合成ZnAgInS2QDs的荧光发射光谱.如图4所示:在一定的范围内随着S2-含量的增加,ZnAgInS2QDs的荧光强度不断增强,但发射波长并无明显改变,这与Deng D等[9]研究一致,当r(In∶S) = 1∶1.8时,ZnAgInS2QDs荧光强度达到最大值.故In/S最佳摩尔比为1∶1.8.

图4 不同S/In 摩尔比所合成的ZnAgInS2 QDs的荧光图谱Fig.4 Fluorescence spectra of ZnAgInS2 QDs prepared at different S/In molar ratios
2.1.5 前驱溶液pH值对ZnAgInS2QDs的影响
合成过程中前驱溶液pH值会极大地影响量子点的荧光强度,考察前驱溶液pH值对合成ZnAgInS2QDs的影响,结果见图5.如图5所示:在pH值从6上升至9.5时,前驱液由浑浊逐渐澄清说明其溶解完全,同时由于溶液均一利于反应进行ZnAgInS2QDs荧光强度不断增强,进一步增大pH值时,量子点的荧光强度呈下降趋势.因此,前驱溶液最佳pH值为9.5.
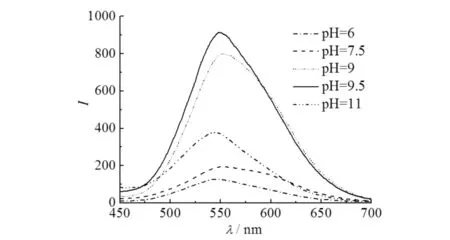
图5 不同pH值下所合成的ZnAgInS2 QDs的荧光图谱Fig.5 Fluorescence spectra of ZnAgInS2 QDs prepared at different pH value
2.1.6 反应时间和温度对ZnAgInS2QDs的影响
固定其他条件不变,考察反应时间及温度对所合成量子点影响.随着反应时间从1 h增至3.5 h,ZnAgInS2QDs的发射峰从587 nm蓝移至550 nm,荧光强度上升了42%.反应时间延长,反应进行得更完全,量子点内部无辐射跃迁逐渐减少,越来越多Zn2+成功掺杂.故选择3.5 h为最佳反应时间.考察温度因素时发现,随着温度的升高,荧光强度逐渐增强,由于高温导致S2-释放加快,ZnAgInS2QDs的生长速率加快,晶体表面缺陷逐渐减小[15].当反应温度大于190 ℃时,量子点荧光强度下降,随着温度的升高,NAC分解,量子点表面配体被破坏,故选择190 ℃为最佳反应温度.在最佳合成条件下,测得其量子产率为10.63%.
2.2 ZnAgInS2 QDs的表征
2.2.1 红外荧光光谱表征结果
运用红外光谱对量子点表面基团进行表征,图6为在4000~500 cm-1范围内扫描的ZnAgInS2QDs的红外谱图.图6中位于644 cm-1处的峰位为C—S键,位于1398 cm-1处的峰为CH2的面外振动,位于1576 cm-1处的峰为—COO—振动,位于2935 cm-1处的峰为CH2反对称伸缩振动,位于3442 cm-1位置的峰为 O—H键伸缩振动.

图6 ZnAgInS2 QDs的IR谱图Fig.6 IR spectra of ZnAgInS2 QDs
2.2.2 EDS和TEM表征结果
EDS是评价材料元素组成的一种手段.采用EDS对所制备的ZnAgInS2QDs进行表征,其结果证实了Zn,Ag,In,S 4种主要元素的存在,其中Zn,Ag,In,S所占摩尔比依次为17.90%,0.96%,3.03%,14.80%,可见Zn成功掺杂进量子点中.制备的量子点形貌的TEM表征结果见图7,图中ZnAgInS2四元量子点具有较清晰的椭球形轮廓,粒径分布较为均一,大约为3 nm.

图7 ZnAgInS2 QDs的TEM图像Fig.7 TEM image of ZnAgInS2 QDs
2.2.3 pH值和盐度对ZnAgInS2QDs荧光强度的影响
为评价所制备量子点的稳定性,分别考察了pH值和离子强度对其荧光强度的影响,结果见图8.由图8可见:pH为7~12时,量子点表现出良好的稳定性,由于在弱酸性到中性时,特别是碱性条件下,NAC的羧酸基团处于去质子化状态,使量子点的表面带负电荷相互排斥,防止聚集,使其更加稳定,荧光增强.而在强酸性溶液中,量子点的荧光强度极剧降低,配体NAC部分巯基发生质子化反应,导致配体从量子点表面脱落,荧光强度降低.这表明在生理条件下,量子点基本能保持强而稳定的荧光性能.
考察ZnAgInS2QDs在不同浓度(0~0.5 mol·L-1) NaCl下的荧光强度发现:ZnAgInS2QDs的荧光强度基本不受环境离子强度的影响,在不同浓度的NaCl溶液中,量子点均具有强且稳定的荧光.这说明所制备的ZnAgInS2QDs具有良好的抗盐性.

图8 pH值对ZnAgInS2 QDs的荧光强度的影响Fig.8 pH effects on fluorescence intensity of ZnAgInS2 QDs
2.3 铜离子的检测
2.3.1 不同pH值下的荧光猝灭情况
Cu2+可以通过电子转移作用,高效地猝灭ZnAgInS2QDs的荧光.为了进一步优化检测条件,考察了pH值分别为6,7.8,9,10,11时Cu2+(1.5 μmol·L-1)对ZnAgInS2QDs荧光的猝灭情况.结果表明:pH值为7.8时,Cu2+对ZnAgInS2QDs的荧光猝灭强度最大,荧光强度下降了84.5%,故选择pH值为7.8的缓冲溶液作为后续Cu2+的检测环境.
2.3.2 Cu2+的检测
加入不同浓度的Cu2+可引起ZnAgInS2QDs荧光不同程度的猝灭,结果如图9所示.图9中随着Cu2+浓度的增加,量子点荧光强度逐渐下降,且荧光光谱发生位移和形状改变.在0.15~1.5 μmol·L-1范围内,Cu2+浓度与ZnAgInS2QDs荧光强度呈线性关系,符合Stern-Volmer方程(见图9内插图),即I0/I=0.90859+1.93011c,其中I0和I是初始荧光强度和加入Cu2+后的量子点荧光强度,c是Cu2+的浓度,R2为0.99628.

图9 不同浓度Cu2+对ZnAgInS2 QDs荧光强度的影响Fig.9 Effect of Cu2+ with different concentration on fluorescence intensity of ZnAgInS2 QDs
2.3.3 金属离子对ZnAgInS2QDs荧光猝灭程度的影响
为了验证实验的选择性和实际应用价值,考察了Hg2+,Cd2+等常见金属离子对该检测体系的影响,结果如图10所示.如图10所示:K+,Ca2+的浓度为100倍Cu2+浓度时仍对测定结果无影响.Cu2+,Cd2+,Fe3+,Hg2+浓度均为1μmol·L-1时,Cu2+产生的猝灭作用远远大于其他金属离子,这是由于除了电子转移作用,ZnAgInS2QDs表面配体NAC上的氮和氧
存在孤对电子,可与Cu2+配位形成金属络合物,使溶液中量子点团聚,发生荧光猝灭作用,表明本体系具有良好的选择性.

图10 金属离子对ZnAgInS2 QDs荧光强度的影响Fig.10 Effects of different metal ions on fluorescence intensity of ZnAgInS2 QDs
2.3.4 加样回收实验
为检验该方法在实际样品检测中的应用价值,固定其他条件不变,配制3种不同Cu2+浓度的混合溶液(浓度在检测范围内).取各混合待测液分别进行3次平行实验,检测结果如表1所示.由表1可见,该方法测定值与实际值基本吻合,结果令人满意.

表1 合成样品的检测结果
3 结语
采用水热法优化各合成条件,获得了性能优良的ZnAgInS2QDs,其最佳合成条件为r[Zn(Ac)2∶In(Ac)2∶AgNO3∶Na2S∶NAC] = 0.2∶1∶0.25∶1.8∶9,pH=9.5,θ=190 ℃,t=3.5 h.所制备的量子点还具有良好的抗盐性并在pH值为7~12具有强而稳定的荧光.以ZnAgInS2QDs为荧光探针,在pH值为7.8的条件下,可实现对铜离子的选择性检测,其线性范围是0.15~1.5 μmol/L,线性相关系数R2为0.99628,该检测体系具有良好的抗干扰能力,拓展了Cu2+的检测手段,为新型ZnAgInS2QDs应用于生化检测中提供了实验基础.
参 考 文 献
[1] Chang Y,Sun D,Zhang Z,et al. High color-rendering-index hybrid whiteLEDs employing CdSe/ZnS core/shell quantum dots[J]. J Nanosci Nanotechnol,2016,16(1): 670-676.
[2] 赵 丹,李娇甜,杨天鸣,等. L-半胱氨酸修饰的水溶性掺杂型CdZnTe量子点的水热法制备和表征[J]. 中南民族大学学报(自然科学版),2013,32(3): 50-53.
[3] Cheng X,Lowe S B,Reece P J,et al. Colloidal silicon quantum dots: from preparation to the modification of self-assembled monolayers (SAMs) for bio-applications[J]. Chem Soc Rev,2014,43(8): 2680-2700.
[4] Wang M,Liu X,Cao C,et al. Synthesis of band-gap tunable Cu-In-S ternary nanocrystals in aqueous solution[J]. Rsc Advances,2012,2(7): 2666-2670.
[5] Regulacio M D,Win K Y,Lo S L,et al. Aqueous synthesis of highly luminescent AgInS2-ZnS quantum dots and their biological applications[J]. Nanoscale,2013,5(6): 2322-2327.
[6] Xiong W W,Yang G H,Wu X C,et al. Aqueous Synthesis of Color-Tunable CuInS2/ZnS Nanocrystals for the Detection of Human Interleukin 6[J]. ACS Appl Materi Interfaces,2013,5(16): 8210-8216.
[7] Deng D,Qu L,Cheng Z,et al. Highly luminescent water-soluble quaternary Zn-Ag-In-S quantum dots and their unique precursor S/In ratio-dependent spectral shifts[J]. J Lumin,2014,146(1): 364-370.
[8] Deng D,Cao J,Qu L,et al. Highly luminescent water-soluble quaternary Zn-Ag-In-S quantum dots for tumor cell-targeted imaging[J]. Phys Chem Chem Phys,2013,15(14): 5078-5083.
[9] Wang J,Zhang R,Bao F,et al. Water-soluble Zn-Ag-In-Se quantum dots with bright and widely tunable emission for biomedical optical imaging[J]. Rsc Advances,2015,5(108): 88583-88589.
[10] Wang J,Zhou X,Ma H,et al. Diethyldithiocarbamate functionalized CdSe/CdS quantum dots as a fluorescent probe for copper ion detection[J]. Spectrochimica Acta A,2011,81(1): 178-183.
[11] Lu X,Zhao Y,Zhang J,et al. Copper ion-induced fluorescence band shift of CdTe quantum dots: a highly specific strategy for visual detection of Cu2+with a portable UV lamp[J]. Analyst,2015,140(23): 7859-7863.
[12] Sun X,Liu P,Wu L,et al. Graphene-quantum-dots-based ratiometric fluorescent probe for visual detection of copper ion[J]. Analyst,2015,140(19): 6742-6747.
[13] 冷泽山. 新型铜铟硫基多色量子点的制备及其性能研究[D]. 武汉:华中农业大学,2014.
