导电凝胶型全固态Ag/AgCl参比电极的制备及性能
2018-06-22尹娜娜李明谦李玉莹赫春香
尹娜娜 李明谦 代 鑫 李玉莹 赫春香
(辽宁师范大学 化学化工学院,辽宁 大连 116029)
前言

1 实验部分
1.1 仪器与试剂
pHS-3C型数字酸度计(上海雷磁仪器厂);饱和甘汞电极为参比电极;pH 玻璃电极;氯离子选择性电极;15B+万用表(美国FLUKE公司);CL-200型恒温加热磁力搅拌器(巩义市英峪予华仪器厂);DKB-501A型超级恒温水槽(上海精宏实验设备有限公司)。
石墨粉(光谱纯,中国医药集团上海化学试剂公司);其余常规试剂均为分析纯;pH2.00~10.00的系列磷酸盐缓冲溶液(PBS)由H3PO4(0.2 mol/L)、NaH2PO4(0.2 mol/L)、Na2HPO4(0.2 mol/L)、Na3PO4(0.2 mol/L)在酸度计监测下配制而成;全部实验用水为石英亚沸二次蒸馏水。
1.2 实验方法
1.2.1Ag丝的预处理
将Ag丝放入HNO3溶液(1+1)中反复清洗几次,将银丝表面氧化层溶解直至乌白色,备用。
1.2.2全固态Ag/AgCl参比电极封口胶的制备
根据聚四氟乙烯管口的大小,向适量的环氧树脂中混合适量的石墨粉,滴入少量的乙二胺作固化剂,充分混合后即制得封口导电胶,待用。
1.2.3导电凝胶型全固态Ag/AgCl参比电极的制备
将0.300 0 g聚乙烯醇加入到10 mL 蒸馏水中,加热至微沸,搅拌使之完全溶解,此为1#溶液。将0.600 0 g琼脂粉分别加入到微沸的10 mL 1.000、3.000 mol/L和饱和 KCl溶液中,搅拌使琼脂粉完全溶解,此为2#溶液。将1#和2#热溶液混合均匀,最后搅拌下加入含有0.250 0 g AgNO3的 3 mL水溶液,混合均匀后加热,使水分蒸发得到糊状物,趁热将糊状物压入洁净的聚四氟乙烯管中,插入洁净Ag丝,导电胶封口,放置24 h即制得固态Ag/AgCl参比电极,其标准电位值由KCl的浓度确定。
2 结果与讨论
2.1 全固态Ag/AgCl参比电极制备条件的优化
本参比电极制作的关键是含有AgCl的全固态导电凝胶的制备。制作的技术指标是含有Ag/AgCl电对、电极电位稳定、固态电解质电阻小、冷热稳定性好、不污染待测液。
琼脂盐桥是经典的导电介质。本实验参照李人宇等[10]制作琼脂盐桥的实验方法,他们将琼脂粉、氯化钾和蒸馏水的质量比控制为3∶30∶100。按此方法,本实验在20 mL饱和KCl溶液中加入0.6 g琼脂粉,加热使之完全溶解。但是我们在实验中发现:这样的琼脂盐桥含水量大,易干涸,导致断路,所以一般只能使用一周左右。聚乙烯醇(PVA)具有形成导电凝胶的特性,因此,本实验试图以PVA改善琼脂盐桥的物理特性,延长其使用寿命。试验了PVA的用量,最后确定将0.300 0 g PVA溶于10 mL热水中,与10 mL 含有饱和KCl的琼脂热溶液混合,制得的凝胶理化性能最好。AgCl 是通过向上述琼脂-PVA-KCl 混合溶液中加入AgNO3而产生的。为保持Ag/AgCl电对电极电位的准确性和稳定性,在凝胶中形成的AgCl应该均匀包裹在Ag丝表面,且没有游离的Ag+。试验了AgNO3的用量对ASRE电极电位的影响:在20 mL 琼脂-PVA-KCl热溶液中,分别加入溶有0、0.005 0、0.010 0、0.100 0、0.200 0、0.250 0 g AgNO3的 3.00 mL 水溶液,搅拌均匀,加热至糊状物,由其组成ASRE。电极电位的测定方法如下:以ASRE与SCE分别连接酸度计的正极和负极,两电极置于KNO3溶液(1 mol/L)中,测定电池电动势(ΔE),实验结果表明:当加入AgNO3的量小于0.100 0 g时,ΔE随AgNO3的增多而减小,当加入AgNO3的量在0.100 0~0.250 0 g时,ΔE在44~46 mV。为了使Ag丝表面充分包裹AgCl,选择加入0.250 0 g 硝酸银。ASRE结构如图1所示。

图1 S-F-Ag/AgCl 结构示意图Figure 1 Structure diagrams of S-F-Ag/AgCl.
2.2 导电凝胶型全固态Ag/AgCl 的理化性能
2.2.1聚乙烯醇对KCl-琼脂凝胶导电性的影响
按实验方法配制一份仅含有KCl-PVA-琼脂的导电凝胶液,相应地配制一份不含聚乙烯醇的凝胶液,将两份溶液分别倒入圆柱形模具中(Φ25 mm×17 mm),等待24 h,水分完全蒸发,形成了固态凝胶。将固态凝胶从模具中取出,用万用表测定凝胶圆柱最大直径之间的电阻,在不同方向上平行测定3次,求平均值。实验显示,掺杂PVA前后KCl-琼脂凝胶的电阻值均约为125 Ω,说明PVA的加入基本不影响KCl-琼脂凝胶的导电性。
2.2.2聚乙烯醇的掺杂对KCl-琼脂凝胶抗变形性的影响
为了表征PVA改善琼脂凝胶易断裂的性能,我们按如下方法测试:将两份0.600 0 g琼脂粉分别溶于10 mL热水中,然后向一份溶液中加入10 mL蒸馏水,另一份中加入10 mL含有0.300 0 g的PVA热溶液,混合均匀后趁热将混合液铺平在玻璃板上(20 mm×60 mm,厚度约为2 mm),放置18 h使水分完全蒸发,在玻璃板观察到一层透明的薄膜。将薄膜揭起,用长尾票夹夹在薄膜两头,用透明胶带加固,将夹子的一头固定于钉上,使薄膜自然下垂,在下面的挂钩上逐渐加载砝码(图2),直至KCl-琼脂凝胶薄膜破裂,期待依据悬挂砝码的质量来比较两种薄膜的韧性。结果是加与不加PVA的薄膜至断裂瞬间分别加载了195 g和500 g 砝码,表明PVA的掺杂极大地提高了凝胶的抗裂性能。

图2 抗拉力实验装置示意图Figure 2 Experimental set-up of pull.
2.2.3氯化钾浓度对全固态Ag/AgCl参比电极标准电极电位的影响
按实验方法所述,分别用1.000、3.000 mol/L 以及饱和KCl制作凝胶,构成三支不同的参比电极,在室温下分别将其放置于对应浓度的KCl溶液中活化30 min,然后与SCE构成电极组,置于KNO3溶液(1.000 mol/L)中,测定电动势,结果分别为41、43和45 mV。实验结果表明:以不同浓度KCl制得的ASRE电位值稍有差异,几乎可以忽略不计。原因可能是由于在制得糊状物时水分不断蒸发,使得游离态的无机盐离子过饱和而析出,因此其糊状物中的Cl-分布趋于一致,使得电极电位值相差甚小。
2.2.4封口胶的导电性及对固态导电凝胶中氯离子的防渗性能
传统的参比电极在应用于Cl-的直接电位法测定时,需要用双盐桥隔离SCE与待测溶液。由固态导电凝胶构成的全固态参比电极应该具有耐冲击、反渗漏性能。为达到此性能,本ASRE采用由碳粉与环氧树脂混合而成的导电碳糊封住电极口,然后考察了ASRE中KCl的溶出情况。实验方法如下:在室温下,将氯离子选择性电极与双盐桥SCE放置于NaCl 溶液(1.000×10-5mol/L)中,测其ΔE。然后将ASRE浸在该NaCl溶液中,测定在 40 min 时间内不同时刻该溶液的ΔE,结果列于表1。实验结果显示,前5 min时间内,电极电位变化了5 mV;在5~25 min 之间时,电极电位有微小变化,25 min 之后基本稳定。分析原因,封口胶是环氧树脂与碳粉的混合物,比例适当时既有隔离作用又有微孔渗透作用,相当于饱和甘汞电极的微孔陶瓷芯。为了证明这种性能,我们做了如下实验:用万用表测定封口胶最大直径两点间的电阻,实验显示电阻为无穷大,表明干燥的封口胶不导电;但是我们将ASRE浸泡到KNO3溶液(1.0 mol/L)中,将万用表的两根接线柱一根插入溶液中,另一根与电极的导线相连,测得电阻为146 Ω,表明封口胶具有导电性。这种导电性应该是由分散在环氧树脂中的碳粉间隙因容纳微量的电解质溶液而产生的。这种微孔透过的微量水溶液也导致了电极内部KCl的微弱溶解。25 min后在含有AgCl的导电凝胶内部达到了溶解平衡,溶液中Cl-的浓度不再发生变化。这提示我们:使用前,应将ASRE浸泡在KCl溶液中活化30 min,使其电极电位达到稳定值。

表1 氯离子渗透对电池电动势的影响Table 1 The inflenence of Cl- permeate on electromotive force
2.2.5全固态Ag/AgCl参比电极的准确性
分别将自制全固态参比电极应用于pH2.00~12.00的磷酸盐缓冲溶液(PBS)的pH值 及NaCl标准溶液(1.000×10-5~1.000×10-1mol/L)中Cl-浓度的测定,并将测定结果与相对于SCE的测定结果进行对比,以相对误差表示测定结果的准确度。测定结果分别用图3和图4表示。图3表明:11份PBS测定结果的相对误差为 -0.8%~0.8%;图4表明:NaCl溶液的浓度 -lgc(Cl-)与ΔE呈线性关系,斜率为 -49.3,与SCE作参比电极时的斜率(-49.9)基本一致,仅存在47 mV的截距,表明,ASRE可以替代双盐桥参比电极准确测定Cl-的浓度。
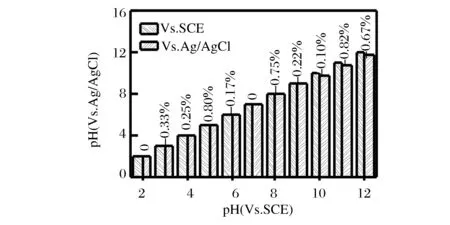
图3 pH测定结果比较(图中数据为相对误差%)Figure 3 Compare for pH detection between Aii-State-Ag/AgCl and SCE (Datas in figture were relative error).

图4 Cl-测定结果比较Figure 4 Compare for Cl- detection.
2.2.6全固态Ag/AgCl参比电极的稳定性及重现性
在室温下,将固态Ag/AgCl参比电极在饱和氯化钾溶液中活化30 min,再将其与SCE组成电极组,分别置于KNO3(1 mol/L)、饱和KCl、pH=2.00、pH=7.00、pH=10.00的PBS中,连续24 h观察ΔE。结果表明,在不同介质溶液中ΔE稳定在45~47 mV,漂移很小,说明ASRE的稳定性和重现性良好。
2.2.7温度对全固态Ag/AgCl参比电极电位的影响
以ASRE和SCE构成电极组,置于由超级恒温器控制温度的KNO3溶液(1 mol/L)中,以10 ℃位间隔,记录10~80 ℃时的ΔE,结果如图5表示。对ΔE与T进行线性回归处理,得到温度系数为0.123 mV/℃,表明温度的改变对两电极间的电位差改变很小,说明ASRE的稳定性非常强。
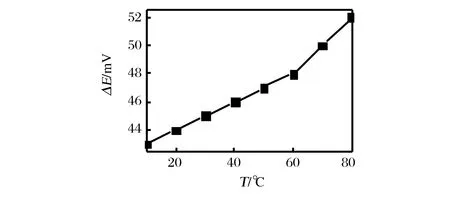
图5 温度对全固态Ag/AgCl参比电极电位值的影响Figure 5 The influence of temperature on E of Ag/AgCl.
2.2.8固态Ag/AgCl参比电极的可逆性
以ASRE为工作电极,SCE为参比电极,Pt丝为对极,在KNO3溶液(1 mol/L)中进行循环伏安扫描。扫描电位从 -0.500 0~+0.500 0 V,扫描速度为0.100 0 V/s,循环次数为10,测得循环伏安曲线如图6所示。由图6可知,除第一圈略有差异以外,第二圈到第十圈ASRE的正向扫描和反向扫描的循环伏安曲线几乎完全重合,表明该电极具有优良的可逆性。

图6 固态Ag/AgCl参比电极循环伏安曲线Figure 6 Cyclic voltammetry curve of Ag/AgCl.
3 结论
研制的全固态四合一Ag/AgCl参比电极是对传统电镀法制备Ag/AgCl参比电极的改进,解决了AgCl层容易剥落和双盐桥的问题,制作方法简单,电位值恒定,使用温度范围宽,温度系数小。期望该电极能够运用于各类组合型全固态电化学传感器的制备中。
[1] VONAUA W , OELBNER W , GUTHA U , et al. An all-solid-state reference electrode[J].SensorsandActuatorsB,2010, 144: 368-373.
[2] 卫云鸽, 曹全喜, 雷梦碧, 等. 全固态Ag/AgCl参比电极的制备工艺研究[J]. 功能材料(FunctionMaterials), 2010, 41(增刊):441-444.
[3] GABRIEL V R A, GIAAN A R A, CARLOS ANDRES G V , etal. Composites: A novel alternative to construct solid state Ag/AgCl reference electrodes[J].SensorsandActuatorsB, 2005, 110: 264-270.
[4] 杨百勤,左芳.全固态Ag/AgCl参比电极的制备及性能测试[J]. 陕西科技大学学报(JournalofShanxiUniversityofScience&Technology),2010,28(3):75-77.
[5] 杨渝,李龙,刘红伟,等.全固态裸露式Ag/AgCl 参比电极的研制与应用[J].化学传感器(ChemicalSensors),2011, 31(3):45-48.
[6] 周海晖, 陈范才,张小华,等. Ag/AgCl 固体参比电极的研究[J]. 腐蚀科学与防护技术(CorrosionScienceandProtectionTechnology),2001, 13(4): 234-235.
[7] 文家新, 刘云霞, 张天. 一种Ag/AgCl全固态复合式参比电极的研制[J]. 广州化工(GuangzhouChemicalIndustry),2014,42(2): 47-49.
[8] 杨百勤, 李靖, 杜宝中, 等. 全固态复合碳纤维氧化钨pH传感器的研制及应用[J]. 分析测试学报(JournalofInstrumentalAnalysis), 2008, 27(11): 1229-1232.
[9] 崔建强. 全固态琼脂凝胶体系Ag/AgCl参比电极制备及性能测试[J]. 科技致富向导(GuideofSci-techMagazine), 2013 (15): 48-49.
[10] 李人宇,李咏梅. 物理化学开放性实验室设计—盐桥的制备[J].甘肃科技(GansuScience&Technology),2010,26(17): 208-209.
