保留乳头乳晕乳房切除联合Ⅰ期扩张器植入术的并发症及处理
2018-06-21王学晶张海林周易冬
王学晶 姚 儒 张海林 周易冬 茅 枫 孙 强
(中国医学科学院北京协和医院乳腺外科,北京 100730)
乳腺癌是当今女性最常见的恶性肿瘤之一,严重威胁女性健康。2012年全球新发乳腺癌患者为167万[1]。手术是治疗早期乳腺癌的主要手段,对于不适合保乳的患者,经典的根治性乳房切除术仍是主要术式[2,3]。随着患者对于乳房切除术后的美学要求和生活质量要求的提高,全乳切除后应用假体进行乳房即刻重建已经成为乳腺癌手术的重要组成部分。我院一直积极探索实施并逐步完善保留乳头乳晕复合体(nipple-areola complex,NAC)乳房切除术(nipple-areola complex-sparing mastectomy,NSM)联合乳房延迟即刻重建术。这一术式是行NSM后Ⅰ期于胸大肌后方埋植软组织扩张器,待放化疗完成后,Ⅱ期手术将扩张器取出更换为乳房硅胶假体。Ⅰ期扩张器植入术有效避免术后放疗对假体造成的不良影响,降低直接应用自体组织或假体重建乳房的手术难度,但NAC血供障碍等并发症的出现仍会对后续肿瘤治疗及乳房重建的美学效果产生不利影响。我院2014年1月~2017年2月行80例NSM联合Ⅰ期扩张器植入,其中22例(27.5%)发生术后并发症,报道如下。
1 临床资料与方法
1.1 一般资料
本组22例,年龄27~49岁,中位年龄37岁。肿瘤位于外上象限14例,外下象限6例,内上象限2例。病灶单发17例,2处4例,弥漫性多发1例。肿瘤最大径0.2~4.0 cm(中位数2.1 cm)。均为单侧乳腺癌,其中导管内癌1例,浸润性导管癌或小叶癌21例。TNM分期:0期1例,Ⅰ期8例,Ⅱ期13例(ⅡA 期9例,ⅡB期4例)。
病例选择标准:①病理学诊断为0~ⅢA期女性乳腺癌;②肿瘤最大径≤5 cm;③无保乳意愿或术前应用影像学(超声、钼靶摄片)评估病变未累及乳头乳晕区;④患者同意完成病历资料采集及进行随访;⑤无精神意识疾病,无理解力、记忆力、定向力等认知障碍。
1.2 方法
1.2.1 术前准备 经乳腺外科和整形外科医生共同评估具有施行NSM联合Ⅰ期扩张器植入术指征;根据乳房形态及体积选择适合的扩张器;签署知情同意书。
1.2.2 手术方法 全身麻醉,仰卧位,患侧肩部下方垫一软枕,患侧上肢外展90°并悬吊。根据肿瘤位置选择切口。尽量选择肿瘤侧环乳晕切口,乳晕切口长度以能够顺利切除全部腺体为准,不超过乳晕周径的1/2;如果乳晕较小,乳房体积较大,考虑术中切除乳腺或处理腋窝困难,适当延长切口,常用切口包括肿瘤侧乳晕边缘弧形切口,“Ω”形切口及“Ω”形切口向一侧放射状外延的“镰刀”形切口。对于不适合乳晕周围切口的患者,选择肿瘤表面放射状或弧形切口。通过上述切口完整切除患侧腺体组织,然后通过该切口或另取腋窝切口行前哨淋巴结切除活检或腋窝淋巴结清扫。患侧全乳切除后,沿胸大肌外缘向内侧分离胸大肌后间隙, 外侧切开部分前锯肌并沿其下向外侧分离至腋前线, 胸大肌后间隙内侧游离至胸骨旁,参照对侧乳房下皱襞水平决定游离腔隙的下缘水平,上缘游离范围以铺平扩张器为准,检查扩张器可以成功扩张并无渗漏后,将300~400 ml圆形软组织扩张器平铺置入胸大肌后方间隙中, 注射壶置于腋后线或胸骨前皮下组织层并用周围组织包裹缝合固定;术中向扩张器内注入生理盐水100~200 ml,待扩张器完全展平后,调整好扩张器位置,缝合胸肌外缘和前锯肌,使扩张器被完整包裹。在扩张器旁及皮瓣下各留置细引流管2根。术后引流管保持负压吸引至少3 d,引流液<20 ml/d,拔除引流管。切口加压包扎1周。
2 结果
NAC血运障碍12例,典型表现为术后早期NAC区域表皮坏死发黑(图1),其中单纯环乳晕切口9例,环乳晕边缘延长切口3例,肿瘤表面放射状或弧形切口无NAC血运障碍出现。单纯环乳晕切口1例NAC完全坏死,再次手术切除乳头乳晕,未取出扩张器,愈合良好。余11例NAC血运障碍者,切口及乳头乳晕区域应用溃疡油纱布换药,保持乳头湿润,不做加压包扎,术后3~6周痂下愈合,愈合后均有部分乳头皮肤缺失及皮肤色素脱失。切口感染1例,经清创换药后愈合,并未取出扩张器。1例皮下积液合并感染,手术取出扩张器,经清创换药后好转。发生扩张器相关并发症8例:①扩张器暴露1例,扩张器植入术后9个月、放疗后3个月发现,因该患者扩张体积已与健侧乳房基本相当,采取手术直接取出扩张器更换假体处理;②扩张器上移7例,下缘高于健侧乳房下皱襞,未特殊处理,拟待Ⅱ期更换假体手术时调整位置。22例随访6~12个月,中位随访时间8个月,无复发、转移及死亡。
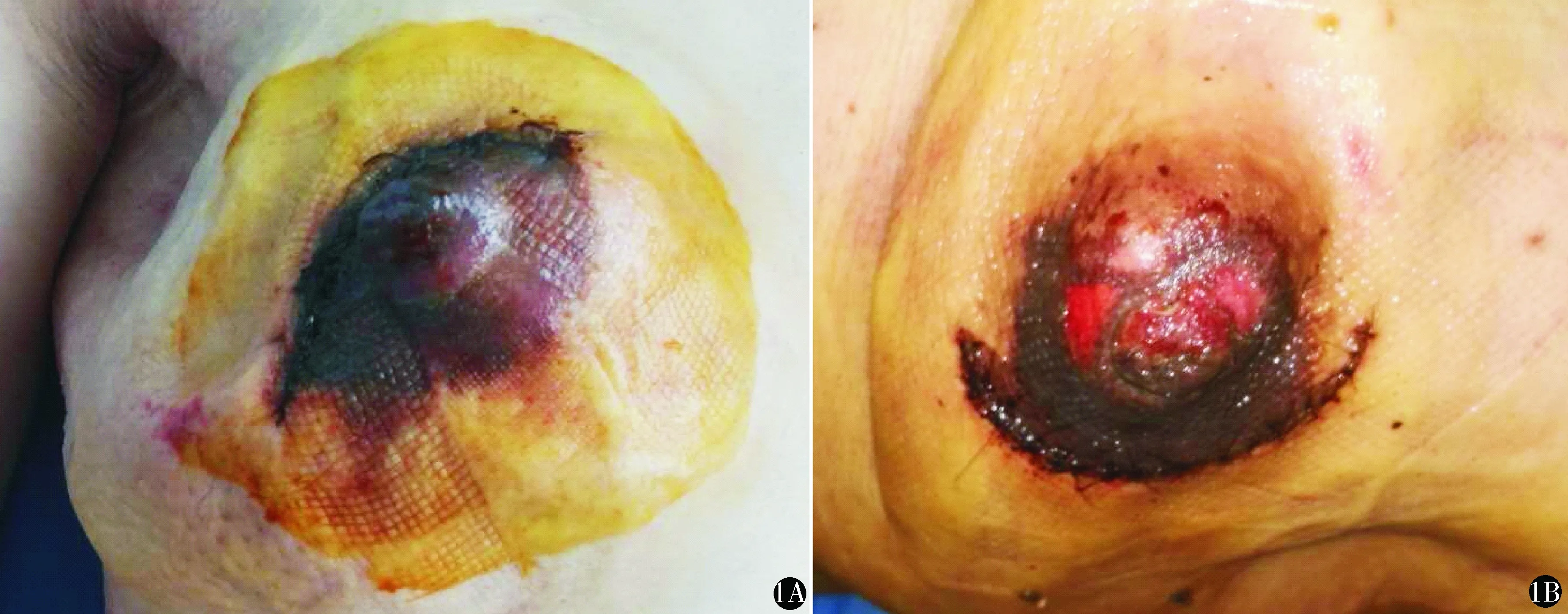
图1 NAC部分坏死典型表现 A.术后8 d;B.术后2周
3 讨论
早期乳腺癌的治疗原则是以手术为主的综合治疗。传统的根治性乳房切除术带来的躯体及心理障碍都会严重影响患者生活质量。近年来,全乳切除术后乳房重建已经成为国内乳腺癌治疗的研究热点。乳房重建手术经历了从皮肤-脂肪移植[4]到假体植入及多种自体组织皮瓣移植的发展过程。目前,美国女性乳腺癌患者的乳房重建率超过40%[5],假体植入占82.7%,是主要的重建方式[6],中国女性乳腺癌患者乳房重建率尚小于5%[7]。中国女性乳腺癌患者的发病年龄[8]、乳房体积等与欧美女性存在差别,因此,探索适合中国女性乳腺癌患者的乳房重建术式非常具有现实意义。
目前,我院将延迟即刻重建术作为乳腺癌患者乳房重建的首选术式[9],优势在于:Ⅰ期手术简化直接植入假体的难度,并减少对患者的副损伤,目的仅为创造Ⅱ期假体植入所需空间,用扩张器替代假体从而有效减少放疗对假体可能产生的不良影响;Ⅱ期手术重点仅在于恢复乳房美学效果,可以再次调整假体位置。这种术式虽然增加手术次数,但是兼顾癌症患者不同时期的主要治疗目标,是一种比较理想的重建方式。是否能够保留自体NAC是影响重建后乳房美学效果的重要因素。在完善评估并保证乳头乳晕下切缘阴性的前提下,NSM并不增加肿瘤复发率而且对预后无不良影响,是一种安全可行的术式[10]。NSM能够保留足够的乳腺皮肤和NAC,将NSM与乳房重建术联合可以保证肿瘤治疗安全性同时获得理想的美学效果。
NSM联合延迟即刻重建较单纯的根治性乳房切除术必然增加手术创伤,减少术后并发症则是手术成功与否的关键。本组并发症主要包括2个方面:①NAC血供障碍、切口愈合不良、皮瓣下感染和积液;②扩张器暴露及移位。
NAC血运障碍是最常见的术后并发症,本组12例,发生率15.0%(12/80)。单纯环乳晕切口患者中,NAC血运障碍的比例为25.0%(9/36),环乳晕边缘延长切口的比例为8.6%(3/35),9例肿瘤表面的非乳晕切口未发生NAC血供障碍,提示单纯的环乳晕切口更容易造成NAC缺血,与Endara等[11]的研究结果一致。Algaithy等[12]报道环乳晕切口的NAC 坏死率高达75%。
有3种原因可能对NAC血供产生影响:①此术式本身的缺陷。NAC的血供来源包括腺体来源的血管及位于乳晕真皮层的毛细血管网。NSM导致来自深部腺体的血供完全中断,只能靠乳晕皮下动脉网供血。乳晕皮下动脉网距乳晕表皮0.3~0.5 cm,术中为保证乳头下肿瘤切缘阴性,过度切除乳头乳晕深部腺体就会损伤这层血管网[13]。②手术不当操作造成的损伤。高温电凝会对乳晕下血管网造成直接损伤;此外,通过乳晕单切口切除全部腺体甚至进行腋窝淋巴结清扫时,由于切口较小过度牵拉操作可进一步对该血管网造成破坏。③术后加压包扎不当。术后早期NAC未与深部组织贴合,处于相对游离状态,无法及时建立新的血供,术后为减少血肿或积液形成,胸壁及腋窝加压包扎,不当包扎尤其是对乳头乳晕区的压迫进一步影响NAC的血供。
为减少NAC的血供障碍的发生,我们在尝试术中术后采取以下措施:①对于乳晕较小的患者,采取环乳晕的变形延长切口或肿瘤表面切口;术中避免对切口及乳头周围组织的过度牵拉,用厚棉垫或凡士林纱布保护乳头。②术中在保证切缘阴性的条件下,至少保留NAC下>0.5 cm厚度组织;尽量减少高温电凝止血且不用电刀游离乳头乳晕下组织,避免高温烧灼破坏皮下血管网。③术中将NAC缝合固定于胸肌筋膜表面,避免其游离移位。④除仔细止血外,术中即向扩张器内注入100~200 ml生理盐水,使其保持对周围组织的一定压力,减少血肿发生。⑤术后仅轻度加压包扎NAC区域外组织,乳头乳晕表面放置一儿童用宽口奶嘴作为保护器,避免乳头乳晕受压,也有利于观察乳头颜色变化,必要时予以及时解除加压包扎。
值得注意的是,虽然NAC血运障碍发生比例较高,本组1例NAC区域完全性坏死,其余NAC血运障碍者虽然也出现NAC表皮坏死发黑的情况,但经局部换药处理后均于痂下愈合,仅出现部分乳头乳晕皮肤缺失和色素脱失。因此,一旦出现血运障碍或出现NAC表面皮肤坏死,不需要急于切除NAC,一般通过切口换药后可以痂下愈合。
术后皮瓣下积液和感染是NSM的另一个常见并发症,Orzalesi等[14]报道发生率3%~8%。本组1例切口感染,经清创换药后愈合,并未取出扩张器;1例感染合并积液后取出扩张器。分析原因:①游离胸肌后间隙导致肌肉组织损伤和渗出增加;②早期扩张器未注水完全,胸肌后间隙有游离腔隙;③扩张器为异物,刺激组织渗出增多;④为减少NAC血供障碍的发生,不能像传统根治术那样将乳腺皮瓣完全加压包扎贴合于胸壁表面。为减少此并发症的发生,除应该注意无菌操作、预防性应用抗菌药物外,我们的经验是:扩张器植入后,即刻注入100~200 ml生理盐水,尽量减小胸肌后间隙及皮瓣下腔隙;止血满意后,于扩张器周围、皮瓣上下缘放置引流管并保持负压,这样既有利于积血和渗出液的引流,也可使皮瓣下及胸肌后间隙内保持负压,有利于组织贴合;术中应尽量避免皮肤切口和植入扩张器的肌肉表面切口相邻,且肌肉后腔隙植入扩张器后应彻底缝合,这样即使皮肤切口感染、愈合不良,也能够最大限度减少感染累及扩张器导致取出的情况发生。
扩张器作为临时假体植入胸肌后间隙,在注水或放疗后也会出现相关并发症,如扩张器破出皮肤、扩张器移位导致双侧下皱襞位置不对称等。本组1例扩张器植入术后3个月已注水基本达到健侧乳房体积,放疗后3个月复查发现扩张器已紧贴皮肤几近突破表皮,局部皮肤菲薄,遂直接行扩张器取出同时行假体植入,术后恢复良好。分析出现这种情况的原因:①放疗损伤导致皮肤弹性减弱,无法承受扩张器持续张力;②患者自身皮下组织和肌肉层较为薄弱,持续压力导致其更加菲薄,无法完整包裹扩张器;③注水时间间隔过短,每次注水量较大超过皮肤软组织扩张能力。结合上述分析,我们给予的处理方法是:①对于皮下组织及肌肉薄弱的患者,术中注意保留较厚的皮下脂肪层,术后减慢注水速度,密切观察皮肤张力和血运情况,少量多次注水;②对于术后需要放疗的患者,可以于放疗前抽出一部分水,以减小皮肤张力,减轻放疗对皮肤的进一步损伤,放疗后,根据皮肤恢复情况,再次注水扩张;③提高随访频率,如果发现皮肤菲薄,扩张器已经接近暴露,可以提前更换扩张器或直接更换假体。本组7例扩张器上移,患侧下皱襞水平高于健侧,分析原因如下:①术中胸肌后腔隙下缘游离不足,上缘游离过高,腔隙范围已经超过扩张器体积,使扩张器有一定游离度;②术后包扎时乳房上下缘压力不均,下缘压力过大导致扩张器上移;③术后早期扩张器周围包膜未完全形成,胸壁肌肉收缩导致扩张器上移。结合上述分析,我们的处理方法是:①Ⅰ期手术中处理胸肌后腔隙下缘时必须游离到达原乳房下皱襞处,根据需要可切开部分胸肌附着点;②胸肌后腔隙上缘不要游离过大,能够保证扩张器平铺即可;③术后早期减少上肢活动,减少扩胸运动导致胸肌收缩。对于已经出现扩张器移位者,不需急于将扩张器取出,Ⅱ期更换假体时调整位置后可取得良好效果。针对上述常见的2种扩张器相关并发症,Hanna等[15]和Chun等[16]术中应用脱细胞真皮基质(acellular dermal matrix,ADM)分别与胸大肌和胸壁缝合,用以包裹扩张器外下极,从而固定扩张器/假体位置及塑造乳房下皱襞形态。但是也有研究[17]提示:ADM的应用对血肿、血清肿的发生有促进作用,并有增加感染率及总并发症发生率的趋势。因此,减少扩张器相关并发症有待通过改善技术来实现。
随着微创外科技术[18]和肿瘤整形外科技术的发展,乳腺癌手术方式逐渐丰富。对于不适合保乳的患者,NSM联合延迟即刻重建术兼顾肿瘤治疗的安全性和女性形态美学,是一种比较理想的术式。外科医生可以通过改进操作技巧及加强术后管理不断优化该术式,使之成为中国女性早期乳腺癌患者手术治疗的重要组成部分。
1 Ferlay J, Soerjomataram I, Dikshit R, et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer,2015,136(5):E359-E386.
2 Lucas DJ, Sabino J, Shriver CD, et al. Doing more: trends in breast cancer surgery, 2005 to 2011.Am Surg,2015,81(1):74-80.
3 Albornoz CR, Matros E, Lee CN, et al. Bilateral mastectomy versus breast-conserving surgery for early-stage breast cancer: the role of breast reconstruction. Plast Reconstr Surg,2015,135(6):1518-1526.
4 Berson MI. Derma-fat-fascia transplants used in building up the breasts. Surgery,1944,15(3):451-456.
5 Morrow M, Li Y, Alderman AK, et al. Access to breast reconstruction after mastectomy and patient perspectives on reconstruction decision making. JAMA Surg,2014,149(10):1015-1021.
6 Gurunluoglu R, Gurunluoglu A, Williams SA, et al. Current trends in breast reconstruction: survey of American Society of Plastic Surgeons 2010. Ann Plast Surg,2013,70(1):103-110.
7 陈 颖,陈嘉健,陈嘉莹,等.中国乳腺癌术后乳房重建现况调查报告.中华肿瘤杂志,2014,36(11):851-857.
8 Li J, Zhang BN, Fan JH, et al. A Nation-wide multicenter 10-year (1999-2008) retrospective clinical epidemiological study of female breast cancer in china.BMC Cancer,2011,11:364.
9 龙 笑,刘志飞,王晓军,等.乳腺癌术后即刻乳房再造治疗流程及其疗效.协和医学杂志,2011,12(11):65-69.
10 Headon HL, Kasem A, Mokbel K. The oncological safety of nipple-sparing mastectomy: a systematic review of the literature with a pooled analysis of 12,358 procedures. Arch Plast Surg,2016,43(4):328-338.
11 Endara M, Chen D, Verma K, et al. Breast reconstruction following nipple-sparing mastectomy: a systematic review of the literature with pooled analysis. Plast Reconstr Surg,2013,132(5):1043-1054.
12 Algaithy ZK, Petit JY, Lohsiriwat V, et al. Nipple sparing mastectomy: can we predict the factors predisposing tonecrosis? Eur J Surg Oncol,2012,38(2):125-129.
13 高德宗,孙靖中,尹群生,等.女性乳房手术预防乳头乳晕坏死的血供研究.中国普通外科杂志,2005,14(4):269-272.
14 Orzalesi L, Casella D, Santi C, et al. Nipple sparing mastectomy: Surgical and oncological outcomes from a national multicentric registry with 913 patients (1006 cases) over a six-year period. Breast,2016,25:75-81.
15 Hanna KR, DeGeorge BR Jr, Mericli AF, et al. Comparison study of two types of expander-based breast reconstruction: a cellular dermalmatrix-assisted versus total submuscular placement. Ann Plast Surg,2013,70(1):10-15.
16 Chun YS, Verma K, Rosen H, et al. Implant-based breast reconstruction using acellular dermal matrix and the risk of postoperative complications. Plast Reconstr Surg,2010,125(2):429-436.
17 董 洁,吴小蔚,田方兴.脱细胞真皮基质对扩张器/假体乳房再造并发症影响的Meta分析.中华整形外科杂志,2013,29(5):356-361.
18 骆成玉.微创时代的乳腺外科——理想与现实的抉择.中国微创外科杂志,2014,14(2):97-101.
