一种便携式无活细胞表达的生物合成新技术及其应用
2018-06-13蔡小玲哈小琴杨波徐倩曾通旭
蔡小玲,哈小琴,杨波,徐倩,曾通旭
一种便携式无活细胞表达的生物合成新技术及其应用
蔡小玲,哈小琴,杨波,徐倩,曾通旭
730050 兰州总医院检验科(蔡小玲、哈小琴、杨波、徐倩、曾通旭);730050 兰州,甘肃省干细胞与基因药物重点实验室(蔡小玲、杨波、徐倩、曾通旭)
1 生物合成新技术概述
合成生物学将工程设计原则合理地应用于分子生物学、新的基因装置设计,在疾病的诊断和治疗的领域发挥作用[1],如,创建全细胞生物传感器[2],基因修饰益生菌[3]以及细胞生物分子加工厂。源自基因工程的生产细胞系基础上,生物合成已成为药品生产[4]、蛋白质疗法[5]、燃料及其他产品[6]的主流技术。然而介导细胞宿主遗传基因进行生物合成,要伴随生物安全、实际障碍、特殊性实验室限制技术的问题,并且疫苗和其他蛋白质的生产需要稳定的冷链配送,但配送成本高,也影响了偏远地区对药物制品的应用。
鉴于上述问题,一种使用冻干、无细胞(freeze drying-cell free,FD-CF)表达系统的安全基因编码工具的生物合成新技术方法产生了,其具有避免冷链运送、降低运送成本等优点[7]。该表达系统不仅保留了活细胞的基本蛋白质合成能力,而且还是无活性、无菌和便携式的平台,该平台有望成为一种新的低成本诊断工具[8]。FD-CF 系统在室温下保持长期(> 1 年)活性,操作简便,可以减少活细胞的生物合成并不受冷链配送要求的限制[9],也可用生物合成方法合成一些便携式药物,治疗性蛋白质和其他生物分子。这充分地支持了按需以及就地生物制造的发展趋势[10-11]。简要步骤是将缓冲液、细胞活性物质和模板分子制成一个冻干反应颗粒,需要时只需要添加水激活,1 ~ 2 个小时即可得到目的产品,不需要特殊的设备和技术,如图 1 所示。
该生物技术可应用于全球健康和个性化医疗,使得大部分分子合成都可以通过冻干试剂和 DNA 编码生物合成来实现。这些直径在几微米的颗粒可轻松地被航天员、士兵或前往偏远地区的医疗工作者携带。它是一种模块化系统,能够经编程后在现场制造所需要的目的蛋白,有上百个不同的 DNA 颗粒可供选择,这些颗粒含有从细胞中提取出的几十种酶和其他分子,能够在室温下保存更长时间,一旦加入水和冻存的 DNA,便开始产生DNA 编码的目的蛋白。
2 生物合成新技术特点
2.1 便携
FD-CF 生物系统新技术是一种便携式生物制造平台,只需加入水并在常温孵化就可以激活生物反应,用来产生多种蛋白质,包括抗菌肽、疫苗、抗体等生物制剂,通过改善集中生产的不足能满足更多的需求。事实上,最近的研究报告表明,以分散的药品生产替代中心化的药物生产有着全球化的需要。此外,FD-CF 生物系统可以扩展到一系列复杂的应用中去,以满足按需治疗,并且是治疗产品分散化生产的可行性选择。
2.2 快速
FD-CF 生物系统新技术非常适用于快速生物合成,在无活细胞表达系统中,表达参数以及 DNA 编码的按需产物可以迅速地被筛选和制造。对于快速、低成本开发和在健康危机时的配送和治疗很重要[12]。
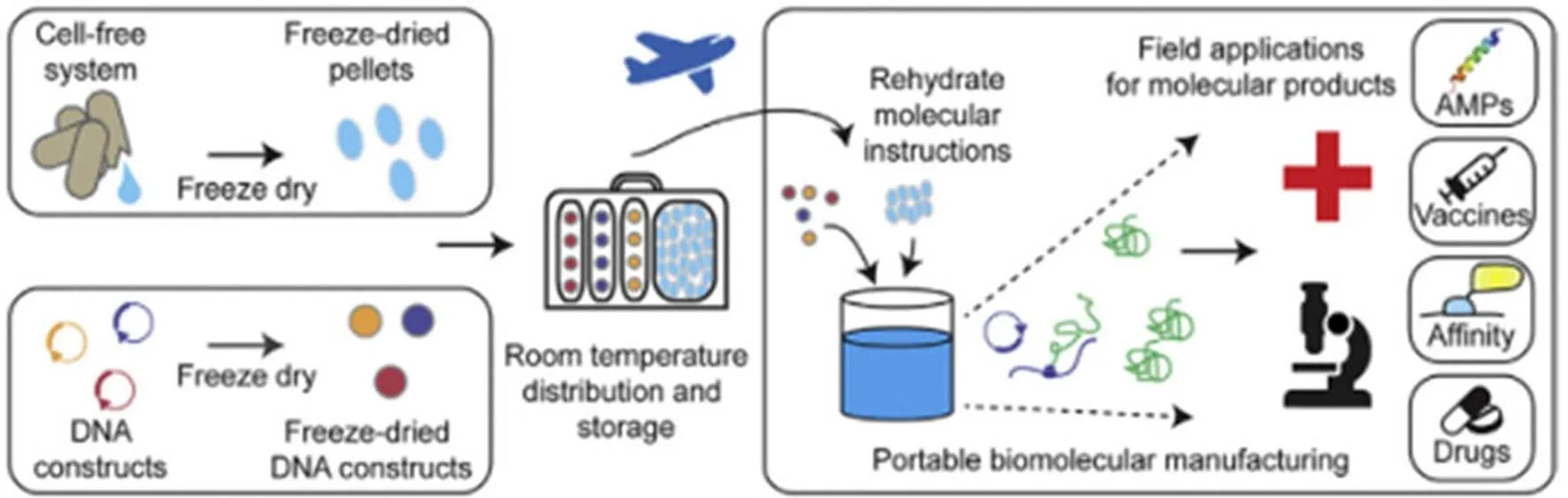
图 1 便携式生物制造平台[1]
生物分子产品对冷链配送和保存的需求增加了其成本,严重影响配送到较远或资源贫乏地区[13-14]。而该新技术在使用之前,FD-CF 试剂和编码 DNA 是互相分开的,这使其有了灵活的制造能力可以紧急应对治疗需要。在应用之前建立一个预混的或单独的分子程序,编码一个虚拟药房,需要时只需水化就可以快速制造。这个概念为疾病爆发时大批生物合成和疫苗配送提供了方法[15]。例如,当发现小批量的流行性感冒病毒亚单位疫苗的有效性变低时,可以迅速重新生产[16-18],传统的疫苗生产很难实现这一点[19-20]。
2.3 经济
疫苗在运输过程中冷链配送费用可以占到疫苗生产成本除外的 80%[21],使用 FD-CF 生物系统新技术的核心益处是可以在常温下运输治疗产品。同时,世界卫生组织和联合国儿童基金会估计在发展中国家疫苗损耗高达 50%,这个问题可通过FD-CF 生物系统按需生产解决,从而减少损失[22-23]。
3 生物合成新技术应用
3.1 抗菌肽
抗菌肽是一类多元化的有潜力的多肽类,它可以作为防御分子通过保护细胞和细胞内的成分抗感染。据非冻干表达的文献报道[24-25],通过FD-CF 表达形式生产的抗菌肽可以替代使用经典的抗生素。
3.2 便携疫苗的生产
疫苗是在儿童时期预防疾病的强有力的工具之一,然而运送到偏远地区具有成本和冷链的要求。有研究者尝试使用 FD-CF 系统进行生物合成疫苗[26-27]。
3.3 按需的组合抗体类似物
抗体类似物如 DARPins 和纳米抗体是强有力的治疗药物,但其生产成本高和冷藏需要限制了产品的配送和效用。因此,通过 FD-CF 生物系统合成 DARPins 和纳米抗体亲和分子方面有重大的意义[28-29]。
基因药物在使用之前往往是液体状态,这不利于药效的稳定,也是储存和运输的一个障碍。因此,改变这种液体状态可以增加其稳定性和简化运输的过程。而“冻干”是长时间保持不稳定分子和无菌条件下储存的良好选择,这有助于疾病的治疗,在基因药物治疗上开辟了新领域。未来发展中,新技术将可以实现现场 DNA 合成,如战争或太空等条件下,可使患者得到高效诊断和治疗,并且生物指导的电子传输可以在现场实现。FD-CF 系统提供了一个新的生物制造的方法,是合成生物学的进一步创新,这种冻存的不含细胞的生物制造平台能够按需合成治疗药物、疫苗、生物化学试剂等,同时展现出一种不需要冷链供应的未来。通过将工厂生产移到第一线,我们可能会得到目前不可能获得的药物,有益于全球健康的改变。但是,该新技术的普及还需大量的实验研究证明,还待进一步的验证确认。
[1] Pardee K, Slomovic S, Nguyen PQ, et al. Portable, on-demand biomolecular manufacturing. Cell, 2016, 167(9):248-259.
[2] Kobayash H, Kaern M, Araki M, et al. Programmable cells: interfacing natural and engineered gene networks. Proc Natl Acad Sci U S A, 2014, 101(11):8414-8419.
[3] Danino T, Prindle A, Kwong GA, et al. Programmable probiotics for detection of cancer in urine. Sci Transl Med, 2015, 7(289):289ra84.
[4] Caschera F. Bacterial cell-free expression technology to in vitro systems engineering and optimization. Synth Syst Biotechnol, 2017, 2(2):97-104.
[5] Moore SJ, MacDonald JT, Freemont PS. Cell-free synthetic biology for in vitro prototype engineering. Biochem Soc Trans, 2017, 45(3): 785-791.
[6] Chubukov V, Mukhopadhyay A, Petzold CJ, et al. Synthetic and systems biology for microbial production of commodity chemicals. NPJ Syst Biol Appl, 2016, 2:16009.
[7] Pardee K, Green A, Ferrante T, et al. Paper-based synthetic gene networks. Cell, 2014, 159(6):940-954.
[8] Adamo A, Beingessner RL, Behnam M, et al. On-demand continuous-flow production of pharmaceuticals in a compact, reconfigurable system. Science, 2016, 352(9):61-67.
[9] Perez-Pinera P, Han N, Cleto S, et al. Synthetic biology and microbioreactor platforms for programmable production of biologics at the point-of-care. Nat Commun, 2016, 7:12211.
[10] Salehi AM, Smith MT, Bennett AM, et al. Cell-free protein synthesis of a cytotoxic cancer therapeutic: Onconase production and a just-add-water cell-free system. Biotechnol Cell, 2016, 11(9):274-281.
[11] Lu Y. Cell-free synthetic biology: Engineering in an open world. Synth Syst Biotechnol, 2017, 2(1):23-27.
[12] Sharma SV, Tong X, Pubill-Ulldemolins C, et al. Living geno chemetics by hyphenating synthetic biology and synthetic chemistry in vivo. Nat Commun, 2017, 8(1):229.
[13] Kanojia G, Have R, Soema PC, et al. Developments in the formulation and delivery of spray dried vaccines. Hum Vaccin Immunother, 2017, 13(10):2364-2378.
[14] Menzies NA, Suharlim C, Geng F, et al. The cost determinants of routine infant immunization services: a meta-regression analysis of six country studies. BMC Med, 2017, 15(1):178.
[15] Plotkin S, Robinson JM, Cunningham G, et al. The complexity and cost of vaccine manufacturing - An overview. Vaccine, 2017, 35(33): 4064-4071.
[16] Kempf N, Remes C, Ledesch R, et al. A novel method to evaluate ribosomal performance in cell-free protein synthesis systems. Sci Rep, 2017, 7:46753.
[17] Martemyanov KA, Shirokov VA, Kurnasov OV, et al. Cell-free production of biologically active polypeptides: application to the synthesis of antibacterial peptide cecropin. Protein Expr Purif, 2012, 21(8):456-461.
[18] Palmenberg AC. In vitro synthesis and assembly of picornaviral capsid intermediate structures. J Virol, 2012, 44(11):900-906.
[19] Torgeman A, Ozeri E, Ben David A, et al. Role of homologous Fc fragment in the potency and efficacy of anti-botulinum antibody preparations. Toxins (Basel), 2017, 9(6). pii: E180.
[20] Saeed AF, Wang R, Ling S, et al. Antibody engineering for pursuing a healthier future. Front Microbiol, 2017, 8:495.
[21] Wang RE, Liu T, Wang Y, et al. An immunosuppressive antibody-drugconjugate. J Am Chem Soc, 2015, 137(9):3229-3232.
[22] Ng CT, Jaworski JP, Jayaraman P, et al. Passive neutralizing antibody controls SHIV viremia and enhances B cell responses in infant macaques. Nat Med, 2010, 16(9):1117-1119.
[23] Kontermann RE. Dual targeting strategies with bispecific antibodies. MAbs, 2012, 4(9):182-197.
[24] Lehar SM, Pillow T, Xu M, et al. Novel antibody-antibiotic conjugate eliminates intracellular S. aureus. Nature, 2015, 527(1):323-328.
[25] Patel KG, Ng PP, Levy S, et al. Escherichia coli-based production of a tumor idiotype antibody fragment-tetanus toxin fragment C fusion protein vaccine for B cell lymphoma. Protein Expr Purif, 2015, 75(4): 15-20.
[26] Stech M, Nikolaeva O, Thoring L, et al. Cell-free synthesis of functional antibodies using a coupled in vitro transcription-translation system based on CHO cell lysates. Sci Rep, 2017, 7(1):12030.
[27] Desmyter A, Spinelli S, Roussel A, et al. Camelid nanobodies: killing two birds with one stone. Curr Opin Struct Biol, 2015, 32(9):1-8.
[28] Plückthun A. Designed ankyrin repeat proteins (DARPins): binding proteins for research, diagnostics, and therapy. Annu Rev Pharmacol Toxicol, 2015, 55:489-511.
[29] Bannas P, Hambach J, Koch-Nolte F. Nanobodies and nanobody-based human heavy chain antibodies as anti-tumor therapeutics. Front Immunol, 2017, 8:1603.
哈小琴,Email:haxiaoqin@163.com
2017-11-29
10.3969/j.issn.1673-713X.2018.03.012
