一种苯并咪唑酮类GSK-3抑制剂的纯度研究
2018-06-13陈换飞邹静白兰贾贵清彭婷陈婷吴小愚张梅
陈换飞,邹静,白兰,贾贵清,彭婷,陈婷,吴小愚,张梅
目前,肿瘤作为影响人类健康的世界性难题,一直是医药领域研究的热点和难点。新型安全、高效、副作用小的抗肿瘤药物的研发则显得意义重大。糖原合成酶激酶-3(GSK-3)是一种多功能的丝氨酸苏氨酸类蛋白激酶,当其在体内异常表达时,引发糖尿病、阿尔兹海默症以及直肠癌、胃癌等多种癌症[1,2]。因此,GSK-3已成为抗肿瘤作用研究的热门靶点,其相应的小分子抑制剂研究是抗肿瘤药物研究的热点。
Dibromophakellstatin是从Phakellia mauritiana分离的一种天然产物,其作为新型的抗肿瘤抑制剂,具有苯并咪唑-2-酮支架[3]。近年来相关研究也表明,具有苯并咪唑-2-酮结构的活性化合物,可以作为酯酶抑制剂、抗菌剂等[4-5]。其中如halopemide、UV0155069等作用于不同的肿瘤靶点时均有显著抗肿瘤活性[6-11]。因此,二氢苯并咪唑-2-酮被用作抗肿瘤药物研究领域的新型支架,受到越来越多的关注。
本实验根据二氢苯并咪唑-2-酮类化合物潜在的抗肿瘤活性,综合分析目前已报道的具有良好抗肿瘤作用的GSK-3小分子抑制剂如SB216763[12]、Azakenpaulllone[13]、compound 6h[14]的结构(IC50及结构见图1),发现GSK-3抑制剂大多具有酰胺或内酰胺结构。且鉴于磺酰胺基团常作为重要药效基团出现在抗肿瘤药物中,本课题组在前期实验中,通过在5位引入磺酰胺基团,设计和合成了一系列新型GSK-3抑制剂—苯并[d]咪唑-2(3H)-酮衍生物(化合物5a-o)。相关体外抗肿瘤活性实验表明,化合物5a-o对人乳腺癌细胞HCC1937、MDA-MB-468、人非小细胞肺癌细胞A549三种不同组织来源的肿瘤细胞具有不同程度的增殖抑制作用,其中化合物5b(结构见图1)在这三种肿瘤细胞中均具有良好的抗肿瘤活性,其IC50分别为2.6 μM,3.1 μM,6.3 μM。因此建立一种简便可行的纯度分析测定方法,对于GSK-3小分子抑制剂化合物的合成、纯度测定以及后续的相关开发研究具有重要意义。

图1 部分文献报道的GSK-3抑制剂(a,b,c)及化合物5b结构
本实验依据相关参考文献[15,16],采用高效液相色谱法,对化合物5b的纯度进行监测,指导其化学合成。其合成路线如图2所示。
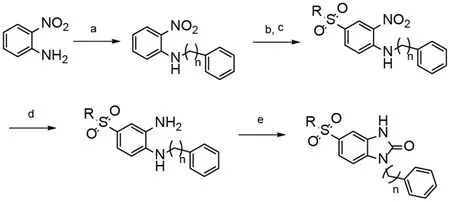
图2 苯并[d]咪唑-2(3H)-酮衍生物(化合物5a-o)的合成路线
1 材料与方法
1.1 仪器
高效液相色谱仪(e2695, 美国waters公司);PDA检测器(2998, 美国waters公司);超声清洗仪(KQ-2200, 昆山超声仪器);电子天平(JA1003,上海顺宇恒平科学仪器);实验室纯水系统(KMUPT-8/15/20, Millipore)。
1.2 试剂
化合物5b属于本实验室自行合成的新型抗肿瘤药物,无市售对照品。化合物5b对照品由本实验室前期合成,采用高效液相色谱面积归一化法对化合物5b的纯度进行检测。根据面积归一化法,计算得化合物5b的相对含量为98.14%,符合对照品的含量要求(大于98%)。 色谱甲醇,购自阿拉丁试剂公司;超纯水由实验室纯水系统制备。
1.3 方法
1.3.1 色谱条件 Phenomenex Gemini C18110A色谱柱(4.6 mm×250 mm,5 μm);流动相甲醇∶水(75∶25);流速1 mL·min-1;柱温为30 ℃;检测波长254 nm;进样量为20 μL。
1.3.2 样品的制备
1.3.2.1对照品溶液的制备 取化合物5b对照品10 mg,精密称定,加入色谱甲醇溶解,定容至10 mL,精密量取1 mL该对照品溶液,稀释至0.1 mg·mL-1,0.45 μm微孔滤膜过滤后,取续滤液用于HPLC进样分析。
1.3.2.2 供试品溶液的制备 取化合物5b供试品1 mg,精密称定,加入色谱甲醇溶解,定容至10 mL,精密量取1 mL该对照品溶液,稀释至0.1 mg·mL-1,0.45 μm微孔滤膜过滤后,取续滤液用于HPLC进样分析。
1.3.3 方法学考察
1.3.3.1 标准曲线的制备 精密吸取化合物5b对照品溶液稀释成浓度分别为100、80、60、40、20 μg·mL-1的对照品溶液,按照上述色谱条件分别进样分析,并记录相应峰面积,以化合物5b的检测浓度为横坐标X,峰面积为纵坐标Y进行线性回归分析。
1.3.3.2 精密度试验 精密吸取同一对照品溶液20 μL,连续进样6次,测定峰面积。
1.3.3.3 稳定性试验 精密吸取同一供试品溶液,分别于配制后0,4,8,12,16,20,24 h时依照上述方法进样测定。
1.3.3.4 重复性试验 精密称取同一批样品,分别依法制备6份供试品溶液并测定含量。
1.3.3.5 加样回收试验 称取6份同一批已知含量为981 mg·g-1的样品1.020 mg,精密称定,置于具塞锥形瓶中,分别精密加入1 mg·mL-1化合物5b对照品溶液 0.8,1.0,1.2 mL,依“1.3.2.2”方法制备供试品溶液,按“1.3.1”色谱条件进行测定,并计算回收率。
2 结果
2.1 方法学考察结果
线性回归考察结果如图3所示,回归方程为Y=3.53×107X+52087,r=0.9999(n=5),结果表明,化合物5b在20~100 μg·mL-1的浓度范围内与峰面积线性关系良好。
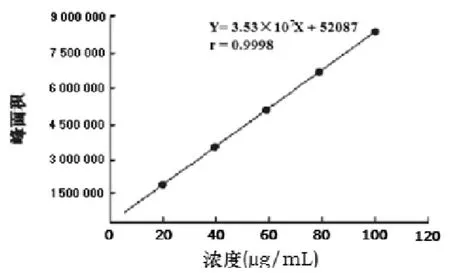
图3 化合物5b标准曲线
精密度试验,峰面积的平均值为5374093,RSD为0.63%(n=6),结果表明方法精密度良好;稳定性试验结果,峰面积的平均值为5369442,RSD为0.94%(n=7),表明供试品溶液在24h内保持稳定,符合测量要求;重复性试验结果如表1所示,化合物5b平均含量为847 mg·g-1,RSD为0.52%(n=6),方法重复性良好;加样回收试验结果如表2所示,化合物5b平均回收率为100.44 %,RSD为0.78 %(n=6)。

表1 重复性实验结果(n=6)

表2 化合物5b加样回收试验结果(n=6)
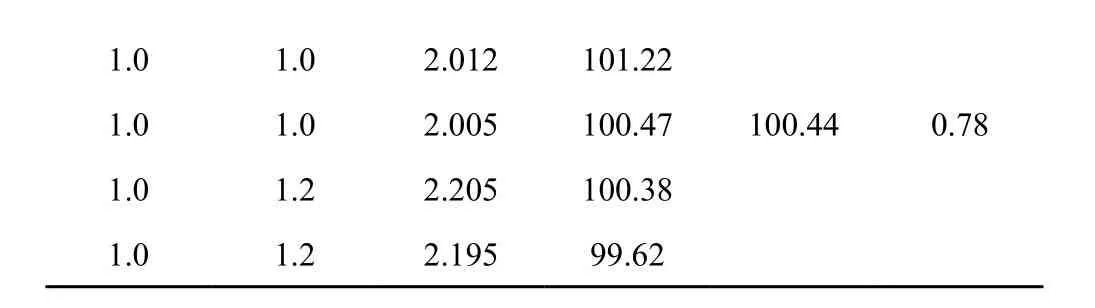
1.0 1.0 2.012 101.22 1.0 1.0 2.005 100.47 100.44 0.78 1.0 1.2 2.205 100.38 1.0 1.2 2.195 99.62
2.2 样品测定结果
取三批合成所得产品,依法测定,测得化合物5b的含量分别为984 mg·g-1、990 mg·g-1、981 mg·g-1,计算结果显示,所合成的化合物5b纯度达98%以上,纯度较高。高效液相色谱图见图4。

图4 化合物5b HPLC图(A.对照品 B.供试品)
3 讨论
HPLC是基于经典液相色谱法而迅速发展起来的可以快速高效分析样品的方法。本实验从化合物5b的物理性质以及实验室现有仪器设备条件和可操作性等方面考虑,选择了可操作性强、分析速度快、精度高的高效液相色谱法来对化合物5b的纯度进行测定,并对测定方法进行了考察。
根据GSK-3抑制剂—苯并咪唑酮衍生物的合成路线,我们推测可能在b,c及d反应过程中,由于硝基为间位定位基,而氨基为邻对位定位基,因此反应中除了在间位生成主产物化合物5b外,也可能会生成邻位的副产物,且磺酰氯自身也会发生相应副反应。另外,在整个反应过程中,由于步骤较多,也会在反应及后处理过程中引入其他杂质。因此,为了获得结构正确,纯度合格的化合物5b,作者首先对化合物5b结构进行1H-NMR,13C-NMR鉴定,在1H-NMR图谱中发现带磺酸基的苯环上3个氢,其中有一个是单峰(s),另外两个成双重峰(d),并没有发现这三个氢的其他裂峰情况,表明该化合物就是目标化合物5b,并没有生成邻位的副产物。同时13C-NMR结果亦显示化合物5b结构正确。其次,将化合物5b对照品进行全波长扫描,扫描结果显示其在254 nm处有最大吸收,灵敏度最高且其余物质对化合物5b的吸收影响最小,因此选择254 nm为测定波长。试验中分别考察了甲醇-水、乙腈-水、甲醇-0.1%磷酸水等不同流动相体系,考察结果表明采用甲醇-水体积比为75∶25作为流动相时,柱效较高且具有较好的分离度,故选择甲醇-水(75∶25)作为化合物5b纯度测定的流动相体系。本试验亦对该分析方法的专属性进行了考察,原料对化合物5b的测定无干扰且绘制的标准曲线的相关系数可以达到0.9999,表明此化合物20~100 μg·mL-1在线性关系良好。加样回收率能够反映分析方法在确定分析条件下样本浓度测定的准确性,一般样品的回收率宜在85%~115%的范围内,本试验的平均加样回收率达到100.44 %,RSD为0.78 %,表明该分析方法测定结果具有较高准确度。另外,精密度试验中的RSD值为0.63 %,说明实验方法具有良好的精密度。
综上所述,HPLC测定化合物5b的纯度,具有操作简便,准确度高,分离度好等特点,符合HPLC的测定要求,可以用于监测的化学合成反应进程和检测GSK-3抑制剂苯并咪唑酮系列衍生物的纯度。
[1]D W, W P.GSK3: a multifaceted kinase in Wnt signaling [J].Trends Biochem Sci, 2010, 35(3): 161.
[2]JEONG W J, YOON J, PARK J C, et al.Ras stabilization through aberrant activation of Wnt/β-catenin signaling promotes intestinal tumorigenesis [J].Sci Signaling, 2012, 5(219): ra30.
[3]CAFIERI F, FATTORUSSO E, MANGONI A.ChemInform Abstract: Longamide and 3,7-Dimethylisoguanine, Two Novel Alkaloids from the Marine Sponge Agelas longissima [J].Cheminform, 1996, 27(6): 7893.
[4]BUDZIK B, GARZYA V, SHI D, et al.Novel N-Substituted Benzimidazolones as Potent, Selective, CNS-Penetrant, and Orally Active M1 mAChR Agonists [J].Acs Med Chem Lett,2010, 1(6): 244.
[5]LI S K, JI Z Q, ZHANG J W.Synthesis of 1-acyl-3-isopropenyl benzimidazolone derivatives and their activity against Botrytis cinerea [J].J Agric Food Chem, 2010, 58(5): 2668.
[6]SCOTT S A, SELVY P E, BUCK J R, et al.Design of isoformselective phospholipase D inhibitors that modulate cancer cell invasiveness [J].Nat Chem Bio, 2009, 5(2): 108.
[7]COLLINS J C, ARMSTRONG A, CHAPMAN K L, et al.Prospective use of molecular field points in ligand-based virtual screening: efficient identification of new reversible Cdc25 inhibitors [J].Medchemcomm, 2013, 4(8): 1148.
[8]BRUNCKO M, TAHIR S K, SONG X, et al.N -Arylbenzimidazolones as novel small molecule HSP90 inhibitors[J].Bioorg Med Chem Lett, 2010, 20(24): 7503.
[9]WU Z, ROBINSON R G, FU S, et al.Rapid assembly of diverse and potent allosteric Akt inhibitors [J].Bioorg Med Chem Lett, 2008, 18(6): 2211.
[10]BALLANTE F, CAROLI A, RAGNO R.Hsp90 inhibitors,part 1: definition of 3-D QSAutogrid/R models as a tool for virtual screening [J].J Chem Inf Model, 2014, 54(3): 956.
[11]RZASA R M, KALLER M R, LIU G, et al.Structure–activity relationships of 3,4-dihydro-1 H -quinazolin-2-one derivatives as potential CDK5 inhibitors [J].Bioorg Med Chem, 2007, 15(20):6574.
[12]张娜, 蒋勇军, 俞庆森, 等.GSK-3抑制剂研究进展 [J].化学进展, 2007, 19(4): 614.
[13]KUNICK C, LAUENROTH K, LEOST M, et al.1-Azakenpaullone is a selective inhibitor of glycogen synthase kinase-3 beta [J].Cheminform, 2004, 14(2): 413.
[14]Shin D, Lee S C, Heo Y S, et al.Design and synthesis of 7-hydroxy-1H-benzoimidazole derivatives as novel inhibitors of glycogen synthase kinase-3beta.[J].Bioorg Med Chem Lett, 2007, 17(20):5686.
[15]王鑫, 李善茂, 李伟, 等.甲氟磷酸异丙脂的纯度测定 [C].公共安全中的化学问题研究进展,2011 .
[16]谌喜珠, 刘洋, 刘伟平.抗癌药顺铂对照品制备及其纯度测定 [J].分析试验室, 2008, 27(2):46.
