两相体系中PW12-TiO2-SiO2固体酸一步催化降解葡萄糖制5-羟甲基糠醛的研究*
2018-06-01吴廷华黄晓林李新生
吴廷华, 何 容, 韩 彬, 黄晓林, 吴 瑛, 李新生
(浙江师范大学 物理化学研究所,浙江 金华 321004)
由于能源消耗的日益增加和化石能源的枯竭问题,科学家专注于寻找替代能源[1].生物质燃料和平台化合物已成为有前途的化石燃料替代品,这归因于其可从储量丰富、可再生和低污染的生物质资源中获取.5-HMF、糠醛和2,5-呋喃二甲酸均为呋喃类衍生物,而5-HMF被美国能源部列为附加值最高的生物质衍生化学品[2].5-HMF中有活性官能团羟基和甲酰基,可经反应转化为许多高附加值产品.如在药物、杀菌剂和功能聚合物生产中有重要意义的2,5-呋喃二甲醛[3]、聚酯单体2,5-呋喃二甲酸[4-5]、2,5-二羟甲基呋喃[6]和2,5-二羟甲基四氢呋喃及潜在的生物燃料替代品(2-甲基呋喃、2,5-二甲基呋喃[7]、5-乙氧基甲基糠醛[8]、乙酰丙酸、乙酰丙酸乙酯和γ-戊内酯[9]).因此,由碳水化合物一步降解制备5-HMF具有重要意义.
在单相体系中,高沸点极性非质子溶剂能高选择性地获得产物5-HMF,如二甲基亚砜、二甲基甲酰胺及铵盐型离子液体[10],但从高沸点极性溶剂中分离5-HMF难度大且能耗高.Peniston等[11]首次使用的连续提取系统可有效地提高碳水化合物脱水制备5-HMF的选择性.Kuster等[12]研究了果糖在甲基异丁基酮-水两相体系中脱水制备5-HMF的反应,但此体系的发展受溶剂毒性和价格限制.Amiri等[13]在两相体系中以廉价且储量丰富的农业废弃物稻草为原料,制备5-HMF的催化活性.5-HMF在两相体系中的收率要比在相应单相体系中高2~3倍,这取决于有机溶剂的性质和沸点的温度范围(120~180 ℃).其中,四氢呋喃(THF)和1-丁醇是最有效的萃取剂.但醇类在酸性和高温下易醚化,降低了反应选择性,因此,选取THF作有机萃取相.另外,水相中低浓度的5-HMF可减少副反应来提高5-HMF收率[14-15],这取决于两相的分配系数R.最后,水相中无机盐NaCl对提高分配系数也有重要作用[11,16].因饱和NaCl溶液和THF两相体系具有分离提纯简单、产物选择性高和利于工业化生产等优点,故采用26.5% NaCl(aq)/THF两相体系.
近年来,研究人员致力于寻找低成本、高选择性和环境友好型催化剂降解糖类制备5-HMF[17].固体酸作为一种酸性可调、热稳定性好、循环利用率高、环境友好等优势的非均相催化剂被广泛应用于酸催化反应.常见固体酸载体有Al2O3,SiO2,TiO2和活性炭等,而TiO2具有酸碱共存性,可催化葡萄糖异构化为果糖.在TiO2中掺入SiO2不仅可增大其比表面,还能改善氧化物的催化性能,利用氧化物间较强的相互作用来促使新催化位点的产生,从而引起混合氧化物表面强的酸碱特性、高的热稳定性和强的机械强度[18].而磷钨酸(PW12)独特的强质子酸性、多功能性(氧化性和光催化性等)、易于调控的分子结构和独特的“准液相”性[19],使其具有避免设备腐蚀和环境污染的优点.但杂多酸易溶于水及大部分有机溶剂,因此,考虑将PW12掺杂在双氧化物TiO2-SiO2中,降低其溶脱率以提高催化活性.这种掺杂型催化剂在降解生物质制备5-HMF方面鲜有报道.因此,本文制备了不同掺杂量的PW12-TiO2-SiO2催化剂,在NaCl(aq)/THF两相体系中催化降解葡萄糖制备5-HMF,并对其进行表征,催化剂表现出良好的催化活性和高的热稳定性.
1 实验部分
1.1 试 剂
葡萄糖(AR)、5-羟甲基糠醛(LR)、NaCl(AR)、钛酸四丁酯(CP)、盐酸(AR)、乙醇(AR)和磷钨酸(AR)均采购于国药集团化学试剂有限公司;四氢呋喃(AR)和乙腈(HPLC)均采购于天津市科密欧化学试剂有限公司;Pluronic F-127采购于Sigma公司.
1.2 PW12-TiO2-SiO2固体酸催化剂的制备
根据文献[20-21]合成PW12-TiO2-SiO2(PW12-TS),具体步骤如下:F-127(2.0 g)溶于15.0 mL蒸馏水和10.4 mL乙醇的混合溶液,搅拌至澄清透明后逐滴加入HCl(12 mol/L,2.6 mL);升温到40 ℃,逐滴加入正硅酸四乙酯TOS(1.2 mL)并预水解45 min;之后逐滴加入钛酸四丁酯TBT(1.8 mL)再预水解1 h;预水解完成后逐滴加入一定物质的量比例的PW12水溶液,40 ℃搅拌24 h;100 ℃水热24 h (升温速率:2 ℃/min),干燥,热乙醇索氏提取24 h去除F-127;450 ℃焙烧3 h制得催化剂PW12-TS.制备过程中各化学物物质的量浓度满足如下比例:c(F-127)∶c(TOS)∶c(TBT)∶c(PW12)∶c(HCl)∶c(H2O)=0.03∶1∶1∶m∶6∶200.
1.3 产物分析方法
5-HMF采用岛津高效液相色谱仪Shimadzu LC-20AT进行外标法定量分析.检测条件:Ultimate Plus C18色谱柱(5 μm,4.6 mm×250 mm),流动相V乙腈∶V水= 4∶6,总流速0.5 mL/min,进样体积5 μL,柱温为室温.5-HMF收率计算如下:

(1)
式(1)中:n为稀释倍数;c5-HMF为5-HMF浓度;V为反应相体积;m葡为葡萄糖质量;M葡为葡萄糖相对分子质量;M5-HMF为5-HMF相对分子质量.
该高效液相色谱采用示差折光检测器对未反应的葡萄糖进行定量分析.检测条件:氨基色谱柱(5 μm,4.6 mm×250 mm),流动相V乙腈:V水= 7∶3,总流速0.5 mL/min,进样体积5 μL,柱温为室温.葡萄糖转化率的计算公式如下:

(2)
式(2)中,c葡为葡萄糖物质的量浓度.
2 结果与讨论
2.1 PW12-TS固体酸催化剂的表征
2.1.1 FT-IR
PW12和PW12-TS的FT-IR图谱如图1所示,400~1 000 cm-1处宽且强的吸收带为O-Ti-O伸缩振动吸收峰;1 100 cm-1处为Ti-OH伸缩振动吸收峰;1 080 cm-1处为Si-O-Si伸缩振动吸收峰;951 cm-1处微弱的吸收峰是Ti-O-Si的伸缩振动吸收峰;469 cm-1处为Si-O摇摆振动吸收峰[20,22-24].Keggin结构PW12在700~1 200 cm-1指纹区的特征峰:1 080 cm-1处为中心四面体PO4中P-Oa伸缩振动吸收峰;983 cm-1处为W=Oa反对称伸缩振动吸收峰;893 cm-1处为W-Oa-W反对称伸缩振动吸收峰;795 cm-1处为W-Ob-W反对称伸缩振动吸收峰[20,24-25].其4个特征峰强度随PW12掺杂量的增加而增强,当PW12掺杂量达0.012时,Ti-OH和P-Oa弯曲振动吸收峰强度明显且出现2个特征峰,同时951 cm-1处Ti-O-Si的伸缩振动吸收峰也逐渐增强;说明PW12和TiO2-SiO2之间存在相互作用,且其掺杂有利于双氧化物间的相互作用,即提高了其热稳定性.
2.1.2 XRD
PW12-TS固体酸XRD如图2所示,TiO2锐钛矿相在25.4°(101),38.6°(112)和48.2°(200)处的特征衍射峰随着PW12掺杂量增加而变宽;同时在53.9°(105)和55.1°(211)处的2个特征衍射峰逐渐归为1个峰且逐渐变宽,这可能是由于锐钛矿相和PW12均在53°附近出峰导致.这表明PW12与TiO2-SiO2间存在相互作用,导致其均匀掺杂从而延缓了其晶相的形成,或PW12含量低于检测限无法显示其特征衍射峰.另外,当PW12掺杂量达0.006时,在26.6°和36.1°处出现微弱石英相SiO2特征衍射峰,这说明PW12掺杂的增加有助于石英相SiO2的形成.

(a)0.001 PW12-TS;(b)0.003 PW12-TS;(c)0.006 PW12-TS;(d)0.012 PW12-TS;(e)0.024 PW12-TS;(f)PW12

(a)PW12;(b)0.024 PW12-TS;(c)0.012 PW12-TS;(d)0.006 PW12-TS;(e)0.001 PW12-TS;(f)TiO2-SiO2
2.1.3 XPS
由图3(a)可知,0.006 PW12-TS固体酸表面存在Ti,Si,P,W和O元素.图3(b)中O 1s光电子能谱峰分别在530.4 eV和532.7 eV处,较纯TiO2中由Ti-O-Ti引起的O 1s (529.7 eV)和纯SiO2中由Si-O-Si引起的O 1s (532.5 eV)偏高,这是由于TiO2-SiO2和PW12中氧原子重叠贡献导致[23,26-28].Si 2p(103.5 eV)与纯SiO2(103.4 eV)及Ti 2p光电子能谱中Ti 2p1/2(464.7 eV)和Ti 2p3/2(458.9 eV)与纯TiO2(458.5 eV)相比均存在一定位移,这可能是由于TiO2,SiO2和PW12之间存在相互作用,改变其原有的化学环境导致.在133.7 eV处观察到弱的P 2p能谱峰归因于P5+,较磷钨酸中P 2p (136.0 eV)偏低[26].W 4f特征峰出现在35.7 eV (7/2)和37.8 eV (5/2)处,较纯磷钨酸中W 4f7/2(35.8 eV)和W 4f5/2(37.9 eV)偏低,说明掺杂PW12后,P和W元素原子核周围电子密度升高,氧化数略有降低,电子偏向PW12[26].同时,W 4f光谱峰相对强度的改变是由于Ti 3p和W 4f结合能的重叠共用导致[27].这进一步表明活性组分PW12和TiO2-SiO2之间存在相互作用力,从而致使其不易溶脱且掺杂良好.

(a)全谱;(b)O 1s能谱;(c)Ti 2p能谱;(d)Si 2p能谱;(e)P 2p能谱;(f)W 4f能谱
2.1.4 催化剂的比表面积、表面酸量和酸密度
由表1可知,催化剂比表面积随PW12掺杂量的增加而减小,但仍在400 m2/g附近.由图4可知,载体在340~530 ℃和530~700 ℃处出现2个宽的氨脱附峰.随着PW12掺杂,此氨脱附峰宽泛到120~460 ℃和460~760 ℃处,且峰位置分别由497 ℃和628 ℃变化为402 ℃和676 ℃,这可能是由于PW12本身性质或其与双金属氧化物间的相互作用导致.且催化剂酸量和酸密度均随PW12掺杂量的增加而增大,这说明掺杂量主要影响强酸和超强酸的酸中心数.而此反应需要适当的酸量和酸密度,过多或过少均不利于5-HMF收率和选择性的提高.
2.2 PW12掺杂量和反应时间的影响

表1 催化剂比表面积、表面酸量和酸密度
注:酸量:估计NH3-TPD测量峰的积分面积;酸密度:酸量和催化剂比表面积之比.

(a)0.024 PW12-TS;(b)0.012 PW12-TS;(c)0.006 PW12-TS;(d)0.003 PW12-TS;(e)0.001 PW12-TS;(f)TiO2-SiO2

T=160 ℃,VNaCl(aq)∶VTHF=1∶7,m催∶m葡=1∶5,650 r/min
图5 PW12掺杂量和反应时间对降解葡萄糖制备5-HMF催化性能的影响
由图5可知,未掺杂PW12时,5-HMF最佳收率较低,仅为29.4%.这是由于高比表面的锐钛矿相双氧化物TiO2-SiO2能有效催化葡萄糖异构化为果糖,但其质子酸量不足,无法有效酸化果糖脱去三分子水形成5-HMF.当PW12掺杂量由0增至0.006时,5-HMF收率显著增加,这归因于0.006 PW12-TS有最佳的表面酸量和酸密度.酸量太弱不利于酸化底物促使其脱水,适量的质子酸可有效催化异构化的果糖脱水,从而提高5-HMF的收率.而PW12掺杂量由0.006增为0.024时,5-HMF收率却逐渐降低.这归因于过量质子酸致使稳定性差的5-HMF转化为副产物甲酸、乙酰丙酸及2,5-呋喃二甲醛等.另外,在1~3 h时,5-HMF收率随时间的增加而升高;超过3 h后,其收率随反应时间的增加而降低.这可能是由于过长反应时间导致反应物和产物、产物和产物之间发生聚合或产物发生副反应生成可溶性聚合物和不溶性腐黑素等.因此,筛选出PW12最佳掺杂量为0.006、最佳反应时间为3 h.
2.3 反应温度的影响
由图6可知,当反应温度由130 ℃上升为160 ℃时,5-HMF收率由5.6%增加到44.3%,葡萄糖转化率由47.1%增加到82.7%.当T=170 ℃时,其收率下降为34.9%,而葡萄糖转化率为98.6%.由宏观图(见图6插图)可知:随着反应温度的升高,有机相由黄色逐渐向橙红色转变,当T=170 ℃时,有机相则变为棕黑色.由Arrhenius公式可知,反应速率常数随温度升高而增大.即葡萄糖降解为5-HMF的速率随温度升高而加快,因此,5-HMF收率升高.但温度过高时,收率和选择性反而降低.这是由于过高反应温度导致副产物增多,如葡萄糖分子间聚合、5-HMF在酸催化下生成乙酰丙酸和甲酸、5-HMF自聚等.因此,最佳反应温度为160 ℃.
2.4 两相体系体积比的影响
由表2可知,随着VTHF的增加,分离系数R先增大后减小,5-HMF收率和选择性也呈此趋势.当两相体积比为1∶5时,R值最大,5-HMF收率和选择性均达最大值.这归因于此时水相中的5-HMF萃取到THF相,阻碍反应物和产物、产物和水的接触,从而抑制副反应,提高其收率和选择性.

0.006 PW12-TS,t=3 h,VNaCl(aq)∶VTHF=1∶7,m催∶m葡=1∶5,650 r/min
表2 两相体系体积比对降解葡萄糖制备5-HMF催化性能的影响

V/mLNaCl(aq)THF5-HMF收率/%NaCl(aq)THF总收率/%转化率/%选择性/%分离系数R3.0-3.3-3.378.84.1-0.50.50.97.28.180.410.17.60.51.50.511.712.289.613.67.70.52.51.248.149.397.950.38.00.53.50.843.544.388.749.97.00.54.50.640.140.784.748.06.8
注:反应条件:0.006 PW12-TS,t=3 h,T=160 ℃,m催∶m葡=1∶5,650 r/min.
2.5 催化剂用量的影响
由图7可知,当催化剂和葡萄糖质量比由1∶9增加到1∶5时,5-HMF收率和选择性逐渐增加.这是由于催化剂量的增加导致体系质子酸量及双氧化物增多,可有效催化葡萄糖异构化及果糖的脱水.而当质量比由1∶5增加到5∶5时,5-HMF收率却逐渐降低.这是由于过量催化剂导致反应体系质子酸量过多,导致副产物增多从而降低反应选择性;同时过多的催化剂减少反应组分之间的接触面积,反应速率减慢从而抑制5-HMF收率的提高.因此,催化剂和葡萄糖最佳质量比为1∶5.

0.006 PW12-TS,t=3 h,T=160 ℃,VNaCl(aq)∶VTHF=1∶5,650 r/min
2.6 磁力搅拌速度的影响
由表3可知,随着反应过程中磁力搅拌速度的加快,分离系数R逐渐增大,5-HMF收率和选择性也逐渐提高.这归因于提高转速可加快反应底物和活性位点有效碰撞及反应的传质传热,从而提高收率和选择性.由于受实验装置的限制,最高转速为1 200 r/min.

表3 磁力搅拌速度对降解葡萄糖制备5-HMF催化性能的影响
注:反应条件:0.006 PW12-TS,t=3 h,T=160 ℃,VNaCl(aq)∶VTHF=1∶5,m催∶m葡=1∶5.
2.7 催化剂的循环利用性
由图8可知,催化剂在重复利用6次后,5-HMF收率仍保持50%以上,且选择性维持在58%左右,这说明催化剂的热稳定性良好.由循环前后FT-IR图谱(见图9)可知,催化剂表面的活性物种PW123个特征吸收峰均减弱,这表明PW12在反应和洗涤过程有部分流失,或催化剂预处理焙烧时造成PW12微量损失.催化剂表面活性位点减少导致5-HMF收率降低.
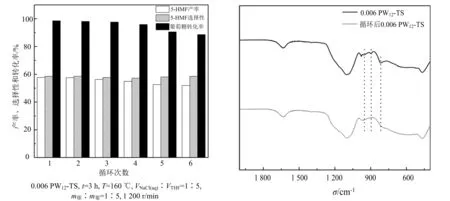
图8 催化剂循环利用性 图9 催化剂循环前后的FT-IR图谱
2.8 可能的催化机理
酸催化碳水化合物的降解反应是一个非常复杂的过程,此过程涉及多种异构化、缩合、分裂和脱水反应.Antal[29],Van Dam[6]和Rosatella[30]通过分析实验中诸多反应中间体,提出了葡萄糖降解制备5-HMF的2种可能机理,本文就一种最可能的机理进行讨论.由文献[18]可知,锐钛矿相TiO2显示了酸碱性共存特性,能够催化葡萄糖异构化生成果糖.因此,葡萄糖在大比表面的锐钛矿相TiO2催化作用下,经烯醇式由醛糖转化为酮糖,随后异构环化为果糖,又由于磷钨酸强的质子酸性[19]和双氧化物的酸性共同催化果糖,经3次H+亲电进攻羟基反应,连续失去三分子水制得5-HMF.
3 结 论
本文探究了PW12掺杂量、反应时间、反应温度、催化剂用量、两相体系体积比及磁力搅拌速度对葡萄糖降解制备5-HMF的影响,同时考察了催化剂的循环利用性.另外,还探讨了该反应可能的催化机理.结果表明:0.006 PW12-TS是筛选出的最佳催化剂,在最佳反应条件:t=3 h,T=160 ℃,m催∶m葡=1∶5,VNaCl(aq)∶VTHF=1∶5和1 200 r/min下,5-HMF的最高收率为57.7%、最高选择性为58.5%.且掺杂型催化剂PW12-TS对实验设备无腐蚀现象、循环利用性良好,是一种环境友好型固体酸催化剂,且对5-HMF大规模工业化生产有重要意义.
参考文献:
[1]Besson M,Gallezot P,Pinel C.Conversion of biomass into chemicals over metal catalysts[J].Chemical reviews,2013,114(3):1827-1870.
[2]Bozell J J,Petersen G R.Technology development for the production of biobased products from biorefinery carbohydrates—the US Department of Energy′s “top 10” revisited[J].Green Chemistry,2010,12(4):539-554.
[3]Fang R,Luque R,Li Y.Efficient one-pot fructose to DFF conversion using sulfonated magnetically separable MOF-derived Fe3O4(111) catalysts[J].Green Chemistry,2017,19(3):647-655.
[4]Saha B,Gupta D,Abu-Omar M M,et al.Porphyrin-based porous organic polymer-supported iron(III) catalyst for efficient aerobic oxidation of 5-hydroxymethyl-furfural into 2,5-furandicarboxylic acid[J].Journal of Catalysis,2013,299(2):316-320.
[5]Casanova O,Iborra S,Corma A.Biomass into chemicals:Aerobic oxidation of 5-hydroxymethyl-2-furfural into 2,5-furandicarboxylic acid with gold nanoparticle catalysts[J].Chem Sus Chem,2009,2(12):1138-1144.
[6]Dam H E V,Kieboom A P G,Bekkum H V.The conversion of fructose and glucose in acidic media:Formation of hydroxymethylfurfural[J].Starch-Stärke,1986,38(3):95-101.
[7]Shi Juanjuan,Wang Yingyu,Yu Xini,et al.Production of 2,5-dimethylfuran from 5-hydroxymethylfurfural over reduced graphene oxides supported Pt catalyst under mild conditions[J].Fuel,2016,163:74-79.
[8]Mascal M,Nikitin E B.Direct,high-yield conversion of cellulose into biofuel[J].Angewandte Chemie,2008,120(41):8042-8044.
[9]Wettstein S G,Alonso D M,Gürbüz E I,et al.A roadmap for conversion of lignocellulosic biomass to chemicals and fuels[J].Current Opinion in Chemical Engineering,2012,1(3):218-224.
[10]Sen S,Martin J D,Argyropoulos D S.Review of cellulose non-derivatizing solvent interactions with emphasis on activity in inorganic molten salt hydrates[J].ACS Sustainable Chemistry and Engineering,2013,1(8):858-870.
[11]Peniston J H,Gold M S,Wieman M S,et al.Tolerability of diclofenac sodium 1% gel with concomitant medications known to interact with diclofenac[J].Therapeutics and Clinical Risk Management,2012,13(4):153-159.
[12]Kuster B F M,Steen H J C D V.Preparation of 5-hydroxymethylfurfural part I.Dehydration of fructose in a continuous stirred tank reactor[J].Starch-Stärke,2006,29(3):99-103.
[13]Amiri H,Karimi K,Roodpeyma S.Production of furans from rice straw by single-phase and biphasic systems[J].Carbohydrate Research,2010,345(15):2133-2138.
[14]Gürbüz E I,Wettstein S G,Dumesic J A.Conversion of hemicellulose to furfural and levulinic acid using biphasic reactors with alkylphenol solvents[J].Chem Sus Chem,2012,5(2):383-387.
[15]吴廷华,轩勇丽,韩彬,等.SO3H-功能化离子液体在双液相体系中催化纤维素降解为5-羟甲基糠醛[J].浙江师范大学学报:自然科学版,2016,39(4):406-411.
[16]Román-Leshkov Y,Dumesic J A.Solvent effects on fructose dehydration to 5-hydroxymethylfurfural in biphasic systems saturated with inorganic salts[J].Topics in Catalysis,2009,52(3):297-303.
[17]Moreau C,Belgacem M N,Gandini A.Recent catalytic advances in the chemistry of substituted furans from carbohydrates and in the ensuing polymers[J].Topics in Catalysis,2004,27(1/2/3/4):11-30.
[18]Reddy B M,Khan A.Recent advances on TiO2-ZrO2mixed oxides as catalysts and catalyst supports[J].Catalysis Reviews,2005,47(2):257-296.
[19]Okuhara T,Mizuno N,Misono M.Catalytic chemistry of heteropoly compounds[J].Advances in Catalysis,1996,41(8):113-252.
[20]Song Daiyu,An Sai,Sun Yingnan,et al.Efficient conversion of levulinic acid or furfuryl alcohol into alkyl levulinates catalyzed by heteropoly acid and ZrO2bifunctionalized organosilica nanotubes[J].Journal of Catalysis,2016,333:184-199.


[23]Li Dayu,Elisabeth S,Granier A,et al.Structural and optical properties of PECVD TiO2-SiO2mixed oxide films for optical applications[J].Plasma Processes and Polymers,2016,13(9):918-928.
[24]Betiha M A,Hassan H M A,El-Sharkawy E A,et al.A new approach to polymer-supported phosphotungstic acid:Application for glycerol acetylation using robust sustainable acidic heterogeneous-homogenous catalyst[J].Applied Catalysis B:Environmental,2016,182:15-25.
[25]邹敏,轩勇丽,周琴,等.双液相体系中Cr([MIMPS]3PW12O40)3催化降解纤维素为5-羟甲基糠醛的研究[J].浙江师范大学学报:自然科学版,2015,38(2):195-200.
[26]Ji Haiyan,Sun Jia,Wu Peiwen,et al.Deep oxidative desulfurization with a microporous hexagonal boron nitride confining phosphotungstic acid catalyst[J].Journal of Molecular Catalysis A:Chemical,2016,423:207-215.
[27]Li Na,Vorontsov A V,Jing Liqiang.Physicochemical properties and photocatalytic activity of H3PW12O40/TiO2[J].Kinetics and Catalysis,2015,56(3):308-315.
[28]Jung S M,Dupont O,Grange P.TiO2-SiO2mixed oxide modified with H2SO4:I.Characterization of the microstructure of metal oxide and sulfate[J].Applied Catalysis A:General,2001,208(1):393-401.
[29]Antal M J,Mok W S L,Richards G N.Mechanism of formation of 5-(hydroxymethyl)-2-furaldehyde from D-fructose and sucrose[J].Carbohydrate Research,1990,199(1):91-109.
[30]Rosatella A A,Simeonov S P,Frade R F M,et al.5-Hydroxymethylfurfural(HMF) as a building block platform:Biological properties,synthesis and synthetic applications[J].Green Chemistry,2011,13(4):754-793.
