难治性精神分裂症多靶点联合毁损术后CT及MRI表现
2018-05-29吴永彬蒋俭峰李萍
吴永彬 蒋俭峰 李萍
(西安市精神卫生中心,陕西 西安 710100)
精神分裂症(schizophrenia)是一种严重的精神疾病,其中,30%~50%的患者经过两年以上及数种传统抗精神病治疗效果不佳,而称为难治性精神分裂症(treatment resistant schizophrenia, TRS)[1],不仅患者及其家庭的带来痛苦,更引发很多严重的社会问题[2]。多靶点联合毁损术一度成为治疗难治性精神分裂症的有效手段应用于临床,但对其术后影像学表现的研究报道不多,本研究分析50例多靶点联合毁损术治疗的难治性精神分裂患者的头部计算机断层扫描(computed tomography, CT)及磁共振成像(magnetic resonance imaging, MRI)表现,以提高对术后影像学表现的认识。
一、对象与方法
1.一般资料:收集我院2012年6月至2016年12月,经多靶点联合毁损手术治疗的难治性精神分裂症患者50例,其中男29例,女21例,年龄24~59岁,平均年龄38岁。
2.临床表现:所有患者临床症状为不同程度幻听、妄想、行为紊乱,自知力受损等精神障碍,反复发作,药物治疗效果不佳,病史4~40年,平均17.22年,体格检查及神经系统检查未见异常。
3.影像学检查:40例患者使用美国通用电气公司(General Electric Co.,GE) BRIVO325 CT机,扫描体位:仰卧位;扫描范围:从鞍底至颅顶,扫描基线:平行于听眦线,采用横断面连续足头方向扫描。扫描参数:层厚10 mm,层间距10 mm。10例患者行GE 750 3.0T超导磁共振扫描仪及头颈联合线圈,行MRI平扫,包括轴位T1WI,轴位T2WI及轴位液体衰减反转恢复序列(fluid-attenuation inversion recovery, FLAIR),扫描参数:层厚5 mm,层间距1.5 mm,矩阵320×320。
4.治疗:50名患者均行多靶点联合毁损术,根据治疗的症状选择不同靶点组合,包括双侧扣带回+双侧内囊前肢;双侧扣带回+双侧内囊前肢+双侧杏仁核。
二、结果
1.毁损灶位置:50例患者共发现毁损灶255个,其中30例患者的毁损灶180个对称分布于双侧杏仁核、内囊前肢及扣带回。另外17例患者共有71个毁损灶,对称分布于内囊前肢与扣带回(63个,其中一个扣带回毁损灶显示不清)或杏仁核与内囊前肢(8个),还有2例患者仅在双侧扣带回存在毁损灶。255个毁损灶内位于杏仁核前部44个,杏仁核内侧群中央部20,位于内囊前肢的前1/5~1/4处62个,内囊前肢前、中1/3交界处34个,位于扣带的毁损灶其内界与中线距离大于3 mm者78个,小于3 mm者17个)。
2.毁损灶影像学表现:255个毁损灶中呈类圆形155个,短条状76个,不规则20个,小点状4个,其中位于杏仁核的毁损灶均为类圆形,内囊前肢多见短条状及类圆形毁损灶,扣带回的毁损灶各种类型均可见到,虽然病灶多呈对称性分布,但其形态不尽相同。大部分毁损灶CT表现为边缘光整、密度均匀的低密度影,少数病灶边界显示不清,呈略低密度,其中仅有1例患者,在毁损区出现点条状高密度,骨窗可见双侧额骨对称性类圆形骨质缺损区;MRI的主要表现为边缘锐利的长T1长T2信号,部分病灶边缘可见胶质增生。约有20%(10/50)的患者出现额、颞叶脑皮质变薄,脑沟裂增宽(图1、2)。
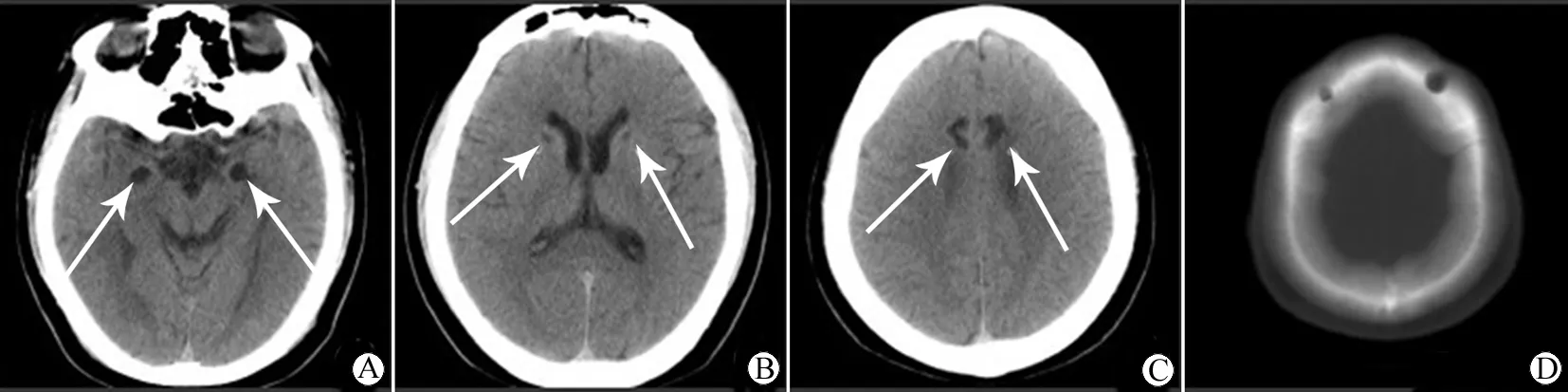
图1 颅脑CT横断:脑窗及骨窗
A~C:双侧杏仁核、内囊前肢及扣带回对称性类圆形、不规则低密度影,密度均匀,边界清晰,周围无水肿;D:额骨对称性骨质缺损

图2 CT轴位及轴位T2WI、轴位T1WI
A~B:双侧杏仁核及内囊前肢可类圆形发低密度影,边界清晰,双侧内囊前肢病灶欠对称,右侧病灶偏向尾状核头部;双侧侧脑室前脚周围白质区呈对称性斑片状稍低密度影;C~D:病灶呈均匀长T2信号;E~F:病灶呈长T1信号
三、讨论
由于精神分裂症的病因及发病机制目前尚不明确,难治性精神分裂症的治疗问题一直是精神科的一大难题,精神外科手术治疗自20世纪30年代发展至今,从单部位单靶点手术发展为多部位多靶点手术,从一侧半球手术到双侧半球同时手术,在减轻损伤的同时提高了手术效果。边缘系统分为内侧环路、外侧环路以及防御反应环路,与基底前脑联系广泛,这些部位与情感、动机等精神因素有关[3]。临床最常用的手术路径包括杏仁核+扣带回毁损术、此外还有杏仁核+额叶底部毁损术、扣带束+胼胝体膝毁损术、杏仁核+隔区毁损术等边缘系统核团毁损术,然而,影像科医生对这种治疗精神分裂症的手术方式认识不足,在实际工作中,我们常无法得到患者的手术史等资料,对诊断造成困扰,甚至误诊,因此,了解多靶点联合毁损术后影像学特点十分必要。
1.影像学表现:CT及MRI能客观、准确的观察多靶点联合毁损术后颅内毁损灶的大小、形态和位置,对临床治疗提供可靠的影像学资料。通过总结本组病例的影像学特点,我们发现:①毁损灶对称分布于杏仁核、内囊前肢及扣带回区域;②毁损灶形态多为类圆形及短条状;③术后急性期病灶边界不清,CT呈稍低密度影,MRI-T1WI呈稍低信号,T2WI呈稍高信号,其周围可见水肿;④慢性期病灶CT呈低密度,边界光整;MRI显示T1WI呈低信号,T2WI呈高信号,周围胶质增生;⑤部分毁损灶呈不对称分布,可能与手术方法、手术损伤及修复有关[4];⑥CT骨窗额骨对称性类圆形骨质缺损可帮助诊断。
2.鉴别诊断:靶点联合毁损术后改变需与基底节区对称性病变进行鉴别,如:营养代谢性疾病(维生素B1缺乏及肝豆状核变性)及中毒性疾病(一氧化碳中毒性脑病):①维生素B1缺乏导致丙酮酸脱羧反应障碍,丙酮酸等代谢产物堆积,乙酰胆碱合成减少,神经传导受阻,出现一系列神经及消化系统病变[5]。豆状核受累最多见,其次是尾状核、丘脑,也可累及内囊、外囊和脑室旁脑白质。CT表现为基底节区对称性低密度影,CT表现为基底节区对称性低密度影,MRI表现为乳头体、丘脑、第三脑室及丘脑中背侧柱、中脑导水管周围对称性长T1长T2异常信号,FLAIR及扩散加权成像(diffusion weighted image, DWI)呈稍高信号。②肝豆状核变性又称为Wilson's病,是一种常染色体隐形遗传性疾病,病变部位主要位于壳核,其次是苍白球、尾状核、丘脑底核、红核、黑质及齿状核,CT为低密度,MRI呈长T1长T2信号。临床上结合肝功、角膜K-F环、血清总铜量降低,尿铜排泄量增加等即可诊断,其中K-F阳性被认为是该病最具特征的体征[6]。③一氧化碳中毒性脑病,典型表现为双侧苍白球受累,也可见于整个豆状核和(或)尾状核头受累,急性期表现为弥漫性脑肿胀,非急性期病灶CT低密度影,MRI呈对称性长T1、长T2信号,边界清晰,结合一氧化碳接触史及碳氧血红蛋白的测定,可明确诊断。
综上,多靶点联合毁损术治疗难治性精神分裂症后的颅内改变有其特征性表现,通过分析本组病例CT及MRI特点,希望能提高影像科医生对多靶点联合毁损术后颅内改变的认识,减少误诊率,提高诊断准确率。
参考文献
1折霞, 何海宁, 印弘, 等. 基于磁共振动脉自旋标记成像的首发精神分裂症脑血流灌注研究 [J]. 中华神经外科疾病研究杂志, 2014, 13(5): 442-445.
2CONLEY R R, BUCHANAN R W. Evaluation of treatment resistant schizophrenia [J]. Schizophr Bull, 1997, 23(4): 663-674.
3BYRUM J, AHEARN E P, KRISHNAN K R. A neuroanatomic modle for depression [J]. Prog Neuropsychopharmacol Biol Psychiatry, 1999, 23(2): 175-193.
4袁新平, 王一方, 徐华强, 等. 难治性精神分裂症CT表现及多靶点联合毁损术后CT征象分析 [J]. 放射学实践, 2007, 22(7): 683-686.
5刘斌, 奚美芳, 王孟鼎, 等. 婴儿维生素B1缺乏颅脑CT研究 [J]. 中华放射学杂志, 1998, 32(8): 537-539.
6黄跃金, 邬至平, 蔡学礼. 肝豆状核变性58例临床特点与CT、MRI分析 [J].中国实用神经疾病杂志, 2006, 9(3): 131-132.
