伴有皮肤表现的真性红细胞增多症2例
2018-05-18王晓萌张玉环张理涛
王晓萌,张玉环,张理涛
(1.天津中医药大学,天津 300100;2.天津市中医药研究院附属医院,天津 300120)
真性红细胞增多症(Polycythemia vera,PV)是一种以克隆性红细胞增多为主的骨髓增生性疾病,可伴有皮肤表现,临床少见,于皮肤科就诊时易误诊。本文报道了2例伴有皮肤表现的真性红细胞增多症,希望可以为临床诊断治疗提供参考。
1 临床资料
例1,患者男,71岁,手指、双下肢红斑、丘疹、水疱、坏死伴下肢疼痛3年余,于2016年10月就诊。患者3年前开始于左手手指、双下肢出现红斑、丘疹、水疱,水疱破溃后局部出现溃疡、坏死,伴有明显的下肢肌肉、关节痛,期间曾口服强的松30 mg/d治疗,上述皮损及伴随症状明显好转。既往PV病史13年,长期交替应用羟基脲、干扰素治疗。
体格检查:球睑结膜充血,脾中度肿大,双下肢关节、肌肉痛,余系统检查无异常。皮肤科检查:左手拇指、中指指腹可见多处溃疡、部分结痂,部分破溃水疱有轻度渗出。双下肢皮肤干燥、脱屑,并可见多处暗红色斑,部分红斑上有溃疡,均已结痂。右侧胫前可见8 cm×5 cm大小坏死,有组织缺损。皮损处触痛明显。口腔(-),见图 1~4。
实验室及辅助检查:血常规:白细胞计数20.85×109,红细胞计数 6.32×1012,血红蛋白 168.0 g/L,血细胞比量59.0%,血小板计数164×109/L,特发性肺纤维化13.0%;血白细胞分类示中性杆状核粒细胞6%;骨髓祖细胞培养示:CFU-E(-EPO)1/105BMMNC;促红细胞水平测定3.66 ng/mL;凝血功能测定:凝血酶原时间(PT)16.9 s,国际标准化比值(INR)1.45,活化部分凝血活酶时间(APTT)63.4s,凝血酶时间(TT)22.0 s;血生化:白蛋白(ALB)28.50 g/L,球蛋白(GLO)42.10 g/L,脂蛋白(LP)206 U/L,总胆红素(TBIL)46.60 μmol/L,直接胆红素(DBIL)9.00 μmol/L,间接胆红素(IBIL)37.60μmol/L,尿酸(UA)767.90μmol/L;骨髓染色体检查未见克隆异常;KAK2/V617F阴性;骨髓病理报告:增生极度活跃(>90%),粒性红细胞比例减少,红系增生伴轻度核左移,网织纤维染色(+~++),见图 5、6。诊断:PV;骨髓片:增生明显活跃,G=34.5%,E55%,G/E0.631,粒系比例减少,核左移,红系比例增高,以中晚幼红细胞为主,见图7。皮肤科皮损处病理示表皮棘层萎缩变薄,基底层色素加深,真皮浅层毛细血管增生,血管周围淋巴细胞,中性粒细胞浸润,深层血管壁增厚,管壁狭窄,血管周围有淋巴细胞,中性粒细胞浸润,见图8、9。诊断:①PV;②变应性皮肤血管炎。
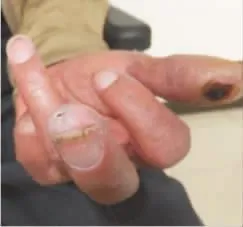
图1 左手中指溃疡
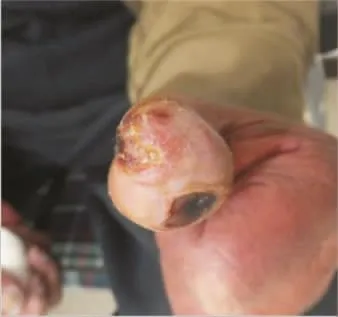
图2 左手拇指红斑、溃疡

图3 左胫前多发暗红斑
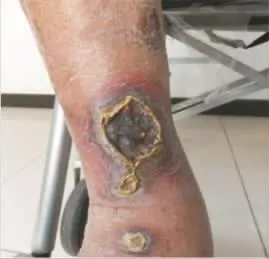
图4 右侧胫前可见红斑、8 cm×5 cm大小坏死,有组织缺损

图5 增生极度活跃(>90%),粒红比例减少,粒系各阶段可见,以中幼及以下阶段为主,原早阶段细胞略增多,以中晚幼红为主(HE染色×100)

图6 红系增生伴轻度核左移(HE 染色×1 000)
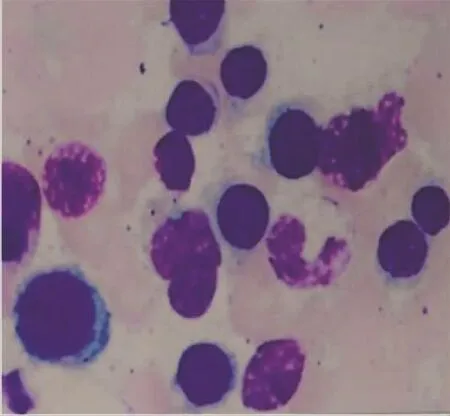
图7 红系比例增高,以中晚幼红为主。粒系比例减少,核左移(HE染色×1 000)
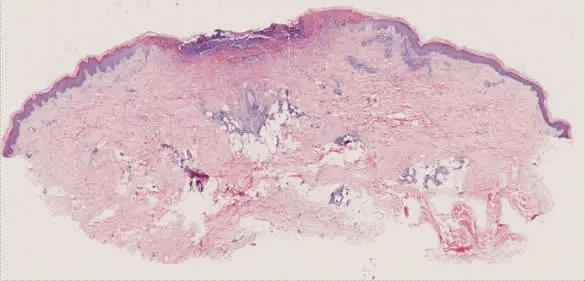
图8 表皮部分坏死、结痂、红染,周围棘层肥厚,血管内皮肿胀,管腔闭塞狭窄,周围中性粒细胞浸润,可见核尘(HE染色×40)

图9 血管周围纤维蛋白样变性,部分红细胞外渗(HE染色×100)
治疗:PV诊断明确,羟基脲1.25 g,口服1次/d,依托泊苷50 mg,口服1次/d,连用5 d,控制病情发展,对于充血的口腔黏膜,用5%NaHCO2漱口;变应性皮肤血管炎诊断明确:局部渗出处抗生素湿敷,给予口服芦丁片、维生素C,原口服强的松依据病情逐渐减量,并辅以中药治疗。治疗2个月后患者原发皮损全部愈合,未见新发皮疹。双下肢关节、肌肉痛仍较明显。9个月后,患者进展为急性白血病,临床死亡。
例2,患者男,67岁,主因躯干、四肢瘙痒,逐渐加重2个月余,于2017年5月就诊。患者2个月前开始于躯干、四肢出现瘙痒,逐渐加剧,2周前就诊当地诊所未明确诊断,按“过敏”应用“氢化可的松”治疗2周未缓解。患者既往体健,否认高血压、糖尿病病史,无家族史。
体格检查:发育正常,营养良好,系统检查无异常。全身浅表淋巴结未触及增大,心、肺、腹未见异常。皮肤科检查:四肢可见散在抓痕及结痂。口腔黏膜充血,局部浅溃疡。
实验室及辅助检查为血常规:红细胞计数5.47×1012,血红蛋白160.0 g/L,白细胞计数13.38×109,血小板557×109/L,血细胞比容52.4%。外周血涂片结果示红细胞数量显著增多,多为正细胞正色素红细胞,成堆、聚集状分布。骨髓涂片示骨髓增生明显活跃,粒系、红系和巨核系比例及形态大致正常,真性红细胞增多症骨髓象。临床基因扩增:融合基因(JAK2/V617F)阳性。氧饱和度0.95。病理诊断报告:骨髓增生大致正常(40%),粒红比例略增大,粒系各阶段细胞可见,以中幼及以下阶段细胞为主,红系各阶段细胞可见,巨核细胞未见明显增多,大部分胞体不太大,分叶核为主。网状纤维染色(-),见图 10、11[1]。诊断:①PV;②瘙痒症。

图10 伴发瘙痒症患者的真性红细胞增多症患者骨髓病理像(HE 染色 ×100)
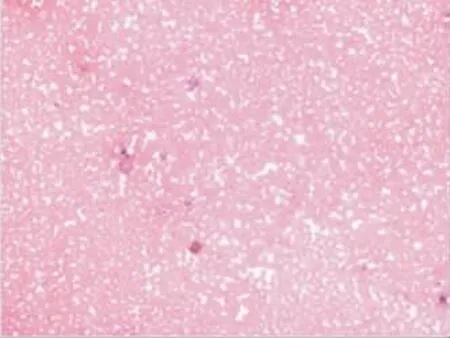
图11 伴发瘙痒症患者的真性红细胞增多症患者外周血涂片(HE染色 ×100)
治疗:对症治疗,口服抗组胺药,抓伤部位外用复方氯霉素搽剂。用5%NaHCO2漱口,护理口腔。明确诊断后,嘱患者口服羟基脲1.25 g,1次/d口服,以及拜阿司匹林100 mg,1次/d口服,抗血小板聚集。因本例患者67岁,故应特别注意预防血栓的生成。同时配以中药制剂血府逐瘀颗粒内服。经治疗病情逐渐好转,皮肤瘙痒明显减轻,血常规大致恢复正常。口腔充血、溃疡痊愈。现持续随访中。
2 讨论
真性红细胞增多症是一种以克隆性红细胞增多为主的骨髓增生性疾病,临床少见,初诊时易误诊。研究表明,PV患者爆式红系集落形成单位(BFU-E)对胰岛素样生长因子(IGF-I)敏感性增加100倍以上,PV患者外周血单个核细胞予IGF-I后,酪氨酸磷酸化水平迅速增加,且PV血浆中IGF-I结合蛋白(IGFBP-3)高正常人4倍。其IGF-I受体β亚单位的基础酪氨酸磷酸化水平较高[2]。研究显示在血管炎性疾病中,胰岛素内皮生长因子、相关受体及胰岛素内皮生长因子结合蛋白的改变被认为参与了血管炎性疾病的发病[3]。如果本患者的血管炎是PV的直接并发症,笔者推测,IGF-I可能是PV的治病因子之一。
皮肤血管炎的疾病中,有学者发现真皮淋巴细胞Bcl-2的高度表达和(FasCD95)表达缺失可能是白塞病皮肤症状慢性周期性发作的原因[4];而在过敏性紫癜患者的IgA1与血管内皮细胞的24 h共培养中,Bax/Bcl-2信号通路与血管内皮细胞的相关[5];有关PV的研究中,EPO介导抗凋亡蛋白Bcl-2高表达是维持红系祖细胞生存的重要机制。在细胞凋亡的机制研究中,Bcl-2高表达,凋亡指数低,Bcl-2低表达或不表达,则凋亡指数高。多个已研究的皮肤血管炎的致病原因与Bcl-2的表达有关,同时在PV的研究中,也观察到Bcl-2的表达增加,提示Bcl-2在皮肤变应性血管炎与PV之间可能存在一定的联系,需要进一步研究证实。
此外,患者因PV服用羟基脲,故不能排除皮肤变应性血管炎为原发疾病,羟基脲可能为致病药物,相关的发病机制不清。羟基脲可以阻止核苷酸还原为脱氧核苷酸,因而选择性地抑制DNA的合成,能抑制胸腺嘧啶核苷酸掺入DNA,并能直接损伤DNA,但对RNA及蛋白质的合成并无抑制作用[6]。其导致血管炎的可能机制是干扰了细胞复制必要的组织修复。羟基脲也导致宏观性红细胞增多症和降低红细胞变形能力,这可能会减少组织氧合和进一步诱发血管炎及溃疡的发生。同时,其可能的机制也包括羟基脲使红细胞平均体积增大,进而影响红细胞变形能力导致微循环障碍继而局部出现血管炎包括严重溃疡的产生[7]。
大约40%的PV患者伴发瘙痒症[8]。其机制尚不清楚,有研究表明,一些物质例如前列腺素E2(PGE2)和五羟色胺,由血小板生产和释放,可以诱发瘙痒。抗组胺类药物可能有效。针对该问题国外曾进行过少量病例数的研究,西咪替丁、补骨脂素光化学疗法(PUVA)及紫外线光疗对PV伴发的瘙痒症有效,且窄谱中波紫外线(UVB)照射治疗效果显著。补充铁制剂可缓解PV患者瘙痒,但停用后可复发,生物制剂如α干扰素和选择性血清素再摄取抑制剂也可改善瘙痒症状。
本病治疗原则是:恢复血容量和红细胞容量使之接近正常,抑制骨髓造血功能。静脉放血疗法,放、化疗及生物制剂是目前临床治疗PV的3种主要方法。静脉放血可在短时间内使血容量降至正常,以助症状减轻;化疗药物首选羟基脲,对PV有良好的骨髓造血抑制作用,且羟基脲临床上不易导致致白血病的发生。如外周血白细胞稳定维持在(3.5~5.0)×109/L,临床即可长期间歇应用羟基脲化疗。烷化剂、三尖杉酯碱、α干扰素有抑制细胞增殖作用,治疗本病有确切疗效,临床可适当选用。放射性磷32P可以控制PV,但需间歇治疗。近些年有报道指出,应用放化疗可能诱发真红恶性变,临床上应尽量减少或者避免放疗。伴发皮肤科疾病按具体病症对症治疗。
PV发病率较低,且于皮肤科就诊时易被误诊。鉴于近年来对PV的发病机制研究一直没有取得明确进展,可以考虑从合并症入手,为阐述PV的发生发展增加一个新的切入点,也可作为病情转归的一个预警,如变应性血管炎的出现,是否是急性白血病发病前的一个信号?有待医者们进一步研究与总结。
参考文献:
[1] 唐嫕文,张理涛.以皮肤瘙痒为首发症状的真性红细胞增多症1例[J] .中国中西医结合皮肤性病学杂志,2014,13(6):393-394.
[2] Correa PN,Eskinazi D,Axelrad AA.Circulating erythroid progenitors in polycythemia vera are hypersensitive to insulin-like growth factor-1 in vitro:studies in an improved serum-free medium[J] .Blood,1994,83:99-112.
[3] Bideci A,Camurdan MO,Cinaz P,et al.Serum zinc,insulin-like growth factor-Ⅰand insulin-like growth factor binding protein-3 levels in children with type 1 diabetes mellitus[J] .J Pediatr Endocrinol Metab,2005,18:1007-1011.
[4]YS,Yildiz L,Sentürk N,et al.Fas(CD95)and bcl-2 expression in active skin lesions of Behçet's disease[J] .J Eur Acad Dermatol Venereol,2005,19:569-572.
[5] Yuan P,Bo Y,Ming G,et al.Apoptosis of human umbilical vein endothelial cells(HUVEC)induced by IgA1 isolated from Henoch-Schonlein purpura children[J] .Asian Pac J Allergy Immunol,2014,32:34-38.
[6] Pan TD,McDonald CJ.Cytotoxic agents.In:Wolverton SE,ed.Comprehensive dermatologic drug therapy[M] .Philadelphia:W.B.Saunders Company,2001:180-204.
[7] Sirieix ME,Debure C,Baudot N,et al.Leg ulcers and hydroxyurea:forty-one cases[J] .Arch Dermatol,1999,135:818-820.
[8] Saini KS,Patnaik MM,Tefferi A.Polycythemia vera-associated pruritusandits management[J] .EurJClinInvest,2010,40:828-834.
