HPLC—ELSD测定安神宝颗粒中3种成分
2018-05-14李丽丽田海伟李晋张赞冯玉蓉哈婧
李丽丽 田海伟 李晋 张赞 冯玉蓉 哈婧


摘要:为完善安神宝颗粒的质量控制标准,采用高效液相色谱法同时测定安神宝颗粒中酸枣仁皂A、东莨菪内酯、槲皮素3种有效成分,采用Agilent Zorbox SB C18色谱柱(4.6 mm×150 mm,5 μm)及蒸发光散射检测器,柱温35 ℃,流动相为甲醇-0.5%的冰醋酸水溶液,梯度洗脱,流速为1.0 mL/min,进样量10 μL。结果表明,在该色谱条件下,3种有效成分均完全分离,峰面积对数与进样量对数呈良好的线性关系(r=0.995 6~0.998 0);精密度、重复性、稳定性试验结果符合要求,各被测组分的平均回收率在94.74%~96.08%之间。液相色谱法操作简单,准确度、灵敏度高,可用于检测安神宝颗粒中的有效成分,对完善安神宝颗粒质量标准,提升药品的质量控制水平具有实际意义。
关键词:色谱分析;高效液相色谱法;安神宝颗粒;酸枣仁皂苷A;东莨菪内酯;槲皮素;质量标准
中图分类号:R283;R284.1文献标志码:A
Determination of 3 ingredients in Anshenbao
granules by HPLC-ELSD
LI Lili1, TIAN Haiwei1, LI Jin1, ZHANG Zan2, FENG Yurong2, HA Jing1
(1.School of Chemical and Pharamaceutical Engineering, Hebei University of Science and Technology, Shijiazhuang, Hebei 050018, China;2. Hebei Yuzhilin Pharmaceutical Company Limited, Xingtai, Hebei 054400, China)
Abstract:In order to improve the quality control standard of Anshenbao granules, a high performance liquid chromatography (HPLC) method is developed for the determination of three active ingredients including Jujuboside A, Scopoletin and Quercetin in Anshenbao granules. The analysis is performed on a Agilent Zorbox SB C18 column(4.6 mm×150 mm,5 μm) with a gradient mobile phase of methanol-0.5% glacial acetic acid at a flow rate of 1.0 mL/min. The evaporative light scattering detector(ELSD) is used, the column temperature is 35 ℃, and the injection is 10 μL. The three active ingredients are separated completely under the given chromatogram system with a good linearity (r=0.995 6~0.998 0) of peak area and the injection. The results of precision, repeatability and stability experiments can meet the requirement, and the mean recoveries of each active ingredients are all in the range of 94.74%~96.08%. The analytical method is simple, accurate and sensitive, and it can be used for determination of active ingredients in Anshenbao granules. It is of practical significance to improve the quality standard of Anshenbao and improve the quality control of medicine.
Keywords:chromatographic analysis; HPLC; Anshenbao granules; jujuboside A; scopoletin; quercetin; quality standard
安神寶颗粒具有补肾益精、养心安神的功效,用于治疗失眠健忘、眩晕耳鸣、腰膝酸软等疾病[1],处方组成中包括酸枣仁、枸杞子与藤合欢,组方科学、配伍合理。其中,酸枣仁药材中含有生物碱、皂苷、氨基酸、阿魏酸、维生素C、植物甾醇、环磷酸腺苷及微量元素等多种成分[2-11];枸杞子药材中含有枸杞多糖、枸杞黄酮、甜菜碱、类胡萝卜素、类胡萝卜素酯、维生素C、莨菪亭、多种氨基酸及微量元素等多种成分[10-14];藤合欢中主要含有黄酮类化合物[10-11,15-21]。安神宝颗粒的质量标准收载于《中华人民共和国药典》[1],仅采用薄层鉴别、正丁醇提取物来进行质量控制,不能很好地控制安神宝颗粒的质量。
安神宝颗粒中3种成分本试验综合考虑药材中的有效成分,建立了液相色谱法[19]同时测定安神宝颗粒中酸枣仁皂A、东莨菪内酯、槲皮素3种有效成分的测定方法,并进行了方法学验证。结果表明,该方法分离度好,精密度高,加标回收率结果令人满意,对完善安神宝颗粒质量标准,提升药品的质量控制水平具有重要意义。
1实验仪器与试药
1.1仪器
LC-16液相色谱仪,岛津科学仪器有限公司提供;UM500蒸发光散射检测器,上海通微分析技术有限公司提供;FA1104N万分之一电子天平,上海民桥分析仪器有限公司提供;BT25S十万分之一电子天平,德国赛多利斯分析仪器有限公司提供;RE-52A旋转蒸发器,上海亚荣生化仪器厂提供。
1.2药品与试剂
安神宝颗粒样品(批号为161201,161202,161203,河北御芝林药业有限公司提供);酸枣仁皂苷A(批号为110814-201409)、东莨菪内酯(批号为110768-200504)、槲皮素(批号为100081-201509)(均购自中国食品药品检定研究院);甲醇(色谱纯),无水乙醇、冰醋酸、盐酸、三氯甲烷(分析纯,北京化工厂提供);氯化钠、无水硫酸钠(分析纯,国药试剂);水为超纯水。
2方法与结果
2.1色谱条件
色谱柱:Agilent Zorbox SB C18(4.6 mm×150 mm,5 μm);流动相:甲醇-0.5%冰醋酸梯度洗脱(洗脱程序见表1);检测器:蒸发光散射检测器;流速:1 mL/min;载气:高纯氮气;流速:2.5 L/min;漂移管温度:75 ℃;进样量:对照品进样量5 μL与10 μL,样品进样量10 μL;柱温:35 ℃。
2.2溶液的配制
1)对照品储备液
精密称取酸枣仁皂苷A5.0 mg、东莨菪内酯8.4 mg、槲皮素10.3 mg,分别置于10 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照品储备液。
2)混合对照品溶液
分别精密量取上述对照品储备液1.0 mL,置于同一个20 mL容量瓶中,加入甲醇定容至刻度,摇匀,制成含酸枣仁皂苷A25.0 μg、东莨菪内酯42.0 μg、槲皮素51.5 μg作为对照品溶液。
3)供试品溶液
取本品粉末(过4号筛)约1.0 g,精密称定,置于具塞锥形瓶中,精密加入70%(体积分数,下同)乙醇50 mL,称定重量,加热回流6 h,放冷,再称定重量,用70%乙醇补足减失的重量,摇匀,滤过。精密量取续滤液25 mL,置烧瓶中,浓缩至约1 mL,加3 mol/L盐酸溶液10 mL,水浴中加热水解2 h,立即冷却,移入分液漏斗中,用水10 mL分次洗涤容器,并入分液漏斗中,加氯化钠2 g,用三氯甲烷强力振摇提取5次,每次15 mL,合并三氯甲烷液,加无水硫酸钠2 g,搅拌,滤过,容器用少量三氯甲烷洗涤,滤过,滤液合并,70 ℃以下浓缩至近干,立即加甲醇使之溶解,转移至10 mL量瓶中,并稀释至刻度,摇匀,即得供试品溶液。
4)阴性对照溶液制备
按处方工艺制备不含酸枣仁、枸杞子、藤合欢药材的阴性样品,依“2.2”项下供试品溶液制备方法制备阴性对照品溶液。
2.3系统适应性试验
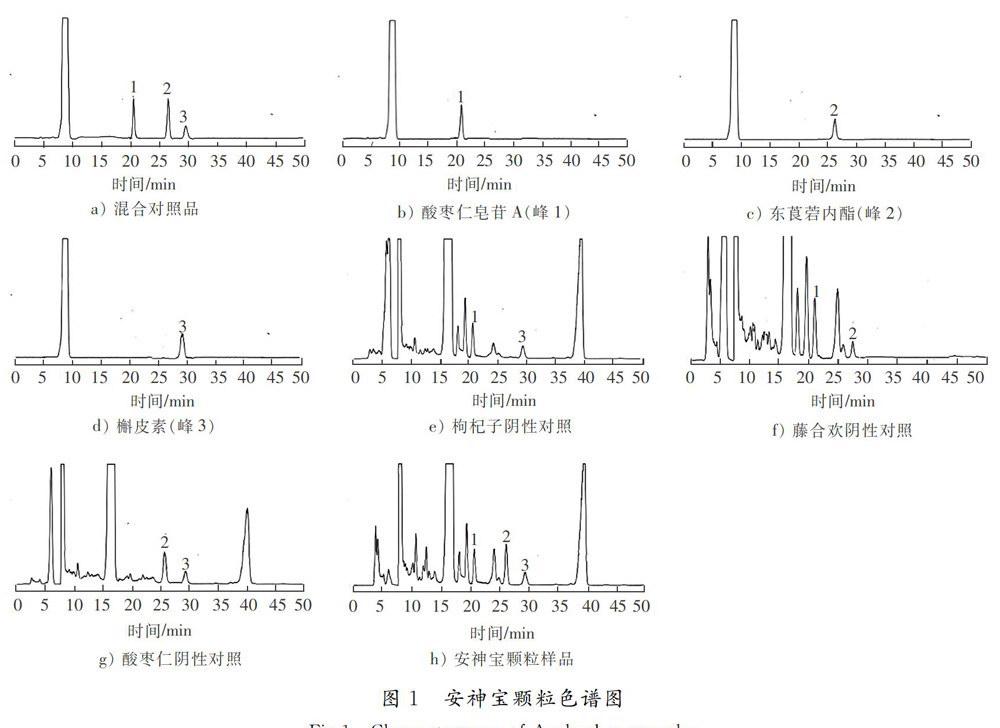
取混合对照品溶液、阴性样品溶液及供试品溶液,按“2.1”项下色谱条件进样分析。结果表明,各成分之间无干扰,混合对照品溶液中各色谱峰的理论塔板数均大于4 000,各相邻峰的分离度大于1.5,色谱图见图1。
2.4线性关系考察
精密量取混合对照品储备液0.1,0.3,0.5,0.7,1.0 mL,分别置于20 mL量瓶中,加甲醇稀释至刻度,摇匀,按“2.1”项下色谱条件进行分析,以进样量(μg)的对数为横坐标,峰面积A的对数为纵坐标进行线性回归,结果见表2。
2.5精密度试验
精密量取混合对照品溶液,按“2.1”项下色谱条件进样分析,连续进样6次,测定峰面积。酸枣仁皂苷A、东莨菪内酯、槲皮素的RSD值分别为1.9%,1.0%,1.2%(n=6),表明色谱系统精密度良好。
2.6重复性试验
取安神宝颗粒(批号为161201)约1.0 g,按“2.2”项下制备供试品溶液6份,按“2.1”色谱条件进样分析,记录色谱图,按外标两点对数法计算结果,得到酸枣仁皂苷A、东莨菪内酯、槲皮素的RSD值分別为2.0%,1.8%,2.2%(n=6),表明系统重复性良好。
2.7供试品稳定性试验
取安神宝颗粒(批号为161201)约1.0 g,按“2.2”项下供试品溶液制备方法制备供试品溶液,分别在0,3,6,9,12,15,21,24 h按“2.1”色谱条件进样分析,记录色谱图,按外标两点对数法计算结果,得到酸枣仁皂苷A、东莨菪内酯、槲皮素RSD分别为2.5%,2.8%,2.0%(n=8),表明样品在24 h内稳定性良好。
2.8检出限与定量限
取各对照品储备液,用甲醇逐级稀释,按“2.1”项下色谱条件进样分析,以信噪比S/N=10为定量限,酸枣仁皂苷A、东莨菪内酯、槲皮素的定量限分别为1.0,0.8,0.8 g/L;以信噪比S/N=3为检测限,分别为0.1,0.05,0.05 g/L。
2.9回收率试验
精密称取安神宝颗粒(批号为161201)样品约1 g,共9份,分别精密加入上述混合对照品溶液0.7,0.8,0.9 mL,每个浓度平行3份,按“2.2”项下供试品溶液制备方法制备供试品溶液,按“2.1”项下色谱条件进样分析,记录色谱图,按外标两点对数法计算,结果见表3。
2.10中间精密度试验
按“2.1”项下色谱条件,由不同操作人员于不同日期测定同一药品,按外标两点对数法计算样品中酸枣仁皂苷A、东莨菪内酯、槲皮素的RSD值分别为2.24%,1.03%,1.91%(n=5),表明仪器的中间精密度良好。
2.11样品测定
取安神宝颗粒样品(批号为161201,161202,161203),按“2.2”项下供试品溶液制备方法制备供试品溶液,每批平行2 份,按“2.1”色谱条件进样分析,按外标两点对数法计算3批样品中酸枣仁皂苷A、东莨菪内酯、槲皮素的含量,结果见表4。
3讨论
本方法针对安神宝颗粒现行质量标准未进行含量测定的问题,提出了对安神宝颗粒同时进行多成分含量测定的方法。将酸枣仁中具有安神功效的主要成分(酸枣仁皂苷A)、枸杞中具有镇静功效的成分(东莨菪内酯)、藤合欢主要成分(槲皮素)作为含量测定参数,使安神宝颗粒的质量标准更具有整体性、特征性和稳定性,并且对检测器、检测波长、色谱流动相等进行了反复研究、优化。通过多指标成分的定量控制,能够综合反映安神宝颗粒的内在质量,提升制剂的质量控制水平,为质量标准的提升做好前期准备。
3.1检测波长的研究确定
几个主要成分的紫外吸收波长各不相同,并且紫外检测背景干扰比较大。为了更好地同时适用多个成分的检测,采用蒸发光散射检测器(HPLC-ELSD)。
3.2流动相的研究
对照品溶液的配制:分别精密称取酸枣仁皂苷A、酸枣仁皂苷B、东莨菪内酯、甜菜碱、槲皮素对照品适量,加甲醇溶液分别配制成0.1 g/L的溶液,作为对照品溶液。首先采用以下流动相进行预试验,色谱柱:Agilent Zorbox SB C18(4.6 mm×150 mm,5 μm),柱温35 ℃,流速1.0 mL/min,蒸发光散射检测器检测,结果如下。
1)流动相为0.5%冰醋酸-甲醇(32∶68,体积比,下同)
分别进样酸枣仁皂苷A、酸枣仁皂苷B、东莨菪内酯、甜菜碱、槲皮素对照品溶液,检出酸枣仁皂苷A、酸枣仁皂苷B、东莨菪内酯、槲皮素,东莨菪内酯及槲皮素出峰时间过早无法分离。
2)流动相为水-甲醇-乙酸(45∶50∶5)
分别进样酸枣仁皂苷A、酸枣仁皂苷B、东莨菪内酯、甜菜碱、槲皮素对照品溶液,检出酸枣仁皂苷A、酸枣仁皂苷B、东莨菪内酯、槲皮素,槲皮素出峰时间过早无法分离,枣仁皂苷A、酸枣仁皂苷B出峰时间过长,峰形不符合要求。
3)流动相为甲醇-水-冰醋酸(32∶68∶0.16)
分别进样酸枣仁皂苷A、酸枣仁皂苷B、东莨菪内酯、甜菜碱、槲皮素对照品溶液,检出槲皮素、其他峰形不符合要求。
根据以上试验结果,同时检测多成分需要进行梯度洗脱分离各类成分。
4)流动相梯度洗脱研究
流动相:A为甲醇,B为0.5%冰醋酸进行梯度洗脱,流动相比例在变化过程中有临界比例,到达临界比例时吸收值会出现较大变化,干扰样品的检测,对几个对照品的出峰均产生干扰。调整梯度斜率,改变位置和峰形,将梯度系统改为渐变系统,减少流动相吸收值突然变化对对照品出峰的干扰。试验发现峰形得到一些改善,其中酸枣仁皂苷A、槲皮素峰形良好,酸枣仁皂苷B、东莨菪内酯、甜菜碱出峰时间处于流动相梯度改变区间,达不到基线分离。继续调整流动相各区间的梯度,峰形改善,酸枣仁皂苷A、酸枣仁皂苷B、东莨菪内酯、甜菜碱、槲皮素出峰时间均处于流动相配比稳定区间,达到基线分离。调整梯度系统,增加30%A流动相的冲洗时间,甜菜碱无出峰,槲皮素、酸枣仁皂苷A、东莨菪内酯出峰良好,无干扰,酸枣仁皂苷B出峰與杂质峰部分重叠,达不到分离。
3.3供试品溶液制备研究
梯度系统用对照品进行研究,由于样品中杂质较多,样品精制方法决定了杂质是否对待测成分产生干扰,本试验进行了供试品溶液精制方法研究。
1)精密称取样品2 g至10 mL的容量瓶中,超声提取20 min,放至室温,用甲醇定容,充分摇匀,过0.45 μm的微孔滤膜,作为供试品溶液1。
2)称取样品2 g于索氏提取器中,加50 mL石油醚,水浴加热提取2 h,弃去石油醚,再用50 mL甲醇索氏提取3 h,收集甲醇提取液,回收甲醇并定量转移至10 mL的容量瓶中,用甲醇定容,充分摇匀,过0.45 μm的微孔滤膜,作为供试品溶液2。
结果发现:供试品溶液1由于无除杂步骤,杂质峰对待测峰产生严重干扰;供试品溶液2除杂不完全,杂质峰仍有干扰;本试验中使用的方法由于加入水解除杂步骤,甜菜碱无出峰,槲皮素、酸枣仁皂苷A、东莨菪内酯出峰良好,无干扰,酸枣仁皂苷B出峰与杂质峰部分重叠,达不到分离。最终选择酸枣仁皂苷A、东莨菪内酯、槲皮素作为指标成分对安神宝颗粒进行质量控制,以完善其质量标准。
4结语
安神宝颗粒作为古典名方和中药保护品种,由枸杞子、酸枣仁、藤合欢组成,疗效确切。目前其质量控制方法相对单一,不能很好地反映安神宝颗粒的内在质量。本试验建立了安神宝颗粒含量的测定方法,灵敏度高、重复性好,可作为对安神宝颗粒质量进行科学评价和全面控制的参考依据。
参考文献/References:
[1]国家药典委员会.中华人民共和国药典[M]. 北京:中国医药科学出版社,2015:885.
[2]赵启铎,舒乐新.酸枣仁总皂苷的含量测定[J].天津中医药大学学报,2013,32(4):229-231.
ZHAO Qiduo, SHU Lexin. Determination of total saponins from semen ziziphi spinosae [J].Journal of Tianjin University of Traditional Chinese Medicine, 2013,32(4):229-231.
[3]郭慧,李斯,郑玉光.酸枣仁质量控制研究[J].河北中医药学报,2017,32(1):35-39.
GUO Hui, LI Si, ZHENG Yuguang.Study on jujube seed quality control[J]. Journal of Hebei Traditional Chinese Medicine and Pharmacology, 2017,32(1):35-39.
[4]夏海燕.复方酸枣仁颗粒质量标准研究[J].世界中西医结合杂志,2017,12(6):787-790.
XIA Haiyan.Research on the quality standards of compound suanzaorengranule[J].World Journal of Integrated Traditional and Western Medicine, 2017,12(6):787-790.
[5]李秋玲,王二丽,郭素华.中药酸枣仁镇静催眠化学成分及药理作用[J].天津药学,2010,22(5):59-61.
LI Qiuling, WANG Erli, GUO Suhua.sedative and hypnotic constituents of Chinese wild jujube seed and their pharmacological actions[J].Tianjin Pharmacy, 2010,22(5):59-61.
[6]李铮,任爽,常增荣,等.中药酸枣仁饮片中3种成分的含量比较研究[J].中国新药杂志,2017,26(1):91-96.
LI Zheng, REN Shuang, CHANG Zengrong,et al. Content comparison of three components in ziziphi spinosae semen pieces[J].Chinese Journal of New Drugs,2017,26(1):91-96.
[7]刘魁,陈向民,戎欣玉,等. 酸枣仁药材的质量标准研究[J]. 河北科技大学学报, 2009, 30(2):103-108.
LIU Kui,CHEN Xiangmin,RONG Xinyu, et al.Research on quality standard of semen ziziphispinosae[J].Journal of Hebei University of Science and Technolog, 2009, 30(2):103-108.
[8]杨军宣,周年华,张建刚,等.HPLC-ELSD法同时测定复方枣仁胶囊中酸枣仁皂苷A和B[J],中成药,2013,35(10):2179-2182.
YANG Junxuan, ZHOU Nianhua,ZHANG Jiangang,et al.Simultaneous determination of jujuboside A and jujuboside B in Compound Zaoren Capsules by HPLC-ELSD[J].Chinese Traditional Patent Medicine, 2013,35(10):2179-2182.
[9]隋利强,黄礼书,陈喆明. HPLC-UV和HPLC-ELSD法测定蜜炙酸枣仁中酸枣仁皂苷 A 含量的比较[J]. 广西中医药大学学报,2015,18(4):68-70.
[10]宋立人.现代中药学大辞典[M].北京:人民卫生出版社,2001.
[11]江苏新医学院.中药大辞典[M].上海:上海人民出版社,1977.
[12]张芳,郭盛,钱大玮,等. 枸杞子中多类型小分子化学物质研究开发现状及前景分析[J].中药材,2016,39(12):2917-2921.
[13]李建学, 樊祥富,刘学龙,等.枸杞化学成分及其药理作用的研究进展[J]. 食品安全导刊, 2016(24):75.
[14]高欢,万鸣.丙基酰胺键合硅胶柱用于测定枸杞子中甜菜碱含量的方法研究[J]. 湖北中醫杂志,2017,39(2):57-58.
[15]王萌.合欢花活性成分的分析及其与藤合欢镇静催眠作用药效的比较[D]. 锦州:辽宁医学院,2014.
WANG Meng. Analyse the Active Ingredient of Flos Albiziae and Compare the Effect of Sedative and Hypnotic of It with the Fruit of Celastrus Orbiculatus[D]. Jinzhou: Liaoning Medical School,2014.
[16]郭璐瑶,邓晶晶.采用HPLC同时进行连花清瘟颗粒多成分含量测定及其指纹图谱研究[J].食品工业科技,2017,38(1):287-291.
GUO Luyao, DENG Jingjing.Determination of multi components and analysis offingerprint of Lianhua Qingwen granules by HPLC[J]. Science and Technology of Food Industry ,2017,38(1):287-291.
[17]武雪,张平,张明童,等.HPLC同时测定瑞香狼毒中瑞香素、伞形花内酯和东莨菪内酯的含量[J].中国现代应用药学,2017,34(5):1171-1174.
WU Xue, ZHANG Ping, ZHANG Mingtong,et al.Simultaneous determination of daphnetin, umbelliferone and scopoletin in Stellera Chamejasme L. by HPLC[J]. Chinese Journal of Modern Applied Pharmacy, 2017,34(5):1171-1174.
[18]杨静,罗廷顺.清火栀麦片HPLC指纹图谱的建立和3种成分含量测定[J].中国药师,2017,20(4):673-677.
YANG Jing, LUO Tingshun.Establishment of the HPLC fingerprint of qinghuo zhimai tablets and determination of three constituents[J].China Pharmacist, 2017,20(4):673-677.
[19]陈华.高效液相色谱法在中药制剂有效成分含量测定中的应用[J].北方药学,2016,13(2):19.
[20]吴江瑞,齐广才,崔生飞,等.高效液相色谱法测定肠胃宁胶囊中6种成分的含量[C]//第二十届全国色谱学术报告会及仪器展览会论文集(第四分册). 西安:[s.n.]:151.
[21]姜鹏,詹常森.麝香保心丸中九种有效成分的含量测定[J].海峡药学,2017,29(6):45-48.
JIANG Peng, ZHAN Changsen.Simultaneous determination of nine bioactive components in Shexiang Baoxin pill[J].Strait Pharmaceutical Journal, 2017,29(6):45-48.
