尼洛替尼和伊马替尼治疗初诊CML-CP患者的疗效及不良反应比较
2018-05-08
慢性髓系白血病(chronic myeloid leukemia,CML)是一种恶性致死性克隆增殖性疾病,初诊患者多处在慢性期(CML-CP),随疾病进展可发展为加速期、急变期[1]。该病重要发病机制为9、22号染色体异位形成费城(Ph)染色体。Ph染色体表达融合基因BCR-ABL,进而产生BCR-ABL融合蛋白,持续激活酪氨酸激酶,抑制细胞凋亡[2]。酪氨酸激酶抑制剂(tyrosine kinase inhibitors,TKI)的问世给CML患者带来了福音。一代TKI伊马替尼可提高CML-CP患者的生存率,但约20%左右的患者对该药不耐受[3-4]。二代TKI尼洛替尼抑制BCR-ABLIS自体磷酸化能力较强,被批准用于治疗新诊断或伊马替尼耐药或不耐受的CML患者[5]。Larson等[6]发现,在治疗CML-CP初诊患者中,尼洛替尼组早期分子生物学反应获得率高于伊马替尼组,两组患者耐受性相当。美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)、欧洲白血病网络(European Leukemia Net,ELN)等指南已将尼洛替尼作为治疗CML-CP的一线药物[3]。本研究拟比较尼洛替尼和伊马替尼治疗CML-CP后早期分子生物学反应获得率,主要分子生物学反应(main molecular biological reaction,MMR)获得率,完全细胞遗传学缓解(complete cytogenetic remission,CCyR)获得率及药物不良反应情况,现报道如下。
1 资料与方法
1.1 一般资料 选取2017年1~10月安徽医科大学第一附属医院门诊随访的初诊为CML-CP且初诊时即服用尼洛替尼超过12个月的患者30例为观察组,其中男性18例,女性12例,平均年龄(41.23±13.79)岁。纳入标准:符合2015年NCCN指南中CML-CP的诊断标准[7],患者服药前生化指标、心功能无异常,初诊时即服用尼洛替尼且服药时间超过12个月,3、6、12个月于门诊进行随诊并完善骨髓分子生物学(BCR-ABLIS转录水平检测)、细胞遗传学(Ph染色体转录水平检测)、血常规、肝肾功能、血糖血脂、心电图检测,相关资料齐全。排除标准:不能定期门诊随诊,服药时间未满12个月,相关检测资料不全者。同时收集30例初诊为CML-CP且初诊时即服用伊马替尼超过12个月的患者为对照组,其中男性14例,女性16例,平均(40.97±12.19)岁。纳入、排除标准同尼洛替尼组。两组患者年龄、性别、服药时间等差异无统计学意义(P>0.05)。伊马替尼组有2例患者疗效不佳。
1.2 研究方法 尼洛替尼组患者予尼洛替尼(规格:每粒150或200 mg,瑞士诺华制药)300~400 mg,每12 h口服1次,服药前禁食2 h,服药后禁食1 h(选择600 mg 17例、800 mg 13例);伊马替尼组予伊马替尼(规格:每粒100 mg,瑞士诺华制药)400 mg,每天1次,进餐时服药。两组疗程均为12个月。观察两组患者服药后早期分子学反应获得率(3个月BCR-ABLIS≤10%、6个月BCR-ABLIS≤1%),MMR获得率(BCR-ABLIS≤0.1%),CCyR获得率(Ph+=0)及药物不良反应。总随访时间为12个月。两组患者服药前均需完善血常规、生化指标(肝肾功能、血糖血脂)、心电图、骨髓细胞学、Ph染色体、BCR-ABLIS融合基因等检查。药物治疗初期每周查血常规,每月复查肝肾功能、血糖、血脂等生化指标,监测心电图。3个月后,每月复查血常规、心电图,相关生化指标改为每3个月复查1次,总随访时间为12个月。服药 3、6、12个月行骨穿检查,监测Ph 染色体、BCR-ABLIS融合基因转录水平(标化的BCR-ABL融合基因结果以BCR-ABLIS表示)。
1.3 疗效评价 参照2013年ELN指南[8],观察其3、6、12个月的BCR-ABLIS转录水平(分子生物学反应),Ph染色体转录水平(细胞遗传学反应)。疗效最佳反应为:在细胞遗传学方面,达到CCyR ,即Ph+=0;在分子生物学方面,3个月至少BCR-ABLIS≤10%,6个月BCR-ABLIS≤1%(3、6个月BCR-ABLIS率即为早期分子生物学反应率);当BCR-ABLIS≤0.1%即为达到MMR。
1.4 不良反应评价 参考NCI / NIH 毒性标准分级[5]进行评估。
2 结果
2.1 疗效评价 3、6、12个月后,两组BCR-ABLIS≤10%、1%、0.1%获得率上,尼洛替尼组分别为80.0%、86.7%、60.0%,伊马替尼组分别为53.3%、63.3%、25.9%,两组差异均有统计学意义(χ2=4.800、4.356、6.175,P=0.028、0.037、0.013),3、6个月BCR-ABLIS转录水平为早期分子生物学反应;在MMR获得率上,尼洛替尼组分别为16.7%、46.7%、60.0%,伊马替尼组分别为6.7%、20.0%、25.9%,其中,治疗6、12个月时,两组差异有统计学意义(χ2=4.800、6.175,P=0.028、0.013);在细胞遗传学方面,两组患者3、6、12个月的CCyR获得率差异无统计学意义(83.3%比66.7%,90.0%比76.7%,92.0%比85.2%,χ2=2.222、1.920、0.591,P=0.136、0.166、0.442)。
2.3 不良反应评估 血液学毒性方面两组均表现为贫血,中性粒细胞、血小板减少。两组较严重的Ⅲ~Ⅳ级不良反应少见,大多数具有自限性或经药物对症治疗后恢复。仅尼洛替尼组中有1例患者因严重血小板减少,经药物对症治疗或适当减量后仍未完全恢复到正常值。非血液学不良反应伊马替尼主要表现为水肿,尼洛替尼主要表现脂肪酶、血糖、血脂的升高。除有3例患者出现Ⅲ-Ⅳ级程度的皮疹(尼洛替尼组2例,伊马替尼组1例),2例患者出现Ⅲ-Ⅳ级程度水肿(伊马替尼组2例),其余患者多为轻中度不良反应,大多数可自行恢复,较严重者经药物干预后恢复。详见表1。
3 讨论
TKI类药物的出现,提高了CML患者的生存率,并逐渐取代造血干细胞移植成为CML的首选治疗方法。第一代TKI伊马替尼已成为初诊CML患者的一线治疗药物,但仍有部分患者因产生耐药性导致治疗失败[9-10]。研究[11-14]显示,二代TKI尼洛替尼活性比伊马替尼高25~50倍,靶向抑制BCR-ABLIS的能力更强,同时能够抑制除T315I、Y253H、F359V/C、E255K/V以外的基因导致伊马替尼耐药性突变。有研究[15]显示,尼洛替尼(300或400 mg,12 h 1次)疗效优于伊马替尼(400 mg,每天1次)。2010年6月尼洛替尼被批准作为CML-CP患者的一线治疗药物[16]。
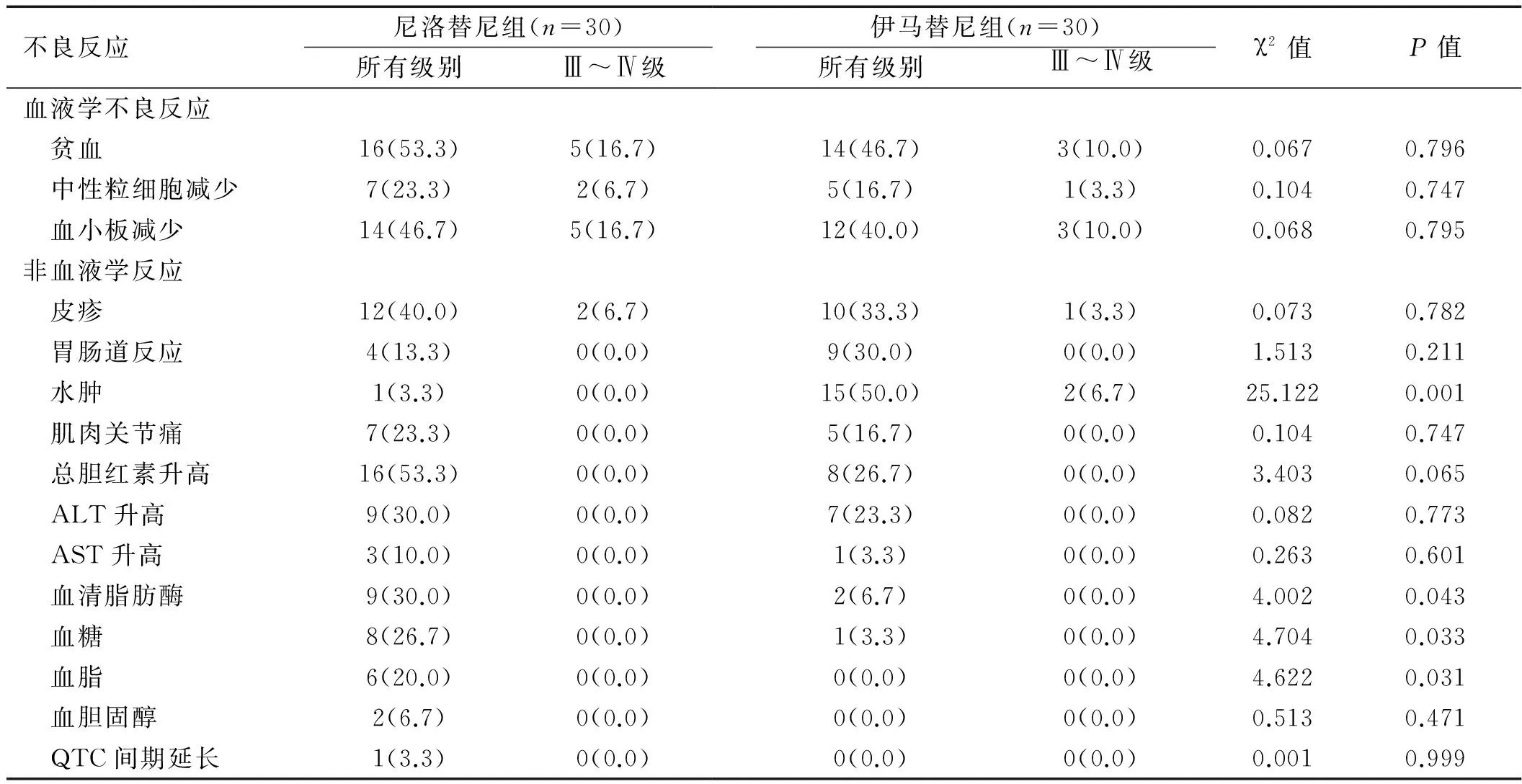
表1 两组患者药物不良反应比较[例(%)]
本研究发现,在早期分子生物学反应(3个月BCR-ABLIS<10%,6个月BCR-ABLIS<1%)获得率上尼洛替尼组优于伊马替尼组。Hughes等[17-18]研究显示,若使用TKI类药物治疗3个月时BCR-ABLIS<10%的患者,5年总体生存率(overallsurvival,OS)达94%,治疗6个月时,BCR-ABLIS<1%,5年OS为97%。同时,若TKI治疗3个月,BCR-ABLIS<10%的患者中其8年OS仍保持明显优势,远期预后获益较大。也有相关研究[19]显示,服用TKI类药物3个月时BCR-ABLIS水平达到疗效最佳标准,其预后较好。同时有报道[18]显示,尼洛替尼能更快降低CML患者的BCR-ABLIS转录水平,若延长临床试验时间,尼洛替尼在OS方面优势更明显。而本研究显示,尼洛替尼组患者较伊马替尼组有较高的早期分子生物学反应获得率,早期有更多的患者有较低的BCR-ABLIS转录水平,预示尼洛替尼组患者的5年OS较伊马替尼组患者高,远期预后更好。
本研究发现,60例CML-CP患者经TKI治疗3、6、12个月,尼洛替尼组在MMR获得率上优于伊马替尼组。有研究[5]显示,CML-CP患者越早获得MMR与其未来获得持续的分子生物反应、细胞遗传学反应密切相关。Ross等[20]认为,早期达到MMR的患者,有可能实现远期停药。本研究显示,尼洛替尼组患者早期就有较好的MMR获得率,预示着尼洛替尼组有更多的患者未来可获得持续的分子生物反应、细胞遗传学反应,甚至未来有部分患者达到远期停药,优势明显。
本研究还发现,在细胞遗传学方面,两组患者3、6、12个月的CCyR获得率上,尼洛替尼组高于伊马替尼组,但差异无统计学意义(P>0.05),这可能与本研究样本量少有关。
在药物不良反应方面,两组患者在血液学毒性方面,两组主要表现为贫血、中性粒细胞及血小板减少,其中Ⅲ-Ⅳ级不良反应少见。出现不良反应后大多数患者具有自限性或经药物治疗后血象可恢复,仅尼洛替尼组中1例患者因严重的血小板减少经药物对症治疗或适当减量后仍未完全恢复到正常值。两组血液学方面毒性反应较小。
在非血液学毒性反应方面,尼洛替尼组易导致血清脂肪酶、血糖、血脂升高,而伊马替尼组易导致水肿。其中大多数患者不良反应较轻,可自行恢复,Ⅲ-Ⅳ级程度不良反应少见,且经药物干预后恢复。该结果类似NESTTndⅢ期临床试验结果[15]。
综上所述,尼洛替尼一线治疗初诊CML-CP患者较伊马替尼疗效更优,其早期分子生物学反应及MMR获得率更高,副作用小,能使新诊断的CML-CP患者获得较长的生存期限。本研究样本量较少,随访时间较短,相关研究还需延长随访时间及增加患者例数来证实。
[1]PICCALUGAPP,PAOLINIS,BERTUZZIC,etal.First-linetreatmentofchronicmyeloidleukemiawithnilotinib:criticalevaluation[J].JBloodMed. 2012,3:151-156.
[2]SAGLIOG,KIMDW,ISSARAGRISILlS,etal.NilotinibversusImatinibfornewlydiagnosedchronicmyeloidleukemia[J].NEngJMed,2010,362(24):2251-2259.
[3] 石小岩,王睿,傅迪,等.早期应用尼洛替尼治疗慢性髓系白血病的疗效观察[J].实用药物与临床,2016,19(1):54-57.
[4]HOCHHAUSA,O′BRIENSG,GUlLHOTF,etal.Six-yearfollow-upofpatientsreceivingimatinibforthefirst-linetreatmentofchronicmyeloidleukemia[J].Leukemia,2009,23(6):1054-1061.
[5] 潘良琴,刘为星,朱雨,等.尼洛替尼和伊马替尼一线治疗慢性髓系白血病的疗效及安全性观察[J].南京医科大学学报(自然科学版),2015,35(6):827-832.
[6]LARSONRA,HOCHHAUSA,HUGHESTP,etal.NilotinibvsimatinibinpatientswithnewlydiagnosedPhiladelphiachromosome-positivechronicmyeloidleukemiainchronicphase:ENESTnd3-yearfollow-up[J].Leukemia,2012,26 (10):2197-2203.
[7]NationalComprehensiveCancerNetwork.NCCNclinicalpracticeguidclinesinoncology:chronicmyelogenousleukemia,V.2015[EB/OL].[2017-09-10].http://www.ascopost.com/issues/may-25-2015/nccn-clinical-practice-guidelines-in-oncology-nccn-guidelines-2015-updates/.
[8]BACCARANIiM,DEININGERMW,ROSTIG,etal.EuropeanleukemiaNetrecommend-ationsforthemanagementofchronicmyeloidleukemia: 2013[J].Blood,2013,122(6): 872-884.
[9]O′BRIENSG,GUILHOTF,LARSONRA,etal.Imatinibcomparedwithinterferonandlow-dosecytarabinefornewlydiagnosedchronic-phasechronicmyeloidleukemia[J].NEnglJMed,2003,348(11):994-1004.
[10]SACHAT.Imatinibinchronicmyeloldleukemia:anoverview[J].MediterrJHematolInfecDis,2014,6(1):e2014007.
[11]O′HARET,EIDECA,DEININGERMW.Bcr-Ablkinasedomainmutations,drugresistance,andtheroadtoacureforchronicmyeloidleukemia[J].Blood,2007,110(7):2242-2249.
[12]MANLEYPW,STIEFLN,COWAN-JACOBSW,etal.Structuralresemblancesandcomparisonsoftherelativepharmacologicalpropertiesofimatinibandnilotinib[J].BioorgMedChem,2010,18(19):6977-6986.
[13]KANTARJIANHM,GILESF,GATTERMANNN,etal.Nilotinib(formerlyAMN107),ahighlyselectiveBCR-ABLtyrosinekinaseinhibitor,iseffectiveinpatientswithPhiladelphiachromosomepositivechronicmyelogenousleukemiainchronicphasefollowingimatinibresistanceandintolerance[J].Blood,2007,110(10):3540-3546.
[14]NICOLINIFE,TURKINAA,SHENZX,etal.ExpandingNilotinibAccessinClinicalTrials(ENACT):anopen-label,multicenterstudyoforalnilotinibinadultpatientswithimatinib-resistantorimatinib-intolerantPhiladelphiachromosome-positivechronicmyeloidleukemiainthechronicphase[J].Cancer,2012,118 (1):118-126.
[15]ABUZZESEE,BRECCIAM,LATAGLIATAR,etal.Second-generationtyrosinekinaseinhibitorsinfirst-linetreatmentofchronicmyeloidleukaemia(CML)[J].BioDrugs,2014,28(1):17-26.
[16]KANTARJIANHM,HOCHHAUSA,SAGLIOG,etal.Nilotinibversusimatinibforthetreatmentofpatientswithnewlydiagnosedchronicphase,Philadelphiachromosome-positive,chronicmyeloidleukaemia:24-monthminimumfollow-upofthephase3randomisedENESTndtrial[J].LancetOncol,2011, 12(9):841-851.
[17]HUGHESTP,HOCHHAUSA,BRANFORDS,etal.Long-termprognosticsignificanceofearlymolecularresponsetoimatinibinnewlydiagnosedchronicmyeloidleukemia:ananalysisfromtheInternationalRandomizedStudyofInterferonandSTI571 (IRIS) [J].Blood,2010,116 (19): 3758-3765.
[18]MARIND,IBRAHIMAR,LUCASC,etal.AssessmentofBCRABL1transcriptlevelsat3monthsIstheonlyrequirementforpredictingoutcomeforpatientswithchronicmyeloidleukemiatreatedwithtyrosinekinaseinhibitors[J].JCliniOncol,2012,30(3):232-238.
[19]BRANFORDS,YEUNGDT,ROSSDM,etal.EarlymolecularresponseandfemalesexstronglypredictstableundetectableBCR-ABL1,thecriteriaforimatinibdiscontinuationinpatientswithCML[J].Blood,2013,121 (19): 3818-3824.
[20]ROSSDM,HUGHESTP.HowIdetermineifandwhentorecommendstoppingtyrosinekinaseinhibitortreatmentforchronicmyeloidleukaemia[J].BrJHaematol,2014,166(1):3-11.
