预防性造口对腹腔镜直肠癌低位前切除术后短期生活质量的影响
2018-05-07师文聪王楠尹智渊韦明光翟玉龙乔庆何显力
师文聪,王楠,尹智渊,韦明光,翟玉龙,乔庆,何显力
(空军军医大学唐都医院 胃肠外科,陕西 西安 710038)
近10年来,我国结直肠癌的发病率逐年上升,现已跃居为居民恶性肿瘤的第5位[1]。2012年中国癌症统计报告显示,直肠癌在结直肠癌中占比约70%,其中低位直肠癌占比约70%~80%[2]。低位直肠癌患者行前切除术后往往会面临一系列肠道症状,如腹泻、便频、便急、排便不尽感等,称之为低位前切除综合征(low anterior resection syndrome,LARS),是影响患者术后生活质量的重要原因之一[3-5]。预防性造口在低位直肠癌前切除术后的主要作用在于通过粪便转流预防吻合口漏或减轻吻合口漏症状的严重程度[6-9]。但是,是否需要预防性造口,目前仍有很多争议。积极主张预防性造口的学者主要看重其对吻合口的保护作用,但是也有学者认为预防性造口伴随的护理问题、精神心理压力及造口相关并发症等会影响患者术后的生活质量,故主张“能不做就不做”[10-14]。那么,预防性造口是否可以通过粪便转流在降低吻合口漏发生率的同时影响低位前切除综合征严重程度,并且影响术后生活质量呢?为此,本研究回顾性地分析了本中心98例低位直肠癌患者的临床资料及术后生活质量随访结果,现报告如下。
1 资料与方法
1.1 一般资料
采用回顾性病例对照研究方法分析98例低位直肠癌患者的临床病理资料及术后随访资料,其中男71例,女27例;年龄38~75岁,平均年龄(61.5±3.2)岁。98例患者均完成腹腔镜根治性低位前切除术,根据有无新辅助放化疗、患者造口意愿、吻合肠管断端血供及术中吻合情况决定是否行预防性造口,其中行预防性回肠造口48例(造口组),未行预防性回肠造口50例(未造口组)。48例预防性造口患者最终均完成造口还纳手术。无患者出现术后局部复发和远处转移。所有患者及家属术前均签署手术知情同意书。
1.2 纳入标准和排除标准
纳入标准:⑴ 年龄18~75岁;⑵ 病理确诊为直肠腺癌,术前硬质肠镜确定肿瘤下缘距肛缘≤7 cm;⑶ 完成腹腔镜根治性低位前切除术,临床及随访资料完整。排除标准:⑴ 合并其他系统恶性肿瘤;⑵ 姑息性手术;⑶ 临床及随访资料缺失。
1.3 资料收集
收集患者临床病理资料,包括性别、年龄、体质量指数(body mass index,BMI)、美国麻醉医师协会(A m e r i c a n S o c i e t y o f Anesthesiologists,ASA)分级、新辅助放化疗、手术时间、术中出血量、淋巴结清扫数目、吻合口漏、术后首次通气时间、术后住院日及病理资料。
术后低位前切除综合征和生活质量随访均已由我科随访人员完成。生活质量随访于前切除术后1、3、6、12个月进行,低位前切除综合征随访于还纳术后(造口组)和前切除术后(未造口组)1、3、6、12个月进行。随访形式采用面对面问卷调查或电话随访,所用量表为直肠低位前切除综合征评分量表[15]和欧洲癌症治疗研究组织发布的生活质量核心评价量表(quality of life questionaire core 30,QLQ-C30)[16]。
1.4 观察指标
观察指标为术后各随访时间点患者低位前切除综合征评分及生活质量评分。前切除综合征分值越高表示症状越重。在QLQ-C30评分量表的15个维度中,选择与低位前切除综合征症状最为相关的4个功能维度(即:躯体功能、角色功能、情绪功能、社会功能)、1个症状维度(即:疲劳)、2个单项维度(即:便秘和腹泻)和1个总体生活质量维度作为生活质量评价的观察指标,所有维度分值范围为0~100 分。功能维度以及总体生活质量维度分值越高,表明生活质量越高;症状维度分值越低,表明生活质量越高。
1.5 统计学处理
采用SPSS 19.0统计软件。计量资料以均数±标准差(±s)表示,组间比较采用独立样本t检验或协方差分析。分类变量用率表示,组间比较采用χ2检验或Fisher精确概率法检验。P<0.05为差异有统计学意义。
2 结 果
2.1 术前临床特征及临床病理资料
比较两组术前临床特征及临床病理资料,造口组接受新辅助放化疗的患者较多[6 2.5%(30/48)vs.24.0%(12/50),P<0.001],且术后病理分期较晚(P=0.008);其余两组间均无统计学差异(P>0.05)(表1-2)。。

表1 造口组与未造口组的术前临床特征比较Table 1 Comparison of preoperative clinical characteristics between ileostomy group and non-ileostomy group
指标 造口组(n=48)未造口组
(n=50)t/χ2P
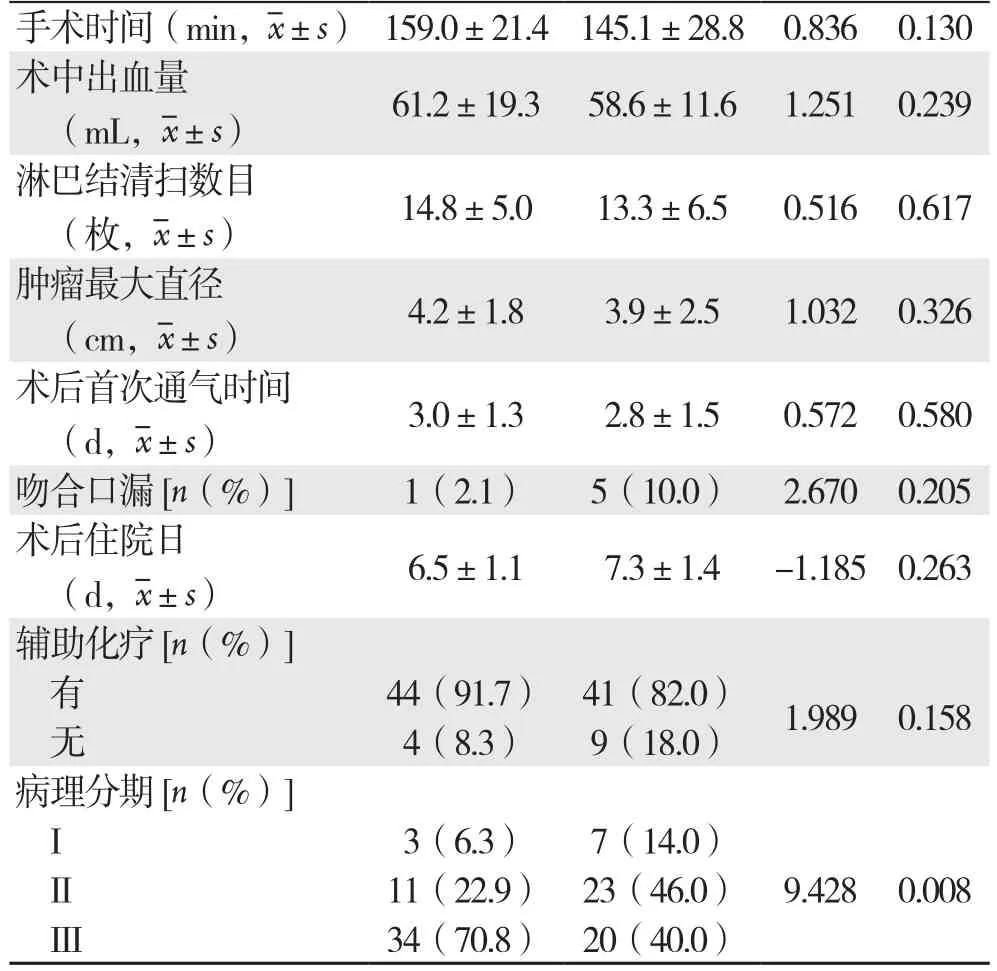
表2 造口组与未造口组的手术近期结果和临床病理特征Table 2 Comparison of short-term outcomes and clinicopathologic features between ileostomy group and non-ileostomy group
2.2 低位前切除综合征评分
两组经肛排便后低位前切除综合征评分均随时间的延长而下降,造口组还纳术后1年内低位前切除综合征评分较未造口组明显降低,差异有统计学意义(P<0.05)(表3)。根据有无新辅助放化疗史对所有患者进行亚组分析,结果显示无论是否接受新辅助放化疗,造口组还纳术后1年内低位前切除综合征评分均较未造口组对应随访时间点明显降低,差异有统计学意义(P<0.05)(表4)。
2.3 生活质量评分
造口组总体健康状况、躯体功能及情绪功能评分在术后3个月和6个月较高,社会功能和角色功能评分在术后3个月较高,腹泻状况在术后半年内较好,差异均有统计学意义(均P<0.05);疲劳和便秘评分组间比较无统计学差异(均P>0.05);其余随访时间点组间比较均无统计学差异(均P>0.05)(表5)。
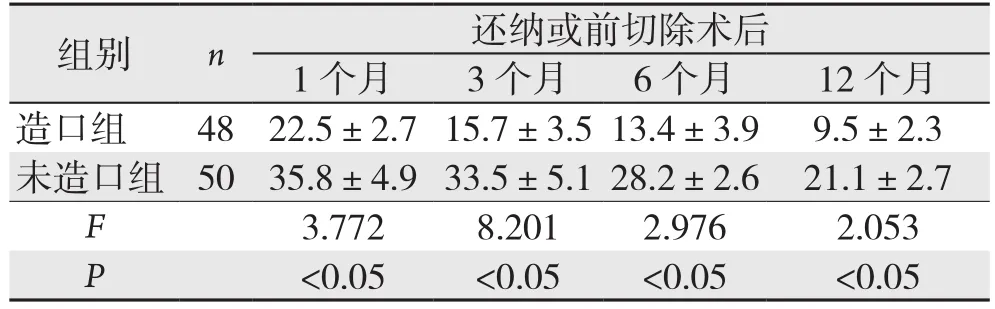
表3 两组低位前切除综合征评分比较Table 3 Comparison of scores for low anterior resection syndrome between the two groups

表4 两组新辅助放化疗相关的低位前切除综合征评分比较Table 4 Comparison of scores for low anterior resection syndrome related to neoadjuvant chemoradiotherapy between the two groups

表5 两组术后1年内生活质量评分比较Table 5 Comparison of scores for quality of life within postoperative one year between the two groups
3 讨 论
50%~90%的低位直肠癌患者行低位前切除术后会经历不同程度的低位前切除综合征[3,5,17],频繁腹泻、便频、便急及排不净感等症状对患者精神及躯体造成一定的打击,容易使患者产生对手术治疗不满意、无法坚持术后辅助化疗等情况,甚至造成患者睡眠障碍及抑郁等精神状况。通过预防性造口使粪便转流,可能会避免频繁腹泻、便频、肛门坠胀感等严重前切除综合征症状。然而,预防性造口的护理问题、造口相关并发症、二次手术以及患者心理上对造口的排斥等也会影响患者的生活质量。因此,低位直肠癌前切除术后是否行预防性造口,其潜在益处更大还是其负面影响更大,目前仍存在争议。
为此,笔者对本中心98例低位直肠癌保肛患者的临床资料及随访信息进行了回顾性分析。本研究中,12例行新辅助放化疗但未行预防性造口的患者中,7例是因为患者拒绝行预防性造口,5例因术中判断直肠残端血供丰富、吻合满意而未行造口。未造口组5例吻合口漏患者中有4例有新辅助放化疗史,两组吻合口漏发生率未见统计学差异可能与样本量较少有关。预防性造口的患者在经肛排便后(还纳后)低位前切除综合征症状较未造口组明显减轻,尤其是对于接受术前新辅助放化疗的患者。在低位前切除术后1年内,两组患者术后生活质量均随时间逐渐改善,预防性造口的患者生活质量优于未造口组,尤其是术后半年内,并且这种优势并未在造口还纳后因经肛排便而削弱。
低位前切除综合征的确切发生机制不明,涉及肛门括约肌损伤、“新直肠”顺应性降低、结肠运动功能紊乱、直肠肛门协调性反射缺乏、盆底神经损伤等机制[3,6,18-19]。预防性回肠造口在低位直肠癌前切除中的重要作用在于预防术后吻合口漏及减轻吻合口漏患者的临床症状[6-9]。但是,预防性回肠造口改善低位前切除综合征的确切机制仍不清楚,低位前切除术后低位前切除综合征可能与“新直肠”周围慢性炎症反应有关,术前放疗对盆腔组织的放射性损伤和粪便刺激会加重这种慢性炎症,导致前切除综合征症状加重。笔者认为,通过预防性回肠造口,一方面避免粪便对吻合口机械性刺激以及粪便所造成的吻合口周围的潜在感染,另一方面给予“新直肠”一定的恢复时间促进炎症反应消退,在适当的时间通过造口还纳实现经肛排便,这种“迂回策略”可以避免术后早期较为严重的低位前切除综合征症状。
笔者认为造口组生活质量较优可能与其低位前切除综合征症状较轻有关。Juul等[5]的研究显示,低位前切除综合征的严重程度与术后生活质量相关,低位前切除综合征症状越严重的患者生活质量越差。国内梁学敏等[20]也认为预防性回肠造口可以提高低位直肠癌保肛术后生活质量。早期经口进食,并且较早改善低蛋白、贫血及高分解代谢等术后常见状况也是造口组术后生活质量较优的原因[21-23]。造口护理问题被认为是影响患者情绪功能及降低生活质量的主要原因之一,而在本研究中,造口组术后3个月和6个月情绪功能优于未造口组,造口护理问题并未影响患者术后情绪功能及生活质量。笔者认为早期、及时的宣教和心理干预,使患者熟练掌握造口护理方法,可以避免造口护理等问题对患者情绪功能的影响[24]。造口护理问题不应该成为预防性造口实施的障碍。此外,本研究中也并未发现临床症状明显的转流性结肠炎患者。
另外值得关注的问题是造口相关并发症的预防和造口还纳时间的界定。造口相关并发症包括造口肠段缺血坏死、营养性并发症、切口感染、腹壁疝等[14,25-28]。笔者的经验是医患充分协商下选择造口位置、造口部位的腹壁开口大小适中及不过多缝合和游离小肠系膜可以有效避免造口肠段缺血。造口还纳时严格保持无菌原则、腹壁切口充分冲洗、预防性使用抗生素及有效确切的缝合可以降低切口感染及腹壁疝的发生。虽然造口还纳手术同样具有一定手术风险,但是笔者认为预防性造口对生活质量的改善更为重要。至于造口还纳时间的界定,目前尚无统一共识。国内外多主张术后早期在患者体力状况允许的情况下尽快还纳,术后辅助化疗期间手术会增加还纳术后并发症的发生率[29-31]。本中心造口还纳手术均在辅助化疗结束后进行。同时,在还纳术前行生理盐水保留灌肠,锻炼肛门括约肌的功能,确保可以保留45 min后方可进行还纳手术。患者多可于术后6~8个月完成造口还纳术。笔者认为,这种方法一方面可避免术后辅助化疗与还纳手术的相互影响,另一方面造口期间较好的生活质量也有利于提高术后辅助化疗的依从性。
综上,预防性回肠造口可以减轻低位直肠癌前切除术后前切除综合征症状的严重程度,改善术后短期生活质量。是否行预防性回肠造口,一方面需要结合患者自身疾病的特点,另一方面也需要有经验的外科医师来综合判断。
[1]Chen W, Zheng R, Baade PD, et al. Cancer statistics in China,2015[J]CA Cancer J Clin, 2016, 66(2):115–132. doi: 10.3322/caac.21338.
[2]赫捷, 陈万青. 2012中国肿瘤登记年报[M]. 北京: 军事医学科学出版社, 2012:100–101.Hao J, Chen WQ. Chinese Cancer Registry Annual Report [M].Beijing: Military Medical Science Press, 2012:100–101.
[3]Ridolfi TJ, Berger N, Ludwig KA. Low anterior resection syndrome: current management and future directions[J]. Clin Colon Rectal Surg, 2016, 29(3):239–245. doi: 10.1055/s-0036–1584500.
[4]Chen TY, Wiltink LM, Nout RA, et al. Bowel function 14 years after preoperative short-course radiotherapy and total mesorectal excision for rectal cancer: report of a multicenter randomized trial[J]. Clin Colorectal Cancer, 2015, 14(2):106–114. doi: 10.1016/j.clcc.2014.12.007.
[5]Juul T, Ahlberg M, Biondo S, et al. Low anterior resection syndrome and quality of life: an international multicenter study[J]. Dis Colon Rectum, 2014, 57(5):585–591. doi: 10.1097/DCR.0000000000000116.
[6]Thoker M, Wani I, Parray FQ, et al. Role of diversion ileostomy on low rectal cancer: a randomized controlled trial[J]. Int J Surg, 2014,12(9):945–951. doi: 10.1016/j.ijsu.2014.07.012.
[7]Mongin C, Maggiori L, Agostini J, et al. Does anastomotic leakage impair functional results and quality of life after laparoscopic sphincter-saving total mesorectal excision for rectal cancer? A casematched study[J]. Int J Colorectal Dis, 2014, 29(4):459–467. doi:10.1007/s00384–014–1833-y.
[8]Tan WS, Tang CL, Shi L, et al. Meta-analysis of defunctioning stomas in low anterior resection for rectal cancer[J]. Br J Surg,2009, 96(5):462–472. doi: 10.1002/bjs.6594.
[9]Matthiessen P, Hallböök O, Rutegård J, et al. Defunctioning stoma reduces symptomatic anastomotic leakage after low anterior resection of the rectum for cancer: a randomized multicenter trial[J].Ann Surg, 2007, 246(2):207–214.
[10]den Dulk M, Smit M, Peeters KC, et al. A multivariate analysis of limiting factors for stoma reversal in patients with rectal cancer entered into the total mesorectal excision (TME) trial: a retrospective study[J]. Lancet Oncol, 2007, 8(4):297–303. doi:10.1016/S1470–2045(07)70047–5.
[11]Tsunoda A, Tsunoda Y, Narita K, et al. Quality of life after low anterior resection and temporary loop ileostomy[J]. Dis Colon Rectum, 2008, 51(2):218–222. doi: 10.1007/s10350–007–9101–7.
[12]Saha AK, Tapping CR, Foley GT, et al. Morbidity and mortality after closure of loop ileostomy[J]. Colorectal Dis, 2009, 11(8):866–871. doi: 10.1111/j.1463–1318.2008.01708.x.
[13]Abegg RM, Brokelman W, van Bebber IP, et al. Results of construction of protective loop ileostomies and reversal surgery for colorectal surgery[J]. Eur Surg Res, 2014, 52(1/2):63–72. doi:10.1159/000357053..
[14]Ihnát P, Guňková P, Peteja M, et al. Diverting ileostomy in laparoscopic rectal cancer surgery: high price of protection[J]. Surg Endosc, 2016, 30(11):4809–4816.doi: 10.1007/s00464–016–4811–3.
[15]Emmertsen KJ, Laurberg S. Low anterior resection syndrome score: development and validation of a symptom-based scoring system for bowel dysfunction after low anterior resection for rectal cancer[J]. Ann Surg, 2012, 255(5): 922–928. doi: 10.1097/SLA.0b013e31824f1c21.
[16]Aaronson NK, Ahmedzai S, Bergman B, et al. The European Organization for Research and Treatment of Cancer QLQ-C30: a quality-of-life instrument for use in international clinical trials in oncology[J]. J Natl Cancer Inst, 1993, 85(5):365–376.
[17]Emmertsen KJ, Laurberg S. Bowel dysfunction after treatment for rectal cancer[J]. Acta Oncol, 2008, 47(6):994–1003. doi:10.1080/02841860802195251.
[18]刘晓波, 童卫东. 直肠前切除综合征的研究进展[J]. 中华结直肠疾病电子杂志, 2015, 4(2):166–169. doi:10.3877/cma.j.issn.2095–3224.2015.02.12.Liu XB, Tong WD. Research progress of anterior rectal resection syndrome[J]. Chinese Journal of Colorectal Diseases, 2015,4(2):166–169. doi:10.3877/cma.j.issn.2095–3224.2015.02.12.
[19]Ziv Y, Zbar A, Bar-Shavit Y, et al. Low anterior resection syndrome(LARS): cause and effect and reconstructive considerations[J]. Tech Coloproctol, 2013, 17(2):151–162. doi: 10.1007/s10151–012–0909–3.
[20]梁学敏, 张力, 谭康联, 等. 预防性造口在低位直肠癌保肛术中的应用[J]. 中国普通外科杂志, 2017, 26(4):533–536. doi:10.3978/j.issn.1005–6947.2017.04.022.Liang XM, Zhang L, Tan KL, et al. Use of preventive stoma in rectum preserving operation for low level rectal cancer[J]. Chinese Journal of General Surgery, 2017, 26(4):533–536. doi:10.3978/j.issn.1005–6947.2017.04.022.
[21]Greco M, Capretti G, Beretta L, et al. Enhanced recovery program in colorectal surgery: a meta-analysis of randomized controlled trials[J]. World J Surg, 2014, 38(6):1531–1541. doi: 10.1007/s00268–013–2416–8.
[22]Vlug MS, Wind J, Hollmann MW, et al. Laparoscopy in combination with fast track multimodal management is the best perioperative strategy in patients undergoing colonic surgery:a randomized clinical trial(LAFA-study)[J]. Ann Surg, 2011,254(6):868–875. doi: 10.1097/SLA.0B013e31821fd1ce.
[23]Byrne BE, Branagan G, Chave HS. Unselected rectal cancer patients undergoing low anterior resection with defunctioning ileostomy can be safely managed within an Enhanced Recovery Programme[J]. Tech Coloproctol, 2013, 17(1):73–78. doi: 10.1007/s10151–012–0886–6.
[24]Danielsen AK, Burcharth J, Rosenberg J. Patient education has a positive effect in patients with a stoma: a systematic review[J].Colorectal Dis, 2013, 15(6): e276–83. doi: 10.1111/codi.12197.
[25]王鸿鹄, 徐昊, 王振宁, 等. 低位直肠癌保肛患者行预防性回肠末端造瘘的优缺点[J]. 中华结直肠疾病电子杂志, 2015, 4(1):78–80.doi:10.3877/cma.j.issn.2095–3224.2015.01.20.Wang HH, Xu H, Wang ZN, et al. The advantages and disadvantages of protective ileostomy in low rectal cancer surgery [J]. Chinese Journal of Colorectal Diseases, 2015, 4(1):78–80. doi:10.3877/cma.j.issn.2095–3224.2015.01.20.
[26]Herrle F, Sandra-Petrescu F, Weiss C, et al. Quality of Life and Timing of Stoma Closure in Patients With Rectal Cancer Undergoing Low Anterior Resection With Diverting Stoma: A Multicenter Longitudinal Observational Study [J]. Dis Colon Rectum, 2016,59(4):281–290. doi: 10.1097/DCR.0000000000000545.
[27]Fazekas B, Fazekas B, Hendricks J, et al. The incidence of incisional hernias following ileostomy reversal in colorectal cancer patients treated with anterior resection[J]. Ann R Coll Surg Engl,2017, 99(4):319–324. doi: 10.1308/rcsann.2016.0347.
[28]Chow A, Tilney HS, Paraskeva P, et al. The morbidity surrounding reversal of defunctioning ileostomies: a systematic review of 48 studies including 6107 cases[J]. Int J Colorectal Dis, 2009,24(6):711–723. doi: 10.1007/s00384–009–0660-z.
[29]Lasithiotakis K, Aghahoseini A, Alexander D. Is early reversal of defunctioning ileostomy a shorter, easier and less expensive operation?[J]. World J Surg, 2016, 40(7):1737–1740. doi: 10.1007/s00268–016–3448–7.
[30]Waterland P, Goonetilleke K, Naumann DN, et al. Defunctioning ileostomy reversal rates and reasons for delayed reversal: does delay impact on complications of ileostomy reversal? a study of 170 defunctioning ileostomies[J]. J Clin Med Res, 2015, 7(9): 685–689.doi: 10.14740/jocmr2150w.
[31]黄榕康, 何丹丹, 赵洁等. 直肠癌保留括约肌术后预防性回肠造口回纳术后并发症的危险因素分析[J]. 中国普外基础与临床杂志, 2016, 23(11): 1335–1338.Huang RK, He DD, Zhao J, et al. Risk Factors of Complications Associated with Reversal of Defunctioning Ileostomy in Patients with Rectal Cancer Undergoing Sphincter Preservation Surgery [J].Chinese Journal of Bases and Clinics in General Suegery, 2016,23(11):1335–1338.
