非哺乳期乳腺炎的临床及钼靶X线诊断
2018-05-04赵如恩王芮陈瑧徐文彪
赵如恩, 王芮, 陈瑧, 徐文彪
非哺乳期乳腺炎(non-lactation mastitis,NLM)也称慢性乳腺炎,临床上发病率有上升的趋势,多见于中年妇女,临床体征及影像表现均酷似乳腺癌[1],临床上较易误诊。笔者通过回顾性分析本院经病理证实的37例非哺乳期乳腺炎患者的临床及影像资料,旨在提高对本病的诊断准确性。
材料与方法
1.一般资料
将本院2014年1月-2017年4月经手术病理证实的37例非哺乳期乳腺炎患者纳入本研究。本组病例均为单乳发病,病变位于左乳22个、右乳15个。患者年龄23~67岁,中位年龄38.8岁;病程1周~11个月。主要临床表现:3例首诊症状为患乳肿大、发红、皮温升高伴疼痛;余34例均表现为乳房肿块或片状增厚、质中或质硬、边界不清、活动度差,其中6例伴压痛、9例伴患侧乳头先天性凹陷、8例乳头溢黄浊液体、7例同侧淋巴结增大。9个病灶为中央型(位于乳晕后或中央区);28个为周围型(周围象限),其中位于乳房外份15个。14例患侧在哺乳期有不同程度哺乳困难、乳汁淤积,1例对侧乳房既往有类似病史,1例既往有肉芽肿性乳腺炎手术史。。
2.检查方法
采用美国豪洛捷(Hologic)钼靶乳腺机,常规摄乳腺头尾位和内外斜位片,其中12例加照局部点压位(TAN)片,7例加照侧位片。乳腺X线诊断报告参照2013版美国放射学会乳腺影像报告和数据系统(breast imaging reporting and data system,BI-RADS)。
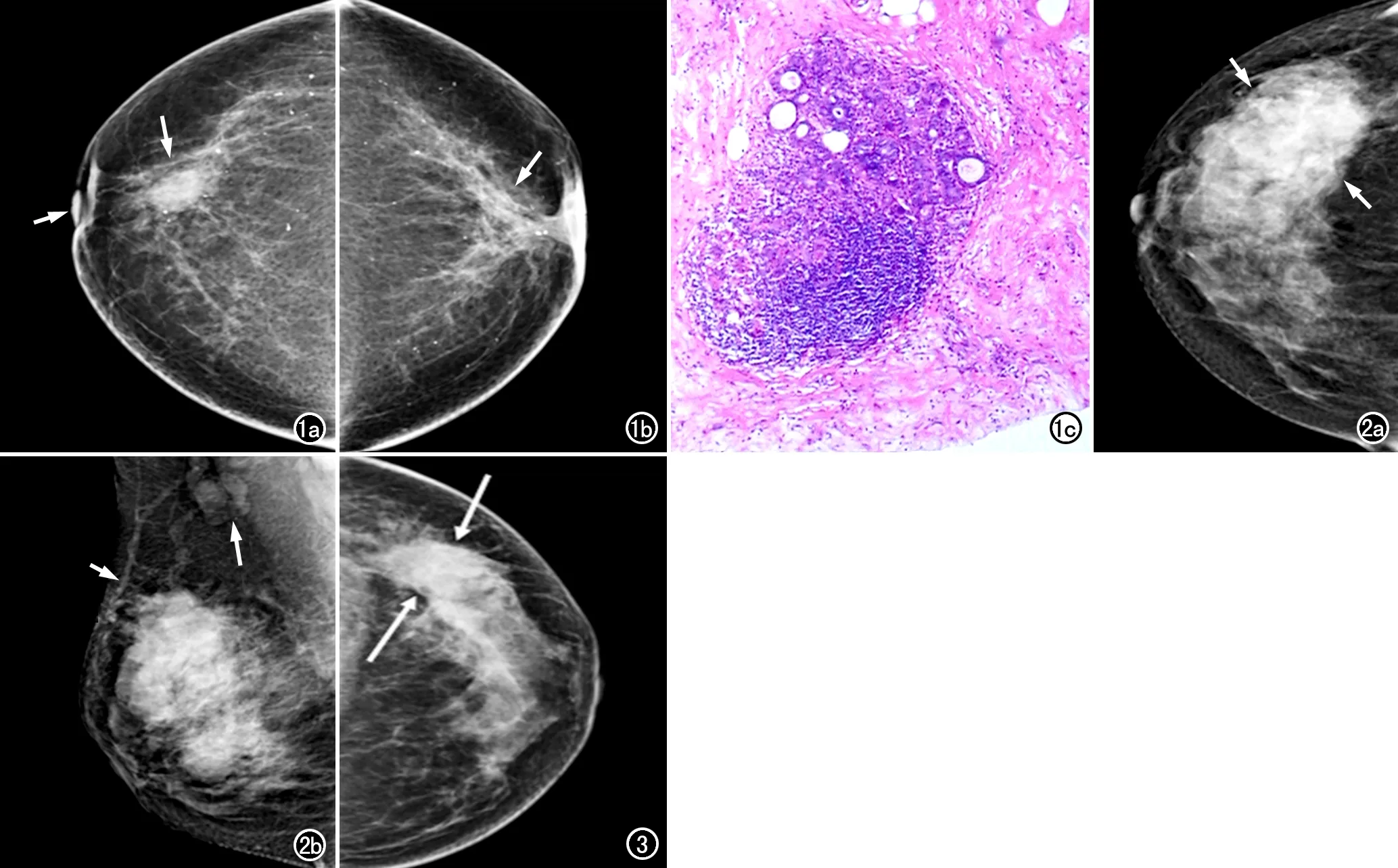
图1 右侧乳腺NLM患者,女,56岁。a) 右乳头尾位片,显示右乳头后方高密度肿块(长箭),大小约2.1cm×2.0cm,部分边界欠规则,周围乳腺小梁结构紊乱,乳头凹陷(短箭): b) 左乳轴位片,显示左乳晕后腺体结构紊乱(箭),乳头凹陷、乳晕及周围皮肤增厚(该侧2年前有浆细胞乳腺炎病史); c) 右乳穿刺组织镜下示大量中性粒细胞、淋巴细胞及少量嗜酸性粒细胞、浆细胞浸润,脂肪细胞坏死,局部小脓肿形灶成(×40,HE)。
结 果
1.钼靶X线表现
37例中11例主要表现为结节肿块型,肿块边界部分欠清,肿块直径2.1~6.3cm,平均4.1cm;病灶呈高密度3个(图1)、等密度8个。26例(26/37)主要表现为腺体不对称性致密,局部乳腺小梁增粗,边缘模糊,乳腺密度增高,其中21例伴结构紊乱(图2);6例表现为沿导管长轴扩展的、密度不均的浸润性病灶,其内见条索状致密影,外缘毛糙,呈火焰状外观(图3)。4例可见(4/37)主乳导管扩张,表现为患侧乳头后方输乳管扩张,呈管状低密度,直径3~5mm(图4)。
其它征象:皮肤增厚6例(图1、5),皮下脂肪间隙呈网状密度增高或消失(图5),伴患侧乳头先天性凹陷9例(图1、4),病灶内见小液气平面3例(图6),患侧腋下淋巴结增大、聚拢或密度增高8例(图2),26例可见病变区域局部血运丰富 (图2),病灶区散在小点状、粗大或环形钙化3例,其中1例病变区内可见多量中间型钙化、部分钙化分布较聚集(图7)。
本组病例的BI-RADS分类结果:3类15例,4A类21例,4C类1例。
2.病理表现
37例非哺乳期乳腺炎患者均经穿刺活检证实,26例经抗生素与激素联合治疗后肿块未能缩小、随后行手术切除。病理诊断为肉芽肿性乳腺炎28例,镜下表现:小叶周围及间质中可见大量中性粒细胞、淋巴细胞、多核巨细胞等,以中性粒细胞为主,伴微脓肿形成13例;病理诊断为浆细胞性乳腺炎共9例,镜下表现:小叶周围及间质中可见以浆细胞、淋巴细胞为主的炎性细胞浸润(图1、4)。
讨 论
非哺乳期乳腺炎(non-lactation mastitis,NLM)也称慢性乳腺炎,是以乳腺内或乳管内残留炎性结节或肿块形成为主要临床表现的一种乳腺迁延性炎症[2]。非哺乳期乳腺炎的疾病谱中,以非特异性慢性乳腺炎中的肉芽肿性乳腺炎、浆细胞性乳腺炎和乳晕下脓肿相对多见[3],本研究中以肉芽肿性乳腺炎居多,共28例。
本研究中均为单侧乳腺发病,肿块边界欠清,活动度较差,伴或不伴疼痛。发生于经产妇且有哺乳史的乳腺炎患者,临床表现复杂多样,在哺乳期后出现类似急性炎症表现的病例归类为非哺乳期乳腺炎,本文见3例此类病例;部分病例口服抗炎药后肿块稍有缩小,部分伴患侧乳头溢液,可挤出黄浊液体。文献报道浆细胞性乳腺炎所形成的肿物绝大多数位于乳晕后区[4]。而肉芽肿性乳腺炎的病理特点为病变以乳腺小叶为中心,呈多灶性分布,小叶内末梢导管或腺泡大部分消失,有多种炎性细胞浸润,以嗜中性粒细胞为主,另可见淋巴细胞,上皮样巨噬细胞和巨细胞等,病灶内常可见微脓肿[5];此型病变是由周围乳腺小叶向乳晕方向呈向心性发展,故肉芽肿性乳腺炎多发生于周围象限。本组9例浆细胞性乳腺炎中7例发生于乳晕后方,28例肉芽肿性乳腺炎中22例发生于周围象限,与文献报道基本相符[4-5]
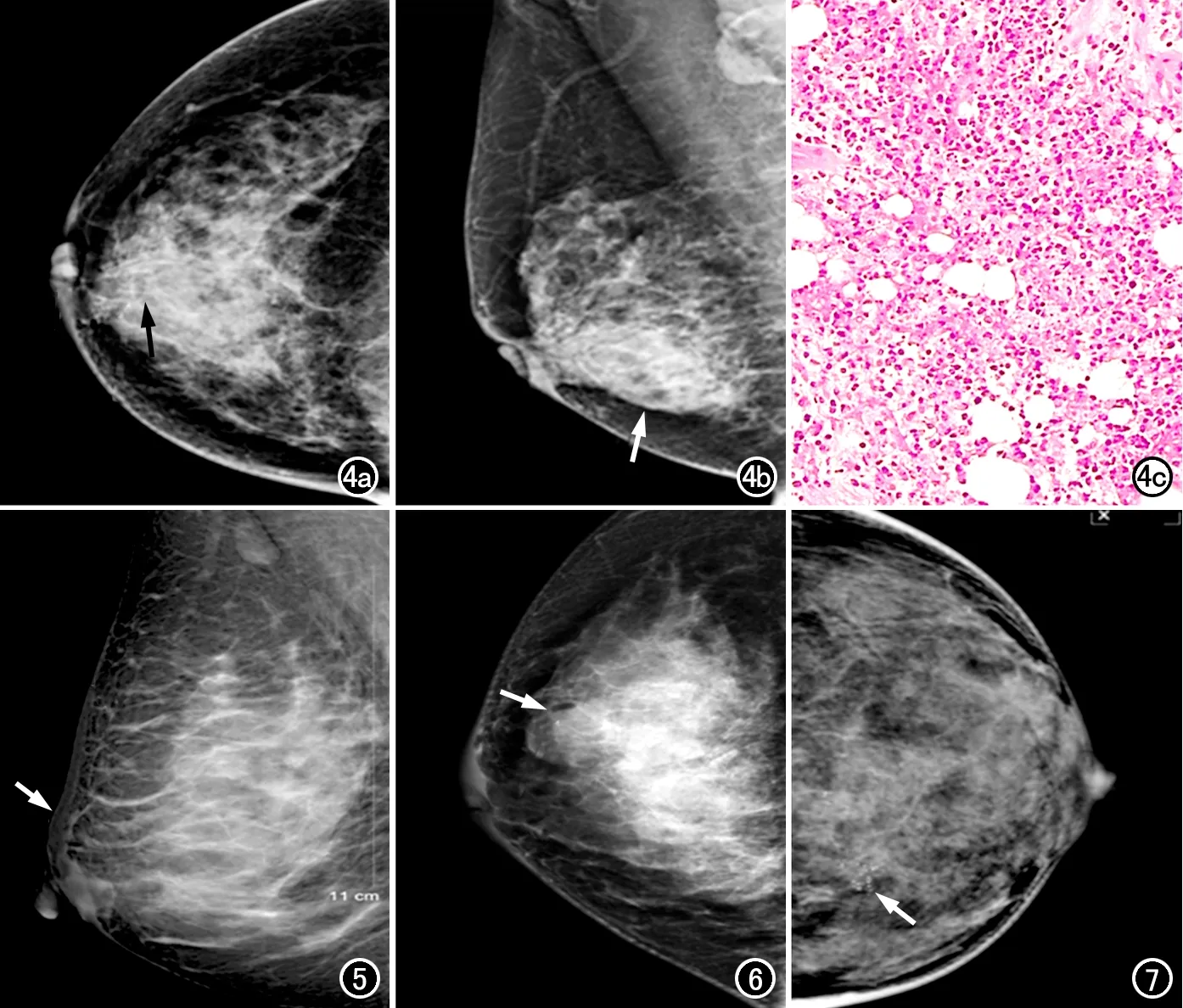
图4 NLM伴脓肿形成患者,女,48岁。a) 头尾位片,显示右乳头后方腺体密度增高,边界欠清,乳晕后方主乳导管扩张达5.1mm(箭); b) 内外斜位片,显示肿块部分边界较轴位显示清晰(长箭),乳头先天性凹陷(短箭); c) 病理切片镜下示乳腺导管未见明显增生,间质内有大量淋巴细胞和中性细胞浸润,局部可见组织细胞及多核巨细胞形成(×100,HE)。图5 NLM患者,女,44岁。右乳内外斜位片,显示右乳外上象限腺体结构稍紊乱,皮下脂肪间隙呈网状密度增高,右乳晕及其外上方的皮肤增厚(箭)。 图6 NLM患者,女,30岁。右乳内外侧位片后显示病灶内可见小气-液平面征(箭)。 图7 NLM患者,女,23岁。左乳头尾位片显示左乳内侧象限内腺体不对称性致密,结构紊乱,乳腺小梁增粗、模糊,可见多量中间型钙化聚集(箭)。
。
NLM的病因尚不完全清楚,目前多认为可能与以下几点有关:①自身免疫性疾病[2,6];②泌乳因素,如妊娠、哺乳和高泌乳素血症可引起肉芽肿性乳腺炎发病[2],本组病例多为经产妇;③内分泌失调,尤其是泌乳素水平升高导致长期溢乳,可能引起分泌物聚集、阻塞乳管而导致乳管周围炎[2];④乳头凹陷或发育不良[7],本组有9例患者伴乳头先天性凹陷,占24%;⑤乳腺导管阻塞和扩张是引起本病的重要原因之一[8],本组中14例患者有哺乳困难及乳汁淤积史,是引起乳管阻塞和扩张的重要原因,与文献报导一致;⑥感染、创伤和化学刺激可导致炎症[9],本组仅一例患者乳房曾有外伤后感染史;⑧急性乳腺炎的失治和误治等[10],本组病例中有1例急性乳腺炎患者因停药后肿块继续增大而就诊(图1)。
非哺乳期乳腺炎的钼靶X线特征:①结节肿块型,肿块部分边界欠清,部分肿块呈等密度,部分呈高密度;②区段性分布的片状不对称性致密浸润阴影,边界模糊,局部乳腺小梁增粗、模糊,典型者表现为沿导管长轴扩展的浸润性改变,导管周围纤维增生使之形成"火焰状"外观;③主乳管扩张,表现为乳头基部主乳导管扩张,管径约3~5mm。④其它伴随征象,包括皮肤增厚、皮下脂肪层间隙呈网状增高或消失、乳头轻度凹陷、乳晕后输乳管扩张、患乳血运丰富和部分病变区可见散在钙化(良性表现)等,较具特征性的改变为病变区可见含小液-气平面,这可能与乳腺炎并脓肿形成有关,此特征在致密型乳腺患者中可在点压位及侧位片上观察。
NLM无论在临床上及钼靶上均易与乳腺癌混淆,笔者复习文献及总结本组病例,认为以下几点可与乳腺癌鉴别。①以不对称性致密为主要表现的乳腺炎多不伴结构紊乱,与乳腺癌的表现有明显不同,本组26例中有5例(19%)符合此表现;而乳腺癌则多表现为局部结构扭曲紊乱,且病变密度往往较炎症病变更高[11]。尤其是呈“火焰状”表现的乳腺炎应与乳腺癌的毛刺相鉴别,乳腺癌的毛刺出现在肿块的边缘,肿块边界不规则或有角状突起,常伴有多形性钙化灶聚集;而乳腺炎的腺体结构紊乱区通常不伴有钙化或伴良性钙化灶,仅少数情况下可见不定形钙化,本组有1例因病变区内有多量不定性钙化灶、部分钙化分布聚集(图7),术前考虑为乳癌可能性大,BI-RADS分类为4C类。②以肿块为主要征象的乳腺炎,病变周围腺体密度不均匀增高,与正常腺体呈移行性改变,边界不请,周边通常无低密度水肿环,本组9例肿块型乳腺炎均未见恶性表现的水肿环,这点对本病与乳腺癌的鉴别有一定意义。③非哺乳期乳腺炎尤其应与炎性乳腺癌鉴别:后者常为乳腺中央区的密度增高,乳晕亦常因水肿而增厚,皮肤增厚则常在乳房的下部最明显,而不像急性炎症那样局限在感染区表面[12],累及整个乳腺的炎性乳癌,可见皮下脂肪层浑浊,皮下水肿明显且分布范围较广泛,是由于皮肤真皮淋巴管被乳腺癌细胞侵袭导致淋巴回流受阻所致,与炎症的过程类似,只有在显微镜下才能发现是癌细胞而不是炎症细胞浸润[13],同时炎性乳癌的肿块边界不清,与乳腺炎较难鉴别,具有炎症征象的肿块在诊断分级时要慎重,必要时应进一步进行穿刺活检,以免延误治疗。④慢性乳腺炎可仅变现为乳晕后大导管区局部增宽、密度增高、乳晕区皮肤增厚[14],故乳晕后导管扩张并乳头溢黄浊液体有助于乳腺炎的诊断。⑤好发部位不同:炎性肿块多好发于乳晕后区,而乳腺癌好发于乳房外上象限[15]。但本组37例中位于乳晕后区者仅9例(24%),故诊断时需慎重。⑥乳腺炎经1~2周抗生素治疗后,炎症肿块可缩小,乳腺癌尤其是炎性乳腺癌的病程进展迅速,呈浸润性特征,若炎症表现仅局限于乳腺、而无体温及白细胞升高的病例强烈提示为炎性乳腺癌[16]。
当临床触诊到质硬、活动度差的肿块并高度拟诊为乳腺癌时,钼靶X线检查是必不可少的,乳腺炎与乳腺癌的影像表现有一定重叠,掌握本病与乳腺癌的鉴别要点及综合分析尤为重要,对于钼靶X线常规照片上阳性征像不明显者,应加照肿块点压位或侧位片,本组3例发现乳腺病灶内有小气-液平面,均是在点压片或侧位片上发现的。对钼靶X线诊断有困难者应结合超声及MRI检查进行综合分析,为临床制订手术治疗方案提供重要依据。
参考文献:
[1] 王钟富.现代实用乳房疾病诊疗学[M].郑州:河南科学技术出版社,2000:328-334.
[2] 肖蔷,张超杰.非哺乳期乳腺炎的现代研究进展[J].医学与哲学,2013,34(3):8-13.
[3] 张超杰.非哺乳期乳腺炎的诊治进展:争议与共识[J].医学与哲学,2013,34(3):7.
[4] 周毅,马丽华,黄其敏.浆细胞性乳腺炎的X线诊断分析[J].中国医学影像技术,2000,16(3):216-217.
[5] 刘佩芳.浆细胞性乳腺炎和肉芽肿性乳腺炎的影像学诊断及鉴别诊断[J].国际医学放射学杂志,2009,32(3):268-273.
[6] Tournant B.Lymphocytic plasma cell mastitis[J].Arch Anat Cytol Pathol,1995,43:88-92.
[7] 张淑群,纪宗正,薛兴欢,等.浆细胞性乳腺炎的诊断和治疗:附124例临床分析[J].临床外科杂志,2007,15(6):378-380.
[8] 刘小燕,孙惠.非哺乳期乳腺炎32例诊治分析[J].齐鲁医学杂志,2003,18(2):197-198.
[9] 崔玉荣,孙贻安.肉芽肿性乳腺炎的现代研究[J].辽宁中医药大学学报,2009,11(10):48-49.
[10] 黄蓉,李棠华,陈祥.非哺乳期乳腺炎钼靶X线诊断与误诊原因分析[J].现代医用影像学,2014,23(6):683-685.
[11] 姚薇薇,杜恒峰,夏军,等.非哺乳期乳腺炎的数字钼靶X线诊断分析[J].海南医学,2012,23(12):91-93.
[12] 鲍润贤.中华影像医学乳腺卷(第2版)[M].北京人民卫生出版社,2010:97.
[13] Molckovsky A,Fitzgerald B,Freedman O,et al.Approach to inflammatory breast cancer[J].Can Fam Phys,2009,55(1):25-31.
[14] 滕妍,曹满瑞,赵弘,等.全数字化乳腺X线摄影对乳腺炎性病变的诊断价值[J].放射学实践,2012,27(2):167-169.
[15] 谢坪,何远智,付凯,等.乳腺癌X射线表现分析[J].实用放射学杂志,2006,22(3):326-348.
[16] Renz DM,Balzer PA,Bottcher J,et al.Magnetic resonance imaging of inflammatory breast carcinoma and acute mastitis:a comparative study[J].Eur Radiol,2008,18(11):2370-2380.
