高氯酸盐毒性及其检测方法研究进展
2018-05-01宋正规张爱芝张书芬满正印刑家凓蔡君美李和生
宋正规,沈 坚,张爱芝,张书芬,满正印,刑家凓,蔡君美,李和生
(1.宁波大学海洋学院,浙江宁波 315211;2.宁波市食品检验检测研究院,浙江宁波 315048)
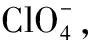
鉴于高氯酸盐严重的污染情况,各国对高氯酸盐污染高度重视。2002年,美国环保局建议饮用水中高氯酸盐的最大容许浓度为1.0 μg·L-1[11-12]。2013年,美国联邦法院制定法律,对饮用水中高氯酸盐含量实行监管。2015年,日本供水司规定地下水高氯酸盐含量不得高于5 μg·L-1。我国的相关法律和含量标准也将近期出台。
高氯酸盐污染具备涉及范围广,持续时间长,流动作用快的特点。对高氯酸盐的毒性研究和检测技术发展是降低污染的重要一环。高氯酸盐残留污染环境和食品,并对内分泌、神经、生殖和遗传等多方面有毒性影响,目前的检测技术有光度计法、离子色谱法、离子色谱-串联质谱联用、液相色谱-串联质谱联用法,可以做到准确定性和定量,达到痕量检测标准,基本满足不同水平的检测要求。文章对高氯酸盐毒性影响和高氯酸盐检测技术进行了综述。
1 高氯酸盐结构
结构决定性质,高氯酸盐中起毒害作用的主要为高氯酸根。高氯酸根离子为阴离子,呈标准正四面体结构,Cl原子处于正四面体中心,四个O原子包围Cl原子,O原子处在正四面体的四个顶点,Cl原子被牢牢包围,因此正四面体结构稳定不易反应。高氯酸根整体体现-1价,结构牢固,动力学稳定,不易分解,可长期存在自然界不被降解,其过程往往延续几十年甚至更久,成为一种持久性污染物[13-15]。

图1 高氯酸根结构式Fig.1 Constitutional formula of perchlorate
2 高氯酸盐对环境和食品的影响
高氯酸盐进入生命机体或进入活体,造成机体损伤,主要是由高氯酸盐进入环境开始,一旦进入自然环境,一方面可以经过饮用水直接进入机体,另一方面可从土壤中吸收富集植物体内,进入生态食物链循环,残留食品,经机体消化吸收,发挥毒性,毒害人类。
2.1 对环境的影响
高氯酸盐因其特性,在自然界普遍分布,高氯酸盐是生产化肥的重要的原料,皮革制品、橡胶制造、涂料生产和润滑油生产等的添加剂[16]。经深入探究,部分高氯酸盐,如高氯酸铵,贮存寿命有限,生产厂家会定期对原有库存进行处理,这就直接导致了大量未经处理的高氯酸盐一次性排入环境中,对自然环境造成持久性的破坏。
高氯酸盐对环境中水体的污染已经逐渐暴露,中国、美国、日本等已经对其开始检测,结果显示,全球范围内已经受到高氯酸盐不同程度的污染,全球水体是一个大环境,一旦大面积的水域受到污染,淡水系统,海洋生态将逐渐蔓延污染破坏[17]。Tang对中国成都地下水、土壤等样品进行了高氯酸盐含量测定,结果发现地下水和土壤中检测到60.2~249 mg/mL浓度不等的高氯酸盐[18]。根据Hutchinson研究,根系土壤中高氯酸盐含量对影响植物体内高氯酸盐的含量有直接作用[19]。
2.2 对食品的影响
高氯酸盐进入食品是对人类的一巨大威胁,已有众多报道证实我们日常食用的肉制品、谷类、果蔬及其饮料等受到高氯酸盐的不同程度的污染。
有研究已经表明,蔬菜、水果、茶叶、肉类和粮食作物可食用部位都能够富集高含量的高氯酸盐[20-22]。植物中可食用部分经人体消化吸收,进入人体,危害生长发育,不可食用部分,或被动物食用,而后随食物链进入人体,或经分解大部分重回自然环境继续循环[23]。Hutchinson等[19]在实验室里用含不同浓度高氯酸根的污水浇灌莴苣,结果表明绝大部分的高氯酸根通过根进入了叶等组织,只有21%的高氯酸根仍留在了沙基中,说明水溶性强的高氯酸根很容易伴随水分的吸收而进入植物体。陈桂葵等[21]在研究高氯酸盐胁迫对水稻生长发育和养分吸收影响时,发现高氯酸盐经根系吸收,吸收后向上运输,贮藏在稻粒及其茎秆中。2016年新京报讯,近期中国出口欧盟茶叶中被爆检出“新型污染物”高氯酸盐,唤起公众对高氯酸盐污染关注。更值得关注的是在饮用水、肉制品、谷类、果蔬及其饮料中普遍检出高氯酸盐污染[24]。2017年高立红对市场上常见的饮料进行检测,其中在红茶、绿茶、可乐等饮料中检出高氯酸盐存在,其中红茶测出浓度为0.769 μg/L,绿茶1.376 μg/L,加多宝6.090 μg/L,可乐0.055 μg/L,雪碧0.02 μg/L以下[17]。同年,陈东对190份茶叶进行了检测,大部分高氯酸盐含量在0.08 mg/kg左右,在3份红茶和2份绿茶中检出了>0.75 mg/kg的高氯酸盐含量[25]。贺巍巍等[26]对北京市销售的163份样品,蔬菜81份、动物源性食品(肉、禽、蛋和水产品)28份、牛奶等饮品20份、谷物17份、香辛料调味品17份进行检测,1份有机小米0.063 mg/kg、1份散玉米面0.54 mg/kg,9份花椒含量高出1.0 mg/kg,牛奶含量范围为1.10~10.30 mg/kg,蔬菜和动物源性食品检出含量在0.08 mg/kg以下。
可见我们日常食用的饮用水、茶叶、饮料、调味料、牛奶、蔬菜、肉制品及其主食中都存在不同程度的高氯酸盐污染,其中茶叶、部分饮料、牛奶和调味品污染较为严重,主食、蔬菜和动物源性食品污染较轻,加强高氯酸盐毒性研究和对市场食品进行高氯酸盐检测显得日益重要。
3 高氯酸盐的毒性
高氯酸盐作为一种流动性极强,易于富集的氯酸盐,近年来对高氯酸盐的毒性研究范围逐渐扩大,内容逐渐深入。高氯酸盐首先作用环境,进入我们日常食品,而后进入人体,发挥毒性作用,目前研究发现高氯酸盐对人体内分泌、神经、生殖、遗传产生毒性作用。
3.1 对机体内分泌及神经的毒性
甲状腺激素包括三碘甲状腺原氨酸(T3)和四碘甲状腺原氨酸(T4)。高氯酸根离子与碘离子性质非常接近,甲状腺在合成甲状腺激素过程中,碘离子的位置被高氯酸根取代,合成了没有促进作用的假甲状腺激素,危害人体健康。
高氯酸盐通过影响甲状腺素的合成,从而对骨骼、大脑、其他腺体和生殖器官造成影响,进一步影响人体正常机能。甲状腺代谢紊乱,引起生长激素减少,造成人体长骨不能正常生长,严重时甚至会患呆小症和无正常生育能力[27]。York等[28]通过饮用水对小鼠进行高氯酸盐暴露实验表明,小鼠饮用高于1.0 mg·(kg·day)-1的高氯酸盐,甲状腺重量明显增加,检测到垂体分泌的促甲状腺激素含量增高,推断合成的甲状腺激素并没有发挥应有的反馈调节作用。
高氯酸盐对幼儿神经系统发育影响更加严重,分娩前,甲状腺激素影响宫内期脑细胞的增殖、分化、发育。分娩后,影响脑细胞之间的连接和传递,甲状腺激素在轴突和树突的生长、突触的形成、髓鞘的形成和特异种群细胞的分化等过程中都起到调节作用[29-30]。T3、T4是酪氨酸衍生物,而酪氨酸是儿茶酚胺生物合成的底物,可能是由于甲状腺激素使中枢儿茶酚胺增加,兴奋上行,刺激系统而间接引起。甲状腺激素本身可能是肾上腺素-神经递质的前身,也可能是肾上腺素-神经递质经过代谢而产生的甲状腺-神经递质,缺少这些会造成脑体积减小,小脑发育不成熟,学习和记忆障碍。Gilbert等[31]在进行高氯酸盐神经毒性研究时,发现较低剂量的高氯酸盐可以造成海马在发育期突触递质受到不可逆的损害,此实验可以推断高氯酸盐影响到神经递质的正常作用,但其中的机理尚不明确。
3.2 生殖毒性

3.3 遗传毒性

4 高氯酸盐检测方法
为最大程度减少毒作用,检测技术的发展优化是降低污染的重要前提,检测方法由最早的分光光度法[38-39],90年代初期开发出离子色谱检测[40],到目前逐渐普及的离子色谱-质谱联用[41],液相色谱-质谱联用[42-43],检测精密度和检出限都得到大幅提高。
4.1 分光光度法

4.2 离子色谱法-电导检测法
离子色谱检测高氯酸盐,主要利用高氯酸根和色谱柱离子交换的原理,再利用强碱洗脱,进行检测。
目前常用的离子色谱柱有Dionex IonPac AS5、Dionex IonPac AS11、Dionex IonPac AS16、Dionex IonPac AS19和Dionex IonPac AS20[46-48],最新的有Dionex IonPac AS21和Dionex IonPac AS26色谱柱。Dionex IonPac AS5为强阴离子交换色谱柱,阴性高氯酸根离子与色谱柱阴离子交换树脂上羟基交换,结合牢固,保留性强。Krynitsky用120 mmol·L-1NaOH溶液洗脱,在流动相中添加2 mmol·L-1对硝基苯酚减弱高氯酸根与固定相树脂的吸附,达到较好的洗脱效果[47]。Dionex IonPac AS11色谱柱,以对高氯酸根有强吸附性的亲水性烷醇季铵为填充物,采用100 mmol/L NaOH溶液为淋洗液,Muhammad进行饮用水检测,检出限为0.3 μg·L-1,回收率达到92%~100%,该方法可以达到痕量检测标准[48]。DionexIonPac AS16是在DionexIonPac AS11基础上研制出来的,以氧化硅为填料,交联季胺功能基团,对高氯酸根离子有强吸附性,同时减少了CO2的干扰,降低基线噪音[49]。Chain等利用该色谱柱,检出限为0.15 μg·L-1,回收率97%~105%[50]。Dionex IonPac AS20柱,采用KOH梯度洗脱,检出限为100 μg·L-1[52]。虽然大大降低了进样量,但检出限却有了大幅度降低,因此通常采取大体积进样。Dionex IonPac AS21[53]和Dionex IonPac AS26色谱柱是为卤素离子开发的色谱柱,部分文献将其用于高氯酸盐的检测,但在检测过程中相比效果并非很好。表1对几种常用检测高氯酸盐离子色谱柱进行了比较。

表1 离子色谱柱优缺点比较Table 1 Comparison of advantages and disadvantages of ion chromatography column
目前离子色谱广泛适用于各种检测机构,对饮用水、水果和蔬菜等各种食品,较为准确的进行定性和定量。但离子色谱-电导检测存在检测假阳性、干扰严重和不能进行痕量定量的缺点,不能满足严苛的进出口检测要求。目前也正在继续研究开发效果更好,稳定性更强,灵敏度更高,吸附作用更彻底,洗脱完全的离子色谱柱。
4.3 离子色谱-质谱联用法
离子色谱-质谱分离原理与离子色谱相同,不同在于检测。质谱主要利用四极杆筛选母离子,施加一定电压打碎母离子,根据碎片子离子进行同时定量和定性检测。具体过程为:色谱柱分离的母离子经离子源高压打散,分裂为离子形态,经电场加速,磁场改变速度方向,不同离子根据各自质核比按照马绍方程螺旋前进,最终按照检测目标离子质核比选出待测离子,离子在第二个四极杆碰撞电压作用下,碎裂成多个碎片离子,碎片离子撞击质谱检测板,引起检测板电信号变化,从而对高氯酸根准确定性和定量。质谱检测消除离子色谱检测过程中其他离子对目标离子的干扰,检测准确度大大提高[55-58]。

Jackson[59]采用Dionex IonPac AS16柱大剂量注射,这种方法排除了常见无机阴离子的干扰,可以较准确检测水中高氯酸根离子,检出限为150 ng·L-1。2013年中国南极科考队在南极利用离子色谱-质谱对冰雪检测,Su Jiang[60]利用浓缩器柱,提高高氯酸盐浓度,Dionex IonPac AS16柱分离,该方法的检出限和定量限分别为0.2和0.5 ng·L-1,准确度高。从南极冰雪中检测到含量从10~340 ng·L-1不等的高氯酸盐,直接反映了高氯酸盐已经危害到了南极,可见高氯酸盐污染已经成为全球性的问题。Balaji使用Dionex IonPac AS20(250 mm×2 mm)分析柱,对土壤和植物浸出液中高氯酸盐含量进行了检测,检出限可达0.2 ng·L-1[57],提高了检出限。美国环境保护局根据离子色谱柱基质与离子结合能力非常高的优势,在样品进入柱子前利用一根35 mm×4 mm样品浓缩柱,浓缩高氯酸根离子,再利用AS16分析柱和AS20分析柱串联组合使用,提高了分离效果,在电导检测过程中,大大降低了干扰离子的存在,同时由于对低浓度离子的浓缩,提高了检出限[58]。
离子色谱-质谱联用是目前比较精确定量和定性的方法,根据其固定荷质比及其质谱检测的灵敏能够准确进行定性和满足痕量要求。离子色谱-质谱联用虽然在定性和检测灵敏度上有了飞跃,但依然存在检测物质洗脱不完全的缺点。离子色谱-质谱检测满足大多科研需要和进出口高精确的检测。
4.4 液相色谱-质谱联用方法
液相色谱-质谱联用分析和离子色谱-质谱联用分析原理基本相当,都是采取先分离后检测的方法。液相色谱-质谱联用主要利用液相吸附柱子,与离子色谱选用离子交换有所差别,离子交换柱主要利用检测离子和柱子离子间进行交换,而后利用稀碱将其洗脱的分离方法,液相色谱主要利用柱子对流动相溶解离子选择性吸附,而后改变流动相洗脱的原理。分离纯化离子方法基本相同,原理存在差异。对于分离物质的检测方法一样,都是利用三重四极杆检验原理,精准稳定。有所不同的是离子色谱-质谱联用,柱子分离后,串联的抑制电导检测器,可将部分干扰离子切出检测系统,减少了干扰离子[61-62]。
Aleksey采用液相色谱-质谱联用建立了快速、高效的检测方法。
使用75 mm×4.6 mm Synergi MaxRP C12液相色谱柱子,对饮用水中高氯酸盐进行检测,检出限达0.1 μg·L-1[63]。Leonidas[64]利用C18色谱柱(XR-ODS,2 mm i.d.×100 mm,2.2 μm),对饮用水中的高氯酸盐进行检测,检出限10 μg·L-1。Tefera[65]利用C18柱子,在对牛奶高氯酸盐检测过程中对前处理和检测方法进行了改进和优化,在牛奶中加入了0.1%的乙酸,乙酸调节pH促使蛋白沉淀,对高氯酸盐的提取作用明显,用可以对样品净化的多模式OASIS HLB固相萃取小柱对高氯酸盐进行萃取,检出限为0.2 μg·L-1,回收率96%~102%。谢永洪[66]利用高效液相色谱-电喷雾离子源-串联三重四极杆质谱对地表水高氯酸盐进行检测。以Dionex IonPac AS20阴离子交换柱为分析柱,方法检出限达0.043 μg·L-1,线性范围为0.2~50 μg·L-1,对含量分别约为2、6、30 μg·L-1的实际样品进样10次得到的相对标准偏差分别为2.47%、4.55%、0.49%,样品加标回收率在80%~109%。吴映璇[67]建立了水果中高氯酸盐的高效液相色谱-串联质谱分析检测方法。样品采用1% 乙酸提取,C18固相萃取柱净化,Waters IC-Pak Anion HR(4.6 mm×75 mm)色谱柱洗脱,采用18O标记高氯酸根离子作为内标进行基质校正,内标法定量,高氯酸盐在0.1~10.0(g·L-1范围内线性关系良好,定量下限为1.0 μg·kg-1;在1.0,2.0,10 μg·kg-13个加标水平下的回收率为92.5%~110%。实际样品检测表明该方法准确可靠,适合于水果中高氯酸盐的测定。2015年,吴映璇发布了《出口食品中高氯酸盐的测定液相色谱-质谱/质谱法》行业标准。对该方法进行了整理完善,将检测范围扩大到瓶装水、水果、牛奶、谷物、水产品和动物组织等[68]。2017年中国山东省食品药品检验研究院,祝建华采用郭志谋研制的TE-Cys(100 mm×2.1 mm i.d,5 μm)对牛奶高氯酸盐进行了分离检测,高氯酸检出限达到10(g/kg)[69]。表2对几种常用检测高氯酸盐液相色谱柱优缺点进行了比较。

表2 液相色谱柱优缺点比较Table 2 Comparison of advantages and disadvantages of liquid chromatography column

4.5 其他方法
文献还有表面增强拉曼散射法,检出限为25 μg·L-1,线性范围为25~50 mg·L-1[70]。X射线荧光光谱法检出限为100 nmol·L-1,线性范围为1~180 μmol·L-1,相关系数为0.9955,操作简便,分析迅速[71]。
5 结论与展望
随着对高氯酸盐毒理学研究的深入,高氯酸盐对机体毒作用机理更加清晰,研究范围已经涉及到人、动物、植物和微生物,部分作用机理已经清晰,目前高氯酸盐对植物富集和毒性机理正在深入研究,微生物作用机理也开始研究并取得一定进展[72-75]。检测技术已经比较成熟,随着痕量检测要求,新的技术还在进步,分光度法已经基本淘汰,离子色谱-电导检测优势在于离子色谱价格相对低廉,但随着检测要求的提高,离子色谱-电导检测对高氯酸盐检出限达0.15 μg·L-1,已经不能满足现在部分出口产品检出要求[49]。离子色谱-质谱联用是现在最为常用、灵敏度高、检出限低、抗干扰能力强的检测方法,饮用水中检出限可达0.2 ng·L-1[60]。部分适合液相使用的离子色谱柱也被用于液相色谱-质谱联用中,经过长期实验,检测过程稳定,即达到了检测的高要求,又同时减少了重新购买仪器的经费负担。色谱检测技术已经基本满足高氯酸盐检测要求,同时检测性能更好的离子交换柱和液相色谱柱也在加快研制,检测过程开始配备除杂柱,减少干扰,提高检测精度。未来的检测方法将向仪器价格低,精密度高,防干扰能力强,检出限高,检测速度快的方向发展。
[1]MOTZER W E. Perchlorate:Problem,detection,and solutions[J].Environmental Forensics,2001(2):301-311.
[2]Su Jiang,Yuansheng Li,Bo Sun.Determination of trace level of perchlorate in Antarctic snow and ice by ion chromatography coupled with tandem mass spectrometry using an automatedsample onlinemethod[J].Chinese Chemical Letters,2013,24(1):311-314.
[3]Brundrett M,Horita J,Anderson T. The use of chlorate,nitrate,and perchlorate to promote crude oil mineralization in salt marsh sediments[J].Environmental Science & Pollution Research,2015,22(20):7-85.
[4]KelleyJA,OstrinskayaA. Reagent approaches for improved detection of chlorate and perchlorate salts via thermal desorption and ionization[J].Rapid Communications in Mass Spectrometry,2016,30(1):191-198.
[5]黎华寿,张修玉,姜春晓.氯酸盐生态毒理研究进展[J].生态学杂志,2005,24(11):1323-1328.
[6]Liebensteiner MG,OosterkampMJ. Microbial respiration with chlorine oxyanions:diversity and physiological and biochemical properties of chlorate-and perchlorate-reducing microorganisms[J].Annals of the New York Academy of Sciences,2016,1365(1):59.
[7]Smith N P,Yu L,Mcmurry T S. Perchlorate in water,soil,vegetation and rodents collected from the Las Vegas Wash,Nevada,USA[J]. Environmental Pollution,2004,132(1):121-127.
[8]Winkler P,Minteer M,Willey J. Analysis of perchlorate in water and soil by LC/MS/MS[J]. Analytical Chemistry,2004,76(2):469-473.
[9]Shi Y L,Zhang P,Wang Y W,et al. Perchlorate in sewage sludge,rice,bottled water and milk collected from different areas in China[J]. Environment International,2007,33(7):955-962.
[10]Her N G,Kim J S,Yoon Y M. Perchlorate in dairy milk and milk-based powdered infant formula in South Korea[J]. Chemosphere,2010,81(6):732-737.
[11]Logan B E. Assessing the outlook for perchlorateremediation[J]. Environmental Science & Technology,2001,35:482-487.
[12]Christen K. EPA perchlorate regulation faces further delay[J]. Envionmental Science & Technology,2003,37:347-348.
[13]CoatesJD. Ecology and physiology of unusual electron acceptors in bacteria:Perchlorate and beyond[J].Annual Review of Microbiology,2016,70(70):435.
[14]BreytusA. Fate of chlorate and perchlorate in high-strength and diluted hypochlorite solutions[J].Acs Symposium Series,2015,12(12):11-19.
[15]Sijimol M R,Mohan M,Dineep D. Perchlorate contamination in bottled and other drinking water sources of Kerala,southwest coast of India[J].Energy Ecology & Environment,2016,1(3):1-9.
[16]FangHE,FuLI,Zhou H H,et al. Removal of perchlorate from drinking water using modified polyester particles as carbon source[J]. Journal of Central South University(Science and Technology),2014,45(10):4452-4457.
[17]高立红,李仁勇,刘慧.离子色谱-串联质谱法检测碳酸饮料中的高氯酸盐[J].环境科学,2017,36(9):52-56.
[18]Tang Y,Zhong B,Qu B. Occurrence of perchlorate in groundwater,paired farmland soil,lettuce,and rhizosphere soil from Chengdu,China[J]. Environmental Science Processes & Impacts,2017,19(5):752-757.
[19]Hutchinson S L.A study on the accumulation of perchlorate inyoung head lettuce[M/OL]. EPA/600/R-03/003,2004 12[2008-08-12].http://www.epa.gov/athens/publications/reports/HutchinsonLettuceReport600R03003.
[20]段雄伟,刘亚玲,黎华寿,等.高氯酸盐和铬复合污染对土壤酶活性及微生物数量的影响[J].农业环境科学学报,2014,33(2):322-331.
[21]陈桂葵,杜宁宁,贺鸿志,等. 高氯酸盐对水稻理生态的影响及其在稻田系统中的分布规律[C].呼和浩特:农业环境科学学报编辑部2011:2137-2144.
[22]刘小芳,方从容,刘慧. 离子色谱-串联质谱法检测茶叶中的高氯酸盐[J].色谱,2016,34(10):986-988.
[23]明双喜,刘伟,张然.食品中高氯酸盐污染及检测[J].食品研究与开发,2017,38(14):208-213.
[24]李栋.不只是茶叶中高氯酸盐污染成世界难题[N].新京报,2016-2-23(B11).
[25]陈东,范赛,沙博郁. 同位素标记-超高效液相色谱-串联质谱法测定茶叶中的高氯酸盐[J].中国卫生检验杂志,2017(16):2298-2300.
[26]贺巍巍,杨杰,王雨昕.超高效液相色谱-串联质谱法测定食品中高氯酸盐[J].中国食品卫生杂志.2017,29(4):438-444.
[27]Jasper JT,YangY,HoffmannMR. Toxic byproduct formation during electrochemical treatment of latrine wastewater[J]. Environmental Science & Technology,2017,51(12):7111-7119.
[28]York RG,Lewis E,Brown WR,et al. Refining the effects observed in a developmental neurobehavioral study of ammonium perchlorate administered orally in drinking water to rats[J]. International Journal of Toxicology,2005(24):403-418.
[29]Ting D,Steinmaus C. Perchlorate:Human toxicity[M]. Encyclopedia of Environmental Health,2011,45(1):364-370.
[30]Strawson J,Zhao Q Y,Dourson M.Reference dose for perchlorate based on thyroid hormone change in pregnant women as the critical effect[J]. Regulatory Toxicology and Pharmacology,2004,39(1):44-65.
[31]Gilbert ME,Sui L. Developmental exposure to perchlorate alters synaptic transmission in hippocampus of the adult rat[J]. Environment Health Perspect,2008,116:752-760.
[32]Bernhardt R R,Vonhippel F A,Cresko W A. Perchlorate induces hermaphroditism in threespine sticklebacks[J]. Environmental Toxicology and Chemistry,2006,25:2087-2096.
[33]任新,赵雪松,杨春维.高氯酸钠急性暴露对斑马鱼胚胎发育及氧化应激的影响[J].吉林师范大学学报:自然科学版,2016,37(3):125-130.
[34]QinJH,ShuYH,LiYJ.Effects of perchlorate bioaccumulation on Spodoptera litura growth and sex ratio[J].Environmental Science & Pollution Research,2016,23(9):8881-8889.
[35]McDougal J N,Jones K L,Fatuyi B,et al. The effects of perchlorate on thyroidal gene expression are different from the effects of iodidedeficiency[J]. Toxicol Env Health A,2011,74:917-926.
[36]Puthirath A B,Patra S,Pal S. Transparent flexible lithium ion conducting solid polymer electrolyte[J]. Journal of Materials Chemistry A,2017,5(22):11152-11162
[37]Wu F,Zhou X,Zhang R.The effects of ammonium perchlorate on thyroid homeostasis and thyroid-specific gene expression in rat[J]. Environmental Toxicology,2012,27(8):445-449.
[38]Takeuchian M,Yoshioka K,Toyama Y,et al. On-line measurement of perchlorate in atmospheric aerosol based on ion chromatograph coupled with particle collector and post-column concentrator[J]. Talanta,2012,97:527-532.
[39]Collinson W J,Boltz D F. Indirect spectrometric and atomic absorption spectrometric methods for determination of perchlorate[J]. Analytical Chemistry,1968,40(12):1896-1898.
[40]张萍,史亚利,蔡亚岐,等.改进的离子色谱法测定环境水样中的高氯酸盐[J].高等学校化学学报,2010,28(7):1246-1250.
[41]戴安公司.离子色谱与API2000(IC/MS/MS)联用分析食品和饮料中的高氯酸盐[J].环境化学,2006,25(1):117-120.
[42]Lee Jw,Sung H,Jeong E. Monitoring of perchlorate in diverse foods and its estimated dietary exposure for Korea populations[J].Journal of Hazardous Materials,2012,243:52-58.
[43]Robertson W D,Roy J W,Brown S J. Natural attenuation of perchlorate in denitrified ground water[J]. National Ground Water Association,2013,28:1-8.
[44]Nabar M G,Ramachandran R C. Quantitative determination of perchlorate ion in solution[J]. Journal of the American Chemical Society,1959,31(2):263-265.
[45]Fritz S J,Abbink E J,Campbell A P. Spectrophotometric determination of perchlorate[J]. Journal of the American Chemical Society,1964,36(11):2123-2126.
[46]Zarei A R,Ghavi A. A new approach for the removal of chlorate impurity from military grade ammonium perchlorate using stabilized zero valent iron nanoparticles[J].International Journal of Energetic Materials & Chemical Propulsion.2016,15(3),225-229.
[47]Krynitsky A,Ran,Nortrup D. Determination of perchlorate by ion chromatograph[J]. Journal of Analytical Science,2011,27(2):253-256.
[48]MuhammadN,SubhaniQ,WangF. Application of a simple column-switching ion chromatography technique for removal of matrix interferences and sensitive fluorescence determination of acidic compounds(pharmaceutical drugs)in complex samples[J].Journal of Chromatography A.2017,07:007-011.
[49]Zhang P,Shi Y L,Cai Y Q,et al. Determination of perchlorate in nature water by ion chromatography with large volume injection[J].Chinese Journal of Analytical Chemistry,2006,34(11):1575-1578.
[50]ChainE.Risks for public health related to the presence of chlorate in food[J].Efsa Journal,2016,13(6):4135-4135.
[51]姬建生,高敬铭,符锋.抑制电导-离子色谱法同时测定肉制品中亚硝酸盐和硝酸盐[J].中国食物与营养,2010,2010(10):38-40.
[52]宁啸骏,朱伟,杜茹芸.离子色谱-串联质谱法测定婴幼儿配方奶粉中的高氯酸盐[J].理化分析:化学分册,2016,1,19-23.
[53]王楼明,林燕奎,王丙涛.离子色谱法测定化肥中高氯酸盐[J].分析科学学报,2011,27(2):253-256.
[54]谢永洪,杨坪,熊杰.高氯酸盐分析方法研究进展[J].四川环境,2014,33(3):140-147.
[55]MavroudakisL,MavrakisE,KouvarakisA. Determination of chlorate,perchlorate and bromate anions in water samples by microbore reversed-phase liquid chromatography coupled to sonic-spray ionization mass spectrometry[J].Rapid Commun Mass Spectrom,2017,31(11):911-918.
[56]LiebensteinerMG,OosterkampMJ,Stams A J. Microbial respiration with chlorine oxyanions:diversity and physiological and biochemical properties of chlorate and perchlorate-reducing microorganisms[J]. Annals of the New York Academy of Sciences,2016,1365(1):59.

[58]Chao Zhang,Jianbo Guo,Jing Lian. Characteristics of electron transport chain and affecting factors for thiosulfate-driven perchlorate reduction[J].Chemosphere,2017,8,23-26.
[59]Jackson PE,Gokhale S. Improved method for the determination of trace perchlorate in ground and drinking waters by ion chromatography[J].Journal of Chromatography A,2000,888(1-2):151-158.
[60]Jiang S,Li YS. Determination of trace level of perchlorate in Antarctic snow and ice by ion chromatography coupled with tandem mass spectrometry using an automated sample on-line preconcentration method[J]. Chinese Chemical Letters,2013,24(4):311-314.
[61]Förstel M,Maksyutenko P,Kaiser R I. A Reflectron time-of-flight mass spectrometric study on the degradation pathways of glycine on mars in the presence of perchlorates and ionizing radiation[J]. Astrophysical Journal,2017,835:241.
[62]Aleksey N,Pisarenkoa B,Benjamin D,et al. Rapid analysis of perchlorate,chlorate and bromate ions in concentrated sodium hypoch-lorite solutions[J]. Analytica Chimica Acta,2010,659(1/2):216-223.
[63]Pisarenko AN,Stanford BD. Rapid analysis of perchlorate,chlorate and bromate ions in concentrated sodium hypochlorite solutions[J].Analytica Chimica Acta,2010,659(1-2):216.
[64]Leonidas M,Emmanouil M,Antonis K,et al.Determination of chlorate,perchlorate and bromate anions in water samples by microbore reversed-phase liquid chromatography coupled to sonic-spray ionization mass spectrometry[J].Rapid Commun.Mass Spectrom.2017,31,911-918.
[65]Tefera S,Ehling S,Ho P. Trace analysis of perchlorate anion in selected food products by reverse-phase liquid chromatography-tandem mass spectrometry[J]. Food Additives & Contaminants,2007,24(11):1203-1208.
[66]谢永洪,杨坪,钱蜀.高效液相色谱-电喷雾离子源-串联三重四极杆质谱法分析地表水中高氯酸盐[J].中国环境监测,2014(1):974-977.
[67]吴映璇,林峰,姚仰勋,等.固相萃取/^18O标记高氯酸根稀释高效液相色谱-串联质谱法测定水果中的高氯酸盐[J].分析测试学报,2016,35(3):355-358.
[68]吴映璇,邵琳智,林峰.进出口食品中高氯酸盐的测定:中国,4089[P].2015-9-1.
[69]祝建华,刘艳明,郭志谋.亲水作用色谱一串联质谱法检测乳粉及婴幼儿配方乳粉中氯酸盐、高氯酸盐和澳酸盐的方
法:中国,37218[P].2016-09-19.
[70]Hao J,Han M,Li J,et al. Surface modification of silver nanofilms for improved perchlorate detection by surface-enhanced Raman scattering[J]. Journal of Colloid and Interface Science,2012,377(1):51-57.
[71]Kumar R,Kumar S,Singh P,et al. A fluorescent chemosensor for detection of perchlorate ions in water[J]. Analyst,2012,137:4913-4916.
[72]Wu F,Zhou X,Zhang R,et al. The effects of ammonium perchlorate on thyroid homeostasis and thyroid-specific gene expression in rat[J]. Environ Toxicol,2012,27:445-452.
[73]Asami M,Yoshida N,Kosaka K. Contribution of tap water to chlorate and perchlorate intake:a market basket study[J]. Science of The Total Environment,2013,12:199-208.
[74]MEH Bergmann,T Iourtchouk,W Schmidt. Laboratoryand technical-scale comparison of chlorate and perchlorate formation during drinking water electrolysis:a field study[J]. Journal of Applied Electrochemistry,2015,45(7):1-14.
[75]Asami M,Kosaka K,Simazaki D. Generation characteristics of chlorate and perchlorate in electrolysis of salt water using six anodes of different materials[J]. Journal of Japan Society on Water Environment,2014,37(5):189-195.
