干醇-水氧化钙的制备及催化水解COS的研究
2018-04-24韩春玉赖君玲罗根祥
韩春玉, 江 鹏, 柳 叶, 赖君玲, 罗根祥
(辽宁石油化工大学 化学化工与环境学部,辽宁 抚顺 113001)
羰基硫(COS)广泛存在于焦炉气、水煤气、天然气、液化石油气等许多与煤化工、石油化工有关的重要工业气体中,在化工生产中COS会腐蚀管线,毒化催化剂。未经处理直接排放到大气的COS会导致酸雨、光化学反应等一系列环境问题[1-2],威胁人类与动植物的安全。水解法脱除COS是目前研究者关注的方法[3-6]。
干水是一个自由流动粉末组成的微液滴,它是由水与疏水性二氧化硅纳米粒子高速搅拌混合而成,它包含质量分数为10%~20%的疏水性纳米二氧化硅。
由于乙二醇本身对于COS具有一定吸收能力[7],干醇-水是将醇与水都包裹进了疏水性二氧化硅纳米粒子中,在添加了碱性活性组分后制成的干醇-水,显著增强了对羰基硫的脱除能力[8]。干水、干碱本身显中性,有着无腐蚀性的优点,对油品及管道都无害[9-12]。本文主要研究了干醇-水氧化钙的制备条件、碱性及其用于催化水解COS的性能,目的在于开发一种新的脱除COS的催化剂。
1 实验部分
1.1 试剂与仪器
试剂:氧化钙(分析纯,国药集团化学试剂有限公司);乙二醇(分析纯,沈阳市东兴试剂厂);疏水性纳米二氧化硅(比表面积230 m2/g,粒径7~40 nm,阿拉丁试剂);COS气体(200.5 mg/m3,大连光明特种气体有限公司)。
仪器:FA2004N电子天平,上海箐海仪器有限公司;GC7900型气相色谱仪,天美(中国)科学仪器有限公司。
1.2 干醇-水的制备
将40 mL去离子水和40 mL乙二醇进行混合,形成醇-水的溶液,然后将醇-水的溶液和20 g疏水性纳米二氧化硅于高速搅拌器中搅拌10 s,得到的产品密封保存[8]。
1.3 干醇-水氧化钙的制备
干醇-水氧化钙的制备方法为[8]:将1 g氧化钙搅拌下加入到40 mL乙二醇和40 mL去离子水形成的醇-水溶液中,然后加入到19 g疏水性纳米二氧化硅中于高速搅拌器中搅拌,高速搅拌10 s,得到混合溶剂的干醇-水催化剂。
1.4 COS催化水解
(1) 装填催化剂:将2 g催化剂装入反应器(内径20 mm、长度15 cm)中,并用玻璃棉密封好;
(2) 检查气密性:装置连接好后,用肥皂水检查装置的气密性,确保装置的气密性良好;
(3) 色谱分析仪脱除COS条件的设定和调试:开启气相色谱仪并设置好色谱分析实验条件(进样口温度120 ℃,柱箱温度120 ℃,FPD检测器温度160 ℃。),直到各参数稳定;
(4) 脱除COS实验:设置好COS催化水解实验条件,开始进行COS催化水解实验,并采用气相色谱测出COS原料气的出口峰面积以及COS催化水解后的出口峰面积,计算出COS的水解转化率:η=(A0-Ai)/A0(其中,A0为COS入口的浓度对应的峰面积;Ai为COS出口的浓度对应的峰面积)。
2 结果与讨论
2.1 干醇-水催化剂催化水解COS的影响
乙二醇有两个羟基,能够与COS中的氧原子形成氢键,具有吸收COS的能力[7],因此实验中选择乙二醇来制备干醇-水催化剂,并用于COS催化水解的研究。
实验条件为:室温、COS体积流量10 mL/min、干醇-水催化剂(该催化剂合成条件为:20 g疏水性纳米二氧化硅、去离子水40 mL、乙二醇40 mL、搅拌10 s)质量2.0 g考察该催化剂用于COS水解的影响,实验结果见图1。

图1 干醇-水对COS转化率的影响Fig.1 The effect of dry glycol-water on COS conversion
从图1可以看出,在反应15 min时COS的转化率接近100%,但随着反应的进行,COS的转化率降低很快,在反应进行到40 min时COS的转化率降低到40%左右。
造成这一实验现象的原因可能是:乙二醇和水混合后使乙二醇分子间的氢键作用受到破坏,乙二醇和水分子之间形成了更多的分子间氢键,从而表现为对COS的吸收能力增强,即表现为在反应15 min时COS的转化率接近100%,但随着反应的进行,该催化剂吸收COS的能力基本达到饱和,从而表现为COS的转化率迅速降低;本实验中制备干醇-水的催化剂中乙二醇和去离子水的体积比为1∶1,即为体积分数50%的乙二醇水溶液,结合文献[7]中体积分数为50%的乙二醇水溶液在室温下对COS的吸收能力为14.436 4 mg/L,通过计算得到干醇-水催化剂吸收COS达到饱和的吸收时间为11 min,这一数值和图1中反应时间为10 min时COS的转化率为100%相一致,因此随着反应的进行,COS的转化率开始降低。
2.2 干醇-水氧化钙催化剂的形态
为了提高干醇-水催化剂的活性,选择氧化钙作为活性组分[9],制备了干醇-水氧化钙。
实验中合成的不同干醇-水氧化钙催化剂的形态见表1和图2。
从表1和图2可以看出,仅有乙二醇的体积为64 mL,去离子水的体积为16 mL时没有得到白砂糖状的干醇-水氧化钙,其它干醇-水氧化钙均为白砂糖状,可以作为脱除COS 催化水解的催化剂,来考察其脱除COS的转化率[12]。

表1 干醇-水氧化钙的形态Table1 The shape of dry glycol-water-calcium-oxide

图2 干醇-水氧化钙的形态图片
Fig.2Thepicturesofdryglycol-water-calciun-oxide
2.3 干醇-水氧化钙的碱性
实验中选择的氧化钙及醇水中的氧化钙pH均显示为碱性,而干醇-水及干醇-水氧化钙的pH均显示为中性。因此合成的产品几乎没有腐蚀性。代表的pH测试结果见图3。

图3 干醇-水氧化钙、醇-水氧化钙及干醇-水氧化钙的pH测试结果Fig.3 The pH pictures of dry glycol-water base,glycol-water calcium oxide and dry glycol-water calcium oxide
其中催化剂合成条件为:a中1.0 g氧化钙、19 g疏水性纳米二氧化硅、去离子水40 mL、乙二醇40 mL、搅拌10 s;b1中乙二醇40 mL、去离子水40 mL、1.0 g氧化钙;b2催化剂的组成同a的组成。
2.4 氧化钙质量对COS转化率的影响
温度室温、体积流量10 mL/min、干醇-水氧化钙 (其中碱性干醇-水氧化钙组成为:40 mL乙二醇、40 mL去离子水、氧化钙和疏水性纳米二氧化硅的质量和为20 g,搅拌时间10 s) 2.0 g。考察不同氧化钙质量的催化剂对COS转化率的影响,实验结果见图4。
从图4可以看出,除了氧化钙质量为0.5 g时COS的转化率低,其它3种含量的催化剂COS的转化率均为100%。在图4中,氧化钙质量为1.0、1.5、2.0 g时三条线重合为一条线,因此得到最佳氧化钙质量为1.0 g。即干醇-水氧化钙制备条件为:1.0 g氧化钙、19 g疏水性纳米二氧化硅、40 mL乙二醇、40 mL去离子水、搅拌10 s。
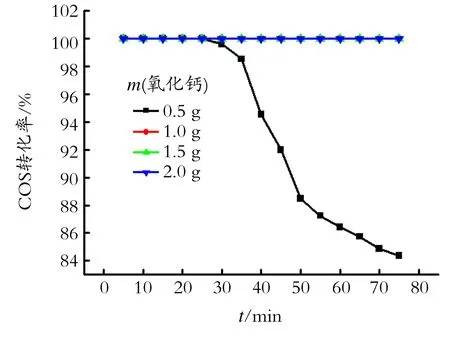
图4 氧化钙质量对COS转化率的影响
Fig.4TheeffectofthedosageofcalciumoxideonCOSconversion
2.5 醇-水体积比对COS转化率的影响
乙二醇和水的体积比关系到催化剂对COS 的吸收能力,因此实验中制备了不同乙二醇水体积比的催化剂,并考察其脱除COS的影响。
脱除COS的实验条件为:温度室温、体积流量10 mL/min、催化剂2.0 g。催化剂制备条件为:1.0 g氧化钙、19 g疏水性纳米二氧化硅,搅拌10 s,其中乙二醇和去离子水的总体积为80 mL,分别考察乙二醇和去离子水4种不同体积比(40∶40、32∶48、24∶56、8∶72)的催化剂对COS转化率的影响,实验结果见图5。

图5 乙二醇和水的体积比对COS转化率的影响
Fig.5Theeffectofvolumeratioofglycol-wateronCOSconversion
从图5可以看出,只有乙二醇和去离子水体积比为40∶40 的催化剂COS的转化率最好,在0~75 min转化率为100%。这一实验结果和文献[9]中的相一致。认为当乙二醇和去离子水的体积比40∶40时,乙二醇和水形成了较强的氢键缔合作用,从而比其它体积比时的作用强,因而表现为在乙二醇和水体积分别为40 mL和40 mL时COS的转化率最高。因此最佳催化剂制备条件为:1.0 g氧化钙、19 g疏水性纳米二氧化硅、40 mL乙二醇、40 mL去离子水、搅拌时间10 s。
2.6 体积流量对COS转化率的影响
实验条件为:温度室温、催化剂质量2.0 g(最佳催化剂配比:1.0 g氧化钙、19 g疏水性纳米二氧化硅、40 mL乙二醇、40 mL去离子水、搅拌时间10 s)。考察不同体积流量对COS转化率的影响,实验结果见图6。
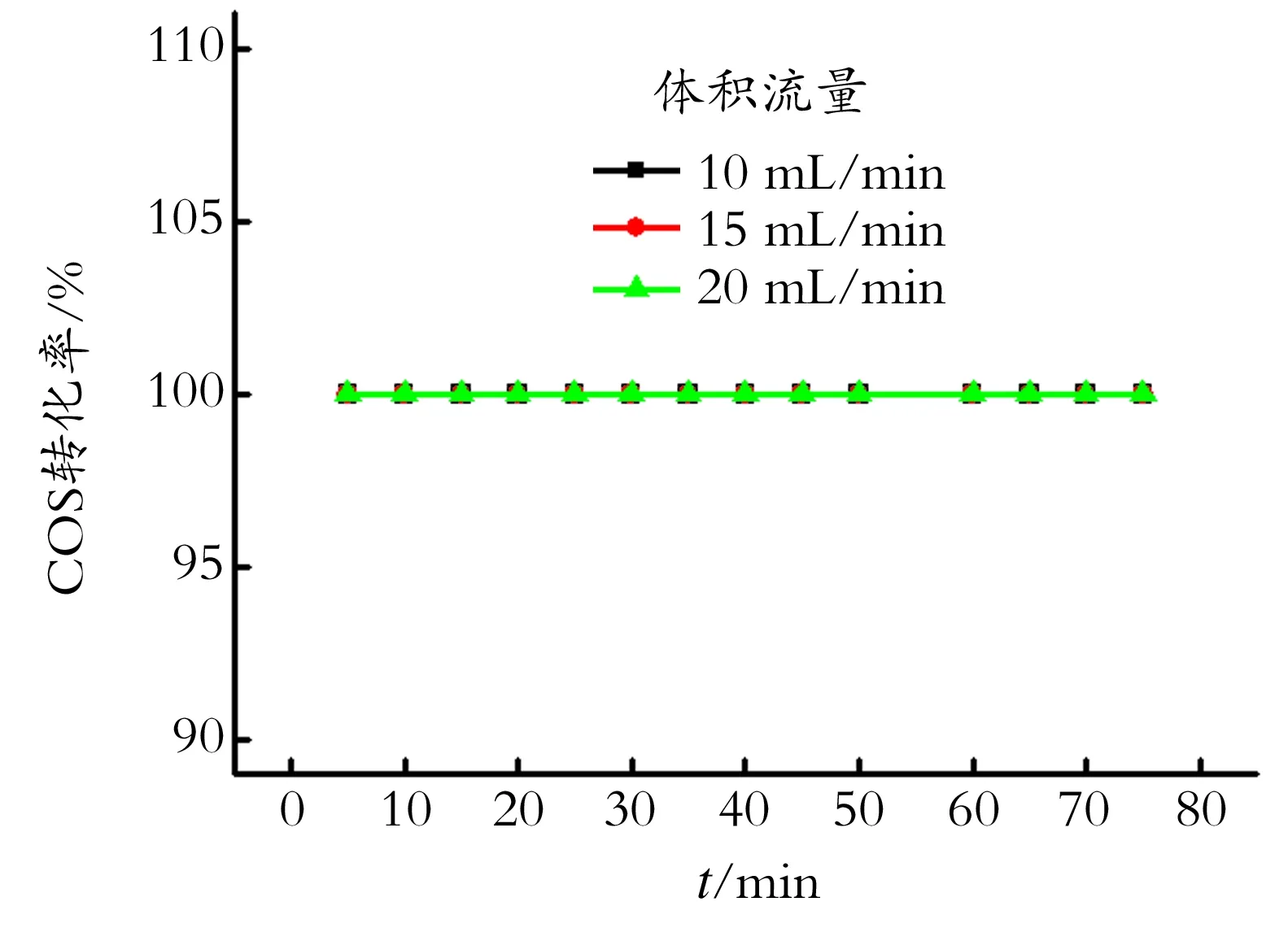
图6 不同气体流量对COS转化率的影响
Fig.6TheeffectofgasflowonCOSconversion
从图6可以看出,在反应时间为0~75 min,体积流量分别为10、15、20 mL/min时COS的转化率均为100%,实验中选择体积流量为10 mL/min作为最佳体积流量。
2.7 使用寿命的考察
温度室温、催化剂2.0 g、体积流量10 mL/min。考察该催化剂的使用寿命,实验结果见图7。从图7可以看出,在反应120 min时COS的转化率接近100%,随着反应的进行,在200 min时,COS的转化率开始降低到90%以下,因此该催化剂的COS转化率高于90%时的使用寿命为3.25 h。
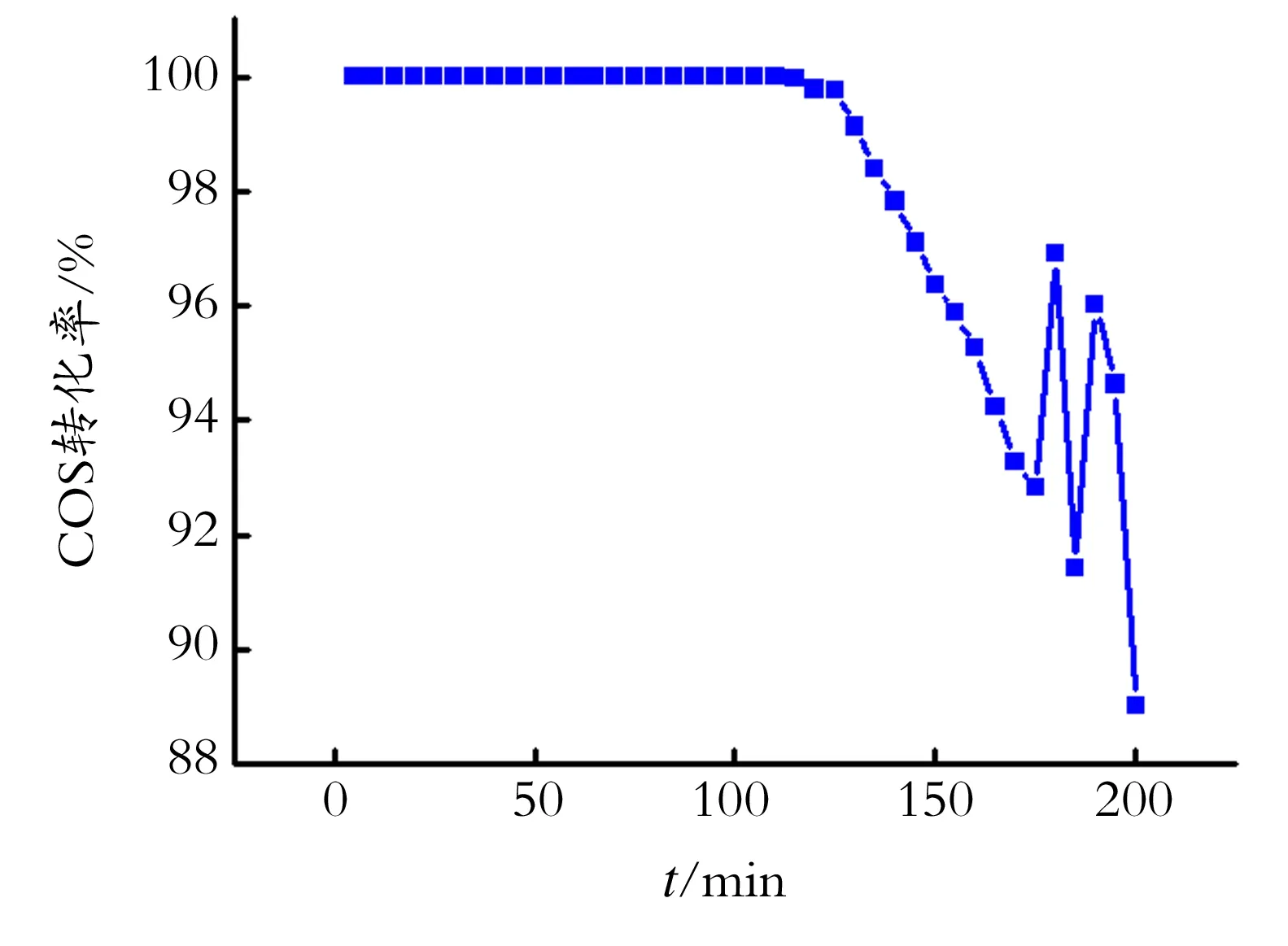
图7 催化剂寿命的考察
Fig.7Theinvestigateofthecatalystonitsservicelife
3 结论
实验中考察了干醇-水氧化钙的制备条件对其形态的影响,并确定该催化剂的pH为中性,无腐蚀性。筛选出干醇-水氧化钙的最佳制备条件为:氧化钙1.0 g、40 mL乙二醇、40 mL去离子水、疏水性纳米二氧化硅19 g、搅拌时间10 s;温度为室温、气体流量10 mL/min、干醇-水氧化钙(最佳催化剂组成)催化剂质量2 g条件下催化COS水解转化率在90%时,该催化剂的使用寿命为3.25 h。
[1] Campbell J E,Whelan M E,Seibt U,et al. Atmospheric carbonyl sulfide sources from anthropogenic activity: Implications for carbon cycle constraints[J]. Geophysical Research Letters, 2015,42(8): 3004-3010.
[2] Commane R,Herndon S C,Zahniser M S,et al. Carbonyl sulfide in the planetary boundary layer: Coastal and continental influences[J]. Journal of Geophysical Research: Atmospheres,2013,118(14): 8001-8009.
[3] 张益群,肖忠斌,马建新,等. 稀土氧硫化物上的羰基硫水解反应[J]. 高等学校化学学报, 2004, 25(4): 721-724.
Zhang Y Q, Xiao Z B, Ma J X,et al. Hydrolysis of COS over rare earth oxysulfides[J].Chemical Journal of Chinese Universities, 2004, 25(4): 721-724.
[4] 王会娜,上官炬, 王晓鹏, 等. 羰基硫催化水解研究进展[J]. 工业催化, 2007, 15(2): 18-21.
Wang H N, Shangguan J, Wang X P,et al. Advances in catalytic hydrolysis of carbonyl sulfide[J]. Industrial Catalysis, 2007,15(2): 18-21.
[5] 陈杰, 李春虎, 赵伟,等. 羰基硫水解转化脱除技术及面临的挑战[J]. 现代化工, 2005, 25(Z1): 293-295.
Chen J, Li C H, Zhao W, et al. Technique for removal of carbonyl sulfide by hydrolysis[J]. Modern Chemical Industry, 2005, 25(Z1):293-295.
[6] 高宇,王景芸,王欣,等.芳酮类化合物脱除苯甲酰基反应的研究[J].辽宁石油化工大学学报,2015,35(1):1-3;7.
Gao Y,Wang J Y,Wang X,et al.Study on thereaction of aromatic ketones removal benzoyl[J].Journal of Liaoning Shihua University,2015,35(1):1-3;7.
[7] 刘文秀. 乙二醇吸收羰基硫的实验及机理研究[D]. 呼和浩特: 内蒙古工业大学, 2007.
[8] Robert D, Benjiamin O, Wang W X. ‘Dry bases’: Carbon dioxide capture using alkaline dry water[J]. Energy & Environmental Science, 2014,7(5): 1786-1791.
[9] 赵风云, 赵华, 赵瑞红, 等. 石灰石和氧化钙脱除H2S和COS动力学研究[J]. 化学工程, 2007, 34(12): 31-35.
Zhao F Y, Zhao H, Zhao R H,et al. Kinetics on removal of H2S and COS with CaCO3and CaO[J]. Chemical Engineering(China), 2007, 34(12):31-35.
[10] 沈丽娟, 王高杰, 郑笑笑,等. Cu-MOFs的生长调控及其催化水解羰基硫的性能[J]. 催化学报,2017,38(8):1373-1381.
Shen L J, Wang G J, Zheng X X,et al. Tuning the growthof Cu-MOFs for efficient catalytic hydrolysis of carbonyl sulfide[J]. Chinese Journal of Catalysis, 2017,38(8):1373-1381.
[11] 柯明,陈冬,冯琪,等. 羰基硫和醇胺溶液反应机理及反应动力学研究进展[J]. 化工科技, 2014, 22(6):71-74.
Ke M, Chen D, Feng Q, et al. Research progress on the reaction mechanism and kinetics of carbonyl sulfide and hydramine[J]. Science & Technology in Chemical Industry, 2014, 22(6):71-74.
[12] 王冠, 孙同华, 张宏波, 等. 催化水解法低温脱除煤气中羰基硫的研究[J].现代化工,2014,34(1):60-63.
Wang G, Sun T H, Zhang H B, et al. Carbonyl sulfide gas removal by catalytic hydrolysis in low temperature[J]. Modern Chemical Industry, 2014,34(1):60-63.
