石墨烯-铜纳米粒子修饰电极电化学检测L-半胱氨酸
2018-04-21程原生吴锁柱
程原生,刘 敏,吴锁柱
(1.山西农业大学实验教学中心,山西晋中 030801;2.山西农业大学食品科学与工程学院,山西晋中 030801)
0 引言
L-半胱氨酸是生物体内一种常见的氨基酸,可参与生物体内许多重要的生化反应,如参与谷胱甘肽的合成及细胞还原过程,具有抗氧化、抗衰老、解毒等功能[1]。L-半胱氨酸也可用于食品加工中,如在面包料中,可促进其发酵、出模,防止老化;在天然果汁中,可防止VC氧化,避免果汁变褐色;在焙烤制品中,是面团改良剂的必需成分,可促进面筋形成等。因此,对L-半胱氨酸的测定具有十分重要的意义。
目前,检测L-半胱氨酸常采用分光光度法[2]、高效液相色谱法[3-4]、荧光法[5]、酶法[6]等。但这些方法大都操作复杂、价格昂贵、重复性差、选择性低,不利于快速分析。与上述方法相比,电化学分析法具有成本低、灵敏度和准确度高、分析速度快等优点,所以,国内外已建立多种对L-半胱氨酸含量测定的电化学方法[7-10]。
试验采用石墨烯-铜纳米粒子修饰的玻碳电极建立一种电化学检测L-半胱氨酸方法。首先对玻碳电极进行预处理,然后在玻碳电极表面依次修饰石墨烯与铜纳米粒子。利用循环伏安法及计时电流法对L-半胱氨酸进行测定,考查了缓冲液pH值对试验测定的影响。在最优pH值条件下,研究了该修饰电极对L-半胱氨酸的响应性能。
1 材料与方法
1.1 试剂与材料
氧化石墨,选用南京先丰纳米材料科技有限公司产品;L-半胱氨酸、蔗糖、硝酸铝、酒石酸、葡萄糖、亚硝酸钠、氯化钙、抗坏血酸、氯化镁、氯化铁、氢氧化钠、高氯酸锂等试剂,选用上海晶纯生化科技股份有限公司产品;试验用水为去离子水。
1.2 石墨烯-铜纳米粒子修饰电极的制作
首先,用粒径为0.5 μm和0.05 μm的氧化铝抛光湿粉对玻碳电极(直径3 mm)预处理,之后在去离子水中超声清洗3 min;接着,采用之前研究的电沉积法将石墨烯修饰在电极表面[11];最后,将石墨烯修饰电极浸入0.05 mol/L硫酸铜和0.1 mol/L硫酸钠混合溶液中沉积铜纳米粒子,沉积电位为-1.0 V,沉积时间为120 s,即可制得石墨烯-铜纳米粒子修饰电极。
1.3 L-半胱氨酸的测定
将石墨烯-铜纳米粒子修饰的玻碳电极作工作电极、银-氯化银电极(3.0 mol/L氯化钾)作参比电极、铂丝为对电极,采用循环伏安法及计时电流法对L-半胱氨酸测定。
2 结果与分析
2.1 L-半胱氨酸在石墨烯-铜纳米粒子修饰电极上的电化学行为
0.1 mol/L L-半胱氨酸在裸玻碳电极上的循环电流见图1,0.1 mol/L L-半胱氨酸在石墨烯修饰的玻碳电极上的循环电流见图2,0.1 mol/L L-半胱氨酸在石墨烯-铜纳米粒子修饰的玻碳电极上的循环电流见图3。
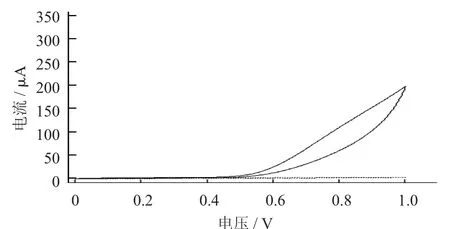
图1 0.1 mol/L L-半胱氨酸在裸玻碳电极上的循环电流
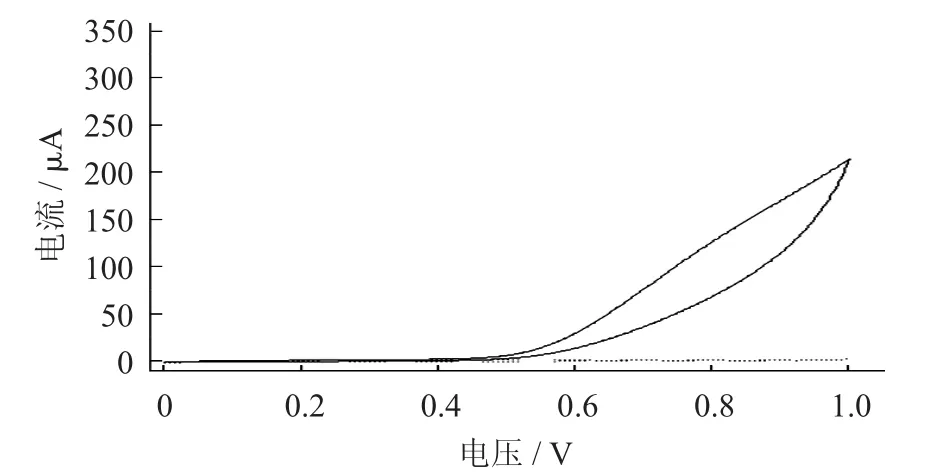
图2 0.1 mol/L L-半胱氨酸在石墨烯修饰的玻碳电极上的循环电流
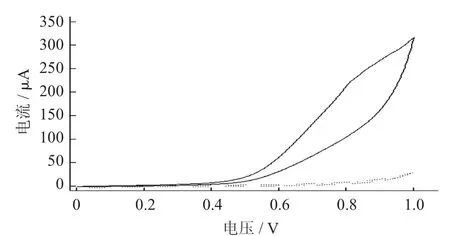
图3 0.1 mol/L L-半胱氨酸在石墨烯-铜纳米粒子修饰的玻碳电极上的循环电流
图1 ~图3分别为0.1 mol/L L-半胱氨酸(支持电解质为0.1 mol/L磷酸缓冲溶液,pH值7.0) 在裸玻碳电极、石墨烯修饰的玻碳电极及石墨烯-铜纳米粒子修饰的玻碳电极上的循环电流图。由这些图可知,与背景信号(虚线)相比,当L-半胱氨酸存在时(实线),在3种电极上均可观察到明显的氧化峰。而且,随着石墨烯、铜纳米粒子的依次修饰,获得L-半胱氨酸的氧化峰电流信号逐渐增大。这些结果表明石墨烯和铜纳米粒子成功修饰在玻碳电极表面,且二者共同修饰对L-半胱氨酸的氧化存在协同作用。
2.2 缓冲液pH值的影响
采用循环伏安法研究了石墨烯-铜纳米粒子修饰电极对0.001 mol/L L-半胱氨酸在不同pH值(4.0~10.0)的磷酸缓冲液的响应,采集0.8 V处的峰电流值对缓冲液pH值作图。
缓冲液pH值对0.001 mol/L L-半胱氨酸峰电流的影响见图4。
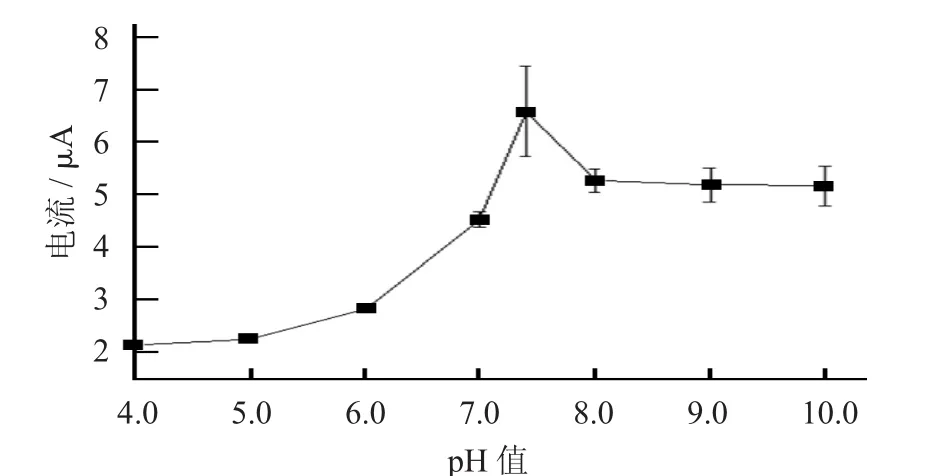
图4 缓冲液pH值对0.001 mol/LL-半胱氨酸峰电流的影响
由图4可知,随着缓冲液pH值从4.0升高至10.0,峰电流值呈现先增加后降低的趋势,且在pH值7.4时达到最大。因此,后续选择pH值7.4的磷酸缓冲液进行L-半胱氨酸的测定。
lncRNA在肺癌、神经系统肿瘤、消化系统肿瘤及其他肿瘤中调节自噬可以增强化疗药物敏感性、减少耐药性;在心肌细胞及脑细胞缺血再灌注中,lncRNA通过调节自噬减少细胞凋亡;lncRNA的改变影响了神经细胞的自噬过程,找到了治疗神经退行性疾病的新方法;在细菌的感染中,lncRNA调节自噬的过程可能成为根除病原体、抵抗炎症反应的重要途径。另外,不仅局限在以上疾病中,还有研究提示,lncRNA通过调节细胞自噬影响治疗药物的敏感性,如胰岛素[31]。因此,在更多领域中进一步研究lncRNA调控自噬过程仍有许多挑战。
2.3 不同浓度L-半胱氨酸的检测
用计时电流法研究了石墨烯-铜纳米粒子修饰的玻碳电极对不同浓度的L-半胱氨酸的响应(施加电位为0.8 V)。在搅拌状态下,待背景信号稳定后,将 0.2,0.5,1.0,2.0,5.0,10.0,20.0,50.0,100.0,200.0,500.0,1 000.0 μmol/L的 L- 半胱氨酸溶液依次加入背景溶液中(每隔30 s加1次,每种浓度填加5次),记录电流信号随时间的变化(图5)。
L-半胱氨酸在石墨烯-铜纳米粒子修饰的玻碳电极上的计时电流图(插图为50~1 000 s时的信号放大图) 见图5。
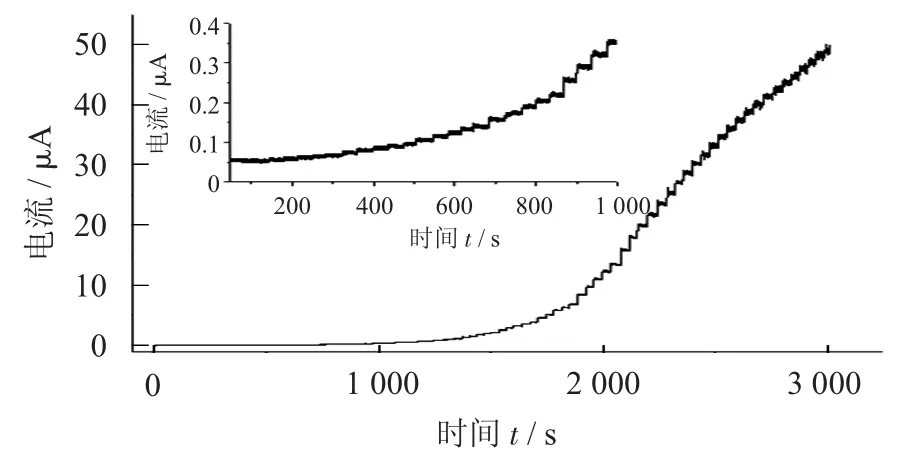
图5 L-半胱氨酸在石墨烯-铜纳米粒子修饰的玻碳电极上的计时电流图(插图为50~1 000 s时的信号放大图)
由图5可知,随着L-半胱氨酸的不断加入,电流值逐渐增大,响应时间为4~5 s,且电流与浓度在 0~4 443.5 μmol/L及 5 443.5~27 443.5 μmol/L时分别呈现良好的线性关系(相关系数分别为0.994 8,0.993 8),检出限为2×10-8mol/L。
电流与L-半胱氨酸浓度的线性拟合图见图6。
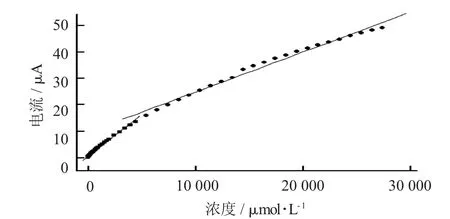
图6 电流与L-半胱氨酸浓度的线性拟合图
2.4 重现性
对0.001 mol/L L-半胱氨酸平行测定7次,获得的峰电流值的相对标准偏差为6.73%,表明该方法的重现性良好。
2.5 选择性
采用计时电流法考查了同浓度的蔗糖、葡萄糖、氯化钙、氯化镁、氯化铁、硝酸铝、酒石酸、亚硝酸钠、抗坏血酸对2×10-5mol/L L-半胱氨酸测定的影响。试验结果表明,除抗坏血酸外,同浓度的上述物质对L-半胱氨酸的检测影响可忽略不计,表明石墨烯-铜纳米粒子修饰的玻碳电极对L-半胱氨酸的测定具有良好的选择性。
3 结论
采用电沉积法依次将石墨烯和铜纳米粒子修饰到玻碳电极表面,构建了一种基于石墨烯-铜纳米粒子修饰电极电化学检测L-半胱氨酸的新方法。经研究缓冲液pH值对L-半胱氨酸检测的影响,获得最佳pH值为7.4。进一步采用计时电流法对不同浓度L-半胱氨酸进行检测,获得该方法对L-半胱氨酸的检测范围为0~0.027 mol/L,检出限为2×10-8mol/L,响应时间为4~5 s。该方法具有检测范围宽、检出限低、分析速度快、重现性好、选择性高等优点。
参考文献:
[1]刘红丽,胡慧,周晓东,等.半胱氨酸传感器的研究进展 [J].分析科学学报,2013,29(2):271-276.
[2]张一敏,乔月纯,李全民.Cu(Ⅱ)为探针-分光光度法测定半胱氨酸 [J].理化检验(化学分册),2012,48(8):943-945.
[3]靳文仙,阎卉,刘衡,等.高效液相色谱法测定复方半胱氨酸注射液中半胱氨酸的含量 [J].天津药学,2008,20 (2):13-15.
[4]王洋,李兆辉,朱海超,等.HPLC法测定蛋白质粉中L-半胱氨酸的含量 [J].中国药房,2012(29):2 753-2 754.
[5]杨志广,任加诚,彭鹏,等.一种半胱氨酸荧光探针的合成及光学性质 [J].食品工业,2017,38(5):200-203.
[6]赵锐,戴雯,徐万州,等.循环酶法检测血清同型半胱氨酸方法学评价及其在肿瘤诊断中的应用 [J].检验医学与临床,2016(24):3 437-3 439.
[7]姜瑞,杨学梅,王明丽,等.富镉离子CdS量子点电化学发光法检测L-半胱氨酸 [J].分析化学,2017,45(3):409-415.
[8]袁爱国,李斌,陈健平,等.氧化石墨烯/二氧化铈-镍铝-层状双金属氢氧化物复合材料制备L-半胱氨酸传感器 [J].食品科学,2016,37(14):144-148.
[9]王青,刘卫,羊小海,等.纳米金颗粒增强信号的电化学生物传感器用于谷胱甘肽和半胱氨酸的检测 [J].高等学校化学学报,2013,34(8):1 845-1 850.
[10]王芳,郑阿萍,王力,等.酸奶中L-半胱氨酸的电化学检测 [J].中国食品学报,2012,12(9):204-208.
[11]吴锁柱,郭俊杰,韩悌云,等.石墨烯修饰电极电化学检测食盐中碘 [J].山西农业大学学报(自然科学版),2015,35 (4):441-444.◇
