口腔鳞状细胞癌中Dickkopf-3基因的表达及甲基化状态
2018-04-12张素欣张鑫陈中李天客包阳郑晶张雨温
张素欣 张鑫 陈中 李天客 包阳 郑晶 张雨温
口腔颌面部恶性肿瘤中90%以上是口腔鳞状细胞癌(oral squamous cell cancer,OSCC)[1]。据统计,中国每年新发的口腔颌面部恶性肿瘤病例约4.65万人,5岁和70岁是两个相对发病最高点[2]。虽然多学科综合序列治疗模式运行多年,患者的5年生存率仍仅停留在60%左右,寻找代表肿瘤侵袭性及复发率的个性化生物标志物,可以促进针对性精准治疗,减少复发率,提高生存率[3]。
DKK-3是Wnt信号传导通路的分泌性拮抗剂之一[4]。有学者发现 DKK-3基因在食管癌[5]、肺癌[6]等组织中存在异常甲基化,但该基因在口腔黏膜鳞癌中的表达及甲基化状态鲜有问津,本实验通过应用RT-PCR和MSP技术检测口腔鳞状细胞癌组织中DKK-3基因mRNA的表达和启动子甲基化状态,并分析mRNA表达和甲基化与临床资料之间的关系,探讨该基因的存在状态在口腔鳞癌发生发展的关系,为肿瘤靶向治疗提供实验依据。
1 资料与方法
1.1 临床资料
随机选取河北医科大学第四医院口腔科2014-09~2015-12期间51例经手术治疗的初诊原发口腔鳞癌患者为研究对象,标本均经病理证实。所有标本均为术后立即取材,-80℃冰箱中冻存。发病部位包括舌、牙龈、颊等部位,年龄在31~88岁之间,中位年龄58岁,男女性别比为1.43∶1。Ⅰ期9例,Ⅱ期27例,Ⅲ期6例,Ⅳ期9例。本实验已获得患者及家属的知情同意。
1.2 主要试剂
5-氮-2′-脱氧胞苷 (5-aza-2deoxycytidine,5-AzadC)、氢醌、亚硫酸氢钠(Sigma,美国);蛋白酶 K(Merck,德国);Wizard DNA纯化试剂盒(Promega,美国);Trizol(Invitrogen,美国),引物(北京赛百胜公司合成);即用型免疫组织化学SP试剂盒(SP-9000)(北京中杉金桥生物技术有限公司)。
1.3 方法
1.3.1 MSP法检测 提取组织DNA并进行亚硫酸氢盐处理,设计甲基化及非甲基化引物进行MSP检测,上下游引物各包含3个CG位点(图1)。DKK-3基因甲基化引物为:上游 5′-GGGGCGGGCGGCGGGGC-3′,下游 5′-ACATCTCCGCTCTACGCCCG-3′;非甲基化引物为:上游 5′-TTAGGGGTGGGTGGTG GGGT-3′,下游5′-CTACATCTCCACTCTACACCCA-3′。PCR反应条件为95℃预变性10 min后,94℃变性45 s,59℃退火45 s,72℃延伸45 s,40个循环后,72℃继续延伸10 min。用经甲基化酶(Sss I)处理以后的基因组DNA作为甲基化的阳性对照,阴性对照则用灭菌双蒸水取代DNA模板进行PCR。另随机选取10%标本进行重复实验以验证结果的可靠性。
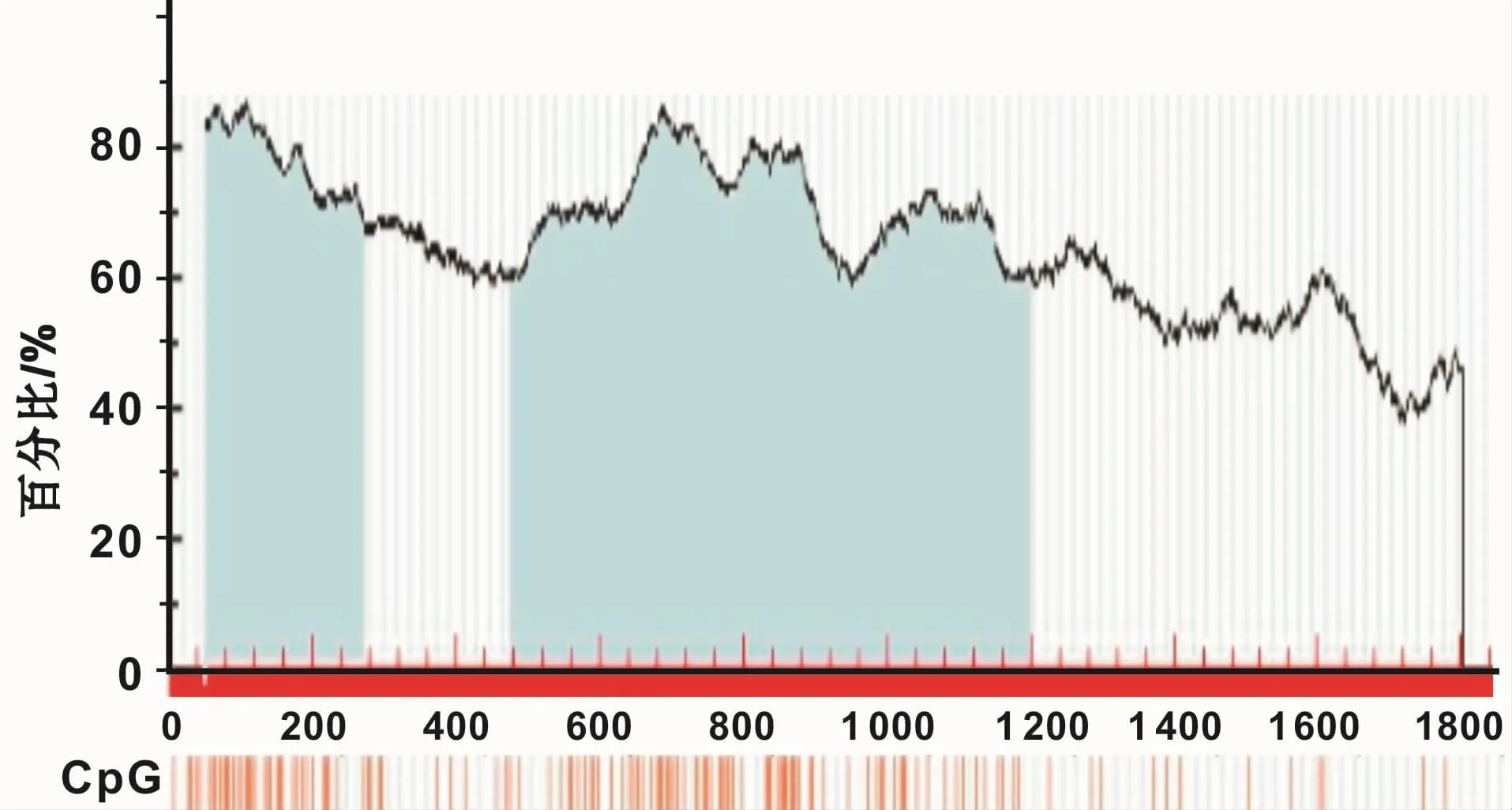
图1 DKK-3基因的CpG岛分布Fig 1 CpG island of DKK-3 gene distribution
1.3.2 RT-PCR检测 按Trizol试剂说明书提取组织总RNA,参照逆转录试剂盒 (Reverse Transcription SystemA 3500,Promega公司)说明将RNA逆转录成cDNA。用于检测DKK-3基因mRNA的引物为:上游5′-ACAGCCACAGCCTG GTGTA-3′, 下 游 5′-CCTCCATGAAGCTGCCAAC-3′(120 bp)。内参照 GAPDH的引物为:上游 5′-AGGTGAAGGTCGGAGTCAACG-3′,下游 5′-AGGGGTC ATTGATGGCAACA-3′(104 bp)。PCR反应条件为:95℃预变性3 min后,94℃变性45 s,59℃退火45 s,72℃延伸45 s,共35个循环,最后72℃继续延伸5 min。PCR产物进行2%琼脂糖凝胶电泳,GAPDH作为内参照。
1.4 统计学处理
应用SPSS 13.0软件进行数据处理及统计学分析,计量资料用配对t检验方法,计数资料用χ2检验。均采用双侧检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 DKK-3基因mRNA在OSCC组织及正常口腔黏膜中的相对表达量(图2)
DKK-3基因mRNA在OSCC组织中的相对表达量为(0.41±0.27),在其对应正常口腔黏膜中相对表达量为(0.50±0.29),二者差异显著(P<0.05)。
DKK-3基因mRNA在OSCC组织中的相对量表达情况与临床特征之间的关系(表1)。
吸烟组、临床Ⅲ期、Ⅳ期组、有淋巴结转移组DKK-3基因 mRNA的相对表达量分别为(0.22±0.16)、(0.28±0.19)、(0.24±0.17),均明显低于对照组(P<0.05),表达量与性别和年龄无关。
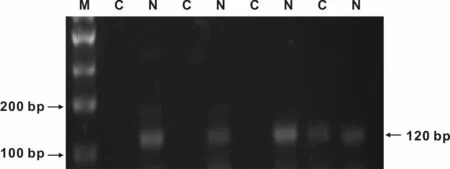
图2 DKK-3 mRNA在口腔鳞癌及正常黏膜组织中的表达Fig 2 The expression of DKK-3 mRNA in OSCC and normal oral mucosa tissue

表1 DKK-3 mRNA的表达与口腔鳞癌患者临床病理特征间的关系Tab 1 The relationship between DKK-3 mRNA expression and clinical data in OSCC tissue
2.2 口腔鳞癌组织和正常口腔黏膜中DKK-3基因启动子区的甲基化状态(图3)
DKK-3基因启动子区在OSCC组织中的甲基化率为49.0%(25/51),明显高于其对应正常口腔黏膜组织的甲基化率7.8%(4/51)(P<0.05)(表 2)。
OSCC组织中DKK-3基因启动子区甲基化情况与临床特征之间的关系(表3)。
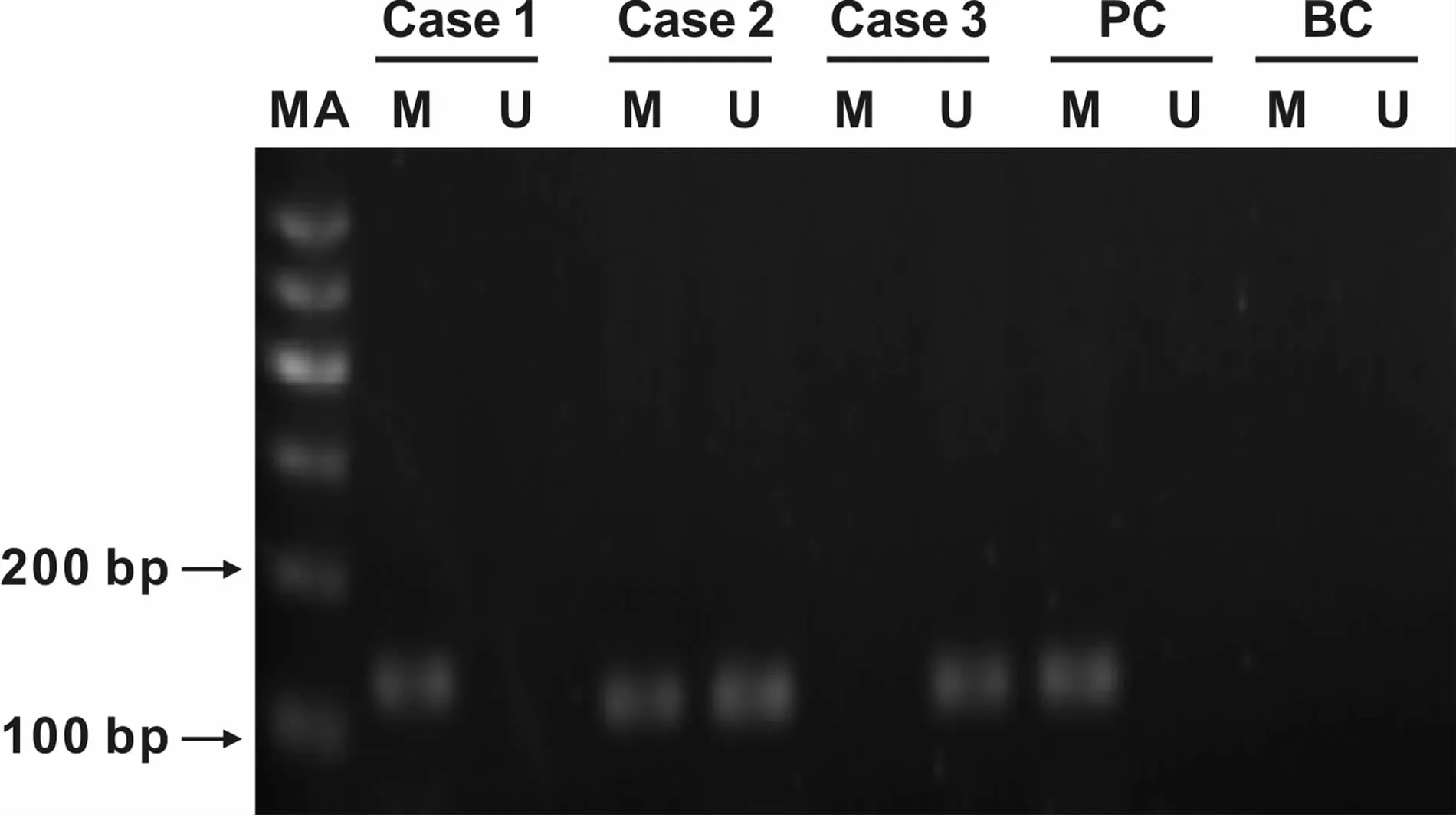
图3 DKK-3基因在口腔鳞癌及正常黏膜组织中的甲基化状态Fig 3 Methylation analysis of DKK-3 gene in OSCC and normaloralmucosa tissue

表2 DKK-3在口腔鳞癌及正常口腔黏膜组织中不同的甲基化状态Tab 2 The difference of the DKK-3 methylation between OSCC and normal oralmucosa tissue
吸烟组、临床Ⅲ期、Ⅳ期组、有淋巴结转移组的甲基化率分别为 64.3%、73.3%、50.0%,均明显高于对照组,甲基化率与性别、年龄及有无淋巴结转移无关(P>0.05)。
2.3 DKK-3基因mRNA相对表达量与甲基化阳性率的关系
DKK-3基因mRNA在甲基化阳性病例中的相对表达量为0.30±0.21,在对照组表达量为0.51±0.29(P<0.05)。

表3 DKK-3甲基化状态与口腔鳞癌患者临床病理特征间的关系Tab 3 The relationship between DKK-3 methylation and chinical data of OSCC
3 讨 论
表观遗传是通过DNA甲基化、组蛋白修饰等方式有选择性地调控目的基因的表达,促使肿瘤的发生[7]。其中DNA甲基化的基因表观修饰方式,集中发生在CpG岛,启动子区CpG岛的高甲基化是引起抑癌基因表达下调的重要机制之一[8]。
DKK-3属于DKK家族,位于染色体11P15.1位点,全长47 100 bp,该家族大都通过竞争性结合特异性受体来有效的抑制Wnt信号传导通路[9],从而参与调控机体的生物学行为。DKK-3在肝癌、乳腺癌等组织中表现为下调和缺失[10-11],本实验发现,DKK-3基因mRNA在OSCC中的相对表达量明显低于对照组,而且该基因在癌组织中表达量的高低与临床分期及淋巴结的转移明显有关,表明DKK-3表达降低可能是口腔癌发展过程中的一个重要事件,随着病变的进展,DKK-3基因mRNA的表达逐渐降低甚至沉默,提示DKK-3基因在OSCC中可能作为抑癌基因而存在,推测它的调控机制可能是因为DKK-3基因编码的蛋白是Wnt受体复合物的对抗物,DKK-3基因表达的下调使其编码的蛋白无法有效对抗Wnt受体复合物,使得游离态 β-catenin在胞内聚集,Wnt通路被异常激活,作用于下游靶基因,从而调控肿瘤细胞的生物学行为[12]。也就是说,DKK-3基因可能是通过调控Wnt信号传导通路中关键因子βcatenin的表达来异常激活经典Wnt通路,从而促进口腔癌的发生。
那么是什么原因导致了OSCC组织中DKK-3基因表达的下降呢?本研究应用MethPrimer软件对DKK-3基因进行预测分析,结果显示DKK-3基因含有9个外显子,该基因的启动子区和第1外显子区富含CpG岛,因此有理由怀疑该基因的异常甲基化可能是其表达下调的机制之一,于是又检测了DKK-3启动子区的甲基化状态,结果显示OSCC组织中DKK-3基因的甲基化率明显高于对照组,而且与临床分期有关,说明随着口腔癌的不断进展,DKK-3基因甲基化状态也不断突显,警示不良预后。另外,DKK-3基因mRNA在其甲基化阳性病例中的相对表达量显著低于对照组,分析原因可能是启动子区CpG岛5'末端调控序列甲基化后阻碍了转录因子与启动子的结合,降低了该基因的转录水平,从而使其表达下降甚至不表达,即DKK-3基因启动子区CpG岛的高甲基化可能是导致该基因表达下降甚至不表达的关键因素之一,间接参与了口腔癌的发生与发展。
因此,本研究认为以DNA甲基化为代表的表观遗传沉默是口腔癌发生发展中的重要机制之一,可以应用去甲基化药物逆转肿瘤细胞中DNA的异常高甲基化状态,修复抑癌基因的正常表达,从而控制肿瘤的发生与发展[13-14],但其可行性需进一步探索及证实。
[1]Chen AY,Myers JN.Cancer of the oral cavity[J].Dis Mon,2001,47(7):275-361.
[2]韩晟,陈衍,谢诚,等.576例口腔癌患者的流行病危险因素研究[J].实用口腔医学杂志,2012,28(1):74-78.
[3]Chauhan SS,Kaur J,Kumar M,et al.Prediction of recurrence-free survival using a protein expression-based risk classifier for head and neck cancer[J].Oncogenesis,2015,4:e147.
[4]Eskander RN,Ali S,Dellinger T,etal.Expression patterns of the Wnt pathway inhibitors dickkopf3 and secreted frizzled-related proteins 1 and 4 in endometrial endometrioid adenocarcinoma:An NRG oncology/gynecologic oncology group study[J].Int JGynecol Cancer,2016,26(1):125-132.
[5]Wang Z,Lin L,Thomas DG,et al.The role of Dickkopf-3 overexpression in esophageal adenocarcinoma[J].JThorac Cardiovasc Surg,2015,150(2):377-385.
[6]Tao L,Huang G,Chen Y,etal.DNAmethylation of DKK3 modulates docetaxel chemoresistance in human nonsmall cell lung cancer cell[J].Cancer Biother Radiopharm,2015,30(2):100-106.
[7]Jia Y,Guo M.Epigenetic changes in colorectal cancer[J].Chin JCancer,2013,32(1):21-30.
[8]Yang HJ.Aberrant DNA methylation in cervical carcinogenesis[J].Chin JCancer,2013,32(1):42-48.
[9]Noguti J,DEMoura CF,Hossaka TA,etal.The role of canonical WNT signaling pathway in oral carcinogenesis:A comprehensive review[J].Anticancer Res,2012,32(3):873-878.
[10]Yang B,Du Z,Gao YT,et al.Methylation of Dickkopf-3 as a prognostic factor in cirrhosis-related hepatocellular carcinoma[J].World JGastroenterol,2010,16(6):755-763.
[11]Kloten V,Becker B,Winner K,etal.Promoter hypermethylation of the tumor-suppressor genes ITIH5,DKK3,and RASSF1A as novel biomarkers for blood-based breast cancer screening[J].Breast Cancer Res,2013,15(1):R4.
[12]Eskander RN,Ali S,Dellinger T,et al.Expression patterns of the Wnt pathway inhibitors dickkopf3 and secreted frizzled-related proteins1 and 4 in endometrial endometrioid adenocarcinoma:An NRG oncology/gynecologic oncology group study[J].Int JGynecol Cancer,2016,26(1):125-132.
[13]Duenas-Gonzalez A,Medina-Franco JL,Chavez-Blanco A,et al.Developmental DNA methyltransferase inhibitors in the treatment of gynecologic cancers[J].Expert Opin Pharmacother,2016,17(3):323-338.
[14]Endo S,Amano M,Nishimura N,et al.Immunomodulatory drugs act as inhibitors of DNA methyltransferases and induce PU.1 up-regulation inmyeloma cells[J].Biochem Biophys Res Commun,2016,469(2):236-242.
