具有抑菌活性的氮杂环铅配合物的合成、结构及构效关系
2018-04-10白凤英王学敏曲长庆邢永恒
白凤英 王学敏 曲长庆 王 玉 邢永恒
近年来,金属铅的配位化学受到人们的广泛关注[1]。Pbギ离子具有较大的半径,配位能力强,其配位数可以在2~12之间变化[2-4],能够形成配位形式多样的配位聚合物,加上惰性电子对效应的存在,使得构筑铅的配位聚合物并研究其结构,对合成以主族金属为配位中心的新型无机-有机杂化及具有孔洞的材料具有十分重要的意义[5-6]。此外,铅也是一种对人体危害严重的微量元素,它所具有的毒性和对环境的污染以及在生产过程中对它的应用,也同样增加了人们对它的研究的浓厚兴趣。因此寻找合适的配体与之配位,利用其良好的溶解性或变成沉淀吸附于排毒剂上,不仅可以排除人体内过量的铅,而且还可以寻找其合理有效的应用途径。氮杂环类配体因其氮原子较强的配位能力,被广泛应用于构筑金属有机骨架配位聚合物。其中,1,10-菲咯啉(phen)具有平面刚性结构,同时含有2个可螯合配位的氮原子,使之成为一种应用广泛的螯合配体。另外phen是很好的π电子受体,与金属离子配位时能够形成反馈π键,可以稳定低价态的金属离子,对于金属具有很好的配位能力[7-9]。许多phen的配合物表现出良好的光化学、电化学和催化性质,并在抗肿瘤方面也具有一定的应用前景,这些配合物无论在配位化学理论研究上还是在科研生产实际过程中,都发挥着重要的作用。此类配体的金属配合物已见报道,但是其抗菌活性研究报道还不是很完善[10-11]。因此,在实验中我们分别以phen为配体设计组装了2个新颖的铅配合物[Pb(phen)(NO3)(H2O)]NO3(1),[Pb(phen)2(NO3)]NO3(2),并测定了它们晶体结构。利用琼脂扩散法测试了配合物1和2的抑菌活性。结果表明配合物1和2对2种受试菌株具有较强的抑菌活性。
1 实验部分
1.1 试剂与仪器
元素分析采用 Perkin-Elmer 240C型元素分析仪测定,红外光谱用JASCO FT/IR-480型傅立叶变换红外光谱仪(KBr压片,400~4 000 cm-1)测定,其他仪器包括RT-2100酶标仪、恒温培养箱、恒温摇床、离心机和超净工作台等。硝酸铅、phen、吲哚乙酸、甲醇、乙醇、氯化钠和二甲基亚砜均为分析纯,蛋白胨、琼脂和牛肉浸膏均为生化试剂,全部购买于上海阿拉丁生化科技股份公司。
1.2 菌种及培养
本实验所用菌种为大肠杆菌(Escherichia coli,以下简称:E.C.),革兰阴性细菌;金黄色葡萄球菌(Golden staph,以下简称 G.S.),革兰阳性细菌,由辽宁师范大学微生物实验室提供。实验所用培养基为LB的配方:牛肉浸膏3 g、蛋白胨10 g、氯化钠5 g、琼脂 15~20 g和蒸馏水 1 L,pH=7.4~7.6。 LB 培养液:不加琼脂,其它成分同固体培养基。
1.3 实验过程
1.3.1 配合物[Pb(phen)(NO3)(H2O)]NO3(1)的合成
称取0.083 g(0.25 mmol)硝酸铅(Pb(NO3)2),用 10 mL乙醇溶解得溶液a,称取0.09 g(0.5 mmol)吲哚乙酸(HIAA)和 0.05 g(0.25 mmol)的 phen,用 10 mL 乙醇溶解得溶液b,把b加入a中,得到浅黄色的有点浑浊的液体。过滤后得到浅黄色的清液。室温放置5 d,最终得到0.103 g浅黄色晶体,产率78%(以Pb计)。配合物1的分子式为C12H10N4O7Pb,元素分析按C12H10N4O7Pb 计算值(%):C 27.22,H 1.90,N 10.58;实验值(%):C 26.98,H 1.87,N 10.53。 IR(KBr,cm-1):3 368(νO-H);3 062(νAr-H);1 517(νC=N);1 496(νC=C);1 385(ν);1 139(νC-C);1 100(νC-N);854,778,725(δAr-H);558(νPb-O);415(νPb-O)。
1.3.2 配合物[Pb(phen)2(NO3)]·NO3(2)的合成
除了把phen的用量改为0.10 g(0.5 mmol),溶剂换为甲醇以外,其余试剂、用量均不变,混合后得到浅黄色的有点浑浊的液体。过滤后得到浅黄色的清液。室温放置15 d,最终得到0.123 g浅黄色晶体,产率71%(以Pb计)。元素分析按C24H16N6O6Pb计算值(%):C 41.68,H 2.33,N 12.15;实验值(%):C 41.61,H 2.29,N 12.15。 IR(KBr,cm-1):3 054(νAr-H);1 514(νC=N);1 496(νC=C);1 386(νN);1 141(νC-C);1 100(νC-N);848,776,724(δAr-H);552(νPb-O);417(νPb-O)。
1.4 晶体结构的测定
选择晶体大小为0.25 mm×0.20 mm×0.15 mm的配合物1和0.78 mm×0.61 mm×0.18 mm的配合物2,用Bruker Smart APEXⅡ CCD(Mo Kα为辐射源,λ=0.071 073 nm),在室温下收集衍射数据。衍射强度数据经Lp因子校正。晶体结构由直接法解出,对所有非氢原子坐标和各向异性温度因子进行全矩阵最小二乘法修正。氢原子坐标由理论加氢程序确定。所有计算均用SHELX-97[12]程序进行。配合物1和2的晶体学参数列于表1,配合物1和2的部分键长(nm)与键角(°)列于表 2。
CCDC:1574687,1;1574688,2。
1.5 抑菌活性实验
LB培养基、所有的实验器皿和Φ5 mm的滤纸片均在121℃灭菌30 min。将灭菌后的培养基融化并冷却到50℃左右,严格按照无菌操作倒入9 cm的培养皿中,使之冷凝成平板,放入(37±1)℃恒温培养箱中培养24 h后,检查有无杂菌产生。如无杂菌产生,则接入大肠杆菌(E.C.)和金黄色葡萄球菌(G.S.),将灭菌后的滤纸片(Φ 5 mm)平摊在含菌的LB培养基上,用二甲基亚砜溶解配合物1、2和硝
酸铅,配制成 20、10、5 和 2.5 mg·mL-1的溶液,而把phen 分别配制成 6.8、3.4、1.7、0.85 mg·mL-1(phen 1)和 10.4、5.2、2.6、1.3 mg·mL-1(phen 2)的溶液,每一片滤纸片上加入药品量10μL,在(37±1)℃ 的恒温培养箱中培养24 h[13],取出测定抑菌环直径(3个重复的平均值)(表4)。根据《消毒技术规范》对抑菌作用进行判断:抑菌圈直径大于20 mm表示具有强抑菌效果;抑菌圈在10~20 mm为中等抑菌;抑菌圈小于10 mm为弱抑菌。
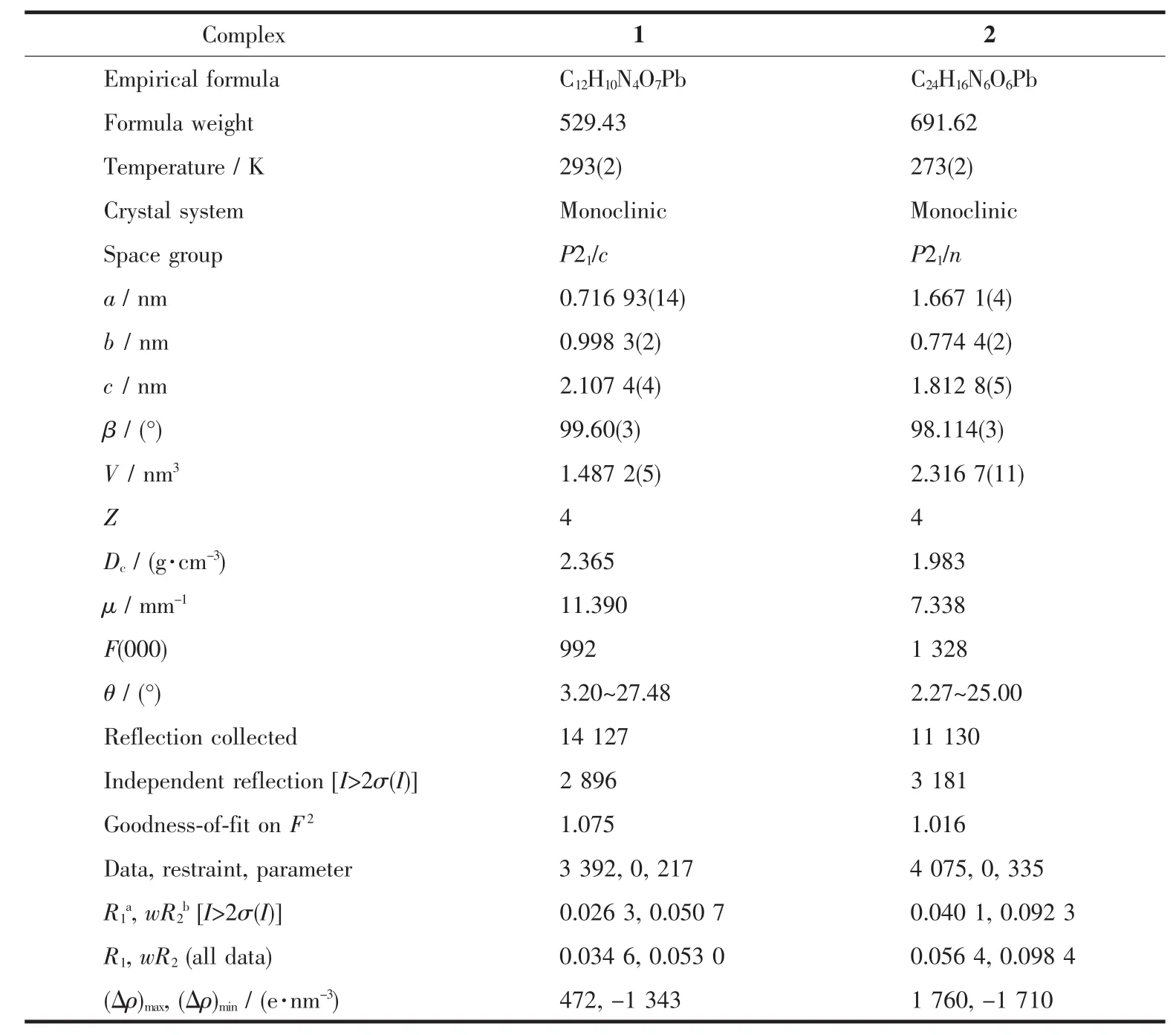
表1 配合物1和2的晶体学数据Table 1 Crystal data for complexes 1 and 2
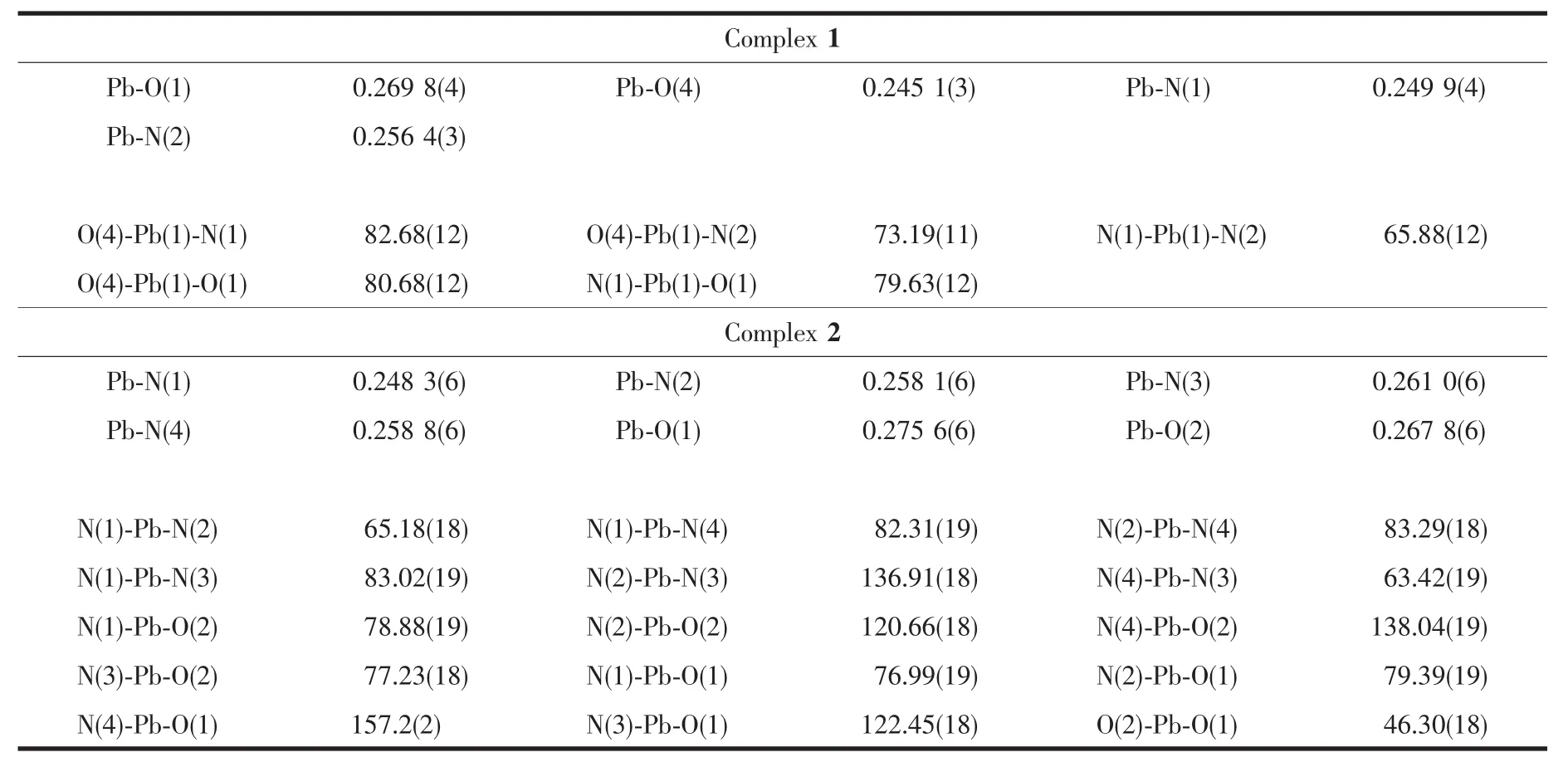
表2 配合物1和2的部分键长(nm)与键角(°)Table 2 Selected bond lengths(nm)and bond angles(°)of complexes 1 and 2
2 结果与讨论
2.1 晶体结构

图1 (a)配合物1中金属Pbギ的配位环境;(b)配合物1的一维链状结构Fig.1 (a)Coordination environment of metal Pbギin complex 1;(b)One-dimensional chain structure of complex 1
配合物1的不对称单元中存在1个四配位的金属Pb2+离子,1个phen分子,1个配位硝酸根离子和1个配位的水分子,以及1个游离的硝酸根离子。金属Pbギ的配位环境如图1a所示,Pb2+离子分别与2个氧原子和2个氮原子进行配位形成扭曲的四面体,其中2个氧原子分别来自于1个配位水分子和1个配位的硝酸根离子(O4和O1),2个氮原子则来自于同一个phen分子 (N1和N2)。铅与phen上的氮形成的Pb-N键长分别是0.249 9(4)和0.256 4(3)nm,与文献值(0.247 8~0.260 3 nm)接近[14]。铅与配位的硝酸根离子形成的Pb-O键长为0.269 8(4)nm,铅与水分子形成的Pb-O键长为0.245 1(3)nm。此外,配合物1中的2个硝酸根离子中的氧原子(O1和O7)与铅之间的距离不同,分别为0.269 8(4)和0.274 9 nm,较短的要比较长的氧与铅之间的距离小0.005 1 nm。根据价键理论,Pb与O7之间可能存在着弱相互作用,不存在共价键。所以O7所在的硝酸根离子是以游离的形式存在于结构当中。配合物1中O-Pb-O之间的键角在80.68(12)°~144.74(11)°范围内,而 N-Pb-N 之间的角度则为65.88(12)°。配合物1中存在配位水分子与硝酸根形成的O-H…O氢键。配合物通过这些氢键将结构单元扩展成一维链状超分子结构(如图1b)。
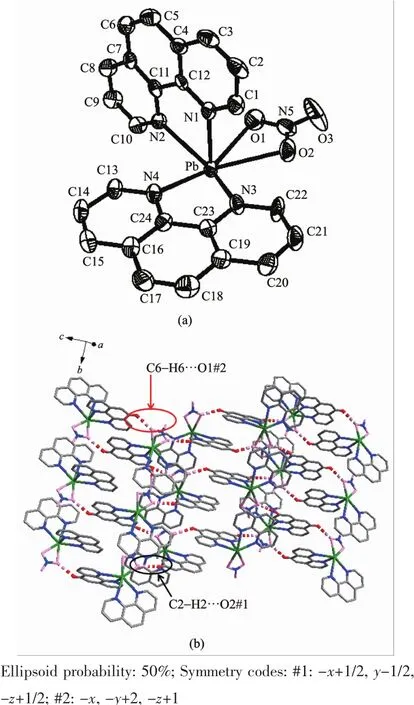
图2 (a)配合物2中金属Pbギ的配位环境;(b)配合物2的三维超分子网络结构Fig.2 (a)Coordination environment of metal Pbギin complex 2;(b)Three-dimensional supramolecular network structure of complex 2
配合物2的不对称单元中存在1个六配位的Pb2+离子,2个phen分子,1个配位硝酸根离子以及1个游离的硝酸根离子。金属Pbギ的配位环境如图2a所示,Pb2+离子分别与4个氮原子和2个氧原子进行配位形成扭曲的八面体,其中4个氮原子则来自于2个phen分子 (N1-N4),2个氧原子来自于1个以双齿螯合配位的硝酸根离子 (O1和O2)。铅与phen上的氮形成的Pb-N键长为0.248 3(6)~0.261 0(6)nm,铅与硝酸根离子形成的Pb-O键长分别为0.268 1(6)和0.275 7(6)nm。O-Pb-O之间的键角为46.29(19)°,而N-Pb-N之间的键角则为63.45(19)°~137.01(19)°。 配合物 2 中也存在大量的由phen上的碳原子和硝酸根上的氧原子形成的C-H…O氢键,所有这些氢键将结构单元扩展连接成三维网络超分子结构(如图2b)。
2.2 红外光谱分析
在配合物1的红外光谱图中,3 368 cm-1的强吸收峰归属为配位水分子的O-H的特征吸收峰;配体1,10-phen特征伸缩振动吸收峰νC=N(1 586 cm-1),在形成配合物后向低波数方向移动(1 517 cm-1),发生了红移,表明配体phen参与了配位;1 385 cm-1为配位的NO3-的特征吸收峰,配合物在558和415 cm-1处的强峰分别为Pb-N和Pb-O的吸收。对于配合物2,配体phen特征伸缩振动吸收峰νC=N(1 586 cm-1),在形成配合物后向低波数方向移动(1 514 cm-1),发生了红移,表明配体phen参与了配位;1 386 cm-1为配位和没配位的NO3-的特征吸收峰,配合物在552和417 cm-1处的强峰分别为Pb-N和Pb-O的吸收。配合物1和2与配体的官能团的特征峰详细指认见表3。
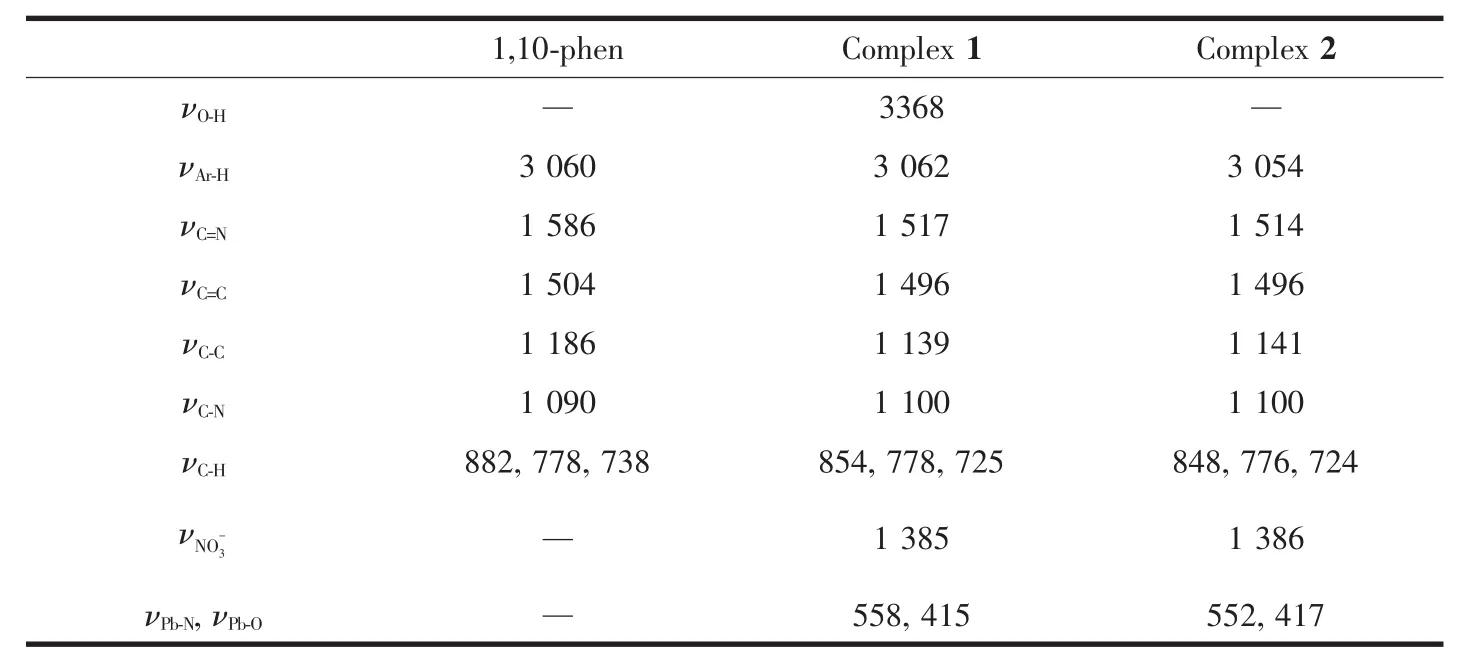
表3 配体与配合物红外光谱的主要特征峰Table 3 IR spectra adscription and comparison of the ligands and the complexes
2.3 抑菌活性
抑菌实验结果(表4,图3~8)表明:配合物的抑菌活性来源于phen,配合物1和2对大肠杆菌和金黄色葡萄球菌具有较强的抑制作用,特别是对革兰氏阴性细菌的大肠杆菌。配合物1和2的抑菌作用明显强于单独的硝酸铅、phen,表明形成配合物后,铅离子对phen的抑菌有正协同作用。配合物的抑菌环直径与其phen含量具有很好的线性关系 (R2=0.959~0.980),因此配合物的浓度越高,对两种细菌的抑制作用越强。

表4 不同样品对金黄色葡萄球菌和大肠杆菌的抑菌活性Table 4 Bacteriostatic activity of different samples on Escherichia coli and Golden staph
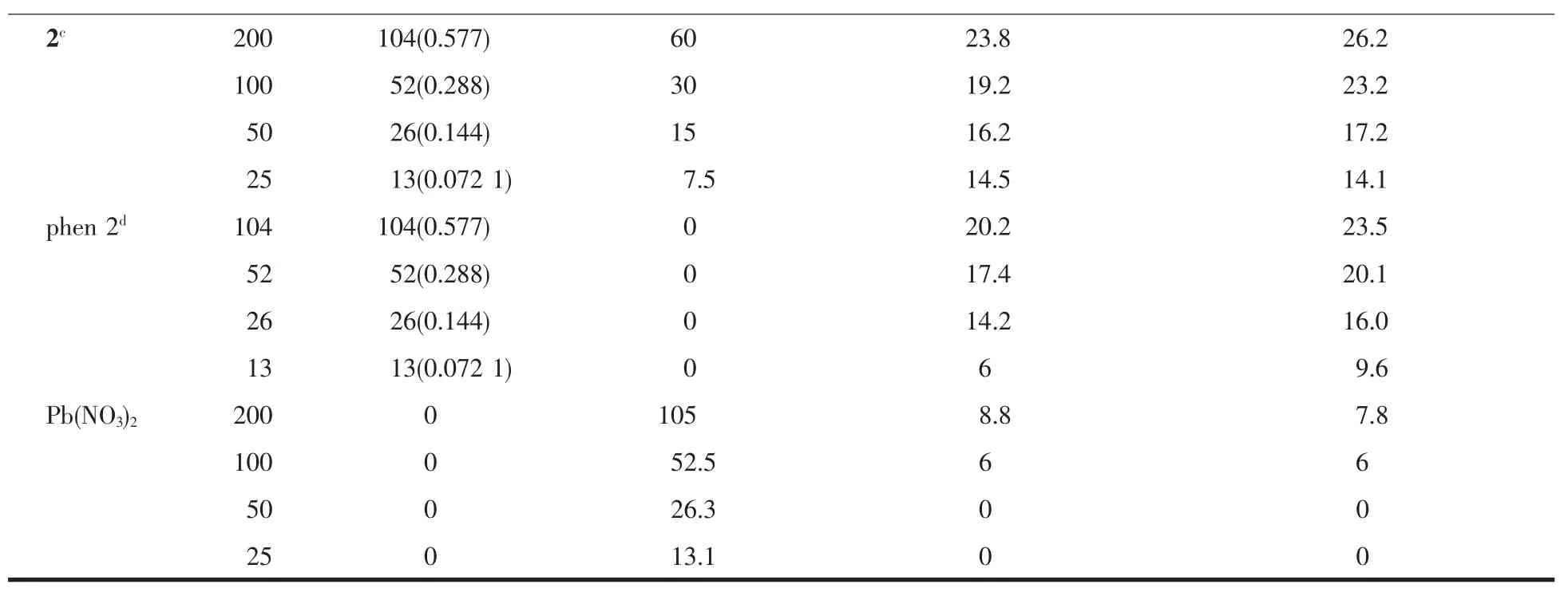
续表4

图3 配合物1及配体对金黄色葡萄球菌的抑制作用Fig.3 Inhibitory effects of 1 and ligands on G.S.

图4 配合物2及配体对金黄色葡萄球菌的抑制作用Fig.4 Inhibitory effects of 2 and ligands on G.S.

图5 配合物1及配体对大肠杆菌的抑制作用Fig.5 Inhibitory effects of 1 and ligands on E.C.

图6 配合物2及配体对大肠杆菌的抑制作用Fig.6 Inhibitory effects of 2 and ligands on E.C.

图7 配合物1和2对金黄色葡萄球菌的抑制作用Fig.7 Inhibitory effect of 1 and 2 on G.S.
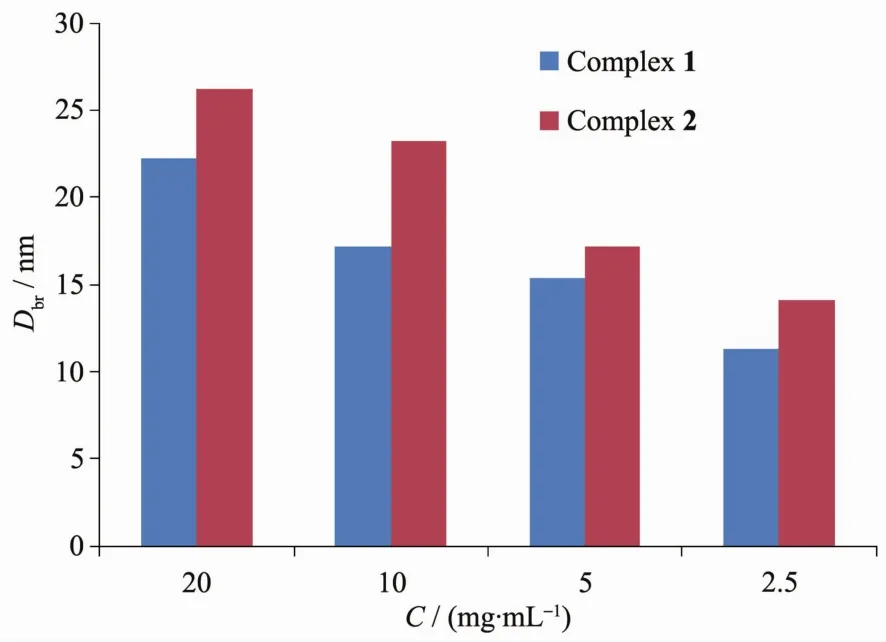
图8 配合物1和2对大肠杆菌的抑制作用Fig.8 Inhibitory effect of 1 and 2 on E.C.
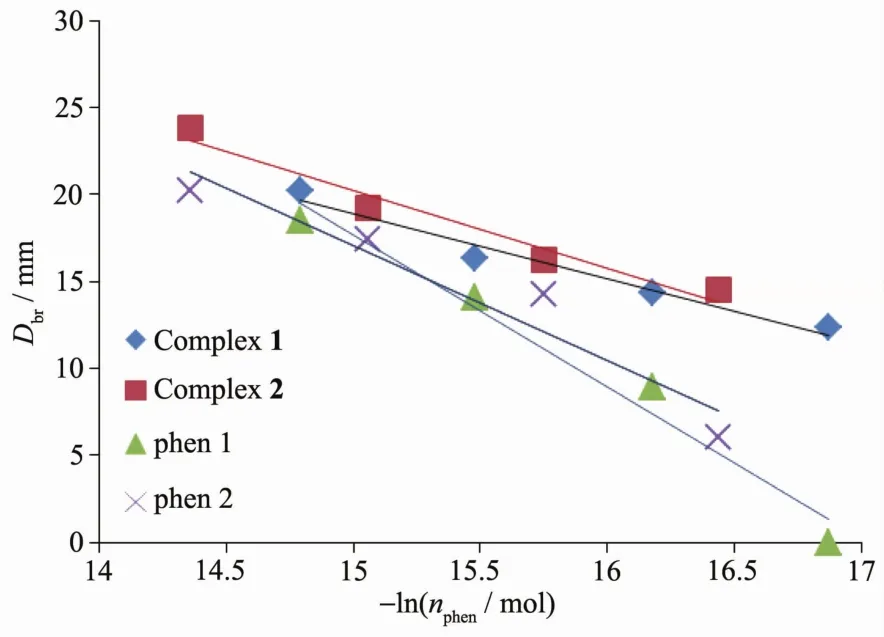
图9 配合物1和2中phen含量与其对金黄色葡萄球菌抑菌圈的线性关系Fig.9 Linear relationship of phen content of 1 and 2 vs D br on G.S.
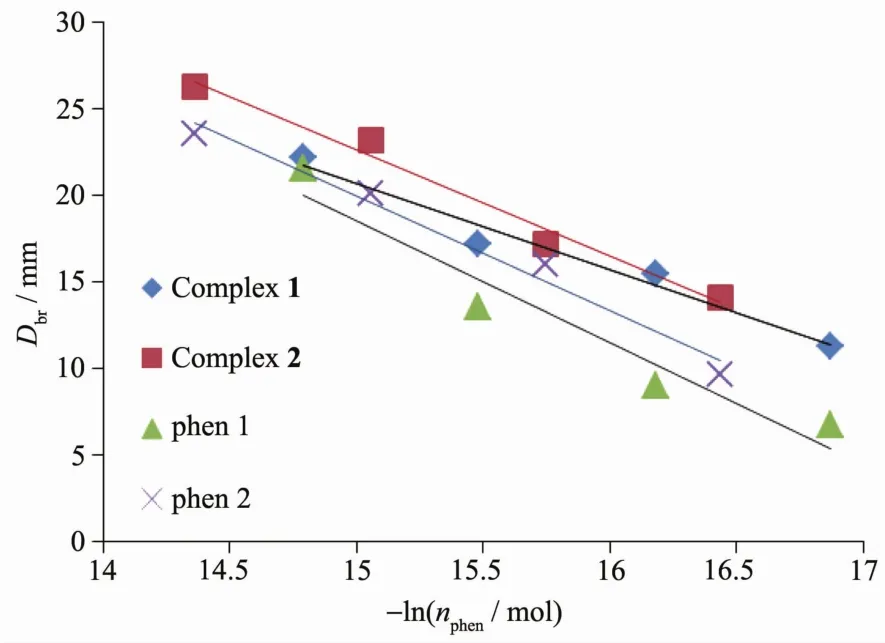
图10 配合物1和2中phen含量与其对大肠杆菌抑菌圈的线性关系Fig.10 Linear relationship of phen content of 1 and 2 vs D br on E.C.
3 结 论
采用溶液合成的方法,以phen为配体与硝酸铅反应合成了2个结构新颖的铅配合物。当nphen∶nPb=1∶1时,在乙醇体系中合成了配合物1;而当nphen∶nPb=2∶1时,在甲醇体系中合成了配合物2。结构分析表明,配合物1通过分子间氢键形成1D链状超分子结构,而配合物2则形成3D超分子网络结构。其中phen配体采取双齿螯合配位模式,硝酸根离子存在单齿桥连和双齿螯合两种配位模式。配合物1和2对金黄色葡萄球菌和大肠杆菌的抑制作用均优于配体,配合物的抑菌活性来源于phen,配合物2的抑菌活性优于配合物1,并且浓度越高,抑制作用越强。
Supportinginformation isavailableat http://www.wjhxxb.cn
参考文献:
[1]DAI Jun(戴俊),Yang Juan(杨娟),CHEN Xi(陈曦).Chinese J.Inorg.Chem.(无机化学学报),2011,27(8):1617-1624
[2]Morsali A,Mahjoub A.Polyhedron,2004,23(15):2427-2436
[3]FENG Jian-Hua(冯建华),WU Gang(吴刚),LI Hui-hui(李会会).Chemical Research and Application(化学研究与应用),2013,25(8):1126-1130
[4]Nordell K J,Schultz K N,Higgins K A,et al.Polyhedron,2004,23(13):2161-2167
[5]LI Chun-Xiang(李春香),WANG Jian(王艰),LIU Chun-Bo(刘春波),et al.Chinese J.Inorg.Chem.(无机化学学报),2009,25(12):2211-2214
[6]LI Dong-Qing(李冬青),TAN Ming-Xiong(谭明雄),DONG Yu-Hua(董玉花).Journal of Yulin Teachers College(玉林师范学院学报),2009,30(3):34-37
[7]WANG Xiao(王潇),HOU Xiang-Yang(侯向阳),MA Diao(马貂),et al.Chemical Reagents(化学试剂),2010,32(9):821-823
[8]BAI Feng-Ying(白凤英),LÜ Xiao(吕晓),LIU Shu-Qing(刘淑清),et al.Chinese J.Inorg.Chem.(无机化学学报),2011,27(7):1261-1264
[9]YANG Shu-Ping(杨树平),HAN Li-Jun(韩立军),PAN Yan(潘燕),et al.Acta Chim.Sinica(化学学报),2012,4(70):519-524
[10]SHAO Cai-Yun(邵彩云),SONG Shuang(宋霜),SONG Min(宋敏),et al.Chinese J.Inorg.Chem.(无机化学学报),2011,22(4):29-33
[11]WANG Jian-Qing(汪剑青),HUANG Xue-Feng(黄雪峰),WEI Yan-Jun(魏燕君),et al.Guangdong Chemical Industry(广东化工),2009,36(12):56-57
[12]Sheldrick G M.SHELX-97,Program for the Solution and the Refinement of Crystal Structures,University of Göttingen,Germany,1997.
[13]Wang Z N,Xu X T,L X,et al.RSC Adv.,2015,5(126):104263-104274
[14]WANG Qing-Wei(王庆伟),LI Xiu-Mei(李秀梅),WANG Zhi-Tao(王志涛),et al.Chinese J.Inorg.Chem.(无机化学学报),2010,26(11):2101-2104
