嵌入配位不饱和金属位对多孔芳香骨架材料储氢性能的影响
2018-04-10吴选军李磊彭亮王叶彤蔡卫权
吴选军,李磊,彭亮,王叶彤,蔡卫权,3,*
1 引言
近年来,采用氢燃料电池驱动的新型汽车因具有高效、清洁、可快速充放的特点而受到全球工业界和学术界的广泛关注,但其推广应用的最大障碍依然是H2体积能量密度远低于传统化石燃料,寻找经济、安全、能提高储氢密度的介质材料具有十分重要的意义1-3。针对车载储氢系统的应用要求,美国能源部(DOE)最近将原来2020年车载储氢系统的阶段性目标推迟到2025年,维持系统储氢目标为质量储氢密度5.50% (w),体积储氢密度40 g·L-14。近年来出现的多孔骨架储氢材料,包括金属有机骨架材料(MOFs)5,6、共价有机骨架材料(COFs)7,8、多孔芳香骨架材料(PAFs)9,10和多孔碳材料11等,由于具有超高孔隙率、比表面积而表现出非凡的气体吸附性能,在储氢材料领域展现出良好应用前景,逐渐成为研究人员关注的焦点。
PAFs是由朱广山、曹达鹏等研究小组12,13共同设计并部分合成的一类新型多孔骨架材料。实验测得 PAF-302材料(亦称 PAF-1或 PPN-6)的Langmuir比表面积高达 7100 m2·g-1,在 77 K、4.8 MPa下绝对质量储氢量高达10.70% (w)。但由于PAFs骨架原子对氢分子亲和力较弱,其常温储氢性出现急骤下降,在298 K、10 MPa下其绝对质量储氢量下降到2.21% (w)。为了提高PAFs等多孔骨架材料的常温储氢性能,可以通过在材料骨架引入功能性基团或配位不饱和金属位(CUS)、利用金属原子掺杂等策略提高材料主体对氢分子的亲和力,从而达到改善材料储氢性能的目的。曹达鹏等14采用Li掺杂以提高COF-202的常温储氢性能,研究表明当掺入质量分数为7.90% (w)的Li时,COF-202的绝对质量储氢量达到4.39% (w),与未掺杂COF-202相比提高了2.87% (w),提升幅度达到了188.8%。向中华等15将Li修饰到COP-1的炔基上,实验测得在77 K、100 kPa时其H2吸附量达到了1.67% (w),相比未被修饰的COP-1储氢量相对提升了 70.4%。在 MOFs材料中引入CUS,包括增加晶胞中无机配体数量和在有机连接体中插入含金属的功能基团如金属化儿茶酚等两种不同途径,都能显著提高骨架与客体分子相互作用,从而改善 MOFs材料吸附性能,包括材料储氢性能16,17。Snurr等18通过在 IRMOF-1、IRMOF-10和UMCM-150等多孔骨架材料的苯环上分别引入含Li、Mg、Mn、Ni和Cu等金属的醇盐,发现引入含金属镁醇盐改性的多孔骨架材料表现出良好的常温储氢性能且具有最高的常温储氢释放性能,如IRMOF-1经镁醇盐改性后,243 K、10 MPa下的绝对 H2吸附量由 1.94% (w)提升到2.97% (w)。H2释放量由 1.89% (w)提升到 2.32%(w)。Snurr等19通过虚拟组装方法设计了 18383种具有不同镁醇基密度的多孔晶体材料,巨正则系综蒙特卡洛(GCMC)计算结果表明,当材料具有高孔隙率(> 0.9)和较低镁密度(0.0-0.5 mmol·cm-3)时,其在243 K下具有最佳的质量储氢释放量。当材料孔隙率为0.75,镁的密度为2.5 mmol·cm-3时,243 K时具有最佳的体积氢气释放量。本课题组在前期工作中也提出了在 PAFs骨架有机联接体中插入炔键20或采用锂掺杂等21策略以提高其常温储氢性能,研究表明改性后的 PAFs材料具有优异的低温和常温质量储氢性能,但其体积储氢性能仍有待进一步提高。
为了获得具备均衡体积储氢和质量储氢性能的多孔骨架材料,本文通过在PAFs材料有机连接体中引入醇镁功能基团,基于密度泛函理论(DFT)和GCMC模拟方法系统研究CUS对PAFs材料储氢性能的影响规律,并结合原子对径向分布函数(RDF)、质心几率密度分布(MCPD)、等量吸附热(Qst)等对配位不饱和金属位影响 PAFs材料储氢性能的机理进行系统分析。
2 分子模型与理论计算
2.1 分子模型
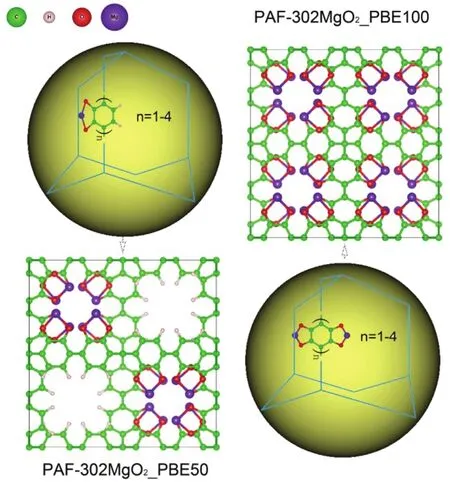
图1 镁基功能化改性PAFs材料设计策略Fig.1 Design strategy of PAFs functionalized with magnesium alkoxide.
先根据Ben等12报导的P1模型建立PAF-30n(n = 1-4, n代表材料有机链接体中苯环数量)材料结构,并按照如图 1所示的结构设计策略在PAF-30n (n = 1-4)骨架材料中引入一定数量的配位不饱和金属位,即醇镁功能团,得到两种不同CUS取代度的PAFs功能改性材料;然后以DFT理论为基础,采用 Vienna Ab-initio Simulation Package (VASP)22软件对材料结构进行完全驰豫,为了节省计算资源,部分P1对称结构转换为具有最高对称性的原胞结构,空间群组为 I41/AMD,优化后的结构分别记作 PAF-30nMgO2_PBE50和_PBE100 (n = 1-4,PBE表示优化后的结构,50和100分别表示50%和100%的CUS取代度,下同)。优化后不同改性 PAFs材料的详细结构参数见表1,自由孔体积Vp、比表面积SSA与孔隙率Φp根据 Snurr方法计算23,而限制孔道直径 PLD及最大孔洞直径LCD则采用zeo++软件计算24;单位晶胞结构参见支持信息图S1,其中嵌入CUS后PAFs骨架中C―O键长为0.1317 nm,Mg―O键长为0.1947 nm,O―Mg―O键角为88.5°。
2.2 理论计算方法
2.2.1量子力学计算方法
对于周期性的镁基功能化PAFs结构,根据密度泛函理论进行构型优化,优化过程由VASP软件完成22。计算采用平面缀加波(PAW)结合广义梯度近似(GGA)形式的PBE交换关联势25-27,平面缀加波函数截断能量为500 eV,所有结构均弛豫至每个原子上的残余力不超过0.1 eV·nm-1。为了节省计算资源,镁基功能化PAFs结构使用原胞和周期性边界条件,布里渊区域的积分采用Monkhorst-Pack 方法取样,产生 1 × 1 × 1 大小的k点网格。构型优化过程针对原胞大小和原胞中所有原子的位置进行完全弛豫,没有任何约束,直至达到全局结构最优。优化过程采用黄金搜索算法28进行控制,实践证明该算法可以成功地搜索到不同材料体系的最优几何构型20。以PAF-301MgO2_PBE100为例,该材料结构优化的能量曲线参见图2,一般搜索起始点为原胞体积加上±3%的形变(具体取决于原胞构型准确程度),经过多次反复地完全弛豫后,能够快速地收敛到能量最低点。
2.2.2GCMC模拟
对采用吸附剂增强储氢密度的系统而言,单位质量储氢密度和单位体积储氢密度是衡量吸附剂优劣的两个最基本性能指标,尤其是后者对储罐体积受限的车载储氢系统更具实际意义。本文通过 GCMC方法对不同温度下 H2在各种镁基功能化改性PAFs材料中的吸附性能进行模拟,获得材料在不同条件下的质量储氢性能与体积储氢性能。GCMC模拟采用本课题组修改后的MUSIC-4.0程序进行计算29,其中不同压力下H2逸度采用Peng-Robinson (PR)状态方程30计算。在GCMC模拟过程中,采用Morse位能函数描述骨架原子与氢分子以及不同氢分子之间的相互作用(力场参数见Supporting Information表S1)31,而保持骨架原子位置固定不动,GCMC模拟总循环步数为107步,前5 × 106步为平衡阶段,后5 × 106步为采样阶段,具体模拟力场参数及控制细节参见Supporting Information S2与S3相关部分。

表1 不同镁基功能改性PAFs材料的结构参数Table 1 Various structure parameters of different PAFs functionalized with magnesium alkoxide.

图2 PAF-301MgO2_PBE100黄金搜索算法优化的能量-体积曲线Fig.2 Energy-volume curve of PAF-301MgO2_PBE100 using golden section search for geometry optimization.
3 结果与讨论
3.1 引入CUS对PAFs材料储氢性能影响
3.1.1CUS-PAFs低温储氢性能

图3 77 K下H2在CUS-PAFs材料中的过量吸附等温线Fig.3 (a) Gravimetric and (b) volumetric excess adsorption isotherms of H2 on CUS-PAFs at 77 K.
为了研究引入CUS对PAFs材料储氢性能的影响规律,采用 GCMC模拟计算了 77 K下不同CUS-PAFs材料的吸附等温线(见图3),该方法和所用力场参数已经在前期工作中被证明了可靠性20,31。PAF-301MgO2_PBE50和_PBE100 (后亦称为CUS50和CUS100改性的PAF-301)在77 K时的等温吸附量随压力基本不变,归因于PAF-301在引入不同数量的CUS后,材料孔隙率出现不同程度下降(见表 1),分别从 0.721下降到 0.227和0.126,材料自由空穴大部分被引入的CUS占住;比表面积也下降明显,从而导致低压力下H2吸附便达到饱和32。与原始PAF-30n (n = 2-4)材料相比,引入CUS后材料的储氢性能出现不同程度增强。如77 K、4.8 MPa下PAF-302的过量H2吸附量为 7.0% (w) (过量吸附量与绝对吸附量的定义与关系见Supporting Information)12,而CUS50和CUS100改性的PAF-302在77 K、2.0 MPa下最大过量H2吸附量分别为7.7% (w)和8.0% (w),分别提高了 10%和 14%;提升幅度最大的是 CUS100改性的PAF-304材料,从原来的7.3% (w)增加30%到9.5% (w) (均为77 K、2.0 MPa下),接近于储氢标志性材料NU-100 (在77 K、5.6 MPa下实测H2吸附量为9.95% (w))33。从引入CUS的数量进行比较发现,在骨架连接体苯环数量相等的条件下,单位晶胞内CUS的数量增加一倍,材料的最大过量H2吸附量变化不大,如在PAF-303材料中分别引入 50%和 100%取代度的 CUS后在 77 K、2.0 MPa下最大过量 H2吸附量分别为 8.9%(w)和9.1%(w)。但是 PAF-301例外,随着引入 CUS数量的增加,材料过量储氢性能出现明显下降,从77 K、2.0 MPa下PAF-301的4.9% (w)分别下降到4.3% (w) (CUS 50%)和 2.9% (w) (CUS 100%),归因于引入CUS后材料自由孔体积与比表面积出现的显著下降(见表 1),如 PAF-301MgO2_PBE100的自由孔体积下降到0.07 cm3·g-1,比表面积下降到 41.6 m2·g-1。
一般而言,多孔吸附剂材料的体积储氢性能与质量储氢性能是一对矛盾因素34,高孔隙率的吸附剂具有良好的质量储氢性能,但仅仅提高孔隙率会降低骨架原子与H2分子之间的亲和力,使其体积储氢性能出现下降。随着 CUS-PAFs材料有机链长度的增加,其PLD、LCD、SSA和孔隙率Φp也随之增加(见表1),但其最大过量体积H2吸附量却呈现下降趋势。因此,在相同CUS取代度的条件下,过量体积储氢性能大小的顺序为PAF-301 > PAF-302 > PAF-303 > PAF-304,其中CUS50改性的 PAF-301过量体积 H2吸附量最高(620 cm3(STP)·cm-3),而 CUS50 改性的 PAF-304为最低(146 cm3(STP)·cm-3)。在有机链长度相同的情况下,除PAF-301外,随着CUS数量的增加,材料过量体积储氢量也明显增强,如对 PAF-302而言,CUS取代度为50%时,过量体积H2吸附量为411 cm3(STP)·cm-3,而随着CUS取代度提高到100%,材料过量体积 H2吸附量达到 589 cm3(STP)·cm-3,较前者提升了43.3%,这说明CUS数量的提高,更有利于改善 PAFs材料的过量体积储氢性能,而对过量质量储氢性能的影响相对较小。
3.1.2CUS-PAFs结构对低温储氢性能的影响

图4 (a) 77 K下H2在CUS-PAFs材料中的绝对吸附等温线;(b) 77 K下H2绝对吸附量与CUS-PAFs材料自由孔体积的关系;(c) 与其它多孔材料储氢性能的比较;(d) 77 K下H2最大过量吸附量与CUS-PAFs等材料质量比表面积的关系Fig.4 (a) Total adsorption isotherms of H2 in CUS-PAFs at 77 K; (b) plots of total H2 uptake at 77 K νersus free pore volume; (c) H2 uptake in CUS-PAFs as well as additional porous materials; (d) plots of maximum excess H2 uptake at 77 K νersus gravimetric surface area of CUS-PAFs et al.
图 4(a)列出了 77 K下 H2在不同 CUS-PAFs材料绝对质量吸附等温线。绝对储氢性能代表了吸附剂完全的储氢性能,其主要贡献来自于材料表面吸附和自由孔穴填充,前者对应于过量储氢量32。在较低压力下,表面吸附的增长较快,对绝对吸附量的贡献也较大,因此不同 CUS-PAFs材料绝对吸附量的变化规律与图 3(a)中过量吸附量的变化规律一致。随着压力的逐渐提高,大约在2 MPa下过量吸附量达到饱和,自由孔穴填充对绝对吸附量的贡献逐渐增大,除了PAF-301MgO2_PBE50因为孔隙率较小以外,其它CUS50改性的PAF-30n (n = 2-4)材料,由于自由孔隙率高于相应 CUS100改性的等链长 PAFs材料,其绝对质量储氢量随着压力的提高而逐渐超过后者。从图4(b)可以看出,77 K、10 MPa下不同 CUS-PAFs材料绝对储氢性能与材料自由孔体积之间呈现线性关系,材料绝对储氢量随自由孔体积的增加而增大。图 4(c)比较了 77 K下不同CUS-PAFs材料最大过量储氢量和10 MPa下的绝对储氢量,同时也列出了几种常见的 MOFs储氢材料及未改性PAFs材料的相关性能。对PAF-302材料而言,CUS改性前后最大过量储氢量变化较大,由改性前 7.1% (w)分别提高到 7.77% (w)(CUS50)和 7.97% (w) (CUS100),但还是略低于MOF-210 (77 K、5.5 MPa下8.60% (w))35和NU-100(77 K、5.6 MPa下 9.95% (w))33。图 4(d)关联了CUS-PAFs材料最大过量氢质量吸附量与其质量比表面积之间的关系,同时与 MOF-5、MOF-177、MOF-210和NU-100等常见多孔材料13,33,35-37储氢性能进行比较。未改性PAFs、CUS50和CUS100改性 PAFs材料最大过量质量储氢量与质量比表面积之间分别呈线性关系,即:
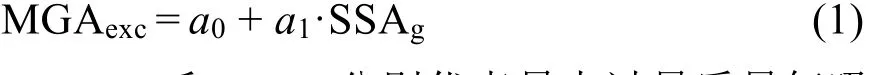
式中MGAexc和SSAg分别代表最大过量质量氢吸附量和质量比表面积,关联系数依次为 a0=27.336, 41.56和 28.86;a1= 0.00799, 0.00949,0.01614,表明随着CUS取代度增加,材料质量储氢受质量比表面积的影响增强。除了 PAF-301以外,其它PAFs材料在CUS取代度相同的情况下,77 K下绝对体积储氢量与体积比表面积之间也存在线性关系(见Supporting Information图S2),并且提高CUS取代度对材料的绝对体积储氢量具有十分明显地增强作用,如当CUS取代度从50%增加到100%时,PAF-302的绝对体积储氢量从53.8 g·L-1增长到 65.9 g·L-1,增幅高达 22.5%,后者甚至超过了NU-1102 (77 K, 10 MPa下模拟值为54.2 g·L-1)32。PAF-303经CUS改性后绝对体积储氢量也都超过了DOE体积储氢标准(分别为43.2 g·L-1,50.5 g·L-1)。
3.1.3CUS-PAFs材料的常温储氢性能

图5 CUS-PAFs材料中H2绝对吸附等温线: (a) 243 K质量吸附; (b) 243 K体积吸附;(c) 298 K质量吸附; (d) 298 K体积吸附Fig.5 Total (a) gravimetric adsorption at 243 K and (b) volumetric adsorption at 243 K; (c) gravimetric adsorption at 298 K; (d) volumetric adsorption isotherms of H2 in different CUS-PAFs.
图5为243 K、298 K下不同CUS-PAFs材料的绝对质量和绝对体积 H2吸附等温线。与 77 K下的H2吸附等温线相似,298 K下不同PAFs材料在引入CUS改性后,绝对体积储氢量的增长幅度都远远超过同一材料绝对质量储氢量的涨幅(部分材料绝对质量储氢量甚至出现下降),243 K下H2吸附等温线变化趋势类似,而且与298 K下相同 CUS-PAFs材料体积储氢量和质量储氢量相比出现明显提升,如 CUS50和 CUS100改性的PAF-304材料在 10 MPa下的质量储氢量分别从7.12% (w)和 6.49% (w)增至 9.12% (w)和 8.43%(w),分别增长 28.1%和 29.9%;同压力下的体积储氢量分别从 10.27 g·L-1和 13.21 g·L-1增至 13.15 g·L-1和 17.17 g·L-1,分别增长 28.0%和 30.0%。与其它多孔材料一样,CUS-PAFs材料的质量储氢量与体积储氢量之间存在相反的变化趋势,对LCD较小的PAF-301而言,CUS50和CUS100改性后其体积储氢量较高,分别是 30.54 g·L-1和 39.9 g·L-1(298 K、10 MPa),39.1 g·L-1和 45.56 g·L-1(243 K、10 MPa);但其质量储氢量只有2.4% (w)和 2.26% (w) (298 K、10 MPa),2.57% (w)和 3.07%(w) (298 K、10 MPa)。比较而言,243 K、10 MPa下CUS100改性的PAF-302具有均衡的质量储氢量和体积储氢量,分别为5.13% (w)和34.19 g·L-1,占DOE质量与体积储氢标准的93.3%和85.5%。
3.2 CUS-PAFs储氢性能强化机理分析
为了明确 CUS-PAFs材料储氢性能的强化机理,采用 MCPD、RDF和 Qst等方法来表征CUS-PAFs材料结构与其储氢性能之间的关系,并进一步探讨了相关材料质量储氢量与体积储氢量此消彼长的制约机制。MCPD、RDF和Qst均采用自编程序进行计算,具体计算方法见支持信息。
3.2.1H2在CUS-PAFs材料中的吸附位
图 6为三种不同温度和三种不同压力下达到吸附平衡时 H2在 PAF-302MgO2_PBE100材料中的质心几率密度分布图。从H2分子填充的方式上看,在不同温度下随着压力的增加,H2分子填充骨架的情形基本类似,首先在低压力占据优先吸附位,然后逐渐向孔道填充。在 77 K、100 kPa下,H2分子优先吸附在骨架材料中金属镁原子附近,该区域存在明显的高几率密度分布;同时也有部分H2分子填充到孔道中心区域。随着压力增加,骨架表面的单层吸附迅速达到饱和,而孔道填充部分会随着压力增加而继续增加;由于低温下孔道填充密度较高,在压力超过2 MPa时单层吸附区域的高几率密度分布基本消失(填充几率无明显差异)。而在常温(243 K 和298 K)下,由于孔道填充密度较小,骨架表面单层吸附的H2分子达到饱的压力随之增大,因此低压力下其高几率密度分布更加明显,而且即使压力增加到 6 MPa时,表面单层吸附的H2分子数量依然要多于骨架自由孔隙中填充的H2分子数量,在靠近金属镁原子附近区域依然存在较为明显的H2分子高几率密度分布,虽然较低压下H2分子分布几率有所降低。
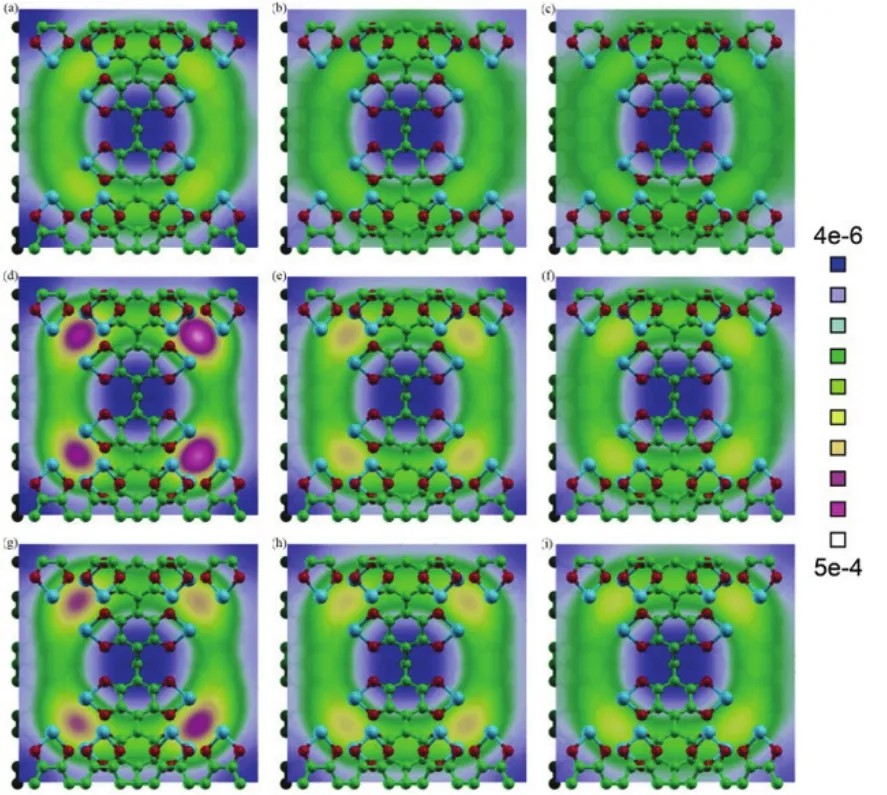
图 6 H2 在 77 K (上)、243 K (中)和 298 K (下)以及100 kPa (左)、2 MPa (中)和 6 MPa (右),PAF-302MgO2_PBE100中吸附平衡时的质心几率密度分布.Fig.6 Mass center probability density distribution(XOY) for H2 adsorption equilibrium in PAF-302MgO2_PBE100 at 77 K (upper row), 243 K(medium row), 298 K (lower row) and 100 kPa (left cloumn), 2 MPa (medium column),6 MPa (right column).
图7(a)为77 K、2 MPa下体系达到吸附平衡时CUS100改性的PAF-302材料中H2分子与不同骨架原子相互作用的原子对径向分布函数。Mg…H_A原子对的径向分布函数在r = 0.236 nm处出现一个窄而强的峰,表明骨架 Mg原子中心附近0.236 nm处存在H2分子优先吸附位,该吸附位表现出十分规整的近程有序性。O…H_A原子对的径向分布函数在r = 0.318 nm处出现一个宽而弱的峰,表明骨架中O原子对H2分子的吸附能力相对较弱。由于C_3处于骨架的中心位置,因此C_3…H_A原子对的径向分布函数在r = 0.383,0.570, 0.736, 0.876 nm多处出现峰值C_R…H_A的径向分布函数未出现明显特征峰,表明在 C_R原子附近没有出现H2分子强优先吸附位。
3.2.2质量和体积储氢量的均衡

图7 (a) PAF-302MgO2_PBE100骨架原子与H2相互作用原子对径向分布函数; (b) 298 K下CUS-PAFs材料H2等量吸附热与CUS数密度之间的关系; (c)常温下CUS-PAFs材料与其它多孔材料的绝对体积吸附量;(d) 77 K、10MPa下多孔材料孔隙率和体积比表面积对体积储氢量的影响Fig.7 (a) Radial distribution function for all kinds of inter-atomic pairs between hydrogen molecules and framework atoms in PAF-302MgO2_PBE100; (b) plots of isosteric adsorption νersus number density of CUS in CUS-PAFs;(c) volumetric total uptake in CUS-PAFs and additional porous materials at ambient temperature; (d) effect of void fraction and volumetric surface area on volumetric capacity of H2 storage in porous materials at 77 K and 10 MPa.
等量吸附热代表了多孔材料即吸附剂分子对H2分子吸附的亲和力,其值越大说明材料对 H2分子吸附作用力越强。图 7(b)表明 298 K下CUS-PAFs材料等量吸附热与CUS数密度之间呈现线性关系,CUS数密度越高,材料对H2分子吸附的亲和力就越强。由于PAF-301材料的LCD孔径最小,CUS改性后其CUS数密度最高,因而对H2分子表现出最强的亲和力,CUS50和 CUS100改性的 PAF-301等量吸附热分别为 19.2 kJ·mol-1和 29.8 kJ·mol-1。图 7(c)比较了常温下不同CUS-PAFs材料与其它几种多孔材料(包括一些含炔键的材料20,31和其它 MOFs材料17,38,39)体积储氢性能,发现LCD孔径对CUS-PAFs材料的体积储氢量有重大影响,LCD孔径越大,其体积储氢量越小,DA等材料也表现出类似规律,但PAF-322系列材料例外,它们的体积储氢量差异并不明显,表明材料的体积储氢性能不仅仅只受孔径的影响。为了理解影响NU-1101等多孔材料体积储氢量的结构因素,Gómez-Gualdrón等32发现可以采用式(2)来描述体积储氢量与孔隙率和体积比表面积之间的关系:
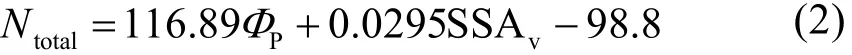
式中 Νtotal为体积储氢量,g·L-1;ΦP为自由孔隙率;SSAv为体积比表面积,m2·cm-3。利用式(2)在图7(d)中表示出要达到一定的体积储氢量所需的条件(即在图中平行的虚线上方)。对 CUS50改性的PAF-30n (n = 2-4)材料在77 K下的体积储氢量和式(4)预测值基本一致,而对 CUS100改性的PAF-30n (n = 2-4)材料预测值偏低。图7(d)中曲线是根据文献32报导的 2133种具有不同拓扑的Zr-MOFs材料在77 K、10 MPa下的体积储氢量与自由孔隙率和体积表面积等结构参数之间的关系拟合出来的高斯分布曲线,基本能够反映 MOFs材料结构对储氢性能影响的统计规律,如具有最高体积储氢量的材料自由孔隙率在0.8左右,体积比表面积在 2100 m2·cm-3左右。从图 7(d)可以看出,只有极少部分Zr-MOFs材料的体积储氢量能达到 60 g·L-1以上,而 CUS100改性的 PAF-302体积储氢量可以达到65.9 g·L-1,得益于其合适的孔隙率和体积比表面积(0.77和1996.5 m2·cm-3);另外,其等量吸附热值(14.91 kJ·mol-1)也在理想区间 10-15 kJ·mol-1之内40。
4 结论
通过在PAF-30n (n = 1-4)材料有机链中引入配位不饱和金属位(CUS),以增强其体积储氢性能。采用DFT理论和GCMC模拟方法系统研究了不同条件下引入CUS对PAFs材料储氢性能的影响规律,结果发现在 77 K下引入 CUS50和CUS100改性的PAF-302和PAF-303的绝对质量和体积储氢量均超过了DOE标准。77 K、10 MPa下不同 CUS-PAFs材料的绝对质量储氢量与自由孔体积之间呈线性关系;CUS-PAFs材料最大过量质量储氢量与质量表面积以及除CUS-PAF-301以外的 CUS-PAFs材料绝对体积储氢量与体积表面积之间也呈线性关系。243 K、10 MPa下PAF-302MgO2_PBE100具有均衡的绝对质量储氢量和体积储氢量,分别为5.13% (w)和34.19 g·L-1,占DOE质量与体积储氢标准的93.3%和85.5%,而298 K、10 MPa下其储氢性能均有所下降,分别为 3.91% (w)和 26.0 g·L-1。结合 Qst、RDF 和MCPD等方法考察引入CUS对PAFs材料储氢性能的影响规律,发现随着PAFs有机链长的增加,其绝对体积储氢量与绝对质量储氢量呈现相反的变化规律;嵌入CUS对提高PAFs材料对H2分子亲和力具有明显作用,嵌入CUS数密度越高,材料对H2分子等量吸附热值越大。CUS100改性的PAF-302具有适宜的孔隙率、比表面积和等量吸附热等性质,表现出最优的综合储氢性能,具有成为新一代多孔储氢材料的潜力。
Supporting lnformation:available free of charge νia the internet at http://www.whxb.pku.edu.cn.
(1)Furukawa, H.; Cordova, K. E.; O'Keeffe, M.; Yaghi, O. M. Science 2013, 341, 1230444. doi: 10.1126/science.1230444
(2)Durbin, D. J.; Malardier-Jugroot, C. Int. J. Hydrog. Εnergy 2013, 38,14595. doi: 10.1016/j.ijhydene.2013.07.058
(3)Cipriani, G.; Dio, V. D.; Genduso, F.; Cascia, D. L.; Liga, R.; Miceli,R.; Galluzzo, G. R. Int. J. Hydrog. Εnergy 2014, 39, 8482.doi: 10.1016/j.ijhydene.2014.03.174
(4)https://energy.gov/eere/fuelcells/physical-hydrogen-storage(accessed 12 June 2017).
(5)Mulder, F. M.; Dingemans, T. J.; Wagemaker, M.; Kearley, G. J.Chem. Phys. 2005, 317, 113. doi: 10.1016/j.chemphys.2005.06.003
(6)Tranchemontagne, D. J.; Park, K. S.; Furukawa, H.; Eckert, J.;Knobler, C. B.; Yaghi, O. M. J. Phys. Chem. C 2012, 116, 13143.doi: 10.1021/jp302356q
(7)Mendoza-Cortes, J. L.; Goddard, W. A., III; Furukawa, H.; Yaghi, O.M. J. Phys. Chem. Lett. 2012, 3, 2671. doi: 10.1021/jz301000m
(8)Ding, S. Y.; Wang, W. Chem. Soc. Reν. 2013, 42, 548.doi: 10.1039/C2CS35072F
(9)Huang, L.; Yang, X.; Cao, D. J. Phys. Chem. C 2015, 119, 3260.doi: 10.1021/jp5128404
(10)Huang, L.; Xiang, Z.; Cao, D. J. Mater. Chem. A 2013, 1,3851. doi: 10.1039/C3TA10292K
(11)Tozzini, V.; Pellegrini, V. Phys. Chem. Chem. Phys. 2013, 15,80. doi: 10.1039/C2CP42538F
(12)Ben, T.; Ren, H.; Ma, S.; Cao, D.; Lan, J.; Jing, X.; Wang, W.;Xu, J.; Deng, F.; Simmons, J. M.; Qiu, S.; Zhu, G. Angew.Chem. 2009, 121, 9621. doi: 10.1002/ange.200904637
(13)Lan, J.; Cao, D.; Wang, W.; Ben, T.; Zhu, G. J. Phys. Chem.Lett. 2010, 1, 978. doi: 10.1021/jz900475b
(14)Lan, J.; Cao, D.; Wang, W. J. Phys. Chem. C 2010, 114, 3108.doi: 10.1021/jp9106525
(15)Xiang, Z.; Cao, D.; Wang, W.; Yang, W.; Han, B.; Lu, J.J. Phys. Chem. C 2012, 116, 5974. doi: 10.1021/jp300137e
(16)Gómez-Gualdrón, D. A.; Simon, C. M.; Lassman, W.; Chen,D.; Martin, R. L.; Haranczyk, M.; Farha, O. K.; Smit, B.;Snurr, R. Q. Chem. Εng. Sci 2017, 159, 18.doi: 10.1016/j.ces.2016.02.030
(17)Gygi, D.; Bloch, E. D.; Mason, J. A.; Hudson, M. R.;Gonzalez, M. I.; Siegelman, R. L.; Darwish, T. A.; Queen, W.L.; Brown, C. M.; Long, J. R. Chem. Mater. 2016, 28, 1128.doi: 10.1021/acs.chemmater.5b04538
(18)Getman, R. B.; Miller, J. H.; Wang, K.; Snurr, R. Q. J. Phys.Chem. C 2011, 115, 2066. doi: 10.1021/jp1094068
(19)Colón, Y. J.; Fairenjimenez, D.; Wilmer, C. E.; Snurr, R. Q.J. Phys. Chem. C 2014, 118, 5383. doi: 10.1021/jp4122326
(20)Wu, X.; Wang, R.; Yang, H.; Wang, W.; Cai, W.; Li, Q.J. Mater. Chem. A 2015, 3, 10724. doi: 10.1039/c5ta01290b
(21)Wu, X. J.; Zhao, P.; Fang, J. M.; Wang, J.; Liu, B. S.; Cai, W.Q. Acta Phys. -Chim. Sin. 2014, 30, 2043. [吴选军, 赵鹏, 方继敏, 王杰, 刘保顺, 蔡卫权. 物理化学学报, 2014, 30,2043.] doi: 10.3866/PKU.WHXB201409222
(22)Kresse, G.; Furthmüller, J. Comp. Mater. Sci. 1996, 6, 15.doi: 10.1016/0927-0256(96)00008-0
(23)Düren, T.; Millange, F.; Ferey, G.; Walton, K. S.; Snurr, R. Q.J. Phys. Chem. C 2007, 111, 15350. doi: 10.1021/jp074723h
(24)Willems, T. F.; Rycroft, C. H.; Kazi, M.; Meza, J. C.;Haranczyk, M. Microporous Mesoporous Mater. 2012, 149,134. doi: 10.1016/j.micromeso.2011.08.020
(25)Blöchl, P. E. Phys. Reν. B 1994, 50, 17953.doi: 10.1103/PhysRevB.50.17953
(26)Kresse, G.; Joubert, D. Phys. Reν. B 1999, 59, 1758.doi: 10.1103/PhysRevB.59.1758
(27)Perdew, J. P.; Burke, K.; Ernzerhof, M. Phys. Reν. Lett. 1996,77, 3865. doi: 10.1103/PhysRevLett.77.3865
(28)Kiefer, J. Proc. Am. Math. Soc.1953, 4, 502. doi:10.2307/2032161
(29)Chempath, S.; Clark, L. A.; Snurr, R. Q. J. Chem. Phys. 2003,118, 7635. doi: 10.1063/1.1562607
(30)Peng, D. Y.; Robinson, D. B. Ind. Εng. Chem. Fund. 1976,15, 59. doi: 10.1021/i160057a011
(31)Wu, X.; Li, L.; Fang, T.; Wang, Y.; Cai, W.; Xiang, Z. Phys.Chem. Chem. Phys. 2017, 19, 9261.doi: 10.1039/C7CP01230F
(32)Gómez-Gualdrón, D. A.; Wang, T. C.; García-Holley, P.;Sawelewa, R. M.; Argueta, E.; Snurr, R. Q.; Hupp, J. T.;Yildirim, T.; Farha, O. K. ACS Appl. Mater. Interfaces 2017,doi: 10.1021/acsami.7b01190
(33)Farha, O. K.; Yazaydın, A. Ö.; Eryazici, I.; Malliakas, C. D.;Hauser, B. G.; Kanatzidis, M. G.; Nguyen, S. T.; Snurr, R. Q.;Hupp, J. T. Νat. Chem. 2010, 2, 944. doi: 10.1038/nchem.834
(34)Gómez-Gualdrón, D. A.; Colón, Y. J.; Zhang, X.; Wang, T.C.; Chen, Y.-S.; Hupp, J. T.; Yildirim, T.; Farha, O. K.;Zhang, J.; Snurr, R. Q. Εnergy Εnνiron. Sci. 2016, 9, 3279.doi: 10.1039/C6EE02104B
(35)Furukawa, H.; Ko, N.; Go, Y. B.; Aratani, N.; Choi, S. B.;Choi, E.; Yazaydin, A. Ö.; Snurr, R. Q.; O’Keeffe, M.; Kim, J.Science 2010, 329, 424. doi: 10.1126/science.1192160
(36)Kaye, S. S.; Dailly, A.; Yaghi, O. M.; Long, J. R. J. Am.Chem. Soc. 2007, 129, 14176. doi: 0.1021/ja076877g
(37)Furukawa, H.; Miller, M. A.; Yaghi, O. M. J. Mater. Chem.2007, 17, 3197. doi: 10.1021/ja9015765
(38)Yuan, D.; Zhao, D.; Sun, D.; Zhou, H. C. Angew. Chem. Int.Εd. 2010, 49, 5357. doi: 10.1002/anie.201001009
(39)Lim, W. X.; Thornton, A. W.; Hill, A. J.; Cox, B. J.; Hill, J.M.; Hill, M. R. Langmuir 2013, 29, 8524.doi: 10.1021/la401446s
(40)Frost, H.; Snurr, R. Q. J. Phys. Chem. C 2007, 111, 18794.doi: 10.1021/jp076657p
