独行菜种子bHLH类转录因子基因家族及幼苗laICE1表达对冷胁迫的响应
2018-04-08袁琳琳王亚茹曾卫军谢红桃赵惠新
袁琳琳,王亚茹,曾卫军,谢红桃,杜 钰,卢 函,赵惠新
(新疆师范大学 生命科学学院,乌鲁木齐830054)
转录因子,又称反式作用因子,在真核生物生长、发育、分化、次生代谢等方面起重要的调控作用[1]。bHLH(碱性/螺旋-环-螺旋,basic/helix-loop-helix)是转录因子中的一个大家族,广泛存在于真核生物中,一般具有一个约60个氨基酸的高度保守的结构域,由2个功能不同的部分组成:碱性区域(basic region)和HLH区域(helix-loop-helix region)[2-3]。自1989年第一个植物bHLH蛋白结构被鉴定出来[4],目前已经有不同植物的1 000多条bHLH序列得到鉴定[5]。bHLH转录因子参与调节植物的黄酮类、单宁类、类萜、生物碱等次生代谢[6-11],还参与了植物的生长发育、信号转导、抗逆胁迫等许多生理过程[12-20]。如有研究证明拟南芥中的bHLH转录因子ICE1(inducer of CBF expression)和ICE2能够调控包括CBF(CRT binding factors)在内的许多冷响应元件,使植物表现出耐冷性和抗冻性[21-23]。山茶树中的CsICE1基因的表达能够被低温诱导,并且表达量显著升高[24]。水稻中的bHLH转录因子OrbHLH001基因与ICE1类似,它在拟南芥中的过量表达增强了拟南芥的抗盐和抗冻的能力[25]。虽然对于植物bHLH转录因子的结构特点、序列鉴定、功能验证等方面的研究取得了很大进展,但是bHLH转录因子家族成员数量众多、调控功能多样且复杂,不同植物的bHLH转录因子结构及调控功能也有不同,因此还需要更深入的研究。
早春短命植物能在早春低温环境中萌发并进行生长,对早春的低温具有较强的适应性[26],这是早春短命植物所必须具备的生态学特性。独行菜(LepidiumapetalumWilld.)分布广泛,世界各地海拔在400~2 000 m的地区几乎都有分布,对温度的适应范围较宽,且其种子为重要中药,具有止咳、消肿、强心等功效,近年来引起众多学者的关注。目前,有关独行菜的研究也较多,如药用开发及研究[27]、栽培方法与技术[28]、组织培养[29]、形态解剖[30]、C4相关结构研究[31]、分子系统学[32]、种衣结构与作用[33]等方面都有报道,国内外还有学者将独行菜作为粉尘、辐射等环境污染对植物及生态系统影响的评估物种[34-35]。对独行菜萌发生理特性[36]、萌发过程对低温耐受特性[37]、幼苗生长耐受低温特性及机制[38]等相关的内容也有一定的研究,但其调控机制仍远不清楚。
前期发现独行菜种子萌发存在低温停滞现象,而短时间较高温度能解除其低温停滞,且对萌发低温停滞与解除停滞的独行菜种子进行了转录组测序,其中发现了大量的bHLH家族基因,它们在独行菜种子低温萌发及幼苗生长过程中的作用,目前还没有研究。因此,本研究对独行菜种子萌发中低温停滞与解除停滞两组间的转录组bHLH家族基因进行比较,并选择植物耐冷相关的bHLH转录因子家族成员的ICE1基因进行克隆、表达分析,为探讨bHLH家族基因对独行菜种子萌发及幼苗生长耐受低温的分子调控作用奠定基础。
1 材料和方法
1.1 材 料
1.1.1独行菜种子采集独行菜种子于2015年5月15日采自乌鲁木齐市鲤鱼山。挑选出饱满的种子,用98%浓硫酸处理45 s后,用滤纸尽量拭去浓硫酸后,蒸馏水清洗种子2~3次,备用。
1.1.2独行菜种子低温萌发耐受组及低温萌发停滞组获得参照李萍萍等的方法,将吸水的独行菜种子置于4 ℃避光层积9 d,为低温萌发停滞组种子,层积9 d后用25 ℃处理60 min,为低温萌发耐受组种子[39-40]。
1.2 方 法
1.2.1独行菜种子bHLH转录本筛选委托北京诺禾致源生物信息科技有限公司进行高通量测序,获得独行菜种子转录组,采用关键词bHLH筛选转录本,进一步分析是否包含bHLH保守结构域,最后对每一条目标序列在GenBank中进行序列分析,并比较注释,去除冗余序列。
1.2.2独行菜种子bHLH转录本分类及注释分析选择Nr(NCBI non-redundant protein sequences)、GO(Gene Ontology)、KOG(euKaryotic Ortholog Groups)三大基因功能分析及蛋白序列分析数据库,对筛选获得的bHLH家族基因的转录本进行分类分析及功能注释分析。
1.2.3独行菜种子bHLH转录本表达显著性分析转录组中bHLH基因表达水平的评估采用FPKM方法[40]。本研究将(实验组表达量-对照组表达量)/对照组表达量≥0.5的基因定义为上调表达基因,实验组表达量/对照组表达量≤0.5的基因定义为下调表达基因,将(实验组表达量-对照组表达量)/对照组表达量<0.5,且实验组表达量/对照组表达量>0.5的基因定义为表达差异不显著基因。
1.2.4转录组独行菜bHLH转录因子表达量有效性分析以独行菜Actin基因为内参基因,采用荧光定量RT-PCR技术,分析c20009_g1在低温萌发耐受组和低温萌发停滞组的独行菜种子中的相对表达量,并与转录组数据库相对表达量进行比较,确定转录组独行菜bHLH转录因子表达量有效性。其中目标基因荧光定量引物为L1(5′-TGACACTGCTTTTGAAT-3′)和L2(5′-ACCACATAACACTGAAT-3′);内参基因荧光定量引物为A1(5′-CCAAAGGCCAACAGAGAGA-3′)和A2(5′-TGA-GACACACCATCACCA-3′)。
1.2.5独行菜IaICE1基因克隆及序列分析将25 ℃培养半个月的独行菜幼苗置于4 ℃处理12 h,采用Trizol试剂法提取独行菜幼苗总RNA;以根据转录本c20009_g1中开放阅读框序列设计的ICE1扩增引物P1(5′-AAAGGTGTCAACTTTGGCG-3′)和P2(5′-TTTAAAGGGACTTAGTTCT-3′)进行PCR扩增。产物经电泳检测回收,委托上海生工进行测序。用DNAMAN软件对获得的序列与c20009_g1进行比对,并与拟南芥ICE1序列进行比对,预测该开放阅读框编码蛋白序列,用ProtParam进行分析该蛋白质的等电点、分子量和亲水特性,用TMHMM2.0进行跨膜结构预测和保守功能结构域预测。
1.2.6独行菜幼苗laICE1基因表达受低温胁迫的影响将25 ℃培养半个月的独行菜幼苗分为6组,分别置于4 ℃处理0、1、2、6、12和24 h,采用荧光定量RT-PCR技术,分析独行菜幼苗laICE1基因表达对低温胁迫的响应。引物见表1。
2 结果与分析
2.1 基于独行菜种子转录组对bHLH类转录因子筛选
独行菜种子转录组经过高通量测序后,使用Trinity软件进行拼接,得到67 045条转录本序列,包含40 303条unigenes。以bHLH关键词进行查找,共找到203条unigenes,其中107条编码产物具有bHLH保守结构域,进一步去除重复注释等冗余,独行菜种子萌发过程有83个bHLH家族成员表达。这83个转录因子对应的unigenes序列最长的为4 656 bp,最短的为204 bp,72%介于1 000~2 500 bp间;56条编码完整阅读框,27条编码转录因子的部分序列。
2.2 独行菜种子bHLH转录因子注释分析
2.2.1独行菜种子bHLH转录因子Nr注释分析Nr是NCBI官方的蛋白序列数据库,能够全面反映被注释的蛋白质序列的信息[41]。由unigenes同源序列注释图(图1)可知,独行菜种子转录组中83个bHLH家族基因unigenes在Nr中被注释到了7个物种中,其中与拟南芥(Arabidopsisthaliana)序列的注释率最高,达到了30.5%,其次是琴叶拟南芥亚种(Arabidopsislyratasubsp.lyrata),达到了28%。
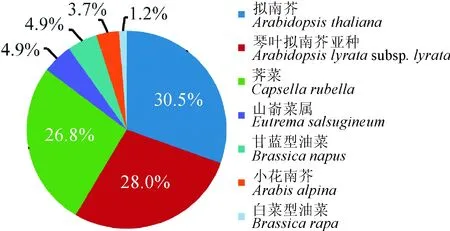
图1 bHLH家族基因unigenes在Nr库中的注释Fig.1 Lepidium apetalum bHLH family unigenes distribution in Nr
2.2.2独行菜种子bHLH转录因子GO分类分析GO是一套国际标准化的基因功能描述的分类系统,用来描述基因编码的产物所参与的生物过程、所具有的分子功能及所处的细胞环境[42]。通过GO分类分析,独行菜种子83条bHLH 中分别有46条、72条和45条被注释到生物过程(biological process,BP)、分子功能(molecular function,MF)和细胞组分(cellular component,CC)上(图2),BP、MF和CC都被注释的有27条(图3)。83条中87%的成员都注释到了分子功能,但还有11条的分子功能没有注释,这为挖掘新功能bHLH转录因子提供了基础。
2.2.3独行菜种子bHLH转录因子KOG分类分析KOG是NCBI的基于基因直系同源关系,针对真核生物。因功能不同,已知植物基因在KOG中被分为26组,按A-Z编号[43]。独行菜种子转录组中的83条bHLH基因序列,只有6条在KOG中被注释。分别注释到K(transcription,转录)、O(posttranslational modification, protein turnover, chaperones,翻译后修饰、蛋白质周转、伴侣)、R(general function prediction only,一般功能预测)和Y(Nuclear structure,核结构)类。其中,有3条与转录有关(表1)。
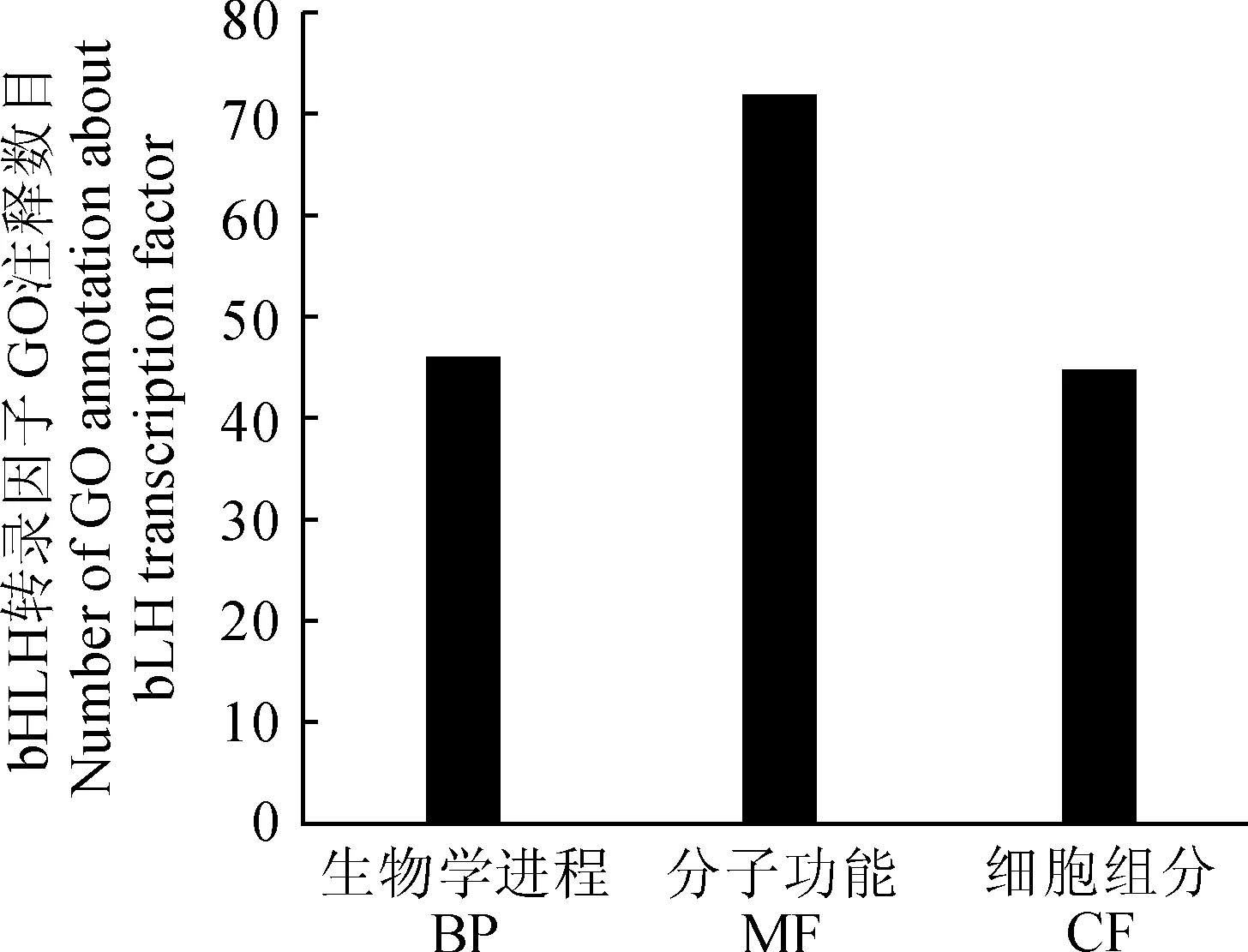
图2 独行菜bHLH家族基因unigenes的GO分类Fig.2 GO classification results of Lepidium apetalum bHLH family unigenes
2.3 独行菜种子bHLH转录因子表达分析
对独行菜种子bHLH家族基因的83个成员表达情况进行分析发现,相对于低温萌发停滞组,在低温萌发耐受组的独行菜种子中,有13个显著上调,17个显著下调,60个表达差异不显著(图4和5)。这显著上调的13个bHLH家族基因,可能与种子萌发进程密切相关,当处于萌发低温停滞期的种子,经过诱导,这些基因及其他相关功能基因表达,从而解除了种子萌发停滞。另外17个下调序列,处于低温下表达量高,经较高温度处理表达量下降,其可能与种子萌发过程中耐受低温胁迫密切相关。其中下调最显著的是c20009_g1序列,其经Nr注释和Blast分析,与植物冷耐受基因ICE1一致性最高,进一步说明下调基因可能与种子萌发的低温耐受有关。
为了进一步检测转录组中bHLH表达量是否相对准确,本研究以c20009_g1为例,通过荧光定量RT-PCR对表达量进行了验证,结果如图6所示,c20009_g1在低温萌发耐受组的行菜种子中,较低温萌发停滞组的表达量极显著下调,与其转录组表达情况(图4)基本相符。
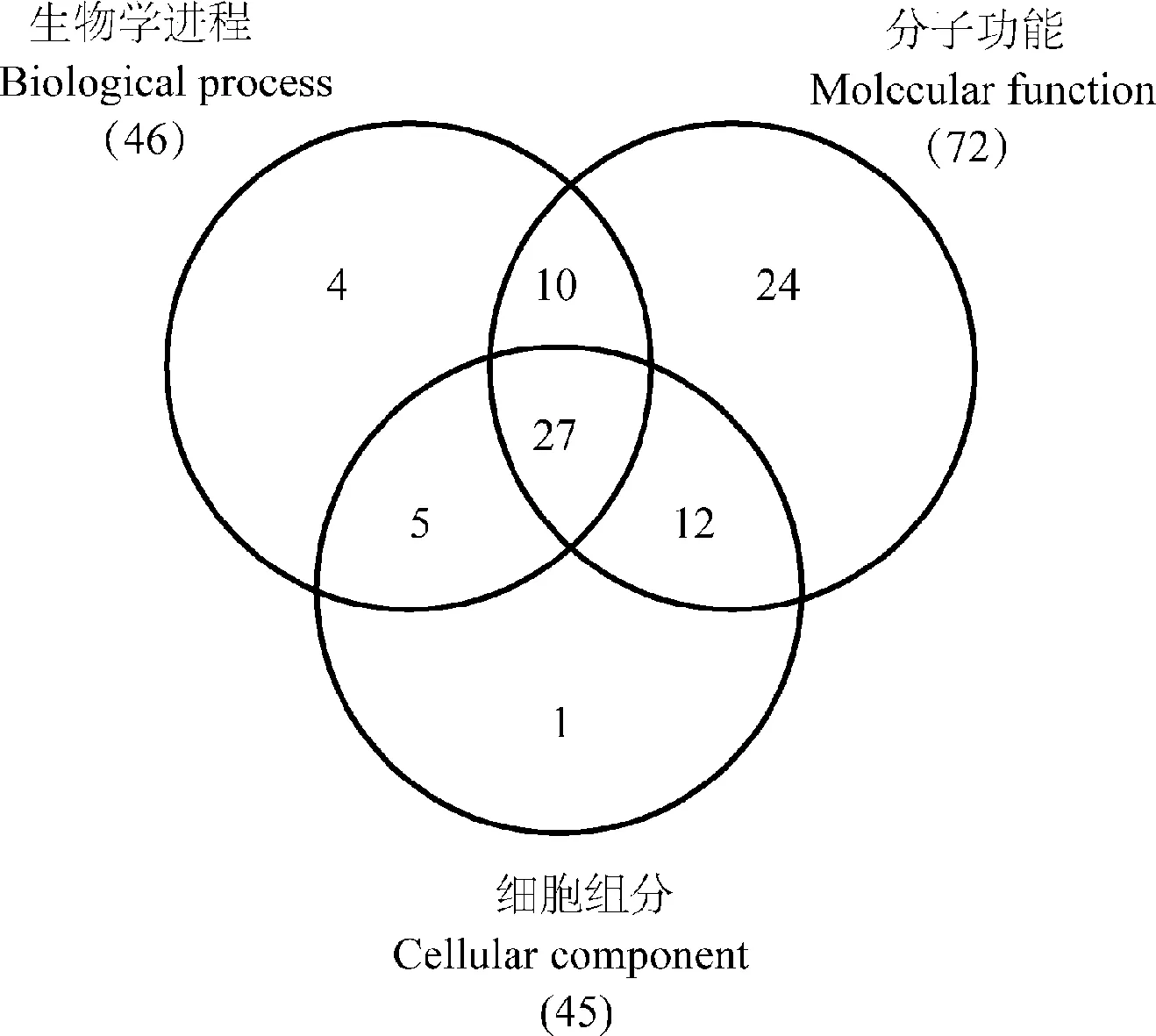
图3 独行菜bHLH家族基因unigenes的GO注释分布Fig.3 bHLH family unigenes Lepidium apetalum distribution in GO

表1 独行菜bHLH家族基因的KOG分类结果
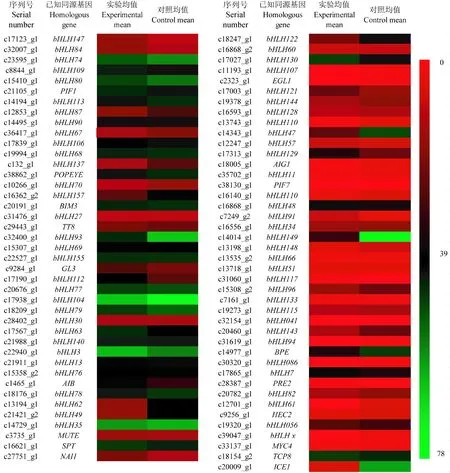
图4 独行菜种子低温萌发停滞解除前后bHLH家族基因相对表达量基于转录组分析Fig.4 Relative expression of bHLH family genes before and after germination at low temperature in the seeds of Lepidium apetalum, based on transcriptome analysis
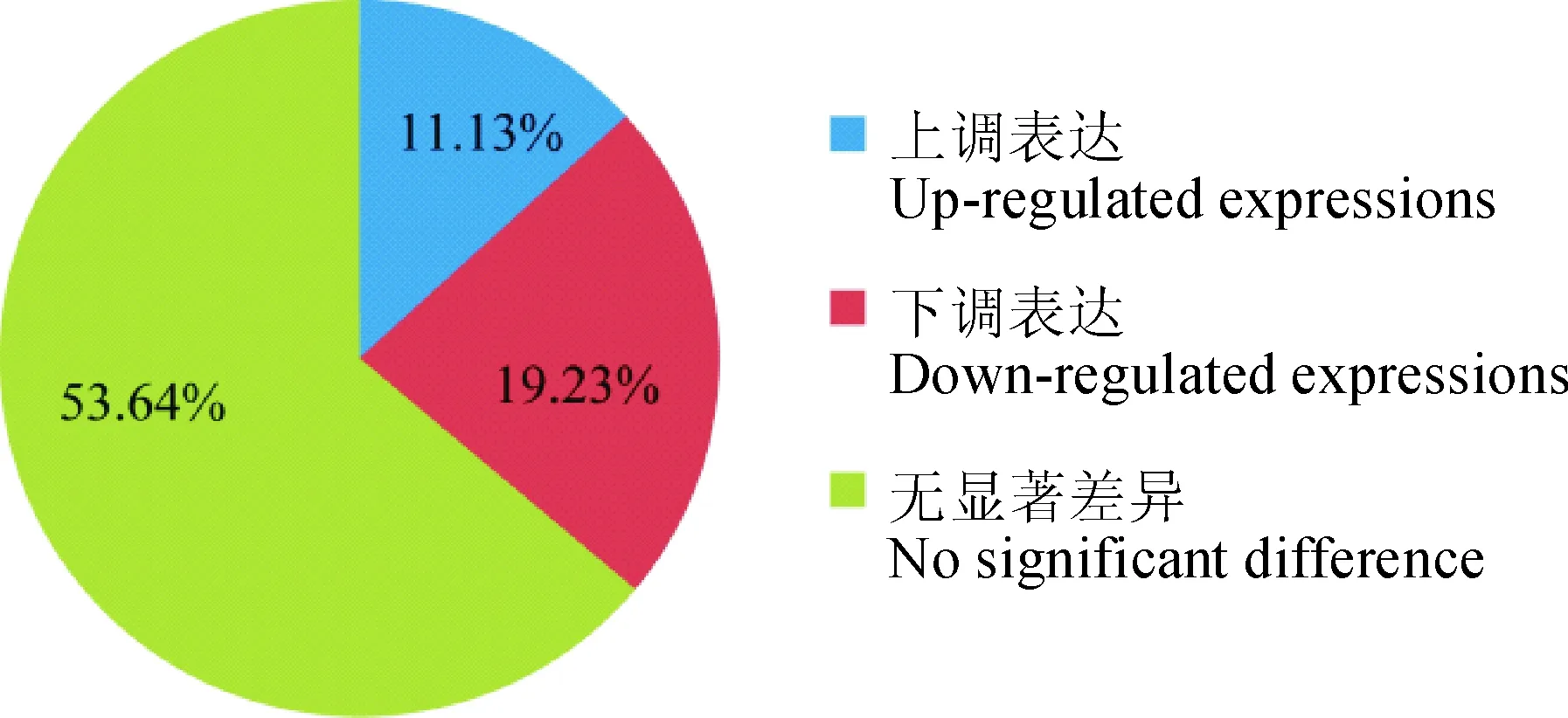
图5 解除停滞后bHLH家族基因相对表达差异Fig.5 Relative expression differences of bHLH family genes relieved germination stagnation at low temperature
对c20009_g1序列分析表明,该序列的开放阅读框为1 503 bp,编码的蛋白与拟南芥bHLH家族转录因子ICE1一致性最高。本研究将c20009_g1序列对应的基因命名为laICE1。
2.4 独行菜laICE1基因克隆及序列分析
如上所述,laICE1在处于低温状态的独行菜种子中表达量高,经较高温度处理后表达量下降,其可能与种子萌发过程中耐受低温胁迫密切相关。进一步采用RT-PCR扩增技术从独行菜幼苗中克隆cDNA序列,克隆产物经测序后,得到与预期完全一致的cDNA序列,编码500个aa组成的蛋白(图7)。该序列与拟南芥ICE1基因相似性很高,达到95%,表明克隆获得的序列为独行菜ICE1基因序列。
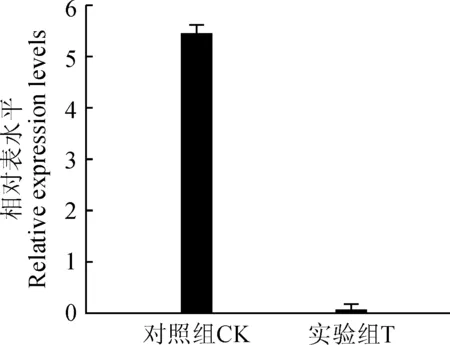
图6 bHLH成员ICE1相对表达量荧光定量PCR分析Fig.6 Relative expression of ICE1 of bHLH members by quantitative PCR
进一步使用ProtParam对独行菜laICE1编码产物进行预测,表明该基因编码一个分子量为54 635.19 kD、理论等电点为5.45、分子式为C2364H3742N688O758S22、不稳定系数为52.25、平均疏水性为-0.494的不稳定蛋白。使用TMHMM2.0进行跨膜结构预测分析表明,该蛋白不含有跨膜结构域。laICE1的功能结构域分析如图8所示,其编码产物包含HLH超家族的保守结构域,HLH结构域靠近肽链的C端,有2个主要由疏水氨基酸组成的α螺旋结构,这2个α螺旋结构由一个环状结构连接,这与已知的bHLH转录因子结构一致,表明laICE1属于bHLH类转录因子家族的编码基因。
2.5 低温胁迫对独行菜幼苗laICE1基因表达的影响
荧光定量PCR结果分析表明,随低温处理时间的增加,laICE1基因表达量出现显著变化,与对照组(0 h)比较,处理12 h时IaICE1基因表达量出现极显著升高,升高倍数达到46倍之多,表明在低温处理的初始阶段,为了抵御低温胁迫,独行菜幼苗中的laICE1基因出现迅速反应;而随着低温胁迫时间的延长,虽然该基因表达量较对照组仍有显著上调,但较处理12 h时不再增加(图9)。这可能是由于独行菜幼苗自身对低温环境能快速适应,基因laICE1在转录水平的表达量已达到抗冷需求。

图7 laICE1的cDNA全长序列及编码氨基酸序列Fig.7 cDNA full-length sequence and putative amino acid sequence of laICE1

图8 laICE1的结构域分析Fig.8 Domain analysis of laICE1
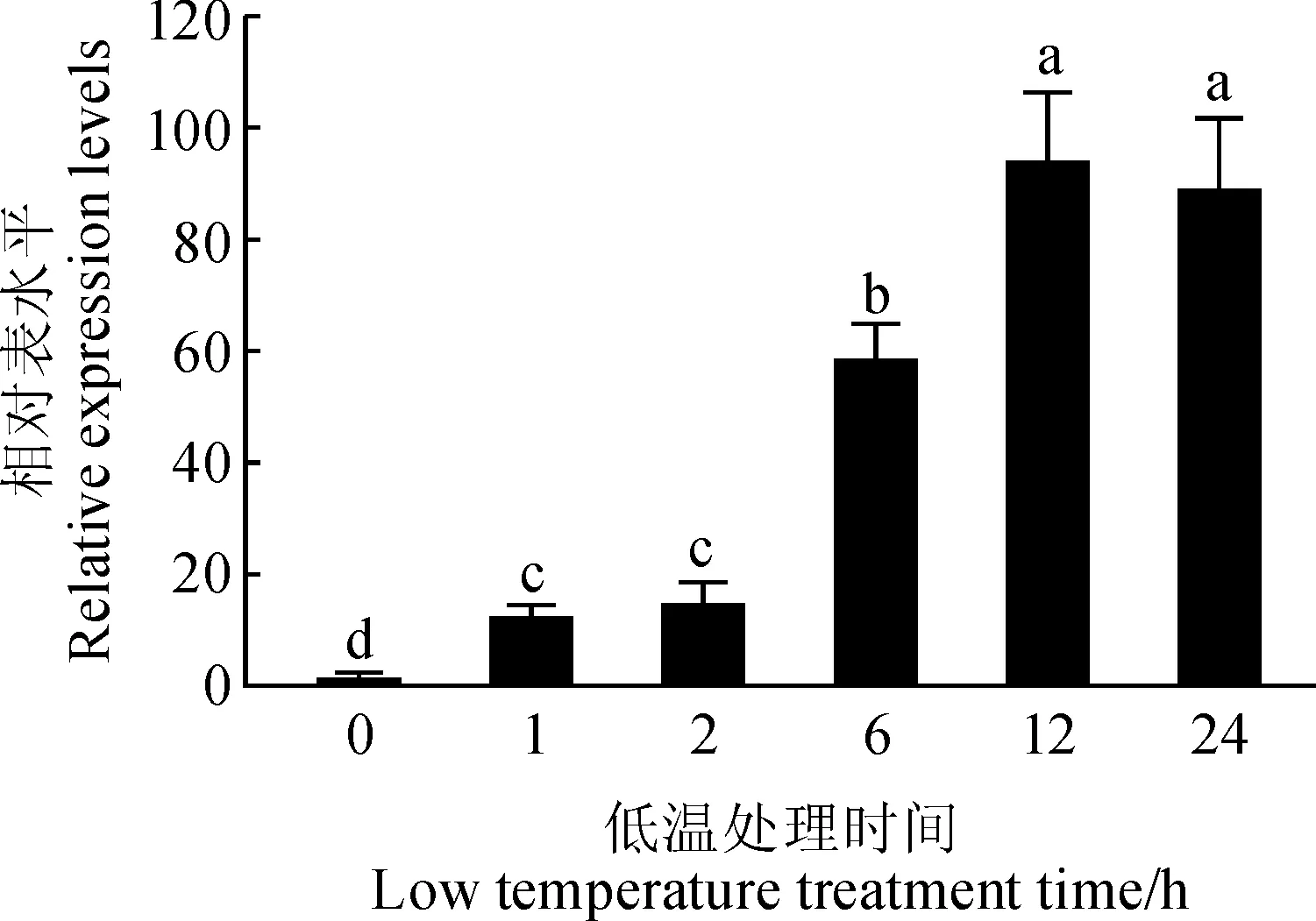
不同小写字母表示同期处理间在0.05水平上差异显著( P < 0.05)图9 低温处理后独行菜幼苗laICE1表达量Different letters indicate significant differences (P < 0.05) according to tukey’s multiple range testFig.9 The expression of laICE1 in seedlings of Lepidium apetalum at low temperature treatment
3 讨 论
从转录组分析来看,bHLH类转录因子不同成员在独行菜种子萌发低温耐受组和低温停滞组的表达量有所不同,有些成员在转录组包含的两组种子中可能不表达,因此说明独行菜bHLH类转录因子家族包含成员数应该远在83个之上。
获得的83个独行菜bHLH转录因子转录本,在Nr中被注释到了7个物种中,这7个物种都是十字花科植物,分别是拟南芥(Arabidopsisthaliana)、琴叶拟南芥亚种(Arabidopsislyratasubsp.
lyrata)、荠菜(Capsellarubella)、山嵛菜属(Eutremasalsugineum)、小花南芥(Arabisalpina)、甘蓝型油菜(Brassicanapus)、白菜型油菜(Brassicarapa),这说明了植物bHLH转录因子在进化中种属间保守性高。
通过对独行菜种子转录组bHLH类转录因子的表达量分析、基因分类与功能注释分析,表明部分独行菜bHLH转录因子在独行菜生长、发育、代谢、应答元素缺乏、低温逆境胁迫中有作用,如c38862_g1注释到POPEYE,可能对缺铁条件下植物根的生长有重要作用[44];如c16621_g1注释到SPT,该基因编码的一种bHLH转录因子在心皮边缘和花粉壳体组织生长的全过程中都有表达,还能够调控叶片、花瓣、柱头和根的一些特别组织的生长过程[45],还与心皮发育有关[46];如c9256_g1注释到HEC2,其能够调节雌性生殖组织的发育[47];如c20009_g1注释到ICE1,能够在低温条件下诱导CBF基因表达,进而调控CBF及其下游基因的表达,增强植物耐受低温的能力。本研究也通过实时荧光定量PCR技术证实了laICE1在独行菜幼苗中表达量受低温诱导显著上调,该基因可能确实对独行菜种子萌发和幼苗生长过程的低温耐受密切相关。
除了laICE1,独行菜bHLH转录因子一些其他成员也可能对独行菜耐受低温胁迫起调控作用,尤其17个下调序列,它们在萌发过程处于低温状态的独行菜种子中的表达量显著高于经较高温度处理的独行菜种子,其可能也与种子萌发过程中耐受低温胁迫密切相关。而另外有13 bHLH家族基因,虽然在处于萌发低温停滞期的种子表达量非常低,但在经过较高温度处理解除了种子萌发停滞的种子中表达量相对显著,很可能它们在解除种子低温萌发中起重要的调控作用,这需要后续进一步实验验证。
参考文献:
[1]TOLEDO-ORTIZ G, HUQ E, QUAIL P H. TheArabidopsisbasic/helix-loop-helix transcription factor family[J].PlantCell,2003,15(8):1 749-1 770.
[2]ATCHLEY W, DRESS A W. Positional dependence, cliques, and predictive motifs in the bHLH protein domain[J].JournalofMolecularEvolution, 1999,48(5):501-516.
[3]LI X, DUAN X, JIANG H,etal. Genome-wide analysis of basic/helix-loop-helix transcription factor family in rice andArabidopsis[J].PlantPhysiology, 2006,141(4):1 167-1 184.
[4]MURRE C, MCCAW P S, BALTIMORE D. A new DNA binding and dimerization motif in immunoglobulin enhancer binding, daughterless, MyoD, and myc, proteins[J].Cell, 1989,56(5): 777-783.
[5]SIMIONATO E, LEDENT V, RICHARDS G,etal. Origin and diversification of the basic helix-loop-helix gene family in metazoans: insights from comparative genomics[J].BmcEvolutionaryBiology, 2007,7(1):33.
[6]CHANDLER V L, RADICELLA J P, ROBBINS T P,etal. Two regulatory genes of the maize anthocyanin pathway are homologous: isolation of B utilizing R genomic sequences.[J].PlantCell, 1989,1(12):1 175-1 183.
[7]GOFF S A, CONE K C, CHANDLER V L. Functional analysis of the transcriptional activator encoded by the maize B gene: evidence for a direct functional interaction between two classes of regulatory proteins[J].Genes&Development, 1992,6(5):864-875.
[8]PARK K I, ISHIKAWA N, MORITA Y,etal. A bHLH regulatory gene in the common morning glory,Ipomoeapurpurea, controls anthocyanin biosynthesis in flowers, proanthocyanidin and phytomelanin pigmentation in seeds, and seed trichome formation[J].PlantJournalforCell&MolecularBiology, 2007,49(4):641-654.
[9]PARK K I. A bHLH protein partially controls proanthocyanidin and phytomelanin pigmentation in the seed coats of morning gloryIpomoeatricolor[J].HorticultureEnvironment&Biotechnology, 2012,53(4):304-309.
[10]KOES R, VERWEIJ W, QUATTROCCHIO F. Flavonoids: a colorful model for the regulation and evolution of biochemical pathways[J].TrendsinPlantScience, 2005,10(5):236-242.
[11]HICHRI I, HEPPEL S C, PILLET J,etal. The basic helix-loop-helix transcription factor MYC1 is involved in the regulation of the flavonoid biosynthesis pathway in grapevine[J].MolecularPlant, 2010,3(3):509-523.
[12]LING H Q, BAUER P, BERECZKY Z,etal. The tomato fer gene encoding a bHLH protein controls iron-uptake responses in roots[J].ProceedingsoftheNationalAcademyofSciencesoftheUnitedStatesofAmerica, 2002,99(21):13 938-13 943.
[13]IVANOV R, BRUMBAROVA T, BAUER P. Fitting into the harsh reality: regulation of iron-deficiency responses in dicotyledonous plants[J].MolecularPlant, 2012,5(1):27-42.
[14]OGO Y, ITAI R N, NAKANISHI H,etal. The rice bHLH protein OsIRO2 is an essential regulator of the genes involved in Fe uptake under Fe-deficient conditions[J].PlantJournalforCell&MolecularBiology, 2007,51(3):366-377.
[15]KUMARI M, TAYLOR G J, DEYHOLOS M K.. Transcriptomic responses to aluminum stress in roots ofArabidopsisthaliana[J].MolecularGenetics&Genomics, 2008,279(4):339-357.
[16]YI K, WU Z, ZHOU J,etal. OsPTF1, a novel transcription factor involved in tolerance to phosphate starvation in rice.[J].PlantPhysiology, 2005,138(4):2 087-2 096.
[17]KIRIBUCHI K, JIKUMARU Y, KAKU H,etal. Involvement of the basic helix-loop-helix transcription factor RERJ1 in wounding and drought stress responses in rice plants[J].BioscienceBiotechnology&Biochemistry, 2005,69(5):1 042-1 044.
[18]SEO J S, JOO J, KIM M J,etal. OsbHLH148, a basic helix-loop-helix protein, interacts with OsJAZ proteins in a jasmonate signaling pathway leading to drought tolerance in rice[J].PlantJournalforCell&MolecularBiology, 2011,65(6):907-921.
[19]DONG Y, WANG C, HAN X,etal. A novel bHLH transcription factor PebHLH35 fromPopuluseuphraticaconfers drought tolerance through regulating stomatal development, photosynthesis and growth inArabidopsis[J].Biochemical&BiophysicalResearchCommunications, 2014,450(1):453-458.
[20]LIU W, TAI H, LI S,etal. bHLH122, is important for drought and osmotic stress resistance inArabidopsis, and in the repression of ABA catabolism[J].NewPhytologist, 2014,201(4):1 192-1 204.
[21]XU W, ZHANG N, JIAO Y,etal. The grapevine basic helix-loop-helix (bHLH) transcription factor positively modulates CBF-pathway and confers tolerance to cold-stress inArabidopsis[J].MolecularBiologyReports, 2014,41(8):5 329-5 342.
[22]CHINNUSAMY V, OHTA M, KANRAR S,etal. ICE1: a regulator of cold-induced transcriptome and freezing tolerance inArabidopsis[J].Genes&Development, 2003,17(8):1 043-1 054.
[23]FURSOVA O V, POGORELKO G V, TARASOV V A. Identification ofICE2, a gene involved in cold acclimation which determines freezing tolerance inArabidopsisthaliana[J].Gene, 2009,429(1-2):98-103.
[24]WANG Y, JIANG C J, LI Y Y,etal. CsICE1 and CsCBF1: two transcription factors involved in cold responses inCamelliasinensis[J].PlantCellReports, 2012,31(1):27-34.
[25]LI F, GUO S, ZHAO Y,etal. Overexpression of a homopeptide repeat-containing bHLH protein gene (OrbHLH001) from Dongxiang Wild Rice confers freezing and salt tolerance in transgenicArabidopsis[J].PlantCellReports, 2010,29(9):977-986.
[26]ZHAO H X, LI Q, LI G,etal. Differential gene expression in response to cold stress inLepidiumapetalum, during seedling emergence[J].BiologiaPlantarum, 2012,56(1):64-70.
[27]李红伟, 郑晓珂, 弓建红. 独行菜和播娘蒿化学成分及药理作用研究进展[J]. 药物评价研究, 2013,36(3):235-240.
LI H W, ZHENG X K, GONG J H. Research progress in chemical constituents ofLepidiumapetalumandDescurainiasophiaand their pharmacological activities[J].DrugEvaluationResearch, 2013,36(3):235-240.
[28]赵凡, 金玉忠, 朱晓天. 独行菜及其栽培技术[J]. 吉林蔬菜, 1999,(2):33.
ZHAO F, JIN Y Z, ZHU X T.Lepidiumand its cultivation techniques[J].JilinVegetable, 1999,(2):33.
[29]徐栋生, 陈莎莎, 油天钰,等. 新疆短命植物独行菜的组织培养与植株再生[J]. 植物生理学报, 2010,46(11):1 183-1 184.
XU D S, CHEN S S, YOU T Y,etal. Tissue culture and plant regeneration of Xinjiang ephemeral plantLepidiumapetalumWilld[J].PlantPhysiologyCommunications, 2010,46(11):1 183-1 184.
[30]孙稚颖, 李法曾. 中国独行菜族部分属种的叶表皮观察[J]. 广西植物, 2008,28(4):431-436.
SUN Z Y, LI F Z. Observation on the leaf epidermis of partial genera and species of Lepidieae from China[J].Guihaia, 2008,28(4):431-436.
[31]李秀明, 刘彭, 谷丽丽,等. 新疆短命植物东方旱麦草和独行菜C4相关结构的初步研究[J]. 新疆农业科学, 2009,46(1):28-33.
LI X M, LIU P, GU L L,etal. Studies on the C4-related structures of two ephemerals-Eremopyrumorientale(L.)andLepidiumapetalumWilld in Xinjiang[J].XinjiangAgriculturalSciences, 2009,46(1):28-33.
[32]孙稚颖, 李法曾. 中国独行菜族(十字花科)部分属种的分子系统学研究[J]. 西北植物学报, 2007,27(8):1 674-1 678.
SUN Z Y, LI F Z. Molecular systematics of partial genera and species in Tribe Lepidieae (Brassicaceae) from China[J].ActaBotanicaBoreali-OccidentaliaSinica, 2007,27(8):1 674-1 678.
[33]袁祯燕, 多力坤·买买提玉素甫, 黄培佑. 早春短命植物独行菜天然种衣与水分的关系[J]. 种子, 2006,25(9):1-3.
YUAN Z Y, D L K.MAIMAITIYUSUFU, HUANG P Y. The relationship between water and the seed coat ofLepidiumapetalum—an ephemeral[J].Seed, 2006,25(9):1-3.
[34]PROKOPIEV I A, ZHURAVSKAYA A N, FILIPPOVA G V. Influence of technogenic dust pollution on changes in the physiological and biochemical adaptation and radio resistance of pepperweed (Lepidiumapetalum, Wild.) seedlings[J].ContemporaryProblemsofEcology, 2013,6(2):199-202.
[35]马宏. 利用独行菜监测土质污染[J]. 环境与可持续发展, 1985,(11):23.
MA H. The use ofLepidiumapetalumin soil pollution monitoring[J].EnvironmentandSustainableDevelopment, 1985,(11):23.
[36]孟君, 李群, 李冠. 两种独行菜种子萌发生理特性研究[J]. 生物技术, 2008,18(2):32-35.
MENG J, LI Q, LI G. Physiological characteristic of seed germination of two species ofLepidiumL.[J].Biotechnology, 2008,18(2):32-35.
[37]赵惠新, 李群, 周晶,等. 短命植物独行菜种子萌发过程对低温的耐受特性[J]. 植物分类与资源学报, 2010,32(5):448-454.
ZHAO H X, LI Q, ZHOU J,etal. The characteristics of low temperature tolerance during seed germination of the ephemeral plantLepidiumapetalum(Cruciferae)[J].PlantDiversity, 2010,32(5):448-454.
[38]杨娜, 赵和平, 葛风伟,等. 2种独行菜萌发对低温胁迫的生理响应[J]. 干旱区研究, 2015,32(4):760-765.
YANG N, ZHAO H P, GE F W,etal. Physiological response of twoLepidiumspecies to low temperature stress during seed germination[J].AridZoneResearch, 2015,32(4):760-765.
[39]李萍萍, 曾卫军, 周茜,等. 解除独行菜种子低温萌发停滞的温度响应蛋白筛选及表达分析[J]. 分子植物育种, 2016,14(3):722-729.
LI P P, ZENG W J, ZHOU Q,etal. Screening and expression analysis of temperature-responsing proteins that can remove low temperature stagnancy of germination inLepidiumseeds[J].MolecularPlantBreeding, 2016,14(3):722-729.
[40]周茜, 赵惠新, 李萍萍,等. 独行菜种子转录组的高通量测序及分析[J]. 中国生物工程杂志, 2016,36(1):38-46.
ZHOU Q, ZHAO H X, LI P P,etal.Denovocharacterization of the seed transcriptome ofLepidiumapetalumWilld[J].ChinaBiotechnology, 2016,36(1):38-46.
[41]PRUITT K D, TATUSOVA T, MAGLOTT D R. NCBI Reference Sequence (RefSeq): a curated non-redundant sequence database of genomes, transcripts and proteins[J].NucleicAcidsResearch, 2005,33(Database issue):D501-504.
[42]CONESA A, TEROL J, ROBLES M. BLAST2GO: a universal tool for annotation, visualization and analysis in functional genomics research[J].Bioinformatics, 2005,21(18):3 674-3 676.
[43]LI L, STOECKERT C J, ROOS D S. OrthoMCL: identification of ortholog groups for eukaryotic genomes[J].GenomeResearch, 2003,13(9):2 178-2 189.
[44]HEIM M A, JAKOBY M, WERBER M,etal. The basic helix-loop-helix transcription factor family in plants: a genome-wide study of protein structure and functional diversity[J].MolecularBiology&Evolution, 2003,20(5):735-747.
[45]HEISLER M G, ATKINSON A, BYLSTRA Y H,etal. SPATULA, a gene that controls development of carpel margin tissues inArabidopsis, encodes a bHLH protein[J].Development, 2001,128(7):1 089-1 098.
[46]GROSZMANN M, PAICU T, SMYTH D R. Functional domains of SPATULA, a bHLH transcription factor involved in carpel and fruit development inArabidopsis[J].PlantJournal, 2008,55(1):40-52.
[47]GREMSKI K, DITTA G, YANOFSKY M F. The HECATE genes regulate female reproductive tract development inArabidopsisthaliana[J].Development, 2007,134(20):3 593-3 601.
