超临界CO2处理玉米秸秆残留木质素形态及脱除研究
2018-04-04张敏华吕惠生吕春柳任苗苗
张敏华,吕惠生,吕春柳,任苗苗
(天津大学石油化工技术开发中心,天津 300072)
纤维素乙醇技术作为一种清洁能源技术,可以用来替代传统的粮食乙醇技术,缓解粮食危机[1]。其中利用可再生木质纤维素生产乙醇,已经成为世界各国的研究热点。木质素是—种天然高分子聚合物,在自然界中的数量仅次于纤维素,是重要的可再生资源之一[2]。目前利用木质纤维素生产乙醇的研究非常多,但多数研究只强调对纤维素组分的转化利用,而对木质素资源化利用的相关研究较少。在纤维素乙醇生产过程中,需要从木质纤维素中除去木质素,使酸或酶可以较容易水解纤维素,再通过发酵将纤维素转化为乙醇[3-4]。超临界流体预处理(Supercritical fluid pretreatment)作为一种新兴的绿色化学工艺,主要应用于木质素的去除预处理,与传统工艺相比较[5],具有避免有害溶剂的使用、降低环境的污染、便于产物分离等优点,受到了人们的广泛关注[6-8]。虽然SCF预处理能够有效脱除玉米秸秆中的大部分木质素,但仍有少量木质素不能被脱除,残留在纤维素表面,从而降低纤维素酶解工艺的经济性[9-11]。因此本试验以SCF预处理玉米秸秆过程难以脱除的残留木质素为对象,通过对处理后的秸秆表面形貌的观察及表征研究,分析残留木质素的存在形式,残留木质素脱除困难的原因。并在这基础上,比较不同洗脱方法对残留木质素的影响,确定最佳的洗脱方法,进一步脱除残留木质素,从而提高后续的酶解效率。
1 材料与方法
1.1 材料、试剂及仪器
材料:玉米秸秆原料由中粮(肇东)公司提供。
玉米秸秆原料主要成分分析:纤维素37.3%,半纤维20.6%及木质素17.5%。将玉米秸秆原料通过风干、粉碎处理,筛选出粒度为0.25~0.42 mm的实验原料,放置于干燥器中储存备用。
试剂:纯度为99.9%的CO2,无水乙醇,二氧六环,浓盐酸,实验试剂均为分析纯规格,生产单位为天津江天化工公司。
仪器:MParr 4843型高压反应器(美国Parr公司);粉碎机(FW177,天津泰斯特公司)。
1.2 试验方法
1.2.1 预处理实验
超临界CO2/乙醇-水处理玉米秸秆原料的实验装置及过程参见图1。实验方法:分别取5 g玉米秸秆、120 mL乙醇及80 mL水加入1000 mL的高压反应器中,密封反应器。开启磁力搅拌器的冷凝水;开启CO2进料泵,向反应器中充入适量的CO2;然后调整磁力搅拌器转速为300 r/min,设定反应温度为180℃,压力为15 MPa;打开高压反应器加热电源,当反应器内温度达到设定温度后,开始计时;反应时间60 min后,关闭加热电源及搅拌器电源,将反应器从加热槽中取出,通风降温至30℃以下,打开反应器放气阀,待釜内压力降至常压后,关闭冷凝水,开启反应器的釜盖,将反应所得混合产物取出;将反应产物采用布氏漏斗抽滤,将滤饼固体放置真空干燥箱中40℃烘干后,放入干燥器中保存。

图1 超临界CO2预处理实验装置图[12]
1.2.2 洗脱实验
通过超临界CO2/乙醇-水处理后的玉米秸秆,木质素基质的复杂结构被破坏,大部分木质素片段从木质纤维素表面脱除,但纤维素表面还会存在残余木质素。玉米秸秆洗脱实验目的是脱除残余木质素。洗脱实验操作:将5 g预处理后的玉米秸秆、200 mL水/乙醇溶液(6∶4/v∶v)和1 wt%NaOH溶液置于反应器中,实验温度80℃;时间1 h,反应器采用水冷却;洗脱处理后的玉米秸秆通过布氏漏斗后再用去离子水清洗;将洗脱样品置于真空烘箱中40℃烘干,存储在干燥器中备用。
1.2.3 扫描电镜分析
采用扫描电镜(SEM,Nanosem 430,FEI)观察处理前后的玉米秸秆原料表面结构变化。实验步骤:分别取适量不同处理条件获得的干燥玉米秸秆样品,通过离子溅射仪金靶溅射镀金,再将镀金后的秸秆样品放置扫描电镜下观察并摄像记录。
扫描电镜的操作参数:加速电压为0.1~30 kV;步长为1 kV;放大倍数为20~80万;分辨率为1 nm;金属膜厚度为5~10 nm;样品台操作范围:X、Y方向50 mm,Z方向30 mm。
1.2.4 傅里叶红外光谱(FT-IR)
取适量充分干燥的待测样品,干燥条件下加入少量KBr粉末,在玛瑙研钵内反复研磨均匀,经压片机压成透明薄片,通过Nicolet 6700型傅立叶变换红外光谱仪进行红外分析。漫反射红外分析采用Smart Preformer Nexus/X700 ATR附件挤压样品片,保证样品和diamond均匀接触。红外分析扫描范围400~4000 cm-1,扫描次数64次。分辨率4 cm-1。
1.2.5 光电子能谱(XPS)
光电子能谱(XPS)是分析材料表面成分构成的有效手段之一。本试验采用PerkinElmer公司的PHI-1600型X光电子能谱仪分析玉米秸秆表面组成。采用Mg靶Kα射线,功率250 W,扫描面积0.8 mm2。样品室真空度为1.2×10-8Torr。各元素的结合能是以C1s电子结合能284.6 eV作为校正标准。
2 结果与分析
2.1 残留木质素形貌分析(图2)

图2SEM图像
采用扫描电镜分析的方法,观察预处理前后的玉米秸秆样品表面的木质素残留的状态。从图2(a)可以看出,未处理的玉米秸秆样品的纤维表面光滑、纤维成束、排列紧密整齐,且分布稀疏微孔。从图2(b)处理后的未做洗脱处理的玉米秸秆样品的扫描电镜图可以发现,处理后的秸秆残渣表面存在大量的球状颗粒。Donohoe等[10]曾对酸处理及热液处理之后的玉米秸秆表面进行观察,发现玉米秸秆纤维表面存在球状颗粒,并采用红外、核磁等手段对球状颗粒进行成分分析,确认该颗粒为木质素。木质素的电子显微镜相关的研究也表明,木质素是以球状质点状态或块状质点状态聚集存在[13]。基于上述研究,可以推断图2(b)所示的球状颗粒为木质素进一步聚合形成的较大分子的残留木质素。球状木质素颗粒也主要存在于纤维中,并且分布不均匀。
图3为玉米秸秆纤维素表面残留木质素颗粒的尺寸和形貌。从图3(a)可看出:木质素颗粒的粒度为0.1~0.9µm。相比之下,沉积在有机溶剂制浆过程的残留木质素的粒度范围为500~2000µm[10]。Donohoe等[10]发现,在稀酸预处理过程中,木质素颗粒沉积的粒度范围为0.02~0.1µm。因此可以看出,不同预处理方法可以改变木质素颗粒的大小。图3是通过在较高的放大倍率下聚焦在单个粒子上获得的。从图3(b)可以看出,颗粒表面并不光滑。根据Donohoe等[10]的研究发现,这些包裹在木质素颗粒表面的不平滑“外壳”可能是碳水化合物或者是木质素-碳水化合物复合体。然而同时还需要更多的研究来探讨颗粒表面的成分组成。图3(c)为一些颗粒聚集在一起,凝结成不规则颗粒,使颗粒变大。这表明这些木质素小颗粒之间存在相互作用。虽然确切的相互作用还不清楚,但仍有理由推测这种相互作用可以促进木质素的聚集。这一假设可以解释各种大小的木质素小球,如图3(a)所示。残留木质素的球状颗粒具有较大的表面积,对后续酶解起到抑制作用,降低酶解效率,需采用有效方法进行脱除。
2.2 残余木质素的脱除研究
基于上述分析,分别选择乙醇水溶液(6∶4/v∶v)和1%(wt%)NaOH水溶液对于残留木质素进行脱除,玉米秸秆残留木质素的脱除在MParr 4843反应釜中操作。分别取5 g预处理秸秆残渣和200 mL处理液于反应釜中。处理温度设置为80℃,时间为1 h。反应釜具体操作方法见1.2。处理完成后,将洗脱液与秸秆混合物取出,布氏漏斗抽滤,滤饼采用去离子水反复洗脱。最后,将固体滤饼取出,40℃真空干燥。干燥后的样品置于4℃下冷藏。

图3 预处理后未洗脱的玉米秸秆表面球状颗粒的尺寸和形貌分析
2.2.1 乙醇水(6∶4/v∶v)洗脱法
温度和溶解度是影响残留木质素沉积的重要因素。研究表明,浓度60%(v∶v)左右的乙醇溶液在80℃时对木质素具有较好的溶解作用[14]。因此,采用80℃乙醇水(6∶4/v∶v)溶液对预处理秸秆表面的残留木质素进行脱除。
图4为乙醇水(6∶4/v∶v)溶液脱除处理之后的预处理秸秆残渣。由图4看出,乙醇水溶液处理之后的预处理秸秆残渣表面仍有大量的球状木质素颗粒,说明部分残留木质素仍不能被乙醇水溶液溶解脱除。根据xu等[15]的研究可知:在60%乙醇水溶液中,当温度在80℃以上时,木质素具有很好的溶解性。然而,如图4所示,在80℃下,60%乙醇溶液不能除去纤维素表面的木质素颗粒。适宜温度的乙醇-水溶液洗脱仍不能脱除部分残留木质素,说明部分残留木质素在乙醇水溶液中的溶解性较差。由此推断,残留木质素与纤维素表面不仅存在物理吸附作用,可能还存在一定的化学键合,使残留木质素难以溶解脱除。

图4 乙醇水(6∶4/v∶v)溶液处理后的预处理秸秆残渣
2.2.2 1%NaOH洗脱法
采用质量分数为1%的NaOH溶液预处理秸秆表面的残留木质素洗脱。采用80℃乙醇水溶液作为洗脱液,为残留木质素的溶解提供适宜的温度和溶剂。
图5为1%NaOH溶液洗脱之后的预处理秸秆残渣。可以看出,纤维素表面更加光滑。但仍有少量木质素颗粒。图5(b)是在1%NaOH溶液洗脱后纤维素表面的残余木质素的球形粒子图像。可见,残留木质素颗粒的表面受到一定程度上的破坏。木质素碳水化合物化合物由于碱性溶液的化学活性而被分解。因此,部分木质素颗粒被除去。结果表明,木质素的沉积既有物理吸附作用,又有化学反应。一方面,溶解的木质素碎片在乙醇溶液中由于温度降低和木质素浓度增加而重新吸附在纤维上;另一方面,由于木质素碳水化合物的结合,一些木质素不能溶解在乙醇中,停留在纤维素表面。
2.2.3 两种洗脱方法的比较
2.2.3.1ATR-FTIR分析比较
ATR衰减全反射光谱技术是红外光谱测试中一种应用极其广泛的技术,是一种有效的表面分析技术[16]。本研究采用ATR-FTIR技术分析经过不同处理的玉米秸秆表面发生的化学变化。图6为分别经过不同处理的玉米秸秆ATR谱图。
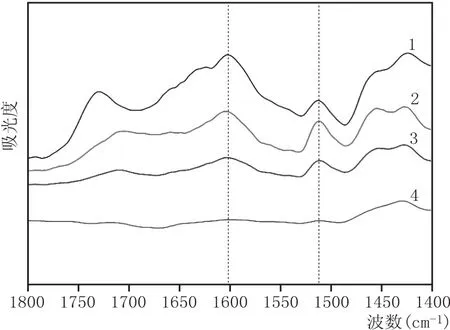
图6 不同处理的玉米秸秆的光谱图
图6中1510 cm-1和1600 cm-1左右处为木质素苯环结构的典型吸收。由图6可以看出,经过超临界预处理之后,未洗脱的秸秆残渣在1510 cm-1处有明显吸收,说明在秸秆表面有大量的残留木质素。分别经过乙醇溶液和NaOH溶液脱除处理之后,苯环峰吸收明显减弱。说明两种脱除方法均能有效脱除秸秆表面的残留木质素。
对比不同的洗脱方法发现,经过乙醇洗脱后的秸秆残渣上苯环峰吸收较未洗脱秸秆残渣减弱,但是仍明显存在,说明残留木质素只有部分被脱除,仍有一部分存在于秸秆表面,不能被洗脱脱除。经过NaOH溶液洗脱的秸秆残渣已经几乎看不到苯环峰的吸收,说明与乙醇水溶液相比,NaOH溶液能更好地脱除秸秆表面的残留木质素。这一点与SEM分析结果相符。
玉米秸秆经过超临界预处理后,木质素脱除率达到78%,大部分的木质素脱离秸秆。但是,由红外分析发现,1510 cm-1处峰的吸收明显增强。由此推断,经过预处理之后,木质素的三维网状结构遭到破坏,木质素小分子从三维骨架中溶出,大部分木质素溶解到预处理液中,脱离秸秆表面,从而达到较高的脱除率。另一部分未脱除的残留木质素则沉积在纤维素表面,因此,使得ATR谱图中苯环峰仍然具有较强的吸收。乙醇水溶液能脱除部分残留木质素,但是仍有部分残留木质素较难被溶解脱除。NaOH溶液洗脱能有效脱除预处理秸秆表面的残留木质素。
2.2.3.2XPS分析比较
XPS是分析纤维素纤维表面成分的有效工具。采用XPS分析不同处理后的秸秆样品,结果见表1。

图5 1%NaOH洗脱预处理秸秆残渣SEM

表1 不同秸秆样品XPS分析结果比较*
对于木质纤维素原料,C1(C-C或C-H或C=C)只存在于木质素中及可溶物中,不存在于纤维素和半纤维素中。因此纤维素表面的残留木质素沉积量可以通过C1含量分析。残留木质素沉积量及残留木质素脱除率计算公式参考相关文献,具体公式如下[17]:

其中,ϕ(lignin)代表表面木质素含量;R代表乙醇水(6∶4/v∶v)溶液和1%NaOH水溶液对表面木质素的脱除率。
由表1可看出,预处理之后,残留木质素沉积量ϕ(lignin)减小,说明超临界预处理可以破坏木质素对纤维素的包裹,更多的纤维素纤维暴露出表面,纤维素表面的木质素减少。结合木质素脱除率分析结果,超临界预处理能脱除大部分木质素。预处理秸秆分别经过乙醇水(6∶4/v∶v)溶液洗脱以及1%NaOH溶液洗脱之后,ϕ(lignin)依次减小,表明两种洗脱方法能有效脱除纤维素表面的残留木质素。乙醇水溶液及NaOH水溶液对残留木质素的脱除率分别为19.2%及22.2%,说明两者均能脱除部分残留木质素。但是可以看出1%NaOH溶液洗脱效果较好。
3 结论
3.1在玉米秸秆超临界CO2/乙醇-水预处理过程中难以脱除的残留木质素以球状颗粒形式不均匀分布在纤维素表面,粒度为0.1~0.9µm,并在纤维素粗糙表面相互聚集,形成多粒度的残留木质素颗粒。
3.2残留木质素的球状颗粒具有较大的表面积,对后续酶解起到抑制作用,降低酶解效率,需采用有效方法进行脱除。
3.3乙醇水(6∶4/v∶v)溶液及1%NaOH水溶液对残留木质素的脱除率分别为19.2%及22.2%,说明两者均能脱除部分残留木质素,并且NaOH水溶液脱除效果优于乙醇水溶液。
参考文献:
[1]马斌,储秋露,朱均均,等.4种木质纤维素预处理方法的比较[J].林产化学与工业,2013,33(2):25-30.
[2]王月阳,苏宝玲,孙钊,等.碱法分离回收水稻秸秆中木质素[J].化工进展,2016,35(B11):369-375.
[3]平清伟,王春,潘梦丽,等.木质纤维生物质精炼中木质素的分离及高值化利用[J].化工进展,2016,35(1):294-301.
[4]周丹丹,庆喜,刘苇,等.利用CaO/PAC选择性去除预水解液中木质素[J].林产化学与工业,2016,36(5):75-80.
[5]LEE K M,NGOH G C,CHUAA S M,et al.Comparison study of different ionic liquid pretreatments in maximizing total reducing sugars recovery[J].Bioresources,2014,9(1):1552-1564.
[6]余强,庄新姝,袁振宏,等.木质纤维素类生物质制取燃料及化学品的研究进展[J].化工进展,2012,31(4):784-791.
[7]刘江燕,武书彬,李擘.超临界CO2萃取脱除毛竹木质素的研究[J].生物质化学工程,2010,44(4):1-7.
[8]NARAYANASWAMY N,FAIK A,GOETZ D J,et al.Supercritical carbon dioxide pretreatment of corn stover and switchgrass for lignocellulosic ethanol production[J].Bioresource technology,2011,102(13):6995-7000.
[9]潘奇,陈介南,张新民,等.纤维乙醇发酵残渣中酶解木质素的提取与表征[J].化工进展,2015,34(1):86-90.
[10]DONOHOE B S,DECKER S R,TUCKER M P,et al.Visualizing lignin coalescence and migration through maize cell walls following thermochemical pretreatment[J].Biotechnology and bioengineering,2008,101(5):913-925.
[11]GAO M,XU F,LI S R,et al.Effect of SC-CO2pretreatment in increasing rice straw biomass conversion[J].Biosystems engineering,2010,106(4):470-475.
[12]任苗苗,吕惠生,张敏华.玉米秸秆木质素的超临界提取及结构表征[J].化学工业与工程,2012,29(5):53-57.
[13]陈洪雷,黄峰,杨桂花,等.草木半纤维素的研究进展[J].林产化学与工业,2008,28(1):119-126.
[14]XU Y J,LI K C,ZHANG M Y.Lignin precipitation on the pulp fi bers in the ethanol-based organosolv pulping[J].colloids and surfaces a:physicochemical and engineering aspects,2007,301(1/3):255-263.
[15]KRISTENSEN J B,THYGESEN L G,FELBY C,et al.Cell-wall structural changes in wheat straw pretreated for bioethanol production[J].Biotechnology for biofuels,2008,1(1):5.
[16]MAXIMOVA N,ÖSTERBERG M,KOLJONEN K,et al.Lignin adsorption on cellulose fi bre surfaces:effect on surface chemistry,surface morphology and paper strength[J].Cellulose,2001,8(2):113-125.
