钨酸铋-石墨烯复合物的制备及其可见光降解甲基橙的性能研究
2018-03-29邢国强尚建鹏
邢国强,尚建鹏∗
(山西大同大学化学与环境工程学院,山西大同037009)
近年来,能源资源枯竭和环境污染问题已成为社会发展的两大制约因素。太阳能是地球能源的总源泉,通过光催化过程,不仅能够将太阳能转化为化学能,还可以降解环境中的污染物。因此,有效利用太阳能在解决能源短缺和环境污染方面有巨大潜力。1972年,日本科学家Fujishima发现TiO2单晶电极在光的作用下可分解水制氢[1],自此,开始了利用太阳能进行光催化的研究。TiO2因其化学稳定性好、无毒、无污染、生产成本低等优点而得到广泛研究[2-4],但是,TiO2基光催化材料禁带宽度较大,只能吸收太阳光中的紫外光部分(约占太阳光的4%),严重影响了太阳能的利用率。基于此,目前光催化的研究工作主要集中在以下2个方面:①促使光生电子与空穴的分离,抑制其复合,从而提高量子效率;②扩大激发光的波长范围,使其向可见光区扩展,以便充分利用太阳能。
铋系光催化剂因其特殊的电子轨道构成,使其禁带宽度变窄,可吸收太阳光中的可见光部分(约占太阳光的40%),引起了科研工作者的关注[5-10]。但是,该类催化剂光生电子和空穴复合快,量子效率低。为此,提高铋系光催化剂的性能关键在于抑制光生电子和空穴的复合速率。
自2004年英国科学家首次制备出由碳原子以sp2杂化连接的单原子层构成的新型二维原子晶体-石墨烯以来,石墨烯作为新型的炭材料引起了全世界的研究热潮[11-13]。石墨烯具有优异的导电性、透光性、大的比表面积、良好的化学稳定性以及易表面功能化等特点,使其成为构筑纳米复合材料的理想材料。特别是石墨烯优良的导电性能,有利于光生电子传输。将石墨烯与传统的半导体光催化材料复合后,石墨烯结构中存在的离域大π键,可以作为一个大的电子接受器,光生电子可以通过石墨烯快速转移,进而降低电子-空穴复合的机率,提高光催化活性。我们利用水热法合成了一系列钨酸铋-石墨烯复合物,在可见光下能有效降解印染行业废水中的有机染料甲基橙。
1 实验部分
1.1 实验仪器与试剂
仪器:722E型分光光度计(上海光谱仪器有限公司);85-1磁力搅拌器(上海青浦沪西仪器厂);CHF-XM-500W短弧氙灯/汞灯稳流电源(北京畅拓科技有限公司);DHG-9070A电热恒温鼓风干燥箱(上海齐欣科学仪器有限公司);SHB-Ⅲ循环水式多用真空泵(郑州长城工贸有限公司医疗设备厂);分析天平(上海天平仪器厂);TGL-20B高速离心机(郑州长城科工贸有限公司);不锈钢高压釜(上海依艺机械设备有限公司)。
无水乙醇,甲基橙(分析纯,北京化工厂);五水硝酸铋(分析纯,天津市化学试剂公司);钨酸铵(分析纯,北京双环化学试剂厂);去离子水(自制);氧化石墨烯(自制)。
1.2 钨酸铋-石墨烯复合物的制备
将10 mL(4.2 mg/mL)的氧化石墨烯溶于10 mL无水乙醇中,超声处理1 h。然后称取0.179 6 g五水硝酸铋和0.049 9 g钨酸铵于10 mL的无水乙醇中,室温下搅拌30 min。将以上溶液混合,用浓氨水滴定至pH=8。所得混合溶液转移到50 mL不锈钢水热反应釜中,在不同温度下反应6 h后,冷却到室温,用蒸馏水洗涤5次,过滤,60oC下干燥12 h。所得产物标为Bi2WO6-GO(24wt%)-150oC、Bi2WO6-GO(24wt%)-180oC、Bi2WO6-GO(24wt%)-200oC。在其他条件不变的情况下,将加入的氧化石墨烯分别加倍至20 mL、减半至5 mL,所得产物标为Bi2WO6-GO(12 wt%)-200oC、Bi2WO6-GO(48wt%)-200oC。
1.3 光催化性能评价
称取0.1 g的催化剂样品放入到100 mL的甲基橙溶液(20 mg/L)中,在暗箱中搅拌30 min使之达到吸附平衡。将暗反应后的混合液转移到氙灯下,用可见光照射。实验过程中每隔15 min取混合液3 mL,高速离心后,取上层清液,用722E型可见光分光光度计测定溶液的吸光度(464nm)。
2 结果与讨论
2.1 水热温度对样品光催化性能的影响
不同水热温度的催化剂在可见光下降解(20 mg/L)甲基橙的活性如图1所示。结果显示,在不加催化剂情况下,在可见光照射下,甲基橙溶液基本不降解;以不同水热温度制备的Bi2WO6-GO(24wt%)为催化剂时,在可见光照射下,甲基橙的降解率显著增加;随着水热温度的升高,甲基橙的降解率增大。以Bi2WO6-GO(24wt%)-200oC为催化剂时,120 min后降解率达到了93。5%,较高的水热温度有利于Bi2WO6与氧化石墨烯的复合,增强两者之间的相互左右,进而提高其光催化性能。
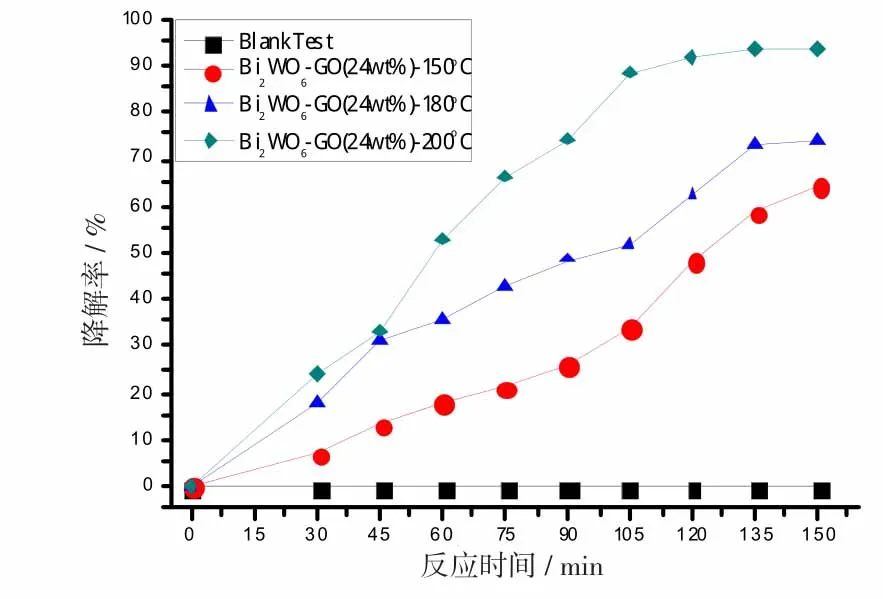
图1 不同煅烧温度对样品光催化性能的影响
2.2 不同石墨烯含量对样品光催化性能的影响
不同石墨烯含量的样品在可见光下降解(20 mg/L)甲基橙的活性如图2所示。结果显示,甲基橙的降解率随石墨烯含量呈先增加后减小的趋势,说明石墨烯含量显著的影响其光催化性能,适量的石墨烯有利于吸收可见光和分离光生电子空穴,从而增加其光催化性能。以Bi2WO6-GO(24wt%)-200oC为催化剂时,甲基橙的降解率可达93.5%。

图2 不同石墨烯含量对样品光催化性能的影响
2.3 Bi2WO6-GO(24wt%)-200oC对不同浓度甲基橙的降解性能
以Bi2WO6-GO(24wt%)-200oC为催化剂,分别考察其对不同浓度(10、20、30 mg/L)的甲基橙溶液的降解效果,结果如图3所示。结果显示,光照120 min后,10、20和30 mg/L甲基橙溶液的降解率分别为93.9%、93.5和60.7%,表明该催化剂对低浓度的甲基橙降解效果更好。

图3 Bi2WO6-GO(24wt%)-200oC对不同浓度甲基橙的光催化性能
3 结论
采用水热法简便快捷的制备了一系列Bi2WO6-GO复合光催化剂,通过降解甲基橙研究了其在可见光下的光催化性能。当水热温度为200oC、石墨烯含量为24wt%时,Bi2WO6-GO催化剂在可见光下对甲基橙的光催化降解性能最好,降解率可达到93.9%。该Bi2WO6-GO复合光催化剂有望在有机染料污染物处理方面得到应用。
[1]Fujishima A,Honda K.Electrochemical photolysis of water at a semiconductor electrode[J].Nature,1972,238:37-38.
[2]Dhananja S B,Vishwas G P,Anthony A B,et al.Solar-assisted photochemical and photocatalytic degradation of phenol[J].Water Chemi Techno,2001,76:363-370.
[3]Jing L Q,Sun X J,Shang J.Light trapping in spherical silicon solar cell module[J].Sol Energ Mat Sol C,2003,79(2):133-124.
[4]Juan Z,Xu D Y.Photocatalytic oxidation for indoor air purification:A literature review[J].Build Environ,200,38(5):645-654.
[5]Li E J,Zhang Q,Li W H,et al.Bismuth-containing semiconductor photocatalysts[J].Prog Chem,2010,22:2282-2289.
[6]Zhang L P,Yuan S,Hu F,et.al.Bismuth(V)-containing semiconductor compounds and their applications in heterogeneous photoca⁃talysis[J].Prog in Chem,2010,22(9):1729-1734.
[7]Shang M,Wang W Z,Ren J,et al.A practical visible light drive Bi2WO6nanofibrous prepared by electrospinning[J].J Materi Chem,2009,19:6213-6218.
[8]Zhang L W,Xu T G,Zhao X,et al.Controllable synthesis of Bi2MoO6and effect of morphology and variation in local structure on pho⁃tocatalytic activities[J].Appl Catal B Environ,2010,98(3-4):138-146.
[9]Zhang X,Ai Z H,Jia F L,et al.Generalized one-pot synthesis,characterization,and photocatalytic activity of hierarchical BiOX(X=Cl,Br,I)nanoplate microspheres[J].J Physi Chem C,2008,112(3):747-753.
[10]Kohtani S,Tomohiro M,Tokumura K,et al.Photooxidation reactions of polycyclic aromatic hydrocarbons over pure and Ag-loaded BiVO4photocatalysts[J].Appl Catal B Environ,2005,58(2):265-272.
[11]Geim A K,Novoselov K S.The rise of grapheme[J].Nat Mater,2007,6:183-191.
[12]Novoselov K S,Geim A K,Morozov S V,et al.Electric field effect in atomically thin carbon films[J].Science,2004,306:666-669.
[13]Chae H K,Siberio P D Y,Kim J.A route to high surface area,porosity and inclusion of large molecules in crystals[J].Nature,2004,427:523-527.
[14]An X Q,Yu J C.Graphene-based photocatalytic composites[J].RSC Advances,2011,1,1426-1434.
