石墨烯增强Ce0.9881Y0.0119O2光催化还原CO2
2018-03-21时圣杰刘守清陈志刚刘成宝
时圣杰,刘守清,陈志刚,刘成宝,陈 丰
(苏州科技大学 化学生物与材料工程学院,江苏 苏州 215009;江苏省环境功能材料重点实验室,江苏 苏州 215009)
1978年,Halmann在Nature上报道了利用GaP半导体光电催化还原CO2的水溶液,制得了甲酸、甲醛和甲醇[1]。随后,Inoue等在Nature上报道利用TiO2、CdS、GaP等半导体悬浮液光催化还原CO2水溶液,制得了甲酸、甲醛、甲醇和甲烷[2]。这些报道持续引发了学术界对光催化还原CO2的研究兴趣。尤其是,甲醇作为一种易储存、便于使用的有机燃料分子,更是CO2光催化还原的目标分子[3-6]。石墨烯是一种由碳原子构成的二维片状结构材料。其快速的电子传输能力能够有效地降低光生电子与光生空穴的复合率,从而提高材料的光催化活性[7]。Chen等用氧化石墨烯(GO)修饰纳米铜粒子,在光辐射下将CO2催化还原为有机燃料分子[8],Xu等评述了rGO作为共催化剂在选择性光催化还原CO2中的作用[9],Gusain等合成了rGO/CuO复合光催化剂,在可见光辐射下光催化还原CO2制得甲醇[10]。笔者曾报道了GO在增强铁酸镍光催化活性中的作用[11]。在此基础上,用钇掺杂CeO2,扩大半导体材料的光谱响应范围,用rGO增强光生电子与光生空穴的分离能力,降低电子-空穴对的复合率,提高氧化铈的光催化还原能力。
1 实验部分
1.1 试剂与仪器
岛津2450型紫外可见分光光度计用于测量漫反射光谱;美国FEI公司Tecnai G22p型高分辨率透射电镜(TEM)用于观测催化剂的形貌和尺寸;X射线衍射仪(Bruker D8)用于表征催化剂的晶体结构;美国安捷伦公司7890B型气相色谱仪用于检测光催化还原产物;法国JY公司LabRam HR800型显微共焦拉曼光谱仪用于表征催化剂的Raman位移;上海比朗仪器有限公司BL-GHX-V型光化学反应器用于光催化反应。
石墨粉购自中国上海试剂总厂,氯化亚铈(CeCl3·7H2O)、硝酸钇(Y(NO3)3·6H2O)、氢氧化钠(NaOH)、碳酸氢钠(NaHCO3)、亚硫酸钠(Na2SO3)、浓硫酸(H2SO4)、高锰酸钾(K2MnO4)、硝酸钠(NaNO3)均为分析纯。
1.2 实验过程
1.2.1 氧化石墨烯制备
采用改进的Hummers法制备氧化石墨烯(GO)[12]。将2.0 g石墨(99.85%,中国上海试剂总厂)与1.0 g硝酸钠放入500 mL烧杯中,加入50 mL浓硫酸,在冰浴条件下缓慢加入6.0 g高锰酸钾,搅拌反应2 h,然后升温至35℃后继续搅拌2 h,接着缓慢加入200 mL的去离子水,持续搅拌20 min,再加入20 mL 5%的双氧水,还原未反应的高锰酸钾,至溶液变成亮黄色后,继续在室温下搅拌2 h。将反应体系静置沉淀,倒出上清液,将下层沉淀进行离心过滤,用5%HCl洗涤至少3次,再用2 000 mL去离子水多次洗涤。将产物在60℃真空干燥箱中干燥6 h即得GO。
1.2.2 rGO/Ce0.9881Y0.0119O2的制备
称取0.004 0 g的GO置于20 mL去离子水中,搅拌2 h,超声震荡3 h,得到均一稳定的GO悬浊液。
依 次 称 取 CeCl3·7H2O (0.433 0 g,1.16 mmol) 和 Y (NO3)3·6H2O (0.008 6 g,0.022 mmol) 溶 解 于20 mL超纯水中搅拌至完全溶解,向溶液中缓慢滴加NaOH(1.0 mol·L-1,15 mL)至pH>10,继续搅拌直至混合液沉淀为亮黄色,得到溶液A。
在磁力搅拌下将GO悬浊液缓慢滴加到溶液A中,搅拌1 h使其混合均匀,再超声3 h。最后将此混合液转入到100 mL的水热反应釜中,置于恒温箱中在180℃下水热反应8 h后,将所得产物离心、洗涤3三次,之后放入真空干燥箱中干燥(60℃,6 h),即得钇掺杂及石墨烯负载的氧化铈杂化材料(rGO/Ce0.9881Y0.0119O2)。
1.2.3 光催化还原CO2及产物的分析
光催化还原CO2反应在光反应器(BL-GHX-V,上海比郎仪器有限公司)中进行,利用250 W Xe灯作为光源,仪器配有冷冻循环水系统保证反应体系温度为恒定值(25±2℃);在浓度均为0.1 mol·L-1的Na2SO3和NaHCO3混合液250 mL中加入0.1 g的催化剂,再向悬浮液中通CO2鼓泡20 min,以除去溶解在溶液里的氧气。光照5 h,每隔1 h抽取反应体系里的溶液,离心取上层清液,用GC-7890B型气相色谱仪测定甲醇产率。
2 结果与讨论
2.1 X射线粉末衍射表征
图1为不同掺杂和负载石墨烯后所制得的CeO2样品的X射线粉末衍射(XRD)图。由图1可知,所制得的一系列氧化铈表现出典型的立方萤石衍射结构,并与CeO2标准图谱JCPDS卡(No.34-0394)一致。3个样品所观察到的特征衍射峰出现在 2θ=28.56°,33.20°,47.28°,56.64°,58.92°,69.30°和 76.89°, 对应的晶面指数分别为(111)、(220)、(311)、(222)、(400)和(331)[13]。图谱中并未观察到氧化钇衍射峰,这表明Y3+掺杂到CeO2晶格中[14]。
根据X射线谱图中28.56°出现的衍射峰的半峰宽,按照 Debye-Scherrer公式:D=kλ/(Wcosθ) 可以计算出杂化材料的晶粒大小。其中D为晶粒的平均直径、λ=0.154 056 nm、k为晶粒的形状因子取0.89、W是衍射峰的半峰宽,计算得到纯CeO2的平均粒径为3.4 nm,钇掺杂的CeO2的粒径为4.7 nm以及负载氧化石墨烯之后的钇掺杂CeO2杂化材料的粒径为5.4 nm,这表明GO的加入和钇的掺杂,促进了CeO2晶体的生长。这也与TEM观察到的结果相一致。

图2 样品的拉曼谱图
2.2 拉曼光谱表征
图 2 分别为 CeO2、Ce0.9881Y0.0119O2、rGO/Ce0.9881Y0.0119O2样品的拉曼光谱(Raman)图。3个样品都在465 cm-1处有一Raman峰,对应于空间群Fm3m,是立方萤石结构的F2g模式Raman峰,这也是CeO2的特征Raman峰[15]。除了在465 cm-1处有一Raman峰外,在595 cm-1处有一小峰。该峰是由于三价铈离子引起的O2-缺陷的二次Raman振动峰,表明所制得的样品中含Ce3+杂质[16]。氧缺位的形成有助于提高材料的催化活性,这些缺陷和Ce3+也被随后的XPS所证实。石墨烯中1 598 cm-1的G带是由C原子中sp2杂化电子E2g对称的双退化声子模式产生的,是石墨中唯一的一阶拉曼散射峰。1 330 cm-1的D带振动,是由K点声子的A1g对称模式产生的,与缺陷和石墨烯结构的不规整有关[17]。曲线C中出现G带和D带,表明Ce0.9881Y0.0119O2分散到石墨烯片上。
2.3 透射电镜观察
图3为rGO/Ce0.9881Y0.0119O2的透射电镜图。图3(a)为rGO的TEM图,从图可以清晰的观察到rGO的二维片状结构。图 3(b-d)分别为不同尺度下的 rGO/Ce0.9881Y0.0119O2的 TEM图。图 3(b)中能够清楚看到Ce0.9881Y0.0119O2分布在石墨烯表面,样品粒径约在5 nm左右,与Debye-Scherrer公式估算的结果基本吻合。图4(d)中能看到明显的晶格条纹,表明得到的样品具有较高的结晶度,与XRD表征的结果一致。

图3 样品的透射电镜图
2.4 紫外可见漫反射光谱表征

图4 样品的紫外可见光漫反射谱图

图 5 以(αhν)2对hν 作图的样品的带隙图
图4为CeO2,Ce0.9881Y0.0119O2和rGO/Ce0.9881Y0.0119O2样品的紫外-可见光漫反射(UV-Vis-DRS)光谱图。图5为由UV-Vis-DRS光谱图所得半导体材料的Tauc图。由图4可见,掺杂钇以及负载GO均使CeO2的吸收带边发生红移,说明掺杂钇和负载GO扩展了CeO2对光谱的响应范围,可望提高对可见光的利用率。这可能是由于CeO2价带和Y3+离子4f能级之间的电荷转移,增强了rGO/Ce0.9881Y0.0119O2杂化材料对光子的吸收能力。
由 Tauc 公式(αhν)2=A(hν-Eg)可计算半导体材料的禁带宽度Eg。式中:α为吸光系数,h为普朗克常数,ν为光的频率,A为常数;Eg为半导体的禁带宽度。作曲线的切线与横坐标的交点即为材料的Eg值。即得rGO/Ce0.9881Y0.0119O2的Eg=2.78 eV,光谱响应波长红移至446.0 nm;未掺杂钇的CeO2禁带Eg=3.16 eV,而掺杂钇后的Eg=2.95 eV。这说明掺杂钇以及负载rGO降低了禁带宽度,增加了催化剂对太阳能的吸收利用率。

图6 样品的XPS宽扫描谱图
2.5 光电子能谱表征

图7 C 1s(a)和 Y 3d(b)的高分辨 XPS 谱图

图8 0.1 g催化剂在250 mL 0.1 mol·L-1NaHCO3溶液中光催化还原CO2制甲醇反应
为进一步研究样品的纯度、表面组成和表面结构,对样品进行X射线光电子能谱(XPS)测试。图6是rGO/Ce0.9881Y0.0119O2样品的XPS宽扫描谱。图6中分别观测到C 1s,O 1s和Ce 3d的电子亲和能。
高分辨XPS图可见C 1s电子亲和能和Y 3d电子亲和能。图7(a)中C 1s出现了两个峰,一个是位于284.6 eV处的主峰,它归属于石墨烯中sp2杂化C的1s电子亲和能;另一个在288.55 eV处,归因于C-O键中C 1s电子亲和能,这表明部分石墨烯处于氧化状态。位于157.18 eV和158.98 eV处的电子亲和能,分别归于Y3d5/2和Y3d3/2峰,表明钇已掺杂到CeO2晶格中。
2.6 光催化还原CO2
在250 mL 0.1 mol·L-1的NaHCO3溶液中,分别加入组成不同的光催化剂0.1 g,以0.1 mol·L-1的Na2SO3作为牺牲剂,250 W Xe灯为模拟太阳光,照射不同时间后,取上层清液1 mL离心分离后用气相色谱仪检测甲醇含量。甲醇产率与光照时间的关系如图8所示。由图8可知,即使光照5 h,纯氧化铈催化剂也几乎没有催化效果(曲线a),而钇掺杂后甲醇产率可提高到 11.9 μmol·g-1cat.·h-1(曲线 b),这表明掺杂 Y 改善了氧化铈的光催化活性;曲线c与a相比表明,负载rGO后CeO2的光催化活性有比较大的提高;而比较曲线d与b可知,负载rGO后的钇掺杂氧化铈杂化催化剂可将甲醇含量显著提高到 111.6 μmol·g-1cat.·h-1,这表明负载 rGO 显著增强了rGO/Ce0.9881Y0.0119O2的光催化活性。
为了获得最佳掺杂比例,制备了掺杂不同质量比Y∶CeO的催化剂,其光催化还原活性如表1所示。
表1的数据表明,当钇含量为CeO2质量的1.0%时,光催化还原二氧化碳为甲醇的产率最高,此时催化剂的分子式可以写为Ce0.9881Y0.0119O2。以此为依据,笔者研究了GO含量对催化剂光催化活性的影响,其结果如表2所示。
由表2可知,当GO的负载量为Ce0.9881Y0.0119O2催化剂质量的2.0%时,甲醇的产率达到最大,等于111.6 μmol·g-1cat.·h-1。 因此,GO 负载率为 2.0%是最佳负载率。

表1 钇掺杂量对甲醇产率的影响

表2 氧化石墨烯负载量对甲醇产率的影响
2.7 甲醇的来源
为了证明甲醇是CO2的还原产物,笔者专门做了空白实验和对照实验。取0.1 g相同质量的催化剂 rGO/Ce0.9881Y0.0119O2, 在 250 mL 0.1 mol·L-1的NaHCO3-Na2SO3溶液中进行暗反应,5 h后未检测到甲醇,这说明光照对CO2还原起着关键作用。在另一组光催化实验中,反应液里不加入NaHCO3以及不用CO2鼓泡,加入0.1 grGO/Ce0.9881Y0.0119O2同样光照5 h后,也未检测到反应体系中有甲醇生成。这说明在光催化反应中,甲醇来自CO2或者HCO3-。
CO2还原为甲醇的标准电极电位E0=-0.38 V(vs NHE)[18],CeO2的导带电位 ECB=-1.02 V[19],因此,光生电子可以将CO2还原为甲醇。催化反应过程,如图9所示。
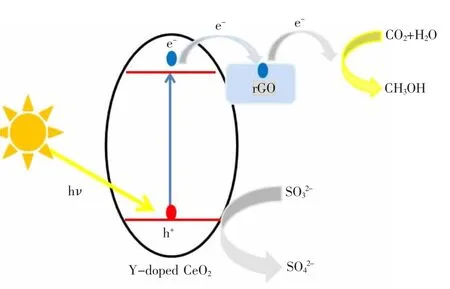
图 9 rGO/Ce0.9881Y0.0119O2杂化光催化剂光催化还原CO2示意图
3 结语
氧化铈是一种稀土金属氧化物半导体材料,通过钇掺杂可以调控其能带结构,实现吸收光谱的红移;通过负载氧化石墨烯,既可以进一步增加半导体杂化材料对可见光的吸收利用率,也可以增强该材料的光催化还原活性,提高光催化还原CO2为甲醇的产率。
[1]HALMANN M.Photoelectrochemical reduction of aqueous carbon dioxide on p-type gallium phosphide in liquid junction solar cells[J].Nature,1978,275:115-116.
[2]INOUE T,FUJISHIMA A,KONISHI S,et al.Photoelectrocatalytic reduction of carbon dioxide in aqueous suspensions of semiconductor powders[J].Nature,1979,5698(277):637-638.
[3]TSAI C W,CHEN H M,LIU R S,et al.Ni@NiO core-shell structure-modified nitrogen-doped in TaO4for solar-driven highly efficient CO2reduction to methanol[J].J Phys Chem C,2011,115(20):10180-10186.
[4]ZENG G T,QIU J,LI Z,et al.CO2reduction to methanol on TiO2-passivated GaP photocatalysts[J].ACS Catal,2014,4(10):3512-3516.
[5]KUMAR P,SAIN B,JAIN S L.Photocatalytic reduction of carbon dioxide to methanol using a ruthenium trinuclearpolyazine complex immobilized on graphene oxide under visible light irradiation[J].J Mater Chem A,2014,2:11246-11253.
[6]YADAV R K,OH G H,PARK N J,et al.Highly selective solar-driven methanol from CO2by a photocatalyst/biocatalyst integrated system[J].J Am Chem Soc,2014,136(48):16728-16731.
[7]CHEN D,ZHANG H,LIU Y,et al.Graphene and its derivatives for the development of solar cells,photoelectrochemical,and photocatalytic applications[J].Energy Environ Sci,2013,6:1362-1387.
[8]SHOWN I,HSU H C,CHANG Y C,et al.Highly efficient visible light photocatalytic reduction of CO2to hydrocarbon fuels by Cu-nanoparticle decorated graphene oxide[J].Nano Lett,2014,14(11):6097-6103.
[9]YANG M Q,XU Y J.Selective photoredox using graphene-based composite photocatalysts[J].Chem Phys,2013,15:19102-19118.
[10]GUSAIN R,KUMAR P,SHARMA OP,et al.Reduced graphene oxide-CuO nanocomposites for photocatalytic conversion of CO2into methanol under visible light irradiation[J].Applied Catalysis BEnvironmental,2016,181:352-362.
[11]LIU S Q,XIAO B,FENG L R,et al.Graphene oxide enhances the Fenton-like photocatalytic activity of nickel ferrite for degradation of dyes under visible light irradiation[J].Carbon,2013,64:197-206.
[12]HUMMERS W,OFFEMAN R.Preparation of graphitic Oxide[J].J Am Chem Soc,1958,80(6):1339-1340.
[13]SOYKAL I I,SOHN H,OZKAN U S.Effect of support particle size in steam reforming of ethanol over Co/CeO2Catalysts[J].ACS Catal,2012,2(11):2335-2348.
[14]JEYANTHI C E,SIDDHESWARARAN R,MEDLIN R,et al.Eletrochemical and structural analysis of the RE3+:CeO2nanopowders from combustion synthesis[J].J Alloy Compd,2014,614:118-125.
[15]WEBER W H,HASS K C,MCBRIDE J R.Raman study of CeO2:Second-order scattering,lattice dynamics,and particle-size effects[J].Phys Rev B:Condens Matter,1993,48:178-185.
[16]LIYANAGE A D,PERERA S D,TAN K,et al.Synthesis,characterization,and photocatalytic activity of Y-doped CeO2nanorods[J].ACS Catal,2014,4(2):577-584.
[17]AKHAVAN O.The effect of heat treatment on formation of graphene thin films from graphene oxide nanosheets[J].Carbon,2010,2(48):509-519.
[18]吴聪萍,周勇,邹志刚.光催化还原 CO2的研究现状和发展前景[J].催化学报,2011,32(10):1565-1572.
[19]CHEN C H,SHIEH J,LIAO H Y,et al.Construction of titania-ceria nanostructured composites with tailored heterojunction for photocurrent enhancement[J].J Eur Ceram Soc,2014,34(6):1523-1535.
