金诃牌清瑞胶囊的毒理学安全性评价
2018-03-19刘有菊马文俊袁发荣曾志斌
刘有菊 马文俊 袁发荣 曾志斌

【摘要】目的:对金诃牌清瑞胶囊的食用安全性进行毒理学评价。方法:依据食品安全性毒理学评价程序和方法进行急性毒性试验、遗传毒性试验(Ames试验、骨髓细胞微核试验和精子畸形试验)、大鼠30d喂养试验。结果:小鼠急性毒性试验经口最大耐受剂量(MTD)均>20g/kg.bw,属无毒级。Ames试验、骨髓细胞微核试验和精子畸形试验结果均为阴性,表明受试物无致突变作用,30d喂养试验,试验动物均生长发育良好,体重、摄食量、血液学、血液生化学、脏器系数及病理组织学相关指标均未见异常变化。结论:金诃牌清瑞胶囊急性毒理分级属无毒级,无遗传毒性,在本试验剂量范围内,金诃牌清瑞胶囊属于安全性保健食品。
【关键词】金诃牌清瑞胶囊;毒理学;安全性
金诃牌清瑞胶囊以蝙蝠蛾拟青霉菌粉、三七、枸杞子提取物、红景天提取物、绞股蓝提取物为主要原料组方。其中蝙蝠蛾青霉菌粉为冬虫夏草的菌株经人工发酵获得的冬虫夏草真菌,其药理学与虫草相似,有补肺肾、止咳、益虚损的作用;三七可补血、活血化瘀枸杞子提取物可补肝益肾、益精明;红景天提取物可益气活血、通脉平喘;绞股蓝提取物消炎解毒、止咳祛痰。本配方主要从调理气血、肾肺三方面来调节人体的免疫功能。全方益气补血、补肾益肺、活血化瘀、解毒、化痰,注意整体调节,扶正驱邪,达到增强免疫力的保健功效。
1 材料与方法
1.1 受试样品
金诃牌清瑞胶囊由金诃藏药股份有限公司提供,人体推荐量为每人4.5g/人·日(成人体重按60kg计),取其内容物作为受试物供实验用。菌种鼠伤寒沙门氏菌组氨酸缺陷型TA 97a、TA 98、TA 100、TA 102四种菌株,由广西疾病预防微生物实验室提供。
1.2 实验动物及饲养环境
SPF级KM种小鼠,体重18-22g,雌雄各半,由山东大学实验动物中心提供,生产许可证号:SCXK(鲁)2009-0001;SPF级ICR小鼠,体重25-30g,雌雄各半;SPF级SD大鼠,体重60-90g,雌雄各半;均由北京华阜康生物科技股份有限公司提供,生产许可证号:SCXK(京)2009-0004;饲养环境为屏障级,实验动物使用许可证号:SYXK(鲁)2008-0005。实验动物标准饲料为北京华阜康生物科技股份有限公司实验动物标准饲料,许可证号:SCXK(京)2009-0008号。
1.3 仪器
CELLY HY318血细胞分析仪(法国Cell公司);HITACHI7180全自动生化分析仪(日立)。
1.4 方法I1-5]
1.4.1 急性毒性试验
按最大耐受量试验方法进行,选择雌雄各10只小鼠,体重18-21g,试验前空腹16h备用(不限制饮水),称取10g受试物,以蒸馏水配至30ml,终浓度为0.33g/ml,分三次灌胃给予实验动物,间隔4h,每次灌胃量为0.2ml/10g-bw,累计染毒剂量为20g/kg-bw,记录动物的中毒表现及死亡情况,连续观察14d。
1.4.2 污染物致突变性检测(Ames)试验
试验按照平板掺入法,经鉴定符合要求的鼠伤寒沙门氏菌组氨酸缺陷型TA97、TA98、TA100、TA102四株菌株进行试验;采用多氯联苯(PCB)诱导的大鼠肝匀浆作为体外活化系统(+S9)。受试样品设5个剂量组:8、40、200、1000、5000ug/皿,同时设立自发回变组、溶剂对照组和阳性对照组。在相同条件下重复做2次。如果受试物的回变菌落数增加超过自发回变菌落数的2倍以上,并具有剂量反应关系者,即为诱变试验阳性。
1.4.3 小鼠骨髓嗜多染红细胞微核试验
昆明种小鼠50只,体重25-30g,随机分为5组,每组10只,雌雄各半。设3个试验组染毒剂量分别为(2.5 g/kg-bw、5g/kg-bw、10 g/kg-bw),同时设阴性对照组(蒸馏水)和阳性对照组(环磷酰胺40mg/kg-bw),分别称取2.5、5.0 g受试物,以蒸馏水配至20ml,终浓度分别为0.125、0.25 g/ml,灌胃给予低、中剂量组实验动物,灌胃容积为0.2ml/lOg-bw;另取10g受试物,以蒸馏水配至30 ml,终浓度为0.33g/ml,灌胃给予高剂量组实验动物,灌胃容积为0.3 ml/lOg-bw,给药后各组均间隔24h两次灌胃,于第2次灌胃6h后采用颈椎脱臼处死小鼠,取胸骨骨髓用小牛血清稀释涂片,甲醇固定,Giemsa染色。在光学显微镜下,每只小鼠计数1000个嗜多染红细胞(PCE ),微核率以含微核的PCE千分率计,同时计数200个嗜多染红细胞,计算PCE与成熟红细胞(NCE)的比值(PCE/NCE)。采用泊松分布均数比较法统计处理。
1.4.4 小鼠精子畸形试验
昆明种雄性小鼠25只,体重28-3 2g,按体重随机分为5组。每组5只。设3个实验组染毒剂量分别为( 2.5、5、10 g/kg-bw),同时设阴性对照组(蒸馏水)和阳性对照组(环磷酰胺40mg/kg·bw)。分别称取2.5、5g受试物,以蒸馏水配至20ml,终浓度分别为0.125、0.25 g/ml,灌胃给予低、中剂量组实验动物,灌胃量为0.2ml/10g·bw;另取lOg受试物,以蒸馏水配至30ml,终浓度为0.33 g/ml,灌胃给予高剂量组实验动物,灌胃量为0.3ml/10g·bw,每天1次,连续灌胃5d,从首次灌胃后第35 d采用颈椎脱臼法处死小鼠,取出两侧附睾涂片,伊红染色。在高倍镜下观察精子形态,每只小鼠检查1000个结构完整的精子,记录畸变类型和数量,计算精子畸形率(以百分率表示)。
1.4.5 30d喂养试验
选用67-88 g健康断乳大鼠80只,随机分成4组,每组20只,雌雄各半,单笼饲养,自由摄食饮水。根据人体推荐量设低、中、高3个试验组和对照组,染毒剂量分别为1.88、3.75、7.5g/kg-bw(分别相当于人体推荐量的25、50、100倍)。各试验组每天按剂量灌胃给药,对照组灌以蒸馏水,连续30 d。按照动物体重的10%计算食物摄入量将受试物掺入饲料中,即1.88%、3.75%、7.5%(质量分数)喂饲实验动物。高剂量组在基础饲料中掺入酪蛋白,调整其蛋白含量为20%(与对照组的基础饲料中蛋白含量一致)。對照组给予基础饲料。单笼喂养,自由饮食,连续观察30d。试验中观察动物一般状况、进食、饮水及活动等;每周称量1次体重和2次食物摄入量,观察体重变化,计算每周的食物利用率和总的食物利用率;实验末期禁食16h,称取动物体重(供计算肝、脾、肾、睾丸等脏器系数使用)后,断头取血,进行血液学和生化血液学指标测定,解剖动物并取材进行病理组织学检查。
1.5 统计学处理
使用Microsoft Excel和spss软件进行均数、标准差的计算和方差分析或秩和检验,数据以均数土标准差(x±s)形式表示。
2 结果
2.1 急性毒性试验
给予受试物后,雌、雄小鼠均未见明显中毒症状,在观察期间内雌、雄小鼠均未见异常反应,生长情况良好,无死亡发生。受试物小鼠经口最大耐受剂量(MTD)均>20.0 g/kg-bw。根据急性毒性分级标准,该样品属实际无毒级。结果见表1。
2.2 遗传毒性试验
2.2.1 Ames试验
由表2、表3可见,两次试验中受试物各剂量组回变菌落数均未超过自发回变菌落数的2倍,亦无剂量一反应关系,说明在加与不加S-9时该样品对鼠伤寒沙门氏菌TA97、TA98、TA100、TA102四株试验菌株均未呈现遗传毒性。
2.2.2 小鼠骨髓嗜多染红细胞微核试验
由表4可见,受试物各剂量组微核率与阴性对照组比较无显著性差异(P>0.05),而环磷酰胺阳性对照组与阴性对照组比较有极显著性差异(P<0.01),说明该样品无致小鼠骨髓嗜多染红细胞微核作用。
2.2.3 小鼠精子畸形试验
由表5,表6可见,受试物各剂量组小鼠精子畸形率与阴性对照组比较无显著性差异(P>0.05),而环磷酰胺阳性对照组与阴性对照组比较有极显著性差异(P<0.01),说明该样品无致小鼠精子畸形作用。
2.3 大鼠30d喂养试验
2.3.1 动物的一般表现
试验周期内各试验组动物总体生长状况良好,体重逐周增长,未见中毒体征及死亡。
2.3.2 体重、食物利用率测定结果
由表7、表8可见,各试验组动物每周体重、进食量、食物利用率和体重增重、总进食量、总食物利用率与对照组比较均无显著性差异(P>0.05)。
2.3.3 血液学测定结果
由表9可见,实验动物各剂量组血液学指标与对照组比较均无显著性差异(P>0.05),且其值均在本实验室正常范围内。
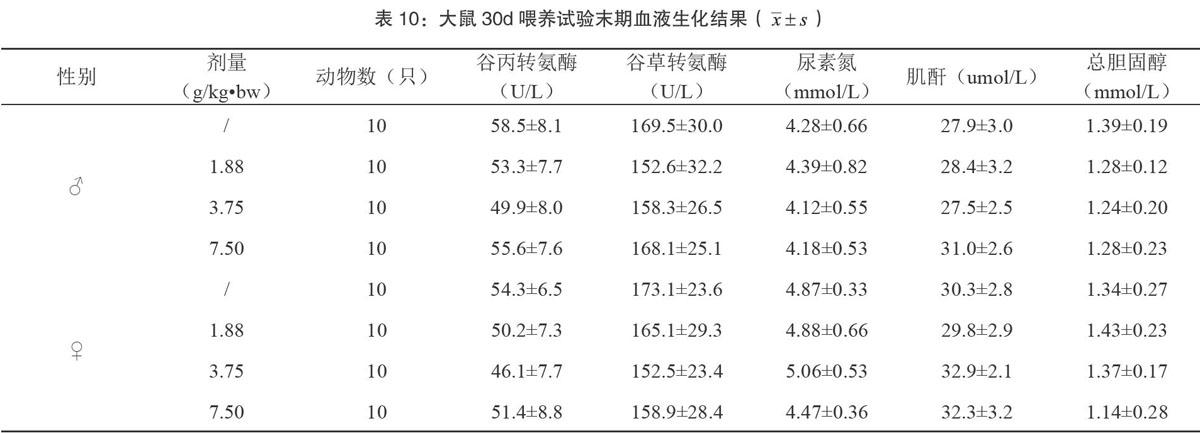
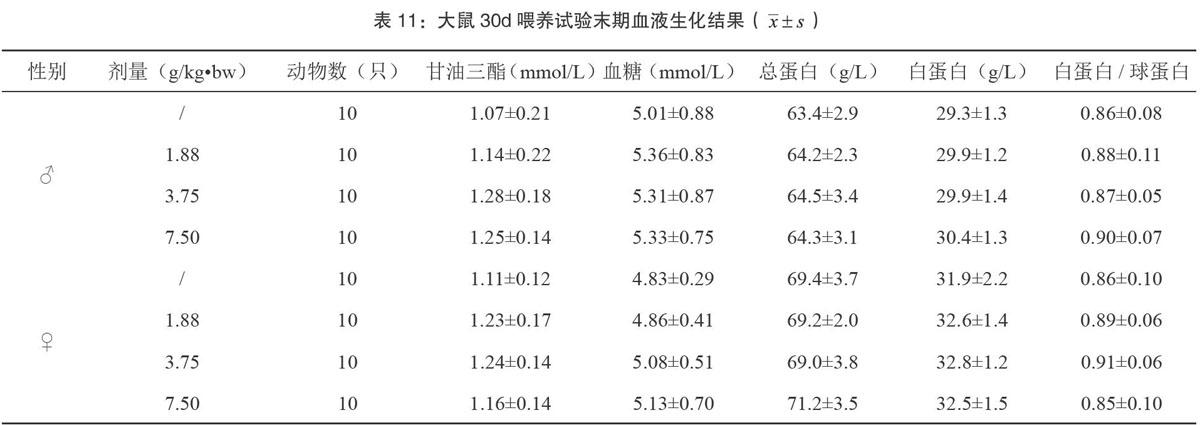
2.3.4 血液生化学测定结果
由表10和表11可见,各实验组动物血液生化各指标与对照组比较均无显著性差异(P>0.05),且其值均在本实验室正常值范围内。
2.3.5 病理检查
2.3.5.1 大体解剖
试验结束时对所有动物进行大体检查,肝脏大小正常、颜色新鲜、表面光滑、质地柔软、边缘锐利、无结节包块等。取出两侧肾和肾上腺,对准肾门将肾以最大剖面剖开,暴露肾盂,检查皮质和髓质的厚度、颜色正常,界限清晰。未见胃肠粘膜出血、溃疡、增厚、淋巴滤泡增生等病变。观察脾切面马氏小体清晰可辨。睾丸、卵巢形态、大小正常。各实验组动物的肝、肾、胃、肠、脾和卵巢、睾丸组织中,未见明显异常。
2.3.5.2 脏器系数测定结果
由表12可见,肝、脾、肾、睾丸等脏器的重量和脏器系数与对照组比较均无显著性差异(P>0.05)。
2.3.5.3 组织病理学检查结果
大体观察各试验组动物的肝、肾、胃、肠、脾和卵巢/睾丸组织中,未见明显异常。组织学检查中,对照组和高剂量组少数动物的标本出现病理改变,但这些病理改变程度较轻且无组间特异性分布,考虑与动物质量有关,与对照组相比,不认为实验组出现有意义的病理改变。
3 结论
研究表明,蝙蝠蛾拟青霉菌粉为冬虫夏草的菌株经人工发酵获得的冬虫夏草真菌,即冬虫夏草发酵菌丝粉(蝙蝠蛾拟青霉菌丝粉paecilomyces hepiali chen),其化学成分与虫草子实体中相应的成分基本一致,主要腺苷、多糖、氨基酸、不饱和脂肪酸和金属元素等。匡彦德[6]等用冬虫夏草水提取液对小鼠胸腺细胞、脾细胞以及脾细胞经除去thy -1+细胞后残存的细胞都有与剂量相关的致有丝分裂作用,说明虫草对T和B淋巴细胞有增殖作用。药理学研究发现三七中含有三七皂苷、三七素、黄铜、挥发油、氨基酸、糖类及各种微量元素等,三七苷为其主要活性成分之一。赵鹏、李彬[7]等探讨三七皂甙对小鼠免疫功能的影响。结果显示,三七皂甙能明显刺激小鼠的脾淋巴细胞增值、转化作用、促进小鼠迟发型变态反应作用,提高小鼠抗体生成细胞数,提高小鼠的血清溶血素水平,促进小鼠单核一巨嗜细胞碳廓清作用,增强小鼠的单核一腹腔巨嗜细胞吞噬能力,提高小鼠NK细胞活性。枸杞子含有枸杞多糖、单糖、甜菜碱、脂肪酸、蛋白质、氨基酸、维生素和微量元素等多种化学成分,具有多种功效作用。王辉、白秀珍[8]研究枸杞煎剂对小白鼠免疫功能的作用。结果显示,枸杞煎剂可明显增加小白鼠的脾指数、胸腺指数、淋巴细胞转化率。红景天主要化学成分有红景天苷、黄酮类化合物、酚类化合物、多糖、蛋白质、脂肪、微量挥发油及微量元素、氨基酸等。增强免疫力为其中功效之一。李立、王秋水[9]等探讨红景天提取物对小鼠免疫功能的影响。结果显示,红景天提取物可提高小鼠碳廓清能力;增强绵羊红细胞诱导小鼠DTH能力,促进NK细胞活性和血清凝血素的生成,增加抗体生成细胞数的生成,并且能提高小鼠腹腔巨嗜细胞吞噬鸡红细胞的能力。绞股蓝含有多种化学成分,如皂苷、氨基酸、糖类、甾醇、有机酸、微量元素、植物蛋白等。具有多种功效,增强免疫力为其中功效之一。周俐、叶开和[10]等探讨绞股蓝总苷免疫增强的药理作用,结果显示,绞股蓝总苷可明显的增强体液免疫功能和细胞免疫功能。
金诃牌清瑞胶囊对小鼠经口最大耐受剂量(MTD)均>20 g/kg-bw,属于实际无毒物;Ames试验、小鼠骨髓嗜多染红细胞微核试验及精子畸形试验结果均为阴性30d喂养大鼠对大鼠毛色、进食、饮水、行为活动、生长发育、食物利用率、血液学指标、血液学生化指标均无明显影响,解剖未见异常症状,肝体比、肾体比和脾体比与阴性对照组无显著差异。结果表明金诃牌清瑞胶囊符合食品安全标准,是安全的保健食品。
参考文献
[1]中国疾病预防控制中心营养与食品安全所.GB15193.1-2003食品安全性毒理学评价程序[M].北京:中国标准出版社,2004.
[2]高慧艳,于贺娟等.杜仲雄花荼的毒理学安全性评价[J].岁中国卫生检验杂志,2015 (25)7:959-962.
[3]郭艳,兰真,曾凡骏等.赶黄草的安全性毒理学评价研究[J].预防医学情报杂志,2016 (32):7:476-481.
[4]田好亮,李立,王勇等.天麻微粉的毒理学安全性评价[J].中国卫生检验杂志,2014 (24)15: 2161-2164。
[5]黄聘和,敬明武,蒋勇等.小鼠精子畸形试验的方法学探讨[J].中国卫生检验杂志,2017 (33)8:809-812.
[6]匡彦德,王美英,钱琴芳等.冬虫夏草免疫增强作用机理的研究[J].上海免疫学杂志,1989,9 (01):6-8.
[7]赵鹏,李彬,何为涛等.三七皂甙对小鼠免疫功能影响的实验研究[J].中国热带医学,2004,4 (04): 522-524.
[8]王輝,白秀珍,包品.枸杞煎剂对小白鼠免疫功能的作用[J].锦州医学院学报,2006,27 (01): 47-49.
[9]李立,王秋水等.红景天提取物对小鼠免疫功能的影响[J].安徽农业科学,2011, 39 (06): 3301-3302.
[10]周俐,叶开和等.绞股蓝总苷对免疫低下小鼠非特异免疫功能的影响[J].中国基层医药.2006.13 (06):979-978.
